在一定条件下,向V L密闭容器中充入 和
和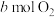 ,发生反应
,发生反应 。
。
(1)反应刚开始时,由于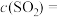
___________ ,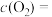
___________ ,而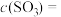
___________ ,所以化学反应速率___________ 最大,而___________ 最小(为零)(填“v(正)”或“v(逆)”)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为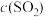
___________ (填“增大”“减小”或“不变”下同),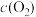
___________ ,而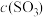
___________ ,从而化学反应速率v(正)___________ ,而v(逆)___________ 。
(3)当反应进行到时v(正)与v(逆)___________ 时,此时可逆反应达到最大限度,若保持外界条件不变时,混合物中各组分的物质的量、浓度、质量分数、体积分数及总压强都___________ 。
(4)以下是反应: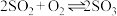 在不同条件下达到平衡状态时
在不同条件下达到平衡状态时 的转化率。
的转化率。
试回答下列问题:
①提高该化学反应限度的途径:___________ 。
②要实现 的转化率为93.5%,需控制的反应条件是
的转化率为93.5%,需控制的反应条件是___________ 。
 和
和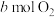 ,发生反应
,发生反应 。
。(1)反应刚开始时,由于
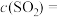
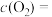
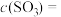
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为
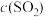
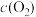
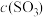
(3)当反应进行到时v(正)与v(逆)
(4)以下是反应:
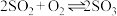 在不同条件下达到平衡状态时
在不同条件下达到平衡状态时 的转化率。
的转化率。压强 转化率 温度 | 0.1 MPa | 0.5 MPa | 1 MPa | 10 MPa |
| 400℃ | 99.2% | 99.6% | 99.7% | 99.9% |
| 500℃ | 93.5% | 96.9% | 97.8% | 99.3% |
| 600℃ | 73.7% | 85.8% | 89.5% | 96.4% |
①提高该化学反应限度的途径:
②要实现
 的转化率为93.5%,需控制的反应条件是
的转化率为93.5%,需控制的反应条件是
22-23高一下·山西忻州·期中 查看更多[2]
更新时间:2023-04-27 21:23:02
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】某温度时,在一个2L的密闭容器中A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,回答下列问题:
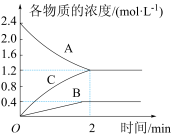
(1)该反应的化学方程式为___________ 。
(2)从开始至2min,B的平均反应速率为___________ ;平衡时,C的浓度为___________ ,A的转化率为___________ 。
(3)反应达平衡时体系的压强是开始时的___________ 倍(用分数表示)。
(4)下列叙述能说明该反应已达到化学平衡状态的是___________(填字母标号)。
(5)在某一时刻采取下列措施能使该反应速率减小的是___________(填字母标号)。

(1)该反应的化学方程式为
(2)从开始至2min,B的平均反应速率为
(3)反应达平衡时体系的压强是开始时的
(4)下列叙述能说明该反应已达到化学平衡状态的是___________(填字母标号)。
| A.B的体积分数不再发生变化 |
| B.相同时间内消耗3nmolA,同时消耗nmol的B |
| C.混合气体的总质量不随时间的变化而变化 |
| D.混合气体的密度不随时间的变化而变化 |
| A.增大压强 | B.降低温度 |
| C.体积不变,充入A | D.体积不变,从容器中分离出A |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】已知放热反应: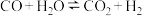 ,起始温度为600℃,在甲、乙、丙三个容积均为4L的恒容绝热(与外界没有热量交换)的密闭容器中分别充入不同物质的量的起始气体(如图所示),开始发生反应,甲容器达到平衡时用时10s,平衡时
,起始温度为600℃,在甲、乙、丙三个容积均为4L的恒容绝热(与外界没有热量交换)的密闭容器中分别充入不同物质的量的起始气体(如图所示),开始发生反应,甲容器达到平衡时用时10s,平衡时 的物质的量为0.6mol。回答下列问题:
的物质的量为0.6mol。回答下列问题:
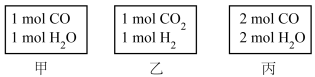
(1)甲容器0~10s内用CO表示的平均反应速率为__________ ,CO的转化率为__________ 。
(2)甲容器达到平衡时体系温度__________ (填“>”“<”或“=”)600℃,乙容器达到平衡时,容器内的温度低于甲容器,可能的原因为__________ 。
(3)下列说法能说明乙容器达到平衡状态的是__________(填序号)。
(4)丙容器达到平衡所需的时间__________ 10s(填“>”“<”或“=”),原因是__________ 。
(5)达到平衡后保持温度不变,向丙容器中通入2molNe,此时反应的速率将__________ (填“增大”“减小”或“不变”)。
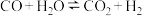 ,起始温度为600℃,在甲、乙、丙三个容积均为4L的恒容绝热(与外界没有热量交换)的密闭容器中分别充入不同物质的量的起始气体(如图所示),开始发生反应,甲容器达到平衡时用时10s,平衡时
,起始温度为600℃,在甲、乙、丙三个容积均为4L的恒容绝热(与外界没有热量交换)的密闭容器中分别充入不同物质的量的起始气体(如图所示),开始发生反应,甲容器达到平衡时用时10s,平衡时 的物质的量为0.6mol。回答下列问题:
的物质的量为0.6mol。回答下列问题: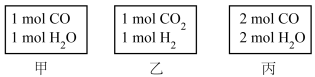
(1)甲容器0~10s内用CO表示的平均反应速率为
(2)甲容器达到平衡时体系温度
(3)下列说法能说明乙容器达到平衡状态的是__________(填序号)。
A.每消耗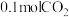 ,同时生成 ,同时生成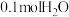 |
| B.容器内CO的体积分数不再改变 |
C.CO、 、 、 和 和 的物质的量之比为1:1:1:1 的物质的量之比为1:1:1:1 |
| D.容器内温度不再变化 |
(5)达到平衡后保持温度不变,向丙容器中通入2molNe,此时反应的速率将
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某温度时,在2 L的密闭容器中,X、Y、Z(均为气体)三种物质的量随时间的变化曲线如图所示。
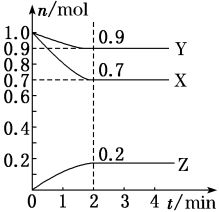
(1)由图中所给数据进行分析,该反应的化学方程式为___________________________ ;
(2)反应从开始至2分钟,用Z的浓度变化 表示的平均反应速率为v(Z)=________________ ;
(3)2min反应达平衡容器内混合气体的平均相对分子质量比起始时__________ (填增大、减小或不变);混合气体密度比起始时_________ (填增大、减小或不变)。
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n (X) = n (Y) =n (Z),则原混合气体中a : b =______________ 。
(5)下列措施能加快反应速率的是_____________ 。
A.恒压时充入He
B.恒容时充入He
C.恒容时充入X
D.及时分离出Z
E.升高温度
F.选择高效的催化剂
(6)下列说法正确的是___________ 。
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢
C.化学反应的限度与时间长短无关 D.化学反应的限度是不可能改变的
E. 增大Y的浓度,正反应速率加快,逆反应速率减慢

(1)由图中所给数据进行分析,该反应的化学方程式为
(2)反应从开始至2分钟,用Z的浓度变化 表示的平均反应速率为v(Z)=
(3)2min反应达平衡容器内混合气体的平均相对分子质量比起始时
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:n (X) = n (Y) =n (Z),则原混合气体中a : b =
(5)下列措施能加快反应速率的是
A.恒压时充入He
B.恒容时充入He
C.恒容时充入X
D.及时分离出Z
E.升高温度
F.选择高效的催化剂
(6)下列说法正确的是
A.升高温度改变化学反应的限度
B.已知正反应是吸热反应,升高温度平衡向右移动,正反应速率加快,逆反应速率减慢
C.化学反应的限度与时间长短无关 D.化学反应的限度是不可能改变的
E. 增大Y的浓度,正反应速率加快,逆反应速率减慢
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】氮是一种重要的元素,其对应化合物在生产生活中有重要的应用。
(1)氮化铝(AlN)可用于制备耐高温的结构陶瓷,遇强碱会腐蚀,写出AlN与氢氧化钠溶液反应的离子方程式_______________ 。
(2)氨是制备氮肥、硝酸等的重要原料②③
①已知:N2(g)+3H2(g) 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/mol
N2(g)+O2(g) 2NO(g) △H=+180 kJ/mol
2NO(g) △H=+180 kJ/mol
2H2(g)+O2(g) 2H2O(1) △H= -571.6 kJ/mol
2H2O(1) △H= -571.6 kJ/mol
试写出表示氨的标准燃烧热的热化学方程式________________ 。
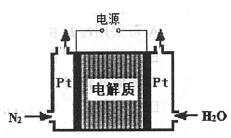
②某电解法制氨的装置如右图所示,电解质只允许质子通过,试写出阴极的电极反应式__________ 。
(3)反应:2NO(g)+O2(g) 2NO2(g)△H<0是制备硝酸过程中的一个反应。
2NO2(g)△H<0是制备硝酸过程中的一个反应。
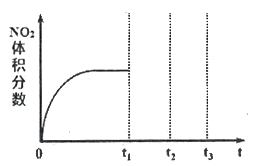
①将NO和O2按物质的量之比为2:1置于恒温恒容密闭容器中进行上述反应,得到NO2体积分数与时间的关系如下图所示。保持其它条件不变,t1时再向容器中充入适量物质的量之比为2:1的NO和O2的混合气体,t2时再次达到平衡,请画出tl-t3时间范围内NO2体积分数随时间的变化曲线:____________ 。
②在研究此反应速率与温度的关系时发现,NO转化成NO2的速率随温度升高反而减慢。进一步研究发现,上述反应实际是分两步进行的:
I 2NO(g) N2O2(g) △H<0
N2O2(g) △H<0
II N2O2(g)+O2(g) 2NO2(g) △H<0
2NO2(g) △H<0
已知反应I能快速进行,试结合影响化学反应速率的因素和平衡移动理论分析,随温度升高,NO转化成NO2的速率减慢的可能原因________ 。
(4)已知常温下,Ka(CH3COOH)=Kb(NH3·H2O)=l.8×l0-5。则常温下0.lmol/L的CH3COONH4溶液中,(CH3COO-):c(NH3·H2O)=________________ 。
(1)氮化铝(AlN)可用于制备耐高温的结构陶瓷,遇强碱会腐蚀,写出AlN与氢氧化钠溶液反应的离子方程式
(2)氨是制备氮肥、硝酸等的重要原料②③
①已知:N2(g)+3H2(g)
 2NH3(g) △H=-92.4kJ/mol
2NH3(g) △H=-92.4kJ/molN2(g)+O2(g)
 2NO(g) △H=+180 kJ/mol
2NO(g) △H=+180 kJ/mol2H2(g)+O2(g)
 2H2O(1) △H= -571.6 kJ/mol
2H2O(1) △H= -571.6 kJ/mol试写出表示氨的标准燃烧热的热化学方程式
②某电解法制氨的装置如右图所示,电解质只允许质子通过,试写出阴极的电极反应式
(3)反应:2NO(g)+O2(g)
 2NO2(g)△H<0是制备硝酸过程中的一个反应。
2NO2(g)△H<0是制备硝酸过程中的一个反应。①将NO和O2按物质的量之比为2:1置于恒温恒容密闭容器中进行上述反应,得到NO2体积分数与时间的关系如下图所示。保持其它条件不变,t1时再向容器中充入适量物质的量之比为2:1的NO和O2的混合气体,t2时再次达到平衡,请画出tl-t3时间范围内NO2体积分数随时间的变化曲线:
②在研究此反应速率与温度的关系时发现,NO转化成NO2的速率随温度升高反而减慢。进一步研究发现,上述反应实际是分两步进行的:
I 2NO(g)
 N2O2(g) △H<0
N2O2(g) △H<0II N2O2(g)+O2(g)
 2NO2(g) △H<0
2NO2(g) △H<0已知反应I能快速进行,试结合影响化学反应速率的因素和平衡移动理论分析,随温度升高,NO转化成NO2的速率减慢的可能原因
(4)已知常温下,Ka(CH3COOH)=Kb(NH3·H2O)=l.8×l0-5。则常温下0.lmol/L的CH3COONH4溶液中,(CH3COO-):c(NH3·H2O)=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】对于反应:2SO2+O2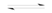 2SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“ 减小”或“不变”)。
2SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“ 减小”或“不变”)。
 2SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“ 减小”或“不变”)。
2SO3,当其他条件不变时,只改变一个条件,将生成SO3的反应速率的变化填入下表格里(填“增大”、“ 减小”或“不变”)。| 编号 | 改变的条件 | 生成的SO3的速率 |
| ① | 降低温度 | |
| ② | 升高温度 | |
| ③ | 增大O2的浓度 | |
| ④ | 恒容下充入Ne | |
| ⑤ | 压缩体积 | |
| ⑥ | 使用催化剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】已知:CH4(g)+2NO2(g) N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:
(1)开展实验1和实验2的目的是:____________________ 。
(2)180℃、反应到40min时,体系______ (填“达到”或“未达到”)平衡状态,理由是:______________ ;此时CH4的平衡转化率为:_________ 。
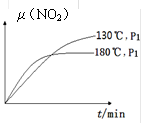
(3)在一定条件下,反应时间t与转化率μ(NO2)的关系如图所示,请在图象中画出180℃时,压强为P2(设压强P2>P1)的变化曲线,并做必要的标注_____ 。
 N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:
N2(g)+CO2(g)+2H2O(g) ΔH=-867 kJ·mol-1。该反应可用于消除氮氧化物的污染。在130℃和180℃时,分别将0.50 molCH4和a molNO2充入1L的密闭容器中发生反应,测得有关数据如下表:| 实验 编号 | 温度 | 时间 min 物质 的量mol | 0 | 10 | 20 | 40 | 50 |
| 1 | 130℃ | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| 2 | 180℃ | n(CH4)/mol | 0.50 | 0.30 | 0.18 | 0.15 |
(1)开展实验1和实验2的目的是:
(2)180℃、反应到40min时,体系
(3)在一定条件下,反应时间t与转化率μ(NO2)的关系如图所示,请在图象中画出180℃时,压强为P2(设压强P2>P1)的变化曲线,并做必要的标注

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】反应2SO2(g)+O2(g)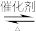 2SO3(g) 在容积为2L的密闭容器中进行,初始时向容器里充入4molSO2和2mol18O2,在T1和T2温度下,SO3的物质的量与时间关系如图所示。请回答下列问题:
2SO3(g) 在容积为2L的密闭容器中进行,初始时向容器里充入4molSO2和2mol18O2,在T1和T2温度下,SO3的物质的量与时间关系如图所示。请回答下列问题:
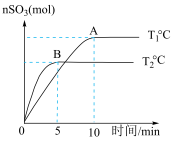
(1)反应后18O原子存在于哪些物质中___ (填化学式)。
(2)上述反应的温度T1___ T2(填“>”“<”或“=”)。
(3)若温度T2时,5min后反应达到平衡,SO2的转化率为90%,则:
①平衡时体系内所含物质总的物质的量为___ 。
②平衡时SO3的浓度为___ 。
③下列说法不正确的是___ 。
A.如在该反应体系中加入适当的催化剂,可加快化学反应速率
B.其它条件相同时,该反应在T1时生成SO3的速率比T2时的小
C.该反应到达平衡时,体系内各组分的体积分数保持不变
D.若密闭容器中混合气体密度不变,则该反应达到化学平衡状态
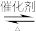 2SO3(g) 在容积为2L的密闭容器中进行,初始时向容器里充入4molSO2和2mol18O2,在T1和T2温度下,SO3的物质的量与时间关系如图所示。请回答下列问题:
2SO3(g) 在容积为2L的密闭容器中进行,初始时向容器里充入4molSO2和2mol18O2,在T1和T2温度下,SO3的物质的量与时间关系如图所示。请回答下列问题:
(1)反应后18O原子存在于哪些物质中
(2)上述反应的温度T1
(3)若温度T2时,5min后反应达到平衡,SO2的转化率为90%,则:
①平衡时体系内所含物质总的物质的量为
②平衡时SO3的浓度为
③下列说法不正确的是
A.如在该反应体系中加入适当的催化剂,可加快化学反应速率
B.其它条件相同时,该反应在T1时生成SO3的速率比T2时的小
C.该反应到达平衡时,体系内各组分的体积分数保持不变
D.若密闭容器中混合气体密度不变,则该反应达到化学平衡状态
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】碘及其化合物在合成杀菌剂、药物、化学研究等方面具有广泛用途。
(1)为了探究FeCl3溶液和KI溶液的反应是否存在一定的限度,取5mL0.5mol·L-1 KI溶液,向其中加入0.1 mol·L-1FeCl3溶液1 mL,充分反应。下列实验操作能验证该反应是否存在限度的是___ 。
A.再滴加AgNO3溶液,观察是否有黄色沉淀产生
B.再加入CCl4振荡后,观察下层液体颜色是否变为紫红色
C.再加入CCl4振荡后,取上层清液,滴加AgNO3溶液,观察是否有白色沉淀产生
D.再加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察溶液是否变成血红色
(2)已知1molH2(g)、1molI2(g)、1molHI(g)分子中化学键断裂时分别需要吸收436kJ、151kJ、 300kJ的能量,则氢气和碘蒸气反应生成HI气体的热化学方程式为_____ 。
(3)Bodensteins研究了下列反应:2HI(g) H2(g) +I2(g),在716K,容积固定为2L的密闭容器中,气体混合物中碘化氢的物质的量n(HI)与反应时间t的关系如下表:
H2(g) +I2(g),在716K,容积固定为2L的密闭容器中,气体混合物中碘化氢的物质的量n(HI)与反应时间t的关系如下表:
0min到20min HI的平均反应速率为_______ ;
反应到达40min时,剩余HI 的物质的量____ 0.82mol(填“﹥” “﹤”或“=”)。
(1)为了探究FeCl3溶液和KI溶液的反应是否存在一定的限度,取5mL0.5mol·L-1 KI溶液,向其中加入0.1 mol·L-1FeCl3溶液1 mL,充分反应。下列实验操作能验证该反应是否存在限度的是
A.再滴加AgNO3溶液,观察是否有黄色沉淀产生
B.再加入CCl4振荡后,观察下层液体颜色是否变为紫红色
C.再加入CCl4振荡后,取上层清液,滴加AgNO3溶液,观察是否有白色沉淀产生
D.再加入CCl4振荡后,取上层清液,滴加KSCN溶液,观察溶液是否变成血红色
(2)已知1molH2(g)、1molI2(g)、1molHI(g)分子中化学键断裂时分别需要吸收436kJ、151kJ、 300kJ的能量,则氢气和碘蒸气反应生成HI气体的热化学方程式为
(3)Bodensteins研究了下列反应:2HI(g)
 H2(g) +I2(g),在716K,容积固定为2L的密闭容器中,气体混合物中碘化氢的物质的量n(HI)与反应时间t的关系如下表:
H2(g) +I2(g),在716K,容积固定为2L的密闭容器中,气体混合物中碘化氢的物质的量n(HI)与反应时间t的关系如下表:| t/min | 0 | 20 | 40 |
| n(HI) | 1 | 0.91 | n |
反应到达40min时,剩余HI 的物质的量
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率。请回答下列问题。
(1)工业合成氨反应 是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂,已知
是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂,已知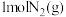 完全反应生成
完全反应生成 可放出92kJ热量。如果将
可放出92kJ热量。如果将 和足量
和足量 混合,使其充分反应,放出的热量
混合,使其充分反应,放出的热量_______ (填“大于”“小于”或“等于”)920kJ。
(2)实验室模拟工业合成氨时,在容积为2L的密闭容器内,反应经过10min后,生成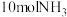 。
。
①反应过程中形成的化学键是_______ (填写“离子键”或“共价键”)。
②一定条件下,能说明该反应进行到最大限度的是_______ (填字母)。
a. 的转化率达到最大值
的转化率达到最大值
b. 、
、 和
和 的体积分数之比为1:3:2
的体积分数之比为1:3:2
c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
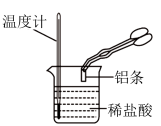
(3)某实验小组同学进行如图所示实验,以检验化学反应中的能量变化,请根据你掌握的反应原理判断,反应后溶液的温度_______ (填“升高”或“降低”),反应物的能量_______ 产物的能量(填写“高于”、“低于”)。
(4)用 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:
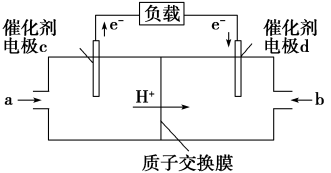
①则电极d是_______ (填“正根”或“负极”),电极c的电极反应式为_______ 。
②若线路中转移 电子,则该燃料电池理论上消耗的
电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为_______ L。
(1)工业合成氨反应
 是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂,已知
是放热的可逆反应,反应条件是高温、高压,并且需要合适的催化剂,已知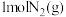 完全反应生成
完全反应生成 可放出92kJ热量。如果将
可放出92kJ热量。如果将 和足量
和足量 混合,使其充分反应,放出的热量
混合,使其充分反应,放出的热量(2)实验室模拟工业合成氨时,在容积为2L的密闭容器内,反应经过10min后,生成
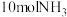 。
。①反应过程中形成的化学键是
②一定条件下,能说明该反应进行到最大限度的是
a.
 的转化率达到最大值
的转化率达到最大值b.
 、
、 和
和 的体积分数之比为1:3:2
的体积分数之比为1:3:2c.体系内气体的密度保持不变
d.体系内物质的平均相对分子质量保持不变
(3)某实验小组同学进行如图所示实验,以检验化学反应中的能量变化,请根据你掌握的反应原理判断,反应后溶液的温度

(4)用
 和
和 组合形成的质子交换膜燃料电池的结构如图:
组合形成的质子交换膜燃料电池的结构如图:
①则电极d是
②若线路中转移
 电子,则该燃料电池理论上消耗的
电子,则该燃料电池理论上消耗的 在标准状况下的体积为
在标准状况下的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】一定温度下,在容积为2L的密闭容器中进行反应:aN(g) bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
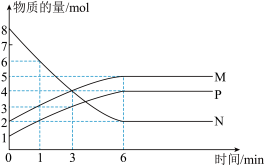
(1)反应化学方程式中各物质的系数比为a:b:c=______ 。
(2)1min到3min这段时刻,以M的浓度变化表示的平均反应速率为:_____ 。
(3)下列叙述中能说明上述反应达到平衡状态的是______ 。
A.反应中当M与N的物质的量相等时
B.P的质量不随时间变化而变化
C.混合气体的总物质的量不随时间变化而变化
D.单位时间内每消耗amolN,同时消耗bmolM
E.混合气体的压强不随时间的变化而变化
F.M的物质的量浓度保持不变
 bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
bM(g)+cP(g),M、N、P的物质的量随时间变化的曲线如图所示:
(1)反应化学方程式中各物质的系数比为a:b:c=
(2)1min到3min这段时刻,以M的浓度变化表示的平均反应速率为:
(3)下列叙述中能说明上述反应达到平衡状态的是
A.反应中当M与N的物质的量相等时
B.P的质量不随时间变化而变化
C.混合气体的总物质的量不随时间变化而变化
D.单位时间内每消耗amolN,同时消耗bmolM
E.混合气体的压强不随时间的变化而变化
F.M的物质的量浓度保持不变
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】如图表示在一定的温度下,容积固定的密闭容器中,A、B、C三种气体的物质的量浓度随时间变化的情况。

试回答下列问题:
(1)该反应的化学方程式为________ 。
(2)0~t1s内气体B的平均反应速率为________ 。
(3)(t1+10)s时,B的物质的量分数为______ ,此时v正(A)_____ v逆(B)(填“>”“<”或“=”),D点是否处于平衡状态_________ (填“是”或“否”)。
(4)下列关于该反应的说法正确的是________ (填序号)。
a.到达t1时刻该反应已停止
b.在t1时刻之前,气体B的消耗速率大于它的生成速率
c.在t1时刻,气体C的正反应速率等于逆反应速率
(5)容器中(t1+10)s时的压强与起始时的压强之比为____ 。

试回答下列问题:
(1)该反应的化学方程式为
(2)0~t1s内气体B的平均反应速率为
(3)(t1+10)s时,B的物质的量分数为
(4)下列关于该反应的说法正确的是
a.到达t1时刻该反应已停止
b.在t1时刻之前,气体B的消耗速率大于它的生成速率
c.在t1时刻,气体C的正反应速率等于逆反应速率
(5)容器中(t1+10)s时的压强与起始时的压强之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】298 K时,将20 mL 3x mol·L−1 Na3AsO3、20 mL 3x mol·L−1 I2和20 mL NaOH溶液混合,发生反应: (aq)+I2(aq)+2OH−(aq)
(aq)+I2(aq)+2OH−(aq)
 (aq)+2I−(aq)+ H2O(l)。溶液中c(
(aq)+2I−(aq)+ H2O(l)。溶液中c( )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
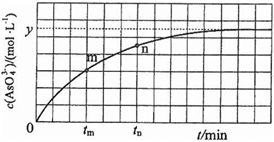
①下列可判断反应达到平衡的是__________ (填标号)。
a.溶液的pH不再变化
b.v(I−)=2v( )
)
c.c( )/c(
)/c( )不再变化
)不再变化
d.c(I−)=y mol·L−1
②tm时,v正_____ v逆(填“大于”“小于”或“等于”)。
 (aq)+I2(aq)+2OH−(aq)
(aq)+I2(aq)+2OH−(aq)
 (aq)+2I−(aq)+ H2O(l)。溶液中c(
(aq)+2I−(aq)+ H2O(l)。溶液中c( )与反应时间(t)的关系如图所示。
)与反应时间(t)的关系如图所示。
①下列可判断反应达到平衡的是
a.溶液的pH不再变化
b.v(I−)=2v(
 )
)c.c(
 )/c(
)/c( )不再变化
)不再变化d.c(I−)=y mol·L−1
②tm时,v正
您最近一年使用:0次



