回答下列问题:
(1)羰基硫( )与
)与 的结构相似,羰基硫(
的结构相似,羰基硫( )分子的结构式为
)分子的结构式为________ ;
(2) 中
中 的空间结构呈
的空间结构呈________ ,与 空间结构相同的一种阴离子的化学式
空间结构相同的一种阴离子的化学式________ 。
(3) 是储氢材料,其由
是储氢材料,其由 和
和 (H为-1价)构成,
(H为-1价)构成, 中心原子B杂化轨道方式为
中心原子B杂化轨道方式为________ 。 中不存在的作用力有
中不存在的作用力有________ 。
A.离子键 B.极性共价键 C.非极性共价键 D.分子间作用力
(4)已知双键成键电子对之间的排斥作用大于单键成键电子对之间的排斥作用, 分子结构如图
分子结构如图 所示,键角大小关系为:
所示,键角大小关系为:
________  (填“>”或“<”)。
(填“>”或“<”)。
(1)羰基硫(
 )与
)与 的结构相似,羰基硫(
的结构相似,羰基硫( )分子的结构式为
)分子的结构式为(2)
 中
中 的空间结构呈
的空间结构呈 空间结构相同的一种阴离子的化学式
空间结构相同的一种阴离子的化学式(3)
 是储氢材料,其由
是储氢材料,其由 和
和 (H为-1价)构成,
(H为-1价)构成, 中心原子B杂化轨道方式为
中心原子B杂化轨道方式为 中不存在的作用力有
中不存在的作用力有A.离子键 B.极性共价键 C.非极性共价键 D.分子间作用力
(4)已知双键成键电子对之间的排斥作用大于单键成键电子对之间的排斥作用,
 分子结构如图
分子结构如图 所示,键角大小关系为:
所示,键角大小关系为:
 (填“>”或“<”)。
(填“>”或“<”)。
更新时间:2024-04-15 17:03:30
|
相似题推荐
【推荐1】金属氢化物是具有良好发展前景的储氢材料。
(1)LiH中,离子半径:Li+_________ H-(填“>”、“=”或“<”)。
(2)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
M是_________ (填元素符号)。
(3)CH4、NH3、H2O、BCl3、HF分子中键角大小顺序是_____ 。
(4)有以下物质:①H2O,②NaOH,③H2O2,④H2,⑤C2H4,⑥Ar,⑦Na2O2,⑧HCN,既有σ键又有π键的是_____________________ ;只含有σ键的是__________ ;含有由两个原子的s轨道重叠形成的σ键的是________ ;不存在化学键的是________ ;含有离子键和非极性键的是_________ 。
(1)LiH中,离子半径:Li+
(2)某储氢材料是短周期金属元素M的氢化物。M的部分电离能如下表所示:
| I1/kJ·mol-1 | I2/kJ·mol-1 | I3/kJ·mol-1 | I4/kJ·mol-1 | I5/kJ·mol-1 |
| 738 | 1451 | 7733 | 10540 | 13630 |
M是
(3)CH4、NH3、H2O、BCl3、HF分子中键角大小顺序是
(4)有以下物质:①H2O,②NaOH,③H2O2,④H2,⑤C2H4,⑥Ar,⑦Na2O2,⑧HCN,既有σ键又有π键的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】①NH3的键角___________ PH3的键角,原因是___________ 。
②NF3的键角___________ NH3的键角,理由是___________ 。
②NF3的键角
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在极性分子中,正电荷重心同负电荷重心间的距离称偶极长,通常用d表示。极性分子的极性强弱同偶极长和正(或负)电荷重心的电量(q)有关,一般用偶极距(μ)来衡量。分子的偶极矩定义为偶极长和偶极上一端电荷电量的乘积,即μ=d·q。试回答以下问题:
(1)HCl、CS2、H2S、SO2四种分子中μ=0的是____ 。
(2)对硝基氯苯、邻硝基氯苯、间硝基氯苯,三种分子的偶极矩由大到小的排列顺序是________ 。
(3)实验测得:μ(PF3)=1.03德拜;μ(BCl3)=0。由此可知,PF3分子是____ 构型,BCl3分子是____ 构型。
(4)冶癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上。已知该化合物有两种异构体。棕黄色者μ>0,淡黄色者μ=0。试画出两种异形体的构型图。
构型图:淡黄色____________________ ,棕黄色____________________ 。
(1)HCl、CS2、H2S、SO2四种分子中μ=0的是
(2)对硝基氯苯、邻硝基氯苯、间硝基氯苯,三种分子的偶极矩由大到小的排列顺序是
(3)实验测得:μ(PF3)=1.03德拜;μ(BCl3)=0。由此可知,PF3分子是
(4)冶癌药Pt(NH3)2Cl2具有平面四边形结构,Pt处在四边形中心,NH3和Cl分别处在四边形的4个角上。已知该化合物有两种异构体。棕黄色者μ>0,淡黄色者μ=0。试画出两种异形体的构型图。
构型图:淡黄色
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)仅由第二周期元素组成的共价分子中,互为等电子体的是:_______ 和_____ ;_____ 和______ 。
(2)HF的沸点比HCl的高,原因是____ ;SiH4的沸点比CH4的高,原因是________ 。
(3)在下列物质①P4 ②NH3 ③HCN ④BF3 ⑤H2O ⑥SO3 ⑦CH3Cl中,属于含有极性键的极性分子的是(填序号)_______ 。
(4)根据价层电子对互斥理论判断下列问题:
CO2分子中,中心原子的杂化方式为__ 杂化,分子的立体构型为________ 。
SO32-中,中心原子的杂化方式为__ 杂化,离子的立体构型为_________ 。
HCHO分子中,中心原子的杂化方式为__ 杂化,分子的立体构型为_________ 。
(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):
HClO4_____ HClO2 H2CO3______ H2SiO3 H2SO3_______ H2SO4
(2)HF的沸点比HCl的高,原因是
(3)在下列物质①P4 ②NH3 ③HCN ④BF3 ⑤H2O ⑥SO3 ⑦CH3Cl中,属于含有极性键的极性分子的是(填序号)
(4)根据价层电子对互斥理论判断下列问题:
CO2分子中,中心原子的杂化方式为
SO32-中,中心原子的杂化方式为
HCHO分子中,中心原子的杂化方式为
(5)试比较下列含氧酸的酸性强弱(填“>”、“<”或“=”):
HClO4
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】I、钙和铜合金可用作电解制钙的阴极电极材料,CaCO3高温分解可制得CaO。CaO与C在一定条件下可生成电石(CaC2),电石与水反应生成Ca(OH)2和一种4原子气体分子。
(1)写出电石与水反应的化学方程式___________ ;反应制得的气体中通常会含有硫化氢等杂质气体,可用___________ 吸收。
(2)CaCO3中阴离子的空间构型为___________ 。
(3)该气体分子中σ键与π键的数目之比为___________ 。
(4)写出2种与 互为等电子体的分子的化学式
互为等电子体的分子的化学式___________ 。
(5)在碱性溶液中,缩二脲HN(CONH2)2与CuSO4反应得到一种特征紫色物质,其结构如图所示,该反应原理可用于检验蛋白质或其他含键的化合物。缩二脲分子中碳原子与氮原子的杂化类型分别为___________ 、___________ 。

Ⅱ.自然界中不存在氟的单质,得到单质氟的过程中,不少科学家为此献出了宝贵的生命。1886年,法国化学家莫瓦桑发明了莫氏电炉,用电解法成功地制取了单质氟,因此荣获1906年诺贝尔化学奖,氟及其化合物在生产及生活中有着广泛的用途。请回答下列问题:
(6)氟气可以用于制取情性强于 的保护气
的保护气 ,也可以用于制取聚合反应的催化剂
,也可以用于制取聚合反应的催化剂 ,
, 可以作为工业制取硅单质的中间物质(
可以作为工业制取硅单质的中间物质( )的原料。
)的原料。
① 分子的空间结构为
分子的空间结构为___________ 。
②S、P、 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为___________ 。
(7)工业上电解 制取单质铝,常利用冰晶石
制取单质铝,常利用冰晶石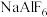 降低
降低 的熔点。
的熔点。 、
、 、F的电负性由小到大的顺序为
、F的电负性由小到大的顺序为___________ ,工业上不用电解 制取铝的原因为
制取铝的原因为___________ 。
(1)写出电石与水反应的化学方程式
(2)CaCO3中阴离子的空间构型为
(3)该气体分子中σ键与π键的数目之比为
(4)写出2种与
 互为等电子体的分子的化学式
互为等电子体的分子的化学式(5)在碱性溶液中,缩二脲HN(CONH2)2与CuSO4反应得到一种特征紫色物质,其结构如图所示,该反应原理可用于检验蛋白质或其他含键的化合物。缩二脲分子中碳原子与氮原子的杂化类型分别为

Ⅱ.自然界中不存在氟的单质,得到单质氟的过程中,不少科学家为此献出了宝贵的生命。1886年,法国化学家莫瓦桑发明了莫氏电炉,用电解法成功地制取了单质氟,因此荣获1906年诺贝尔化学奖,氟及其化合物在生产及生活中有着广泛的用途。请回答下列问题:
(6)氟气可以用于制取情性强于
 的保护气
的保护气 ,也可以用于制取聚合反应的催化剂
,也可以用于制取聚合反应的催化剂 ,
, 可以作为工业制取硅单质的中间物质(
可以作为工业制取硅单质的中间物质( )的原料。
)的原料。①
 分子的空间结构为
分子的空间结构为②S、P、
 的第一电离能由大到小的顺序为
的第一电离能由大到小的顺序为(7)工业上电解
 制取单质铝,常利用冰晶石
制取单质铝,常利用冰晶石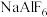 降低
降低 的熔点。
的熔点。 、
、 、F的电负性由小到大的顺序为
、F的电负性由小到大的顺序为 制取铝的原因为
制取铝的原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】铜的化合物用途非常广泛。已知下列反应:[Cu(NH3)2]++NH3+CO [Cu(NH3)3CO]+,2CH3COOH+2CH2=CH2+O2
[Cu(NH3)3CO]+,2CH3COOH+2CH2=CH2+O2 2CH3COOCH=CH2+2H2O。
2CH3COOCH=CH2+2H2O。
(1)Cu2+基态核外电子排布式为_______ 。H2O中中心原子上的孤电子对数为_______ 。
(2)NH3分子的空间结构为_______ ,其中心原子的杂化类型是_______ 。
(3)CH3COOCH=CH2分子中碳原子的杂化类型是_______ ,1 mol CH3COOCH=CH2中含σ键的数目为_______ 。
(4)相同条件下,CO2与SO2在水中的溶解度较大的是_______ (填分子式), 中的O-C-O键角
中的O-C-O键角_______ (填“>”“<”或“=”)  中的O-S-O键角。
中的O-S-O键角。
 [Cu(NH3)3CO]+,2CH3COOH+2CH2=CH2+O2
[Cu(NH3)3CO]+,2CH3COOH+2CH2=CH2+O2 2CH3COOCH=CH2+2H2O。
2CH3COOCH=CH2+2H2O。(1)Cu2+基态核外电子排布式为
(2)NH3分子的空间结构为
(3)CH3COOCH=CH2分子中碳原子的杂化类型是
(4)相同条件下,CO2与SO2在水中的溶解度较大的是
 中的O-C-O键角
中的O-C-O键角 中的O-S-O键角。
中的O-S-O键角。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】 有电极化特性、非磁绝缘性、光致发光性等多种优异性能。回答下类问题:
有电极化特性、非磁绝缘性、光致发光性等多种优异性能。回答下类问题:
(1) 、
、 、
、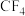 的键角由大到小的顺序为
的键角由大到小的顺序为_______ ;C、N、O、F的第一电离能由大到小的顺序为_______ 。
(2)碱金属离子镶入适合的冠醚空腔可形成特殊材料,两种冠醚结构如图所示。

①冠醚中O原子的杂化形式为_______ ;H、C、O的电负性由小到大的顺序为_______ 。
②K+不能镶入甲中而易镶入乙中的原因为_______ 。
 有电极化特性、非磁绝缘性、光致发光性等多种优异性能。回答下类问题:
有电极化特性、非磁绝缘性、光致发光性等多种优异性能。回答下类问题:(1)
 、
、 、
、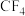 的键角由大到小的顺序为
的键角由大到小的顺序为(2)碱金属离子镶入适合的冠醚空腔可形成特殊材料,两种冠醚结构如图所示。

①冠醚中O原子的杂化形式为
②K+不能镶入甲中而易镶入乙中的原因为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)NH3分子的立体结构为________ ,H2O分子的立体结构为________ .
(2)碳原子有4个价电子,在形成化合物时价电子均参与成键,但杂化方式不一定相同。在乙烷、乙烯、乙炔三种分子中,碳原子采取sp2杂化的分子是________ .
(2)碳原子有4个价电子,在形成化合物时价电子均参与成键,但杂化方式不一定相同。在乙烷、乙烯、乙炔三种分子中,碳原子采取sp2杂化的分子是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】三乙酸锰([Mn(CH3COO)3])是一种锰的配合物,在有机合成中有重要的应用价值。CH3COO―为该配合物的配体,其所含元素的电负性最大的是___________ ;FCH2COO-、ClCH2COO-也可作为配体使用,相同条件下,FCH2COO-、ClCH2COO-结合H+的能力较强的是___________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】现有①Na2S、②金刚石、③NH4Cl、④Na2SO4、⑤干冰、⑥碘片六种物质,按下列要求回答:
(1)熔化时不需要破坏化学键的是____________ ,熔化时需要破坏共价键的是____________ ,熔点最高的是____________ ,熔点最低的是_____________ (填序号)。
(2)属于离子化合物的是_______________________ ,只有离子键的物质是____________ ,以分子间作用力结合的物质是____________________ (均填序号),③的电子式____________________ 。
(3)用电子式表示①的形成过程是______________________ ,用电子式表示⑥的形成过程是_______________________ 。
(1)熔化时不需要破坏化学键的是
(2)属于离子化合物的是
(3)用电子式表示①的形成过程是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】2019年12月17日,经中央军委批准,中国第一艘国产航母命名为“中国人民解放军海军山东舰”,舷号为“17”。2020年9月24日下午,国防部举行例行记者会,国防部新闻局副局长、国防部新闻发言人谭克非大校称:中国海军山东舰已完成例行训练和海上试验。
(1)航母用钢可由低硅生铁冶炼而成,则晶体硅、金刚石、碳化硅的熔点由高到低的顺序为___ ,原因:___ 。
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是___ 。
(3)航母螺旋桨主要用铜合金制造。含铜废液可以利用铜萃取剂M,通过如图反应实现铜离子的富集,进行回收。
Cu2++2 →
→ +2H+
+2H+
①上述物质M中含有的作用力有___ 。
A.离子键B.金属键C.共价键D.氢键E.配位键
②X难溶于水、易溶于有机溶剂,则X晶体中铜元素与氮原子之间的共价键类型为___ 。
(1)航母用钢可由低硅生铁冶炼而成,则晶体硅、金刚石、碳化硅的熔点由高到低的顺序为
(2)Ti的四卤化物熔点如表所示,TiF4熔点高于其他三种卤化物,自TiCl4至TiI4熔点依次升高,原因是
| 化合物 | TiF4 | TiCl4 | TiBr4 | TiI4 |
| 熔点/℃ | 377 | -24.12 | 38.3 | 155 |
(3)航母螺旋桨主要用铜合金制造。含铜废液可以利用铜萃取剂M,通过如图反应实现铜离子的富集,进行回收。
Cu2++2
 →
→ +2H+
+2H+①上述物质M中含有的作用力有
A.离子键B.金属键C.共价键D.氢键E.配位键
②X难溶于水、易溶于有机溶剂,则X晶体中铜元素与氮原子之间的共价键类型为
您最近一年使用:0次




