X、Y、Z、W是4种原子序数依次增大的短周期主族元素。其中Y和Z的价层电子数相同,Y原子的s能级与p能级填充的电子数相等。四种元素形成如图所示两种化合物,它们均能水解生成对应的酸和氧化物。下列说法错误的是
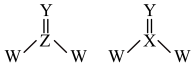
A.X的核外电子排布式为 |
B. 的空间构型为平面三角形 的空间构型为平面三角形 |
C.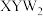 的中心原子采取 的中心原子采取 杂化 杂化 |
D.2种化合物水解得到氧化物分别为 和 和 |
更新时间:2024-04-21 08:54:22
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子的核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。则下列说法不正确的是
| A.W位于元素周期表第三周期第ⅤA族 |
| B.Z的简单离子与W的氢化物形成的配合离子中,W原子提供孤对电子 |
| C.X、Y形成的化合物X2Y3在水中会发生双水解 |
| D.Y的基态原子的核外电子排布式:1s22s22p63s23p4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列微粒组成与结构的化学用语表达正确的是
A.基态 原子的价电子排布式: 原子的价电子排布式: |
B.基态 原子的价电子轨道表示式: 原子的价电子轨道表示式: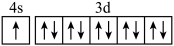 |
C. 的电子式: 的电子式: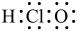 |
D.镁离子的结构示意图: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】X、Y、Z、M四种元素原子序数依次增大。X核外未成对电子数为3,Z是周期表中电负性最大的元素,M是地壳中含量最多的金属元素。下列说法不正确的是
| A.简单氢化物的沸点:Z>Y | B.第一电离能:X>Y |
| C.简单离子半径:Y>M | D. 分子空间构型为三角锥形 分子空间构型为三角锥形 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列推测不合理 的是
A. 和足量 和足量 反应可以生成两种盐 反应可以生成两种盐 |
| B.卤素与磷单质反应可得到五卤化物,其热稳定性随卤素原子序数的递增而减弱 |
C.由实验测得 中含有正四面体的阳离子和正八面体的阴离子,则 中含有正四面体的阳离子和正八面体的阴离子,则 中存在 中存在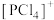 和 和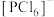 |
D. 与 与 反应比 反应比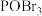 与 与 反应更难 反应更难 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】冠醚是一种超分子,它能否适配碱金属离子与其空腔直径和离子直径有关。二苯并-18-冠-6与 形成的螯合离子的结构如图所示。下列说法错误的是
形成的螯合离子的结构如图所示。下列说法错误的是
 形成的螯合离子的结构如图所示。下列说法错误的是
形成的螯合离子的结构如图所示。下列说法错误的是
| A.该螯合离子所形成的物质是离子晶体,晶体中存在离子键、极性键、非极性键。 |
| B.该螯合离子有4种一氯代物,中心离子的配位数为6 |
| C.该螯合离子有分子识别和自组装的功能 |
D.该螯合离子中C原子杂化方式有2种,6个O原子与 可能在同一平面上 可能在同一平面上 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列化学用语表示或描述不正确 的是
| A.Ca的电子排布式是[Ar]3d2 |
| B.BF3 的VSEPR的模型名称是平面三角形 |
| C.NH4+中心原子N上的孤电子对数为0 |
| D.在[Cu(NH3)4]2+里,NH3的氮原子给出孤电子对,形成配位键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】下列说法正确的
① 分子中P原子采用的轨道杂化方式为
分子中P原子采用的轨道杂化方式为
② 分子中只有以s轨道与
分子中只有以s轨道与 杂化轨道“头碰头”方式重叠而成的
杂化轨道“头碰头”方式重叠而成的 键
键
③ 的熔点高于
的熔点高于 的熔点
的熔点
④ 中
中 键角比
键角比 中
中 键角大
键角大
⑤ 比
比 稳定是由于
稳定是由于 分子之间存在氢键
分子之间存在氢键
①
 分子中P原子采用的轨道杂化方式为
分子中P原子采用的轨道杂化方式为
②
 分子中只有以s轨道与
分子中只有以s轨道与 杂化轨道“头碰头”方式重叠而成的
杂化轨道“头碰头”方式重叠而成的 键
键③
 的熔点高于
的熔点高于 的熔点
的熔点④
 中
中 键角比
键角比 中
中 键角大
键角大⑤
 比
比 稳定是由于
稳定是由于 分子之间存在氢键
分子之间存在氢键| A.①② | B.③④⑤ | C.①②③ | D.①③④ |
您最近一年使用:0次

 的沸点较低
的沸点较低 可发生反应:
可发生反应:
 与
与
 的电负性较大,使双键电子云向中心碳原子偏移;
的电负性较大,使双键电子云向中心碳原子偏移; 和
和


