钽(Ta)和铌(Nb)的性质相似,因此常常共生于自然界的矿物中。一种以钽铌伴生矿(主要成分为SiO2、MnO2、Nb2O5、Ta2O5和少量的TiO2、FeO、CaO、MgO)为原料制取钽和铌的流程如下:
已知:①MIBK为甲基异丁基酮;
②KspCaF2=2.510-11,KspMgF2=6.410-9
(1)“浸取”时通常在_____材料的反应器中进行(填标号)。
(2)浸渣的主要成分是_____ ,Ta2O5与氢氟酸反应的离子方程式为_____ 。
(3)“浸取”时,HF的浓度对铌、钽的浸出率的影响如下图所示,则HF的最佳浓度为_____ 。
①流程中钠热还原法制备铌粉的化学方程式为_____ 。
②传统的熔盐电解法采用的电解质体系通常为K2NbF7-NaCl,电解总化学反应方程式为_____ 。
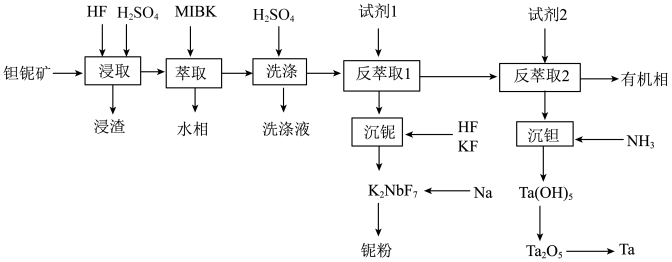
已知:①MIBK为甲基异丁基酮;
②KspCaF2=2.510-11,KspMgF2=6.410-9
(1)“浸取”时通常在_____材料的反应器中进行(填标号)。
| A.陶瓷 | B.玻璃 | C.铅 | D.塑料 |
(2)浸渣的主要成分是
(3)“浸取”时,HF的浓度对铌、钽的浸出率的影响如下图所示,则HF的最佳浓度为

①流程中钠热还原法制备铌粉的化学方程式为
②传统的熔盐电解法采用的电解质体系通常为K2NbF7-NaCl,电解总化学反应方程式为
更新时间:2024-04-23 10:38:46
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】有一包白色固体样品,可能含碳酸钠、硫酸钠、氯化钠、氢氧化钠中的一种或几种。小科同学为探究其成分做了以下实验:
步骤I:取少量固体样品置于烧杯中,先加足量水溶解,再加入足量的 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。
步骤Ⅱ:继续向烧杯中滴加稀盐酸并不断搅拌,烧杯内固体质量随加入稀盐酸质量的变化如图所示,请回答下列问题:
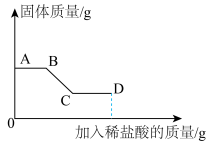
(1)写出AB段的离子方程式___________ 。
(2)BC段观察到的现象是___________ 。
(3)C点时溶液中一定含有的溶质是___________ (填化学式)。
(4)根据以上信息可以确定白色固体样品中一定含有___________ (填化学式)。
(5)设计实验检验D点溶液中主要阴离子___________ 。
步骤I:取少量固体样品置于烧杯中,先加足量水溶解,再加入足量的
 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。步骤Ⅱ:继续向烧杯中滴加稀盐酸并不断搅拌,烧杯内固体质量随加入稀盐酸质量的变化如图所示,请回答下列问题:

(1)写出AB段的离子方程式
(2)BC段观察到的现象是
(3)C点时溶液中一定含有的溶质是
(4)根据以上信息可以确定白色固体样品中一定含有
(5)设计实验检验D点溶液中主要阴离子
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】空气吹出法工艺,是目前“海水提溴”的最主要方法之一、其工艺流程如下:___________ 。
(2)步骤④利用了SO2的还原性,反应的离子方程式:___________ 。
(3)从含溴海水中吹出的溴也可用纯碱吸收,纯碱吸收溴的主要反应是3Na2CO3+3Br2=NaBrO3+5NaBr+3CO2;吸收1 mol Br2时,转移的电子为___________ mol。纯碱吸收后再用硫酸酸化,单质溴又从溶液中析出。

(2)步骤④利用了SO2的还原性,反应的离子方程式:
(3)从含溴海水中吹出的溴也可用纯碱吸收,纯碱吸收溴的主要反应是3Na2CO3+3Br2=NaBrO3+5NaBr+3CO2;吸收1 mol Br2时,转移的电子为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】菱锰矿的主要成分为 ,主要杂质为
,主要杂质为 、
、 、
、 、
、 、
、 。已知
。已知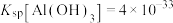 利用菱锰矿制晶体
利用菱锰矿制晶体 的流程如下:
的流程如下:
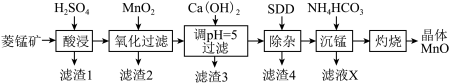
(1)酸浸时含锰组分发生反应的化学方程式为___________ 。
(2)氧化过滤时体系溶液的pH=3,此时发生反应的离子方程式为___________ 。
(3)滤渣3的主要成分为___________ 。
(4)加入沉淀剂SDD是为了除去 生成重金属螯合物沉淀。
生成重金属螯合物沉淀。
①SDD可表示为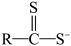 ,中性螯合物沉淀的结构式为
,中性螯合物沉淀的结构式为___________ 。
②若使用Na2S做沉淀剂,除了因体系pH过低会产生H2S外,还会产生絮状无定型沉淀,造成___________ 。
(5)沉锰时发生反应的离子方程式为___________ ;滤液X中含有___________ ,经浓缩结晶可做化肥。
(6)通过 在MnO晶体(正极)中嵌入和脱嵌,实现电极材料充放电的原理如图所示。
在MnO晶体(正极)中嵌入和脱嵌,实现电极材料充放电的原理如图所示。
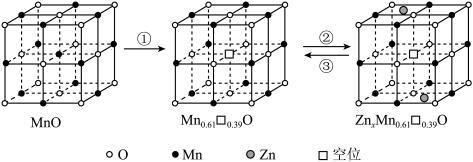
②代表电池___________ (填“充电”或“放电”)过程,该过程的电极反应式为___________ 。
 ,主要杂质为
,主要杂质为 、
、 、
、 、
、 、
、 。已知
。已知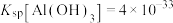 利用菱锰矿制晶体
利用菱锰矿制晶体 的流程如下:
的流程如下:
(1)酸浸时含锰组分发生反应的化学方程式为
(2)氧化过滤时体系溶液的pH=3,此时发生反应的离子方程式为
(3)滤渣3的主要成分为
(4)加入沉淀剂SDD是为了除去
 生成重金属螯合物沉淀。
生成重金属螯合物沉淀。①SDD可表示为
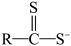 ,中性螯合物沉淀的结构式为
,中性螯合物沉淀的结构式为②若使用Na2S做沉淀剂,除了因体系pH过低会产生H2S外,还会产生絮状无定型沉淀,造成
(5)沉锰时发生反应的离子方程式为
(6)通过
 在MnO晶体(正极)中嵌入和脱嵌,实现电极材料充放电的原理如图所示。
在MnO晶体(正极)中嵌入和脱嵌,实现电极材料充放电的原理如图所示。
②代表电池
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】2020年5月5日晚18时00分,我国载人空间站货物返回舱试验舱在我国文昌航天发射场点火升空, 5月8日飞船试验船返回舱在东风着陆场预定区域成功着陆,试验取得圆满成功。金属铍(Be)是火箭、航空、宇宙航行的重要材料,工业上以含铍废渣(主要成分是Be和MgF2)为原料制备金属铍的工艺流程如图:

已知:MgF2和CaF2难溶于水。回答下列问题:
(1)提高浸出速率的方法有________ 、_______ (任写两项);已知滤液Ⅰ中铍元素的存在形式为H2BeF4,写出“浸出”过程中发生反应的化学方程式:____________ 。
(2)过滤所得滤渣I的主要成分为________ (填化学式)。
(3)该流程中可循环利用的物质是____________________ ;滤渣Ⅱ与浓硫酸发生反应的化学方程式为__________________________________________________ ;已知(NH4)2BeF4易溶于水,且其在水中的溶解度随温度的升高而大幅度增大,从NH4F与滤液Ⅱ发生反应后所得溶液中获得(NH4)2BeF4晶体的“一系列操作”具体是指____________________ 过滤、洗涤、干燥。
(4) “分解”过程中产生的BeF2在熔融状态下不能导电,其电子式为_____________ ;“还原”过程可以用金属镁制备金属铍的原因是__________________________ 。

已知:MgF2和CaF2难溶于水。回答下列问题:
(1)提高浸出速率的方法有
(2)过滤所得滤渣I的主要成分为
(3)该流程中可循环利用的物质是
(4) “分解”过程中产生的BeF2在熔融状态下不能导电,其电子式为
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】草酸与草酸钠在生产、科研中应用广泛。
(1)草酸(H2C2O4)又名乙二酸,为无色透明晶体,是二元有机酸,是化学分析中常用的还原剂,也是一种重要的有机化工原料。
某小组同学通过查阅文献资料得知:用Hg(NO3)2作催化剂时,浓硝酸氧化乙炔制取H2C2O4,实验装置如下图所示:
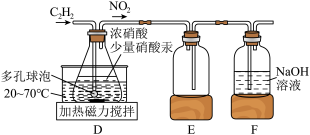
①装置D不能用明火加热的原因是___________ 。
②写出装置D中制备H2C2O4的化学方程式___________ 。
③下列实验设计不能证明草酸是弱酸的是________________ 。
A.室温下,用pH计测定0.1mol•L-1H2C2O4水溶液pH,pH=1.3
B.室温下,取pH广泛试纸测定Na2C2O4溶液pH,pH>7
C.室温下,取pH=1的H2C2O4溶液稀释100倍后,测其pH<3
D.标准状况下,取0.10mol∙L-1的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL
(2)草酸钠(Na2C2O4)为白色结晶性粉末,是一种还原剂,也常作为双齿配体,可以被酸性高锰酸钾溶液氧化。某小组利用配制的草酸钠溶液测定高锰酸钾(M=158g/mol)产品纯度,步骤如下:
I.称取4.0g高锰酸钾产品,配成100mL溶液。
Ⅱ.准确量取0.10mol/LNa2C2O4溶液100mL,置于锥形瓶中
Ⅲ .将瓶中溶液加热到75~80℃,再加入少量硫酸酸化,趁热用I中配制的高锰酸钾溶液滴定,滴定终点消耗高锰酸钾溶液20.00mL。
①步骤I中用到的玻璃仪器除了小烧杯、玻璃棒、胶头滴管外,还有___________ 。
②滴定过程中反应的离子方程式为___________ 。
③在室温下,该反应的速率缓慢,因此常将溶液加热至343~358K进行滴定。但温度不宜过高,加热温度高于363K,会使部分H2C2O4发生分解,会导致测得的高锰酸钾产品纯度___________ 。(填“偏高”、“偏低”或“无影响”)
④实验测得高锰酸钾的纯度为___________ 。
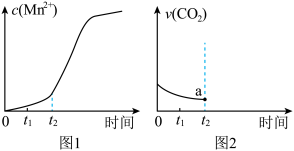
⑤若该实验中测得反应液中Mn2+的浓度随反应时间t的变化如图1所示,结合图1信息,请在图2画出t2后生成CO2的速率图像___________ (从a点开始作图)。
(1)草酸(H2C2O4)又名乙二酸,为无色透明晶体,是二元有机酸,是化学分析中常用的还原剂,也是一种重要的有机化工原料。
某小组同学通过查阅文献资料得知:用Hg(NO3)2作催化剂时,浓硝酸氧化乙炔制取H2C2O4,实验装置如下图所示:

①装置D不能用明火加热的原因是
②写出装置D中制备H2C2O4的化学方程式
③下列实验设计不能证明草酸是弱酸的是
A.室温下,用pH计测定0.1mol•L-1H2C2O4水溶液pH,pH=1.3
B.室温下,取pH广泛试纸测定Na2C2O4溶液pH,pH>7
C.室温下,取pH=1的H2C2O4溶液稀释100倍后,测其pH<3
D.标准状况下,取0.10mol∙L-1的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL
(2)草酸钠(Na2C2O4)为白色结晶性粉末,是一种还原剂,也常作为双齿配体,可以被酸性高锰酸钾溶液氧化。某小组利用配制的草酸钠溶液测定高锰酸钾(M=158g/mol)产品纯度,步骤如下:
I.称取4.0g高锰酸钾产品,配成100mL溶液。
Ⅱ.准确量取0.10mol/LNa2C2O4溶液100mL,置于锥形瓶中
Ⅲ .将瓶中溶液加热到75~80℃,再加入少量硫酸酸化,趁热用I中配制的高锰酸钾溶液滴定,滴定终点消耗高锰酸钾溶液20.00mL。
①步骤I中用到的玻璃仪器除了小烧杯、玻璃棒、胶头滴管外,还有
②滴定过程中反应的离子方程式为
③在室温下,该反应的速率缓慢,因此常将溶液加热至343~358K进行滴定。但温度不宜过高,加热温度高于363K,会使部分H2C2O4发生分解,会导致测得的高锰酸钾产品纯度
④实验测得高锰酸钾的纯度为
⑤若该实验中测得反应液中Mn2+的浓度随反应时间t的变化如图1所示,结合图1信息,请在图2画出t2后生成CO2的速率图像

您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】高铁酸钾(K2FeO4)是一种绿色、高效的水处理剂。实验室设计如下实验制备K2FeO4并探究其性质。
已知:①K2FeO4为暗紫色固体,可溶于水,微溶于KOH溶液。
② 具有强氧化性,在酸性或者中性溶液中能快速产生O2,在碱性溶液中较稳定。回答下列问题:
具有强氧化性,在酸性或者中性溶液中能快速产生O2,在碱性溶液中较稳定。回答下列问题:
(1)制备K2FeO4(夹持装置略)
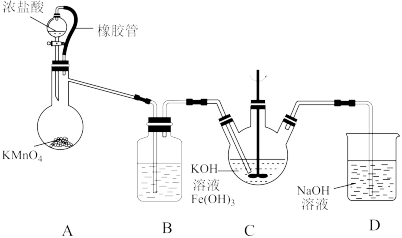
①如图所示,装置A为氯气发生装置,A中盛放KMnO4的仪器名称是__ ,橡胶管的作用是__ 。
②装置B中盛放的溶液是____ 。
③装置C中的KOH溶液需过量,目的是______ 。
④装置C中生成暗紫色固体K2FeO4的化学方程式为____ ,此外,氯气还与过量的KOH溶液反应,反应的离子方程式为____ 。
(2)探究K2FeO4的性质
某同学取装置C中的紫色溶液少许,加入稀硫酸,产生黄绿色气体,经检验气体中含有氯气。该现象________ (填“能”或“不能”)证明“酸性条件下 的氧化性强于Cl2”,理由是
的氧化性强于Cl2”,理由是________ 。
已知:①K2FeO4为暗紫色固体,可溶于水,微溶于KOH溶液。
②
 具有强氧化性,在酸性或者中性溶液中能快速产生O2,在碱性溶液中较稳定。回答下列问题:
具有强氧化性,在酸性或者中性溶液中能快速产生O2,在碱性溶液中较稳定。回答下列问题:(1)制备K2FeO4(夹持装置略)

①如图所示,装置A为氯气发生装置,A中盛放KMnO4的仪器名称是
②装置B中盛放的溶液是
③装置C中的KOH溶液需过量,目的是
④装置C中生成暗紫色固体K2FeO4的化学方程式为
(2)探究K2FeO4的性质
某同学取装置C中的紫色溶液少许,加入稀硫酸,产生黄绿色气体,经检验气体中含有氯气。该现象
 的氧化性强于Cl2”,理由是
的氧化性强于Cl2”,理由是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】一定条件下,通过下列反应可实现燃煤烟气中硫的回收:2CO(g)+SO2(g)=2CO2(g)+S(l)∆H
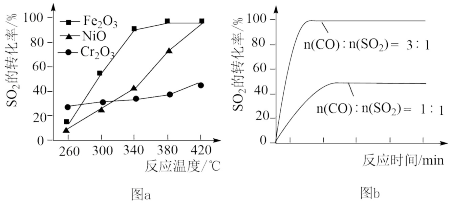
(1)已知:2CO(g)+O2(g)=2CO2(g)∆H1=-566kJ/mol;S(l)+O2(g)=2SO2(g)∆H2=-296kJ/mol,则反应热∆H=___ kJ/mol。
(2)其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图a所示。260℃时__ (填“Fe2O3”、“NiO”或“Cr2O3”)作催化剂反应速率最快。Fe2O3和NiO作催化剂均能使SO2的转化率达到最高,不考虑价格因素,选择Fe2O3的主要优点是___ 。
(3)科研小组在380℃、Fe2O3作催化剂时,研究了不同投料比[n(CO):n(SO2)]对SO2转化率的影响,结果如图b所示。请分析当n(CO):n(SO2)=1:1时,SO2转化率接近50%的原因___ 。
(4)工业上还可用Na2SO3溶液吸收烟气中的SO2:Na2SO3+SO2+H2O=2NaHSO3。某温度下用1.0mol/LNa2SO3溶液吸收纯净的SO2,当溶液中c(SO )降至0.2mol/L时,吸收能力显著下降,应更换吸收剂。此时溶液中c(HSO
)降至0.2mol/L时,吸收能力显著下降,应更换吸收剂。此时溶液中c(HSO )约为
)约为___ mol/L,溶液的pH=__ 。(已知该温度下亚硫酸的平衡常数Ka1=1.75×10-2,Ka2=1.25×10-7)
(5)利用硫酸钠溶液吸收SO2,再用惰性电极电解处理SO2。将阴极区溶液导出,经过滤分离出硫磺后,可循环吸收利用,装置如图所示。

阴极的电极反应式为___ 。
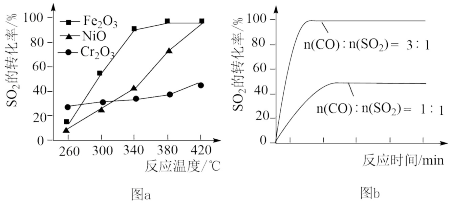
(1)已知:2CO(g)+O2(g)=2CO2(g)∆H1=-566kJ/mol;S(l)+O2(g)=2SO2(g)∆H2=-296kJ/mol,则反应热∆H=
(2)其他条件相同、催化剂不同时,SO2的转化率随反应温度的变化如图a所示。260℃时
(3)科研小组在380℃、Fe2O3作催化剂时,研究了不同投料比[n(CO):n(SO2)]对SO2转化率的影响,结果如图b所示。请分析当n(CO):n(SO2)=1:1时,SO2转化率接近50%的原因
(4)工业上还可用Na2SO3溶液吸收烟气中的SO2:Na2SO3+SO2+H2O=2NaHSO3。某温度下用1.0mol/LNa2SO3溶液吸收纯净的SO2,当溶液中c(SO
 )降至0.2mol/L时,吸收能力显著下降,应更换吸收剂。此时溶液中c(HSO
)降至0.2mol/L时,吸收能力显著下降,应更换吸收剂。此时溶液中c(HSO )约为
)约为(5)利用硫酸钠溶液吸收SO2,再用惰性电极电解处理SO2。将阴极区溶液导出,经过滤分离出硫磺后,可循环吸收利用,装置如图所示。

阴极的电极反应式为
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氮的氧化物和氮的氢化物的任意排放均会对环境造成污染,因此关于其转化的研究对于消除环境污染有着重要意义。
(1)已知T℃时,有如下反应:
反应I:4NH3g+6NOg 5N2g+6H2Og ΔH=a
5N2g+6H2Og ΔH=a
反应II:N2g+2O2g 2NO2g)ΔH=b
2NO2g)ΔH=b
反应III:2NOg+O2g 2NO2g ΔH=c
2NO2g ΔH=c
试写出T℃时,NH3与NO2反应生成不污染环境的物质的热化学反应方程式________ 。
(2)T℃时,向2L密闭容器中加入一定量的NO2、NO和O2,发生(1)中反应III,不同时间测得各物质的部分浓度(molL-1)如下表所示:
①温度不变,反应达平衡后容器中的压强与最初加入气体时的压强之比为________ 。
②反应的前20min的平均反应速率vNO=________ molL-1min-1。
③若温度不变,平衡后将反应容器压缩为1L,达到新的平衡后,cO2________ 0.48molL-1(填“”“”或“”)。
(3)某化学兴趣小组利用电解原理设计实验消除NH3与NO对环境的影响,并制取KOH溶液和H2SO4溶液,其工作原理如下图所示:
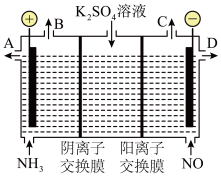
①从出口B、C产生的气体相同,该气体是________ ;从出口D得到的溶液是________ 。
②电解槽左池中发生的电极反应式为________ 。
③电解一段时间,两电极共收集到22.4L气体(标准状况下)时,理论上将生成________ molKOH。
(1)已知T℃时,有如下反应:
反应I:4NH3g+6NOg
 5N2g+6H2Og ΔH=a
5N2g+6H2Og ΔH=a反应II:N2g+2O2g
 2NO2g)ΔH=b
2NO2g)ΔH=b反应III:2NOg+O2g
 2NO2g ΔH=c
2NO2g ΔH=c试写出T℃时,NH3与NO2反应生成不污染环境的物质的热化学反应方程式
(2)T℃时,向2L密闭容器中加入一定量的NO2、NO和O2,发生(1)中反应III,不同时间测得各物质的部分浓度(molL-1)如下表所示:
| 时间(min) | NO | O2 | NO2 |
| 0 | a | 0.30 | 0.10 |
| 10 | 0.14 | 0.27 | b |
| 20 | 0.10 | c | 0.20 |
| 30 | d | 0.24 | 0.22 |
| 40 | 0.08 | e | f |
②反应的前20min的平均反应速率vNO=
③若温度不变,平衡后将反应容器压缩为1L,达到新的平衡后,cO2
(3)某化学兴趣小组利用电解原理设计实验消除NH3与NO对环境的影响,并制取KOH溶液和H2SO4溶液,其工作原理如下图所示:

①从出口B、C产生的气体相同,该气体是
②电解槽左池中发生的电极反应式为
③电解一段时间,两电极共收集到22.4L气体(标准状况下)时,理论上将生成
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】铁是一种在生产和生活中应用很广泛的金属元素,请回答下列钢铁腐蚀和防护的相关问题。
(1)已知:
反应Ⅰ:Fe2O3(s)+3H2(g)═2Fe(s)+3H2O(g)ΔH1═+89.6kJ·mol−1
反应Ⅱ:4Fe2O3(s)+Fe(s)═3Fe3O4(s)ΔH2═+2833.4kJ·mol−1
反应Ⅲ:Fe3O4(s)+4H2(g)═4H2O(g)+3Fe(s)ΔH3
反应Ⅰ的平衡常数表达式K═__ ,ΔH3═__ 。
(2)在水膜酸性不强的情况下,钢铁在潮湿的空气中腐蚀生锈主要属于__ 腐蚀。(填“吸氧”或“析氢”)
(3)电化学除锈法具有侵蚀能力强,侵蚀速度快等优点。电化学除锈分为阳极除锈和阴极除锈。阳极除锈是利用阳极的电化学溶解和氧气泡析出时对铁锈的机械剥离作用进行除锈;阴极除锈是利用氢气的还原作用和氢气泡析出的机械剥离作用而除锈。如图为一种电化学除锈示意图。
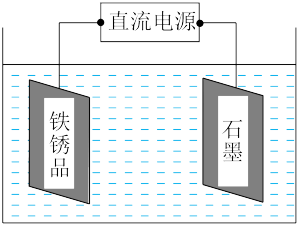
①若采用阳极除锈,以H2SO4(aq)为电解质溶液,则阳极的电极反应式为__ 。
②若采用阴极除锈,以Na2CO3(aq)为电解质溶液,则阴极的电极反应式为___ 。
(4)钢铁工件除锈后,还可采用电镀进行防护,若要在工件上镀上金属铬,应把钢铁工件放在电镀池的___ 极(填“阴”或“阳”)。
(1)已知:
反应Ⅰ:Fe2O3(s)+3H2(g)═2Fe(s)+3H2O(g)ΔH1═+89.6kJ·mol−1
反应Ⅱ:4Fe2O3(s)+Fe(s)═3Fe3O4(s)ΔH2═+2833.4kJ·mol−1
反应Ⅲ:Fe3O4(s)+4H2(g)═4H2O(g)+3Fe(s)ΔH3
反应Ⅰ的平衡常数表达式K═
(2)在水膜酸性不强的情况下,钢铁在潮湿的空气中腐蚀生锈主要属于
(3)电化学除锈法具有侵蚀能力强,侵蚀速度快等优点。电化学除锈分为阳极除锈和阴极除锈。阳极除锈是利用阳极的电化学溶解和氧气泡析出时对铁锈的机械剥离作用进行除锈;阴极除锈是利用氢气的还原作用和氢气泡析出的机械剥离作用而除锈。如图为一种电化学除锈示意图。

①若采用阳极除锈,以H2SO4(aq)为电解质溶液,则阳极的电极反应式为
②若采用阴极除锈,以Na2CO3(aq)为电解质溶液,则阴极的电极反应式为
(4)钢铁工件除锈后,还可采用电镀进行防护,若要在工件上镀上金属铬,应把钢铁工件放在电镀池的
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】以绿晶石(主要成分 )为原料,采用氟化法制备
)为原料,采用氟化法制备 的工业流程如下:
的工业流程如下:
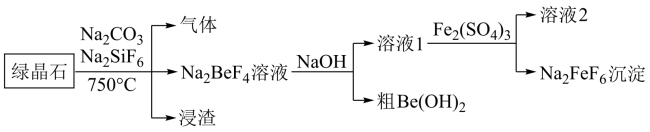
回答下列问题:
(1)绿晶石在750℃下的化学反应方程式为_______ ,烧结块磨细、用冷水多级逆流浸出,目的是_______ 。
(2)溶液1的主要成分是_______ ,溶液2的主要成分是_______ 。
(3)溶液1中加 溶液的目的是
溶液的目的是_______ 。本流程中可重复利用的物质是_______ 。
(4)提纯粗 常用醋酸,将粗
常用醋酸,将粗 溶解醋酸中生成
溶解醋酸中生成 ,在573-673K温度下蒸馏出
,在573-673K温度下蒸馏出 ,然后在873-973K下分解得到
,然后在873-973K下分解得到 。
。
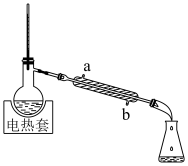
用上述方法提纯可得到高纯 ,原理是
,原理是_______ ,蒸馏装置中冷凝管进水口不能选a的原因是_______ 。
 )为原料,采用氟化法制备
)为原料,采用氟化法制备 的工业流程如下:
的工业流程如下:
回答下列问题:
(1)绿晶石在750℃下的化学反应方程式为
(2)溶液1的主要成分是
(3)溶液1中加
 溶液的目的是
溶液的目的是(4)提纯粗
 常用醋酸,将粗
常用醋酸,将粗 溶解醋酸中生成
溶解醋酸中生成 ,在573-673K温度下蒸馏出
,在573-673K温度下蒸馏出 ,然后在873-973K下分解得到
,然后在873-973K下分解得到 。
。
用上述方法提纯可得到高纯
 ,原理是
,原理是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】铜和锌是重要的工业原料,废旧电池的铜帽中主要含有铜和少量的锌,实验室利用废弃电池铜帽回收Cu并制备纳米ZnO的部分实验过程如图所示:
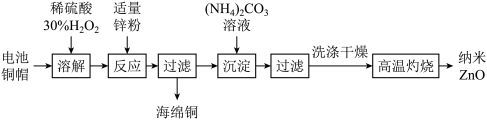
回答下列问题:
(1)在“溶解”过程中,铜溶解所发生反应的离子方程式为______ 。
(2)加入适量锌粉的目的是______ 。
(3)“洗涤干燥”操作中的洗涤方法是______ 。
(4)某同学提出用足量碳酸钠溶液代替(NH4)2CO3溶液,得到其中一种产物是碱式碳酸锌[Zn2(OH)2CO3],其反应的离子方程式为______ 。
(5)Cu-PbO2电池是一种新型电池,电解质为K2SO4、H2SO4和KOH,由两种膜将三种电解质溶液分成A、B、C三个不同的区域,其中a为阳离子交换膜,b为阴离子交换膜,该电池结构如图所示:
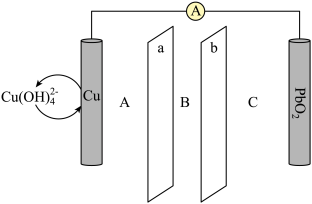
①电池放电过程中PbO2极表面发生的反应为______ 。
②电解质K2SO4溶液在______ 区域(填“A”“B”或“C”)。电池放电后,该区域K2SO4物质的量______ (填“增大”“减小”或“不变”)。

回答下列问题:
(1)在“溶解”过程中,铜溶解所发生反应的离子方程式为
(2)加入适量锌粉的目的是
(3)“洗涤干燥”操作中的洗涤方法是
(4)某同学提出用足量碳酸钠溶液代替(NH4)2CO3溶液,得到其中一种产物是碱式碳酸锌[Zn2(OH)2CO3],其反应的离子方程式为
(5)Cu-PbO2电池是一种新型电池,电解质为K2SO4、H2SO4和KOH,由两种膜将三种电解质溶液分成A、B、C三个不同的区域,其中a为阳离子交换膜,b为阴离子交换膜,该电池结构如图所示:

①电池放电过程中PbO2极表面发生的反应为
②电解质K2SO4溶液在
您最近半年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
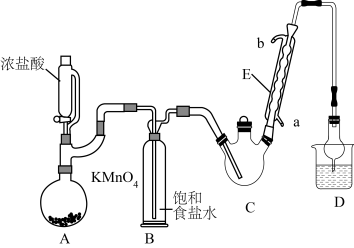
【推荐3】三氯乙醛是生产农药、医药的重要中间体。某化学兴趣小组设计如图所示装置(夹持、加热仪器略),模拟工业生产进行制备三氯乙醛(CCl3CHO)的实验。
查阅资料,有关信息如下:
①制备反应原理:C2H5OH + 4Cl2 → CCl3CHO + 5HCl
可能发生的副反应:C2H5OH + HCl → C2H5Cl + H2O、CCl3CHO + HClO → CCl3COOH + HCl
②相关物质的部分物理性质:
回答下列问题:
(1)仪器E的名称是___________ ,冷凝水的流向是____________ 口进水(填“a”或“b")。
(2)有同学认为应在B、C之间加一干燥装置,理由是_________ 。
(3)装置C应控制反应温度在70℃左右,可采用_______ 加热的方法。
(4)装置D干燥管的作用为导气、________ ,装置D烧杯中的试剂是__________ 。
(5)反应结束后,从C中的混合物中分离出CCl3COOH的方法是____________ (填名称)。

查阅资料,有关信息如下:
①制备反应原理:C2H5OH + 4Cl2 → CCl3CHO + 5HCl
可能发生的副反应:C2H5OH + HCl → C2H5Cl + H2O、CCl3CHO + HClO → CCl3COOH + HCl
②相关物质的部分物理性质:
C2H5OH | CCl3CHO | CCl3COOH | C2H5Cl | |
熔点/℃ | -114.1 | -57.5 | 58 | -138.7 |
沸点/℃ | 78.3 | 97.8 | 198 | 12.3 |
溶解性 | 与水互溶 | 可溶于水、乙醇 | 可溶于水、乙醇、三氯乙醛 | 微溶于水,可溶于乙醇 |
回答下列问题:
(1)仪器E的名称是
(2)有同学认为应在B、C之间加一干燥装置,理由是
(3)装置C应控制反应温度在70℃左右,可采用
(4)装置D干燥管的作用为导气、
(5)反应结束后,从C中的混合物中分离出CCl3COOH的方法是
您最近半年使用:0次



