芯片作为科技产业,以及信息化、数字化的基础,自诞生以来,就一直倍受关注,也一直蓬勃发展。芯片制造会经过六个最为关键的步骤;沉积、光刻胶涂覆、光刻、刻蚀、离子注入和封装。
(1)“沉积”是将导体、绝缘体或半导体材料薄膜沉积到纯硅晶圆上。GaN、GaAs是制造芯片的新型半导体材料。
①镓为第四周期元素,基态Ga原子的核外电子排布为:___________ ;
②GaN、GaP、GaAs的结构类似于金刚石,熔点如表所示:试分析三者熔点变化的原因___________ 。
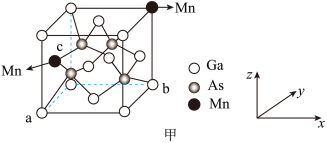
③将Mn掺杂到GaAs的晶体中替换部分Ga得到稀磁性半导体材料,晶体结构如甲图。___________ 。
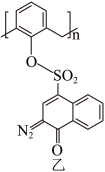
(2)“光刻胶涂覆”中用到一种701紫外正型光刻胶,结构如图乙所示,其S的杂化方式为___________ 。 及清洗剂
及清洗剂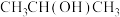 ,三种物质中除H外的各元素的电负性由大到小的顺序为
,三种物质中除H外的各元素的电负性由大到小的顺序为___________ ,HF分子的极性___________ (填“大于”“等于”或“小于”)HCl,1mol氟硼酸铵 中含有
中含有___________ mol配位键。
(4)LiF晶体结构属于氯化钠型。
①LiF的熔点和沸点比NaCl的高,请解释原因___________ 。
②LiF晶体的密度约为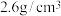 ,LiF晶胞的体积约为
,LiF晶胞的体积约为___________ cm3(计算结果保留一位有效数字)。
(1)“沉积”是将导体、绝缘体或半导体材料薄膜沉积到纯硅晶圆上。GaN、GaAs是制造芯片的新型半导体材料。
①镓为第四周期元素,基态Ga原子的核外电子排布为:
②GaN、GaP、GaAs的结构类似于金刚石,熔点如表所示:试分析三者熔点变化的原因
| 物质 | GaN | GaP | GaAs |
| 熔点/℃ | 1700 | 1480 | 1238 |
(2)“光刻胶涂覆”中用到一种701紫外正型光刻胶,结构如图乙所示,其S的杂化方式为
 及清洗剂
及清洗剂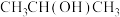 ,三种物质中除H外的各元素的电负性由大到小的顺序为
,三种物质中除H外的各元素的电负性由大到小的顺序为 中含有
中含有(4)LiF晶体结构属于氯化钠型。
①LiF的熔点和沸点比NaCl的高,请解释原因
②LiF晶体的密度约为
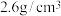 ,LiF晶胞的体积约为
,LiF晶胞的体积约为
更新时间:2024-04-25 15:44:23
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】(1)GaAs是新型半导体材料,第一电离能As__________ Ga(填“>”或“<”),GaCl3与AsCl3的中心原子的杂化方式分别为______ 、______ ,分别写出一个与它们互为等电子体的分子______ 、________ 。
(2)TiO2离子晶体的其中一种晶胞如图1所示,则Ti、O配位数之比为_________ ;影响离子晶体结构类型的因素有______ 、______ 、键性因素。
(3)基态铜原子的电子排布式是______ 。基态铜原子价电子层排布依据的原理,可用于解释下列事实的是_____ (填标号)。
A.Fe2+易被氧化为Fe3+ B.铜丝灼烧时焰色呈绿色
C.N的第一电离能大于O的第一电离能 D.NaCl的熔点比KCl的高
(4)铜的堆积方式(如图2)和晶胞结构(如图3)所示。若晶胞顶点A与堆积方式中的A球相对应,则晶胞中x、y、z三点与堆积方式中C球相对应的点是______ 。
已知铜原子的半径为r cm、摩尔质量为Mg/mol、晶体的密度为_________ g/cm3(阿伏伽德罗常数取NA)
(2)TiO2离子晶体的其中一种晶胞如图1所示,则Ti、O配位数之比为

(3)基态铜原子的电子排布式是
A.Fe2+易被氧化为Fe3+ B.铜丝灼烧时焰色呈绿色
C.N的第一电离能大于O的第一电离能 D.NaCl的熔点比KCl的高
(4)铜的堆积方式(如图2)和晶胞结构(如图3)所示。若晶胞顶点A与堆积方式中的A球相对应,则晶胞中x、y、z三点与堆积方式中C球相对应的点是

已知铜原子的半径为r cm、摩尔质量为Mg/mol、晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】氮及其化合物与人类生产、生活息息相关.回答下列问题:
(1)基态N原子中电子在2p轨道上的排布遵循的原则是__________ ,前4周期元素中,基态原子核外电子排布成单电子数最多的元素的价层电子排布式为__________ 。
(2)C、N、O三种元素第一电离能从大到小的顺序是__________ 。
(3)N2F2分子中N原子的杂化方式是__________ ,l mol N2F2含有__________ molσ键.
(4)NF3的键角__________ NH3的键角(填“<”“>”或“=”),原因是__________ .
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一.l mol NH4BF4__________ mol配位键.
(6)安全气囊的设计原理为6NaN3+FeIO3 Na2O+2Fe+9N2↑
Na2O+2Fe+9N2↑
①等电子体的原理是:原子总数相同,价电子总数相同的分子或离子具有相似的化学键特征,具有许多相近的性质.写出两种与N3-互为等电子体的分子或离子__________ .
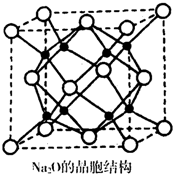
②Na2O的晶胞结构如图所示,晶胞边长为566pm,晶胞中氧原子的配位数为__________ ,Na2O晶体的密度为__________ g•cm-3(只要求列算式,不必计算出结果)。
(1)基态N原子中电子在2p轨道上的排布遵循的原则是
(2)C、N、O三种元素第一电离能从大到小的顺序是
(3)N2F2分子中N原子的杂化方式是
(4)NF3的键角
(5)NH4BF4(氟硼酸铵)是合成氮化硼纳米管的原料之一.l mol NH4BF4
(6)安全气囊的设计原理为6NaN3+FeIO3
 Na2O+2Fe+9N2↑
Na2O+2Fe+9N2↑①等电子体的原理是:原子总数相同,价电子总数相同的分子或离子具有相似的化学键特征,具有许多相近的性质.写出两种与N3-互为等电子体的分子或离子
②Na2O的晶胞结构如图所示,晶胞边长为566pm,晶胞中氧原子的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】 是一种高迁移率的新型热电材料,能将较低温度下的热量转化为电能。回答下列问题:
是一种高迁移率的新型热电材料,能将较低温度下的热量转化为电能。回答下列问题:
(1)已知基态 原子的价层电子排布式为
原子的价层电子排布式为 ,则基态
,则基态 原子N层上电子的运动状态有
原子N层上电子的运动状态有___________ 种。下列状态下的砷(第4周期VA族),失去第一个电子需要能量最多的是___________ (填字母)。
A.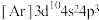 B.
B.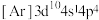 C.
C.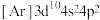
(2)已知四氯化锡的熔点为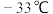 、沸点为
、沸点为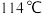 ,则其晶体类型为
,则其晶体类型为___________ ,四氯化锡中锡的杂化类型是___________ ,空间构型是___________ 。
(3)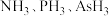 的沸点:
的沸点: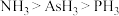 ,其原因是
,其原因是___________ 。
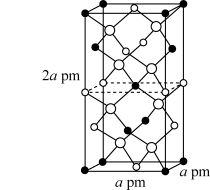
(4)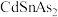 的晶胞结构如图所示,设
的晶胞结构如图所示,设 表示阿伏加德罗常数的值,则该晶体的密度为
表示阿伏加德罗常数的值,则该晶体的密度为_______  (用含
(用含 的代数式表示)。
的代数式表示)。
 是一种高迁移率的新型热电材料,能将较低温度下的热量转化为电能。回答下列问题:
是一种高迁移率的新型热电材料,能将较低温度下的热量转化为电能。回答下列问题:(1)已知基态
 原子的价层电子排布式为
原子的价层电子排布式为 ,则基态
,则基态 原子N层上电子的运动状态有
原子N层上电子的运动状态有A.
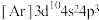 B.
B.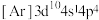 C.
C.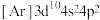
(2)已知四氯化锡的熔点为
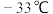 、沸点为
、沸点为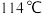 ,则其晶体类型为
,则其晶体类型为(3)
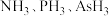 的沸点:
的沸点: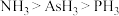 ,其原因是
,其原因是(4)
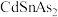 的晶胞结构如图所示,设
的晶胞结构如图所示,设 表示阿伏加德罗常数的值,则该晶体的密度为
表示阿伏加德罗常数的值,则该晶体的密度为 (用含
(用含 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】硼单质及其化合物有重要的应用。阅读下列材料,回答问题:
硼晶体熔点为2076℃。BF3可与NH3反应生成NH3·BF3。乙硼烷(B2H6)具有还原性,易水解生成H3BO3 (一元弱酸);乙硼烷可与NH3反应生成氨硼烷(NH3·BH3),其在一定条件下可以脱氢,最终得到氮化硼;乙硼烷也可与NaH反应生成NaBH4。
(1)下列说法正确的是___________(填字母)。
(2)基态硼原子的最高能级电子排布式是___________ ;单质硼的晶体类型是___________ ;写出H3BO3的电离方程式:___________ ;F-B-F键角比较:BF3___________ (填写“>”“<”) NH3·BF3; 的空间结构是
的空间结构是___________ 。
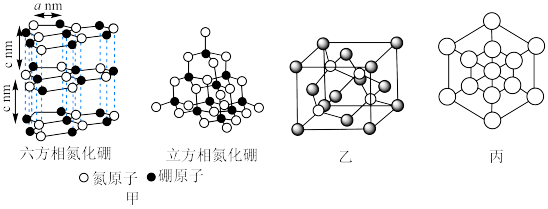
(3)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图甲所示。
①六方氮化硼中,距离B原子最近的B原子个数为___________ 。若阿伏加德罗常数的数值为NA,晶体相关参数如图所示,晶体密度为___________ g/cm3(用含有a、c、NA的式子表示)。
②另一种立方BN晶体与金刚石结构相似,其晶胞结构如图乙。图丙中 表示N原子的投影位置,在图中用
表示N原子的投影位置,在图中用 标出B原子的投影位置
标出B原子的投影位置___________ 。
硼晶体熔点为2076℃。BF3可与NH3反应生成NH3·BF3。乙硼烷(B2H6)具有还原性,易水解生成H3BO3 (一元弱酸);乙硼烷可与NH3反应生成氨硼烷(NH3·BH3),其在一定条件下可以脱氢,最终得到氮化硼;乙硼烷也可与NaH反应生成NaBH4。
(1)下列说法正确的是___________(填字母)。
| A.元素的电负性大小顺序是O>N>B>H |
| B.乙硼烷水解方程式为B2H6+6H2O=2H3BO3+6H2↑ |
| C.氨硼烷分子中N提供孤电子对,B提供空轨道形成配位键 |
| D.NaBH4晶体中存在的相互作用有离子键、共价键、氢键 |
(2)基态硼原子的最高能级电子排布式是
 的空间结构是
的空间结构是(3)氮化硼(BN)晶体有多种相结构。六方相氮化硼是通常存在的稳定相,与石墨相似,具有层状结构,可作高温润滑剂,但不能导电。立方相氮化硼是超硬材料,有优异的耐磨性。它们的晶体结构如图甲所示。
①六方氮化硼中,距离B原子最近的B原子个数为
②另一种立方BN晶体与金刚石结构相似,其晶胞结构如图乙。图丙中
 表示N原子的投影位置,在图中用
表示N原子的投影位置,在图中用 标出B原子的投影位置
标出B原子的投影位置
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】卤素单质及其化合物在科研和工农业生产中有着广泛的应用。回答下列问题:
(1)下列表示的是氟原子激发态电子排布式且能量最高的是_______。
(2)一氯乙烯(C2H3Cl)分子中,C的一个sp3杂化轨道与Cl的3px轨道形成σ键,并且Cl的3px轨道与C的2pz轨道形成3中心4电子的大π键(Π )。C的杂化轨道中s成分越多,形成的C-Cl键越强;Cl参与形成的大π键越多,形成的C-Cl键越强。则一氯乙烷(C2H5Cl)、一氯乙烯(C2H3Cl)、 一氯乙炔(C2HCl)分子中,C-Cl的键长依次
)。C的杂化轨道中s成分越多,形成的C-Cl键越强;Cl参与形成的大π键越多,形成的C-Cl键越强。则一氯乙烷(C2H5Cl)、一氯乙烯(C2H3Cl)、 一氯乙炔(C2HCl)分子中,C-Cl的键长依次_______ 。(填“递增”、“递减”或“无法判断”)
(3)卤化物CsICl2受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。Y的化学式为_______ 。
(4)α-AgI晶体中I- 离子作体心立方堆积(如图所示),Ag+主要分布在由I-构成的四面体、八面体等空隙中。在电场作用下,Ag+不需要克服太大的阻力即可发生迁移。因此,α-AgI晶体在电池中可作为_______ 。

(5)已知阿伏加德罗常数为NA,则α-AgI晶体的摩尔体积
_______ m3·mol-1(列出算式)。
(1)下列表示的是氟原子激发态电子排布式且能量最高的是_______。
| A.1s22s22p5 | B.1s22s22p43s1 | C.1s22s22p33p2 | D.1s22s22p43d2 |
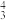 )。C的杂化轨道中s成分越多,形成的C-Cl键越强;Cl参与形成的大π键越多,形成的C-Cl键越强。则一氯乙烷(C2H5Cl)、一氯乙烯(C2H3Cl)、 一氯乙炔(C2HCl)分子中,C-Cl的键长依次
)。C的杂化轨道中s成分越多,形成的C-Cl键越强;Cl参与形成的大π键越多,形成的C-Cl键越强。则一氯乙烷(C2H5Cl)、一氯乙烯(C2H3Cl)、 一氯乙炔(C2HCl)分子中,C-Cl的键长依次(3)卤化物CsICl2受热发生非氧化还原反应,生成无色晶体X和红棕色液体Y。Y的化学式为
(4)α-AgI晶体中I- 离子作体心立方堆积(如图所示),Ag+主要分布在由I-构成的四面体、八面体等空隙中。在电场作用下,Ag+不需要克服太大的阻力即可发生迁移。因此,α-AgI晶体在电池中可作为

(5)已知阿伏加德罗常数为NA,则α-AgI晶体的摩尔体积

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】I.快离子导体是一类具有优良离子导电能力的固体电解质,研究得最多的是Ag、Cu、Li、Na、F、O等的快离子导体。
(1)Cu-e-=Cu+的过程中,失去的电子是基态Cu中_____ 轨道上的电子。
(2)N、O、F的第一电离能从小到大的顺序为______ (用元素符号表示);NH3、H2O、HF的沸点由低到高的顺序为_____ (用化学式表示,下同),其中NH3、H2O的键角由小到大的顺序为_____ 。
(3)二乙二胺合铜配离子{[Cu(H2NCH2CH2NH2)2]2+}的结构如图,1mol该配合物中所含的配位键为____ mol。

II.碳及其化合物广泛存在于自然界中,回答下列问题:
(4)基态碳原子的价电子轨道表示式是______ 。
a.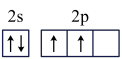 b.
b.
请阐述其原因是______ 。处于一定空间运动状态的电子在原子核外出现的概率密度分布可用_____ 形象地描述。在基态14C原子中,核外存在_____ 对自旋相反的电子。
(5)碳在形成化合物时,其键型以共价键为主,原因是______ 。写出两个与CS2互为等电子体的分子或离子______ 。
(6)甲醚(CH3OCH3)中氧原子的杂化方式为______ ,甲醚的沸点比乙醇(CH3CH2OH)的沸点_____ 。
(1)Cu-e-=Cu+的过程中,失去的电子是基态Cu中
(2)N、O、F的第一电离能从小到大的顺序为
(3)二乙二胺合铜配离子{[Cu(H2NCH2CH2NH2)2]2+}的结构如图,1mol该配合物中所含的配位键为

II.碳及其化合物广泛存在于自然界中,回答下列问题:
(4)基态碳原子的价电子轨道表示式是
a.
 b.
b.
请阐述其原因是
(5)碳在形成化合物时,其键型以共价键为主,原因是
(6)甲醚(CH3OCH3)中氧原子的杂化方式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
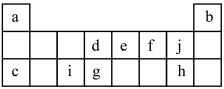
【推荐1】下表是元素周期表中短周期的一部分,表中所列字母分别代表一种元素。
(1)上述元素的单质中熔点最高的可能是________ (填字母);dh4比gh4稳定,其原因是______ 。
(2)f和a所形成的物质的沸点在f相应主族元素的同类型化合物中比较高,其原因是_____________ 。
(3)f的氢化物属于___ 晶体,a与d形成的化合物da4的立体构型是___ ,它的晶体属于_____ 晶体。
(4) c、i、j可组成离子化合物cxij6,其晶胞结构如下图所示,阳离子c+(用○表示)位于正方体棱的中点和正方体内部;阴离子ij6x-(用●表示)位于该正方体的顶点和面心。该化合物的化学式是________ 。
(1)上述元素的单质中熔点最高的可能是
(2)f和a所形成的物质的沸点在f相应主族元素的同类型化合物中比较高,其原因是
(3)f的氢化物属于
(4) c、i、j可组成离子化合物cxij6,其晶胞结构如下图所示,阳离子c+(用○表示)位于正方体棱的中点和正方体内部;阴离子ij6x-(用●表示)位于该正方体的顶点和面心。该化合物的化学式是

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】配位化合物广泛应用于物质分离、定量测定、医药、催化等方面。SiC俗称金刚砂,晶体结构与金刚石相似。
(1)已知CuCl2溶液与乙二胺H2N-CH2CH2-NH2作用,可形成配离子(如图所示),该配合物中铜离子的配位数是_______ ,乙二胺分子中N原子成键时采取的杂化类型是_______ 。

(2)利用氧化法可制备某些配位化合物。如2CoCl2+2NH4Cl+8NH3+H2O2=2[Co(NH3)5Cl]Cl2+2H2O提供孤电子对的成键原子是_______ 和_______ ,1mol[Co(NH3)5Cl]Cl2的配离子中σ键的物质的量为_______ mol。
(3)SiC晶体晶胞结构如下图所示:
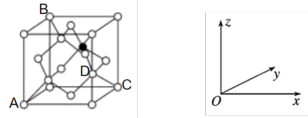
①已用黑球表示了其中一个硅原子,那么在该晶胞图中还需要涂黑的硅原子有_______ 个。
②该晶体类型为_______ ,在SiC晶体中,每个Si原子的配位数为_______ 个,若晶胞的边长为anm(NA代表阿伏加德罗常数的值),则该晶体的密度表达式为_______ g/cm3。
③原子坐标参数表示晶胞内部各原子的相对位置。上图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为_______ 。
(1)已知CuCl2溶液与乙二胺H2N-CH2CH2-NH2作用,可形成配离子(如图所示),该配合物中铜离子的配位数是

(2)利用氧化法可制备某些配位化合物。如2CoCl2+2NH4Cl+8NH3+H2O2=2[Co(NH3)5Cl]Cl2+2H2O提供孤电子对的成键原子是
(3)SiC晶体晶胞结构如下图所示:

①已用黑球表示了其中一个硅原子,那么在该晶胞图中还需要涂黑的硅原子有
②该晶体类型为
③原子坐标参数表示晶胞内部各原子的相对位置。上图中各原子坐标参数A为(0,0,0);B为(0,1,1);C为(1,1,0);则D原子的坐标参数为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】锰单质及其化合物应用十分广泛。回答下列问题:
(1)Mn位于元素周期表中第四周期__ 族,基态Mn原子核外未成对电子有__ 个。
(2)MnCl2可与NH3反应生成[Mn(NH36]Cl2,新生成的化学键为__ 键。NH3分子的空间构型为___ ,其中N原子的杂化轨道类型为___ 。
(3)金属锰有多种晶型,其中δ—Mn的结构为体心立方堆积,晶胞参数为apm,δ—Mn中锰的原子半径为__ pm。已知阿伏加 德罗常数的值为NA,δ—Mn的理论密度ρ=___ g·cm-3。(列出计算式)
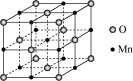
(4)已知锰的某种氧化物的晶胞如图所示,其中锰离子的化合价为__ ,其配位数为__ 。
(1)Mn位于元素周期表中第四周期
(2)MnCl2可与NH3反应生成[Mn(NH36]Cl2,新生成的化学键为
(3)金属锰有多种晶型,其中δ—Mn的结构为体心立方堆积,晶胞参数为apm,δ—Mn中锰的原子半径为
(4)已知锰的某种氧化物的晶胞如图所示,其中锰离子的化合价为

您最近一年使用:0次



