在氨硼烷(BH3-NH3)及催化剂作用下将 X 转化成 Y的反应过程如下。设 NA为阿伏加德罗常数的值。下列说法正确的是
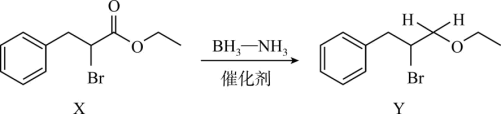
| A.BH3-NH3 分子中氢的化合价相同 |
| B.1molBH3-NH3分子中所含电子数为18NA |
| C.等物质的量的 X与 Y ,Y比 X多NA个σ键 |
| D.X、Y、BH3-NH3中C、B、N原子均为sp2杂化 |
更新时间:2024-05-04 10:39:06
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】用NA表示阿伏加 德罗常数的值,下列说法不正确的是
| A.常温下将5.6 g 铁加到足量浓硫酸中,转移电子数为0.3 NA |
| B.常温常压下,28 g丙烯中所含C-H键的数目为4 NA |
| C.1 L 3.0 mol·L-1的 NH4Cl溶液中,NH4+ 数目小于3 NA |
| D.2.0 g重水 (D2O) 中含有的中子数为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数,则下列叙述中正确的是
| A.6.02×1022个H2SO4分子含有4NA个O原子 |
| B.在标准状况时,22.4L水中所含水分子的数目为NA |
| C.18g水中含有10NA个电子 |
| D.在常温常压下,11.2LN2含有的分子数为0.5NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】10月23日6:02这个时刻可记为6:02 10/23(美式记法),该记法与阿伏加德罗常数的值 外观相似,因此每年的10月23日上午6:02到下午6:02被称为“摩尔日”。设
外观相似,因此每年的10月23日上午6:02到下午6:02被称为“摩尔日”。设 代表阿伏加德罗常数的值,下列说法不正确的是
代表阿伏加德罗常数的值,下列说法不正确的是
 外观相似,因此每年的10月23日上午6:02到下午6:02被称为“摩尔日”。设
外观相似,因此每年的10月23日上午6:02到下午6:02被称为“摩尔日”。设 代表阿伏加德罗常数的值,下列说法不正确的是
代表阿伏加德罗常数的值,下列说法不正确的是| A.常温常压下,1.06gNa2CO3含有的Na+个数为0.02NA |
| B.在1L物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA |
C.8.5 g氨气的原子数为 |
| D.标准状况下,11.2L NO和CO的混合气体的分子数为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列类比或推理合理的是
| 选项 | 已知 | 方法 | 结论 |
| A | 钠保存在煤油中 | 类比 | 锂保存在煤油中 |
| B |  是离子化合物 是离子化合物 | 类比 |  是离子化合物 是离子化合物 |
| C | 非金属性: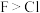 | 推理 | 沸点: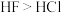 |
| D |  是正盐 是正盐 | 推理 |  是一元酸 是一元酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列关于物质结构与性质的说法,不正确的是
| A.Na、Mg、Al原子的电负性依次增大 |
| B.HCl和HI化学键的类型和分子的极性都相同 |
C.氨分子间存在氢键, 分子间没有氢键,故 分子间没有氢键,故 的熔沸点及稳定性均大于 的熔沸点及稳定性均大于 |
| D.基态钾原子核外电子共有19种运动状态,且其3s与4s轨道形状相同,能量不相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列有关化学用语表示正确的是
A.CaC2的电子式: |
B.异戊二烯的键线式为: |
C.能体现环己烷(C6H12)稳定空间构型的键线式: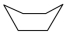 |
D.甲醛中π键的电子云轮廓图: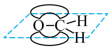 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】NH3是重要的化工原料,可用于某些配合物的制备,如NiSO4溶于氨水可以形成[Ni(NH3)6]SO4。下列有关[Ni(NH3)6]SO4的说法正确的是
| A.配体为NH3,其空间结构为平面三角形 |
| B.1mol [Ni(NH3)6]2+中σ键的数目为18mol |
| C.[Ni(NH3)6]2+中H-N-H的键角大于NH3中的键角 |
| D.由于[Ni(NH3)6]SO4是配合物,故向其中滴加BaCl2溶液不会产生沉淀 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】在光照下,螺吡喃发生开、闭环转换而变色,过程如下。下列关于开、闭环螺吡喃说法不正确的是

| A.闭环螺吡喃有手性,开环螺吡喃没有手性 |
B.第二电离能: |
C.由闭环螺吡喃转换为开环螺吡喃时,氮原子杂化方式由 转化为 转化为 |
| D.闭环螺吡喃亲水性更好 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
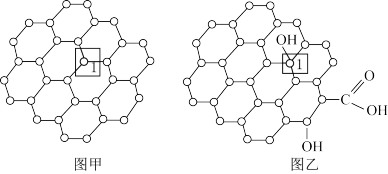
【推荐2】石墨烯是一种由碳原子组成六角形呈蜂巢晶格的二维碳纳米材料(如图甲),石墨烯中部分碳原子被氧化后,其平面结构会发生改变,转化为氧化石墨烯(如图乙)。
下列说法错误的是

下列说法错误的是
| A.图甲中,全为非极性共价键,图乙中,既有非极性共价键,也有极性共价键 |
| B.图乙中,1号C的杂化方式是sp2 |
| C.图甲中,1mol石墨烯中含有1.5mol的碳碳单键 |
| D.将50nm左右的石墨烯或氧化石墨烯溶于水,在相同条件下所得到的分散系后者更为稳定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】周期表中VIIA族元素及其化合物应用广泛。Cl2是一种重要的化工原料,大量用于制造盐酸、有机溶剂、农药、燃料和药品等;ClO2用作自来水消毒剂;NaClO、Ca(ClO)2既可用作漂白棉麻、纸张的漂白剂,又可用作游泳池等场所的消毒剂;氯可形成多种含氧酸HClO、HClO2、HClO3、HClO4;AgBr可用作感光材料;AgI可用于人工降雨;KIO3常用作食盐中的补碘剂。下列说法正确的是
A.ClO 中O-Cl-O夹角大于ClO 中O-Cl-O夹角大于ClO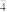 中O-Cl-O夹角 中O-Cl-O夹角 |
| B.ClO2是由极性键构成的非极性分子 |
| C.碘原子(53I)基态核外电子排布式为5s25p5 |
| D.前五周期的VIIA族元素单质的晶体类型相同 |
您最近一年使用:0次

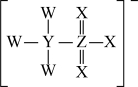


 含有
含有 键
键 中含有σ键、π键、离子键
中含有σ键、π键、离子键 的空间结构为直线形,中心原子的杂化方式为sp
的空间结构为直线形,中心原子的杂化方式为sp 的基态原子的电子排布式为
的基态原子的电子排布式为


