Ⅰ.研究铁的腐蚀,实验步骤如下:
步骤1:将铁粉放置于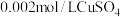 溶液中浸泡,过滤后用水洗涤。
溶液中浸泡,过滤后用水洗涤。
步骤2:向 溶液(用盐酸调至
溶液(用盐酸调至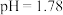 )中加入浸泡过的Fe粉。
)中加入浸泡过的Fe粉。
步骤3:采集溶液pH随时间变化的数据。_______ 。
(2)第二、三阶段主要发生吸氧腐蚀。
①析氧腐蚀时Cu上发生的电极反应为_______ 。
②第一阶段和第二阶段发生不同种类腐蚀的主要影响因素是_______ 。
Ⅱ.研究铁的防护
(3)在铁表面镀锌可有效防止铁被腐蚀
已知: 放电的速率缓慢且平稳时有利于得到致密、细腻的镀层。
放电的速率缓慢且平稳时有利于得到致密、细腻的镀层。
①镀件Fe应与电源的_______ 相连。
②向 电解液中加入NaCN溶液,将
电解液中加入NaCN溶液,将 转化为
转化为 ,电解得到的镀层更加致密、细腻,原因是
,电解得到的镀层更加致密、细腻,原因是_______ 。
(4)电镀后的废水中含有 ,一种测定其含量的方法是取废水50mL,再加KI溶液1mL,用
,一种测定其含量的方法是取废水50mL,再加KI溶液1mL,用 溶液滴定,达到滴定终点时,消耗
溶液滴定,达到滴定终点时,消耗 溶液
溶液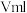 。
。
已知 (无色)
(无色) 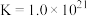
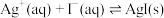 (黄色)
(黄色) 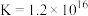
①滴定终点的现象是______________ 。
②废水中 的含量是
的含量是_______ g/L(用含C、V的代数式表示)。
步骤1:将铁粉放置于
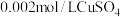 溶液中浸泡,过滤后用水洗涤。
溶液中浸泡,过滤后用水洗涤。步骤2:向
 溶液(用盐酸调至
溶液(用盐酸调至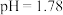 )中加入浸泡过的Fe粉。
)中加入浸泡过的Fe粉。步骤3:采集溶液pH随时间变化的数据。
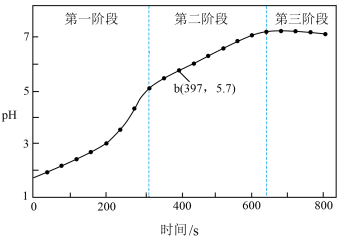
(2)第二、三阶段主要发生吸氧腐蚀。
①析氧腐蚀时Cu上发生的电极反应为
②第一阶段和第二阶段发生不同种类腐蚀的主要影响因素是
Ⅱ.研究铁的防护
(3)在铁表面镀锌可有效防止铁被腐蚀
已知:
 放电的速率缓慢且平稳时有利于得到致密、细腻的镀层。
放电的速率缓慢且平稳时有利于得到致密、细腻的镀层。①镀件Fe应与电源的
②向
 电解液中加入NaCN溶液,将
电解液中加入NaCN溶液,将 转化为
转化为 ,电解得到的镀层更加致密、细腻,原因是
,电解得到的镀层更加致密、细腻,原因是(4)电镀后的废水中含有
 ,一种测定其含量的方法是取废水50mL,再加KI溶液1mL,用
,一种测定其含量的方法是取废水50mL,再加KI溶液1mL,用 溶液滴定,达到滴定终点时,消耗
溶液滴定,达到滴定终点时,消耗 溶液
溶液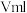 。
。已知
 (无色)
(无色) 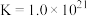
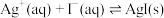 (黄色)
(黄色) 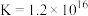
①滴定终点的现象是
②废水中
 的含量是
的含量是
更新时间:2024-05-09 20:11:10
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
I.如图装置中,U 形管内为红墨水,a、b 试管内分别盛有氯化铵(显酸性)溶液和食盐水,各加入生铁块,放置一段时间均被腐蚀,这两种腐蚀都属于____ 腐蚀。

(1)红墨水柱两边的液面变为左低右高,则_____ (填“a”或“b”)边盛有食盐水。
(2)b 试管中铁发生的是_____ 腐蚀。
II.下面两个图都是金属防护的例子。
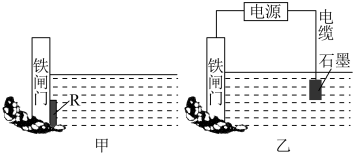
(3)为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R 可以采用_______ (从下面选项中选择),此方法叫做_____ 保护法。 A.铜 B.钠 C.锌 D.石墨
(4)图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的______ 极。
(5)采取以上两种方法,_________ (填“甲”或“乙”)种能使铁闸门保护得更好。
I.如图装置中,U 形管内为红墨水,a、b 试管内分别盛有氯化铵(显酸性)溶液和食盐水,各加入生铁块,放置一段时间均被腐蚀,这两种腐蚀都属于

(1)红墨水柱两边的液面变为左低右高,则
(2)b 试管中铁发生的是
II.下面两个图都是金属防护的例子。

(3)为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R 可以采用
(4)图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的
(5)采取以上两种方法,
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】电化学的发展对人类文明的进步起到了推动作用。
Ⅰ.用如图装置研究化学能转化为电能的过程。

(1)连接前,该装置中主要的能量转化形式为:___________ 能→___________ 能。连接后,Cu表面电极反应式为___________ 。
(2)连接前后,装置中现象的差异有___________ 。(任写两条)
(3)用如图装置实现“Zn表面镀Cu”。需要将溶液改为___________ (填写溶质化学式),此时,Cu发生的电极反应式为___________ 。
Ⅱ.研究金属的腐蚀过程及防腐蚀对人们的日常生活有重大意义。
(4)如图1中的铁棒为纯铁,则其腐蚀过程属于___________ 腐蚀。
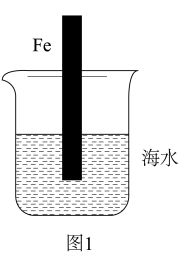
(5)如图1中的铁棒(含碳量为10.8%)越靠近烧杯底部发生电化学腐蚀就越___________ (选填“轻微”、“严重”)。该实验说明___________ 因素会影响铁的腐蚀速率。腐蚀时正极的电极反应式为___________ 。(已知:海水pH约为8.1)
(6)用图2研究铁的腐蚀过程。预测恒温条件下反应一段时间后,U形管内液面的变化情况。
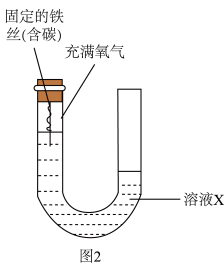
(已知:起始时两管内液面相平,实验过程中铁丝始终不接触溶液,选填“左高右低”、“左低右高”或“几乎不变”)
该组实验目的:研究___________ 、___________ 等因素对铁的腐蚀过程产生影响。
(7)用图3所示装置研究铁的防腐蚀过程:

①K1、K2、K3只关闭一个,则铁腐蚀的速度最快的是只闭合___________ (填“K1”、“K2”或“K3”下同)。
②为减缓铁的腐蚀,应只闭合___________ ,该防护法称为___________ 。
③只闭合K3,石墨电极附近的pH将___________ (填“变大”、“变小”或“不变”)。
(8)图4为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。
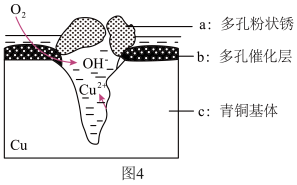
①腐蚀过程中,负极是___________ (填“a”、“b”或“c”)。
②环境中的 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl。青铜器发生电化腐蚀并最终生成Cu2(OH)3Cl的总离子方程式为
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl。青铜器发生电化腐蚀并最终生成Cu2(OH)3Cl的总离子方程式为___________ 。
(9)①金属在发生电化学腐蚀时,总是作为原电池___________ (阳极)的金属被腐蚀,作为___________ (阴极)的金属不被腐蚀,如果能使被保护的金属成为___________ ,就不易被腐蚀。
②牺牲阳极法

原理:原电池原理
要求:被保护的金属作___________ ,活泼性更强的金属作___________ 。
应用:锅炉内壁、船舶外壳、钢铁闸门安装镁合金或锌块。
实例 实验1:
如图装置反应一段时间后,往Fe电极区滴入2滴K3[Fe(CN)6](铁氰化钾)溶液,观察实验现象。
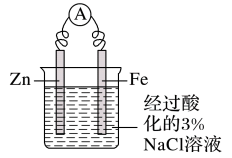
已知Fe2+与[Fe(CN)6]3-反应生成带有特征蓝色的KFe[Fe(CN)6]沉淀。
实例 实验2:
培养皿中放入含有NaCl的琼脂,并注入5~6滴酚酞和K3[Fe(CN)6]溶液,取两个2~3 cm的铁钉,用砂纸擦光,将裹有锌皮的铁钉放入a,缠有铜丝的铁钉放入b.
③外加电流法

原理:电解池原理
要求:被保护的金属作为___________ ,与电源的___________ 相连。
应用:钢铁闸门,高压线铁架,地下管道连接直流电源的___________ 。
Ⅰ.用如图装置研究化学能转化为电能的过程。

(1)连接前,该装置中主要的能量转化形式为:
(2)连接前后,装置中现象的差异有
(3)用如图装置实现“Zn表面镀Cu”。需要将溶液改为
Ⅱ.研究金属的腐蚀过程及防腐蚀对人们的日常生活有重大意义。
(4)如图1中的铁棒为纯铁,则其腐蚀过程属于

(5)如图1中的铁棒(含碳量为10.8%)越靠近烧杯底部发生电化学腐蚀就越
(6)用图2研究铁的腐蚀过程。预测恒温条件下反应一段时间后,U形管内液面的变化情况。

(已知:起始时两管内液面相平,实验过程中铁丝始终不接触溶液,选填“左高右低”、“左低右高”或“几乎不变”)
| 溶液X | 浓硫酸 | 浓盐酸 | 稀硫酸 |
| 液面情况 |
(7)用图3所示装置研究铁的防腐蚀过程:

①K1、K2、K3只关闭一个,则铁腐蚀的速度最快的是只闭合
②为减缓铁的腐蚀,应只闭合
③只闭合K3,石墨电极附近的pH将
(8)图4为青铜器在潮湿环境中发生电化学腐蚀的原理示意图。

①腐蚀过程中,负极是
②环境中的
 扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl。青铜器发生电化腐蚀并最终生成Cu2(OH)3Cl的总离子方程式为
扩散到孔口,并与正极反应产物和负极反应产物作用生成多孔粉状锈Cu2(OH)3Cl。青铜器发生电化腐蚀并最终生成Cu2(OH)3Cl的总离子方程式为(9)①金属在发生电化学腐蚀时,总是作为原电池
②牺牲阳极法

原理:原电池原理
要求:被保护的金属作
应用:锅炉内壁、船舶外壳、钢铁闸门安装镁合金或锌块。
实例 实验1:
如图装置反应一段时间后,往Fe电极区滴入2滴K3[Fe(CN)6](铁氰化钾)溶液,观察实验现象。

已知Fe2+与[Fe(CN)6]3-反应生成带有特征蓝色的KFe[Fe(CN)6]沉淀。
| 实验装置 | 电流表 | 阳极(负极区) | 阴极(正极区) |
| 现象 | 指针 | Zn溶解 | 有 |
| 有关反应 | — | Zn-2e-=Zn2+ | 2H++2e-=H2↑ |
| 结论 | 溶液中不含 | ||
培养皿中放入含有NaCl的琼脂,并注入5~6滴酚酞和K3[Fe(CN)6]溶液,取两个2~3 cm的铁钉,用砂纸擦光,将裹有锌皮的铁钉放入a,缠有铜丝的铁钉放入b.
| 实验装置 | 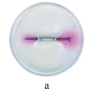 | 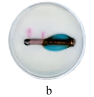 |
| 现象 | 铁钉周围 | 铁钉周围生成 |
| 结论 | 铁作为 | |

原理:电解池原理
要求:被保护的金属作为
应用:钢铁闸门,高压线铁架,地下管道连接直流电源的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】Ⅰ、已知下面在298K时的热化学方程式:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1,CH4(g)+2O2(g)=CO2(g)+2H2O (l) ΔH=-890.3 kJ·mol-1,C(s)+O2(g)=CO2(g) ΔH=-393.5kJ·mol-1。根据上面的热化学方程式完成下列问题:
(1)通过计算说明等质量的H2、C、CH4完全燃烧时放出热量最多的是___ 。
(2)根据以上反应,则C(s)+2H2(g)=CH4(g)的焓变ΔH=___ 。
(3)已知H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
试写出甲烷燃烧生成二氧化碳和水蒸气的热化学方程式:___ 。
Ⅱ、为了解金属腐蚀的原因和寻求防止金属腐蚀的方法具有重要意义。
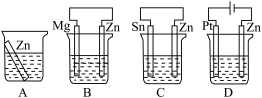
(1)分别放在以下装置(都盛有0.1mol·L-1的H2SO4溶液)中的四块相同的纯锌片,其中腐蚀最快的是___ 。
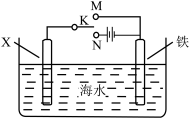
(2)利用如图装置,可以模拟铁的电化学防护。其中X为碳棒,为减缓铁的腐蚀,开关K应置于___ 处。若X为锌,开关K置于M处,该电化学防护法称为___ 。
(1)通过计算说明等质量的H2、C、CH4完全燃烧时放出热量最多的是
(2)根据以上反应,则C(s)+2H2(g)=CH4(g)的焓变ΔH=
(3)已知H2O(l)=H2O(g) ΔH=+44.0kJ·mol-1
试写出甲烷燃烧生成二氧化碳和水蒸气的热化学方程式:
Ⅱ、为了解金属腐蚀的原因和寻求防止金属腐蚀的方法具有重要意义。
(1)分别放在以下装置(都盛有0.1mol·L-1的H2SO4溶液)中的四块相同的纯锌片,其中腐蚀最快的是

(2)利用如图装置,可以模拟铁的电化学防护。其中X为碳棒,为减缓铁的腐蚀,开关K应置于

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】以NaCl为主要成分的融雪剂会腐蚀桥梁、铁轨等钢铁设备。某研究小组探究NaCl溶液对钢铁腐蚀的影响。
(1)将滤纸用3.5%的NaCl溶液润湿,涂上铁粉、炭粉的混合物,贴在表面皿上。在滤纸上加几滴检验试剂,再缓慢加入NaCl溶液至没过滤纸,操作如图1所示。_____ ,炭粉的作用是_____ 。
②为了说明NaCl的作用,需要补充的对照实验是_____ 。
(2)向图2所示装置的烧杯a、b中各加入30mL3.5%的NaCl溶液,闭合K,指针未发生偏转。加热烧杯a,指针向右偏转。取a、b中溶液少量,滴加 溶液,a中出现蓝色沉淀,b中无变化,b中铁片作
溶液,a中出现蓝色沉淀,b中无变化,b中铁片作_____ 极。外电路中电子流动方向为_____ (填“a→b”或“b→a”)。
实验Ⅱ中,b中电极发生的电极反应为_____ 。根据上述实验可知,对钢铁腐蚀有影响的因素是_____ 和NaCl溶液的浓度。
(1)将滤纸用3.5%的NaCl溶液润湿,涂上铁粉、炭粉的混合物,贴在表面皿上。在滤纸上加几滴检验试剂,再缓慢加入NaCl溶液至没过滤纸,操作如图1所示。

②为了说明NaCl的作用,需要补充的对照实验是
(2)向图2所示装置的烧杯a、b中各加入30mL3.5%的NaCl溶液,闭合K,指针未发生偏转。加热烧杯a,指针向右偏转。取a、b中溶液少量,滴加
 溶液,a中出现蓝色沉淀,b中无变化,b中铁片作
溶液,a中出现蓝色沉淀,b中无变化,b中铁片作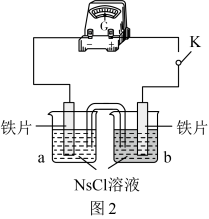
| 实验 | a | b | 指针偏转方向 |
| Ⅰ | 0.1% | 0.01% | 向右 |
| Ⅱ | 0.1% | 3.5% | 向左 |
您最近一年使用:0次
【推荐2】研究金属腐蚀和防腐的原理很有现实意义.
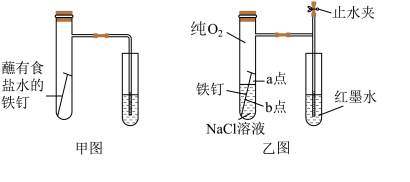
(1)甲图为人教版教材中探究钢铁的吸氧腐蚀的装置,某兴趣小组按装置试验,导管中液柱的上升缓慢,为更快更清晰地观察到液柱上升的现象,下列措施错误的________ (填序号)
A.用纯氧气代替试管内空气
B.用酒精灯加热试管提高温度
C.将铁钉换成铁粉和炭粉混合粉末
D.换成更细的导管,水中滴加红墨水
(2)为探究铁钉腐蚀实验a、b两点所发生的反应,张老师进行以下实验,证明铁发生电化学腐蚀。请完成表格空白:
(3)孔老师认为仅通过b中现象不能证明铁发生了电化学腐蚀,补充进行下列实验,在实验几分钟后的记录如下:
以上实验表明,K3[Fe(CN)6]具有________ 性
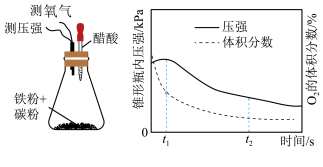
(4)赵老师设计下面装置研究弱酸性环境中腐蚀的主要形式,测定锥形瓶内气压和空气中氧气的体积分数随时间变化见图,从图中可分析,t1~t2之间主要发生_________ 腐蚀(填吸氧或析氢)
(5)金属阳极钝化形成保护膜是一种电化学防腐方法,将Fe作阳极置于H2SO4溶液中,一定条件下Fe表面形成致密Fe3O4氧化膜,试写出该阳极电极反应式_________ 。

(1)甲图为人教版教材中探究钢铁的吸氧腐蚀的装置,某兴趣小组按装置试验,导管中液柱的上升缓慢,为更快更清晰地观察到液柱上升的现象,下列措施错误的
A.用纯氧气代替试管内空气
B.用酒精灯加热试管提高温度
C.将铁钉换成铁粉和炭粉混合粉末
D.换成更细的导管,水中滴加红墨水
(2)为探究铁钉腐蚀实验a、b两点所发生的反应,张老师进行以下实验,证明铁发生电化学腐蚀。请完成表格空白:
| 实验操作 | 实验现象 | 实验结论 |
| ⅰ.向NaCl溶液中滴加2~3滴酚酞指示剂 | a点附近溶液出现红色 | a点电极反应为 |
| ⅱ.然后再滴加2~3滴铁氰化钾溶液 | b点周围出现蓝色沉淀 | b点电极反应为 沉淀的化学式为 |
(3)孔老师认为仅通过b中现象不能证明铁发生了电化学腐蚀,补充进行下列实验,在实验几分钟后的记录如下:
| 实验 | 滴管 | 现象 |
 1.0 mol·L-1NaCl溶液 | 0.5 mol•L﹣1K3[Fe(CN)6]溶液 | 铁片表面产生大量蓝色沉淀 |
(4)赵老师设计下面装置研究弱酸性环境中腐蚀的主要形式,测定锥形瓶内气压和空气中氧气的体积分数随时间变化见图,从图中可分析,t1~t2之间主要发生

(5)金属阳极钝化形成保护膜是一种电化学防腐方法,将Fe作阳极置于H2SO4溶液中,一定条件下Fe表面形成致密Fe3O4氧化膜,试写出该阳极电极反应式
您最近一年使用:0次
【推荐3】某小组同学利用下图所示装置进行铁的电化学腐蚀原理的探究实验:
(1)小组同学认为以上两种检验方法,均能证明铁发生了吸氧腐蚀。
①实验 i 中的现象是_____ 。
②用化学用语解释实验i中的现象:_____ 。
(2)查阅资料:K3[Fe(CN)6]具有氧化性。
①据此有同学认为仅通过ii中现象不能证明铁发生了电化学腐蚀,理由是_____ 。
②进行下列实验,在实验几分钟后的记录如下:
a.以上实验表明:在_____ 条件下,K3[Fe(CN)6]溶液可以与铁片发生反应。
b.为探究Cl-的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净) 后再进行实验 iii,发现铁片表面产生蓝色沉淀。此补充实验表明 Cl-的作用是_____ 。
(3)有同学认为上述实验仍不严谨。为进一步探究K3[Fe(CN)6]的氧化性对实验 ii 结果的影响,又利用(2)中装置继续实验。其中能证实以上影响确实存在的是_____ (填 字母序号)。
| 装置 | 分别进行的操作 | 现象 |
 | i. 连好装置一段时间后,向烧杯中滴加酚酞 | |
| ii. 连好装置一段时间后,向烧杯中滴加K3[Fe(CN)6]溶液 | 铁片表面产生蓝色沉淀 |
①实验 i 中的现象是
②用化学用语解释实验i中的现象:
(2)查阅资料:K3[Fe(CN)6]具有氧化性。
①据此有同学认为仅通过ii中现象不能证明铁发生了电化学腐蚀,理由是
②进行下列实验,在实验几分钟后的记录如下:
| 实验 | 滴管 | 试管 | 现象 |
 | 0.5 mol·L-1 K3[Fe(CN)6] 溶液 | iii. 蒸馏水 | 无明显变化 |
| iv. 1.0 mol·L-1NaCl溶液 | 铁片表面产生大量蓝色沉淀 | ||
| v. 0.5 mol·L-1Na2SO4溶液 | 无明显变化 |
b.为探究Cl-的存在对反应的影响,小组同学将铁片酸洗(用稀硫酸浸泡后洗净) 后再进行实验 iii,发现铁片表面产生蓝色沉淀。此补充实验表明 Cl-的作用是
(3)有同学认为上述实验仍不严谨。为进一步探究K3[Fe(CN)6]的氧化性对实验 ii 结果的影响,又利用(2)中装置继续实验。其中能证实以上影响确实存在的是
| 实验 | 试剂 | 现象 |
| A | 酸洗后的铁片、K3[Fe(CN)6]溶液(已除O2) | 产生蓝色沉淀 |
| B | 酸洗后的铁片、K3[Fe(CN)6]和 NaCl 混合溶液(未除O2) | 产生蓝色沉淀 |
| C | 铁片、K3[Fe(CN)6]和NaCl 混合溶液(已除O2) | 产生蓝色沉淀 |
| D | 铁片、K3[Fe(CN)6]和盐酸混合溶液(已除 O2) | 产生蓝色沉淀 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】络氨铜[Cu(NH3)4SO4]是一种高效、安全的广谱杀菌剂,也是植物生长激素,常温下溶于水,在空气中不稳定,受热易分解。某兴趣小组以孔雀石[主要成分为Cu2(OH)2CO3,含少量Fe2O3和SiO2杂质]为原料制备络氨铜并测定样品中氨含量。
I.制备络氨铜
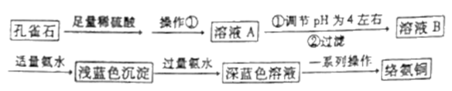
已知:Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH如表。
(1)操作①的目的是___ 。
(2)调节溶液pH时,可选用的物质为___ 。
A.稀硫酸B.CuO C.Na2CO3D.CuCO3
(3)已知浅蓝色沉淀为Cu2(OH)2CO4,试写出生成此沉淀的离子方程式___ 。
(4)深蓝色溶液为络氨铜溶液,经过一系列操作:加入乙醇、减压过滤、洗涤、干燥,即可获得络氨铜晶体。析出晶体时采用加入乙醇的方法,不采用浓缩结晶的原因是___ 。减压过滤时所用装置如图所示,关于减压过滤下列说法正确的是___ 。
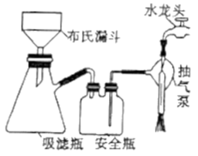
A.减压过滤可得到较干燥固体,且过滤速度快,适合分离所有的固体与溶液
B.洗涤晶体时,要先关小水龙头
C.当吸滤瓶中的液体接近支管口时,应拔掉吸滤瓶.上的橡皮管并将液体从支管口倒出
D.滤纸大小应略小于布氏漏斗内径并能将全部小孔盖住,用蒸馏水将滤纸润湿,微开水龙头,抽气使滤纸紧贴布氏漏斗
II.样品中氨含量的测定
精确称取0.250g样品,加适量水溶解,注入如图所示的三颈烧瓶中,然后逐滴加入15mL10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用30mL0.500mol·L-1的盐酸完全吸收蒸出的氨。取下接收瓶,用0.500mol·L-1NaOH标准溶液滴定剩余的HCl(选用甲基橙作指示剂),到滴定终点时消耗22.00mLNaOH标准溶液。
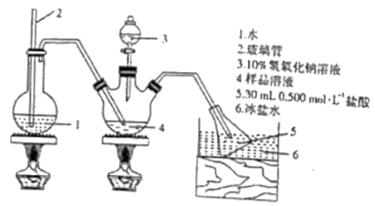
(5)该样品中氨的质量分数为___ 。
(6)下列实验操作可能使氨含量测定结果偏低的是___ 。
A.滴定时未用NaOH标准溶液润洗滴定管
B.读数时,滴定前平视,滴定后俯视
C.滴定过程中选用酚酞作指示剂
D.取下接收瓶前,未用蒸馏水冲洗插入接收瓶中的导管外壁
I.制备络氨铜

已知:Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH如表。
| Fe3+ | Fe2+ | Cu2+ | |
| 开始沉淀的pH | 2.7 | 7.6 | 4.7 |
| 完全沉淀时的pH | 3.7 | 9.6 | 6.7 |
(2)调节溶液pH时,可选用的物质为
A.稀硫酸B.CuO C.Na2CO3D.CuCO3
(3)已知浅蓝色沉淀为Cu2(OH)2CO4,试写出生成此沉淀的离子方程式
(4)深蓝色溶液为络氨铜溶液,经过一系列操作:加入乙醇、减压过滤、洗涤、干燥,即可获得络氨铜晶体。析出晶体时采用加入乙醇的方法,不采用浓缩结晶的原因是

A.减压过滤可得到较干燥固体,且过滤速度快,适合分离所有的固体与溶液
B.洗涤晶体时,要先关小水龙头
C.当吸滤瓶中的液体接近支管口时,应拔掉吸滤瓶.上的橡皮管并将液体从支管口倒出
D.滤纸大小应略小于布氏漏斗内径并能将全部小孔盖住,用蒸馏水将滤纸润湿,微开水龙头,抽气使滤纸紧贴布氏漏斗
II.样品中氨含量的测定
精确称取0.250g样品,加适量水溶解,注入如图所示的三颈烧瓶中,然后逐滴加入15mL10%NaOH溶液,通入水蒸气,将样品溶液中的氨全部蒸出,并用蒸馏水冲洗导管内壁,用30mL0.500mol·L-1的盐酸完全吸收蒸出的氨。取下接收瓶,用0.500mol·L-1NaOH标准溶液滴定剩余的HCl(选用甲基橙作指示剂),到滴定终点时消耗22.00mLNaOH标准溶液。

(5)该样品中氨的质量分数为
(6)下列实验操作可能使氨含量测定结果偏低的是
A.滴定时未用NaOH标准溶液润洗滴定管
B.读数时,滴定前平视,滴定后俯视
C.滴定过程中选用酚酞作指示剂
D.取下接收瓶前,未用蒸馏水冲洗插入接收瓶中的导管外壁
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】水中的溶解氧是水生生物生存不可缺少的条件。某课外小组采用碘量法测定学校周边河水中的溶解氧。实验步骤及测定原理如下:
I.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI混合,反应生成 MnO(OH)2,实现氧的固定。
II.酸化、滴定
将固氧后的水样酸化,MnO(OH)2被I-还原为Mn2+,在暗处静置5min,然后用标准Na2S2O3溶液滴定生成的I2(2S2O32-+I2===2I-+S4O62-)
回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是:______________________ 。
(2)“氧的固定”中发生反应的化学方程式为:_________________________________ 。
(3)Na2S2O3溶液不稳定,使用前需标定。①配制该溶液时需要的玻璃仪器有烧杯、玻璃棒、试剂瓶和______________________ ;
②配制时使用的蒸馏水必须经过煮沸、冷却后才能使用其目的是杀菌、除___________ 及二氧化碳。
(4)取200.00mL水样经固氧、酸化后,用amol·L-1Na2S2O3溶液滴定,以淀粉溶液作指示剂,终点现象为___________ ;若消耗Na2S2O3溶液的体积为bmL,则水样中溶解氧的含量为___________ mg·L-1。
(5)上述滴定过程中,若滴定前俯视刻度,而滴定后仰视刻度,会使得所测溶解氧含量___________ 。(填“偏高”、“偏低”或“不变”)
I.取样、氧的固定
用溶解氧瓶采集水样。记录大气压及水体温度。将水样与Mn(OH)2碱性悬浊液(含有KI混合,反应生成 MnO(OH)2,实现氧的固定。
II.酸化、滴定
将固氧后的水样酸化,MnO(OH)2被I-还原为Mn2+,在暗处静置5min,然后用标准Na2S2O3溶液滴定生成的I2(2S2O32-+I2===2I-+S4O62-)
回答下列问题:
(1)取水样时应尽量避免扰动水体表面,这样操作的主要目的是:
(2)“氧的固定”中发生反应的化学方程式为:
(3)Na2S2O3溶液不稳定,使用前需标定。①配制该溶液时需要的玻璃仪器有烧杯、玻璃棒、试剂瓶和
②配制时使用的蒸馏水必须经过煮沸、冷却后才能使用其目的是杀菌、除
(4)取200.00mL水样经固氧、酸化后,用amol·L-1Na2S2O3溶液滴定,以淀粉溶液作指示剂,终点现象为
(5)上述滴定过程中,若滴定前俯视刻度,而滴定后仰视刻度,会使得所测溶解氧含量
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2·6H2O的流程如下:
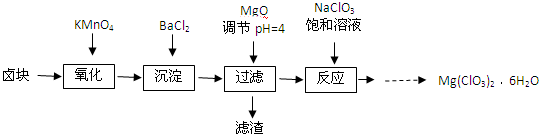
已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
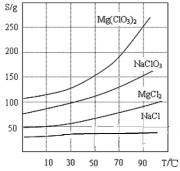
②Mg(ClO3)2、NaClO3 、MgCl2 、NaCl 四种
化合物的溶解度(S)随温度(T)变化曲线如图所示。
(1)加速卤块在KMnO4溶液中溶解的措施有:_________________________ (写出一点即可)。
(2)加入MgO的作用是_________________ ;过滤后所得滤渣的主要成分为__________________ 。
(3)加入NaClO3饱和溶液后发生反应的化学方程式为_______________ ,再进一步制 Mg(ClO3)2·6H2O晶体的实验步骤依次为:①加热蒸发;②_____ ;③_____ ;④过滤洗涤。
产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.0 g产品配成100 mL溶液。
步骤2:取10.00 mL试液于锥形瓶中,加入10.00 mL稀硫酸和20 .00mL 1.000 mol/L的FeSO4溶液,微热,将Fe2+氧化成Fe3+。
步骤3:冷却至室温,用0.100 mol/L K2Cr2O7 溶液滴定剩余的Fe2+至终点。
此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+→2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次
(4)①写出步骤2中发生反应的离子方程式:___________________________________ ;
②步骤3中若滴定前不用标准液润洗滴定管,将会导致最终结果____ (填“偏大”、 “偏小”或“不变”);
(5)若平均消耗K2Cr2O7 溶液15.00 mL,则产品中Mg(ClO3)2·6H2O的质量分数为________ 。

已知:①卤块主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质。
②Mg(ClO3)2、NaClO3 、MgCl2 、NaCl 四种
化合物的溶解度(S)随温度(T)变化曲线如图所示。

(1)加速卤块在KMnO4溶液中溶解的措施有:
(2)加入MgO的作用是
(3)加入NaClO3饱和溶液后发生反应的化学方程式为
产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量3.0 g产品配成100 mL溶液。
步骤2:取10.00 mL试液于锥形瓶中,加入10.00 mL稀硫酸和20 .00mL 1.000 mol/L的FeSO4溶液,微热,将Fe2+氧化成Fe3+。
步骤3:冷却至室温,用0.100 mol/L K2Cr2O7 溶液滴定剩余的Fe2+至终点。
此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+→2Cr3++6Fe3++7H2O。
步骤4:将步骤2、3重复两次
(4)①写出步骤2中发生反应的离子方程式:
②步骤3中若滴定前不用标准液润洗滴定管,将会导致最终结果
(5)若平均消耗K2Cr2O7 溶液15.00 mL,则产品中Mg(ClO3)2·6H2O的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】某兴趣小组用如图所示装置(夹持装置略)收集某葡萄酒中的 ,并对其含量进行测定。
,并对其含量进行测定。
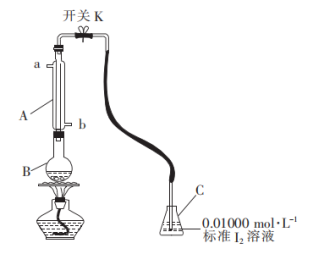
回答下列问题:
(1)实验开始前,首先应_________________ ,方法是___________________________ 。
(2)仪器B的名称为__________ ,冷却水的进出方向为_________ (填“a进b出”或“b进a出”)。
(3)向仪器B中加入 葡萄酒和适量的稀硫酸,仪器C中加入
葡萄酒和适量的稀硫酸,仪器C中加入 标准
标准 溶液,加热使
溶液,加热使 全部进入仪器C中(不考虑气体逸出)。
全部进入仪器C中(不考虑气体逸出)。
①量取 标准
标准 溶液时,应选用
溶液时,应选用_________ (填标号)。
a.量筒 b.酸式滴定管 c.碱式滴定管
②仪器C中发生反应的离子方程式为_____________________________ 。
③若仪器C中标准 溶液与
溶液与 恰好完全反应,则
恰好完全反应,则 的含量为
的含量为_________  。
。
 ,并对其含量进行测定。
,并对其含量进行测定。
回答下列问题:
(1)实验开始前,首先应
(2)仪器B的名称为
(3)向仪器B中加入
 葡萄酒和适量的稀硫酸,仪器C中加入
葡萄酒和适量的稀硫酸,仪器C中加入 标准
标准 溶液,加热使
溶液,加热使 全部进入仪器C中(不考虑气体逸出)。
全部进入仪器C中(不考虑气体逸出)。①量取
 标准
标准 溶液时,应选用
溶液时,应选用a.量筒 b.酸式滴定管 c.碱式滴定管
②仪器C中发生反应的离子方程式为
③若仪器C中标准
 溶液与
溶液与 恰好完全反应,则
恰好完全反应,则 的含量为
的含量为 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】检验甲醛含量的方法有很多,其中银-Ferrozine法灵敏度较高。测定原理为甲醛把氧化银还原成Ag,产生的Ag与Fe3+定量反应生成Fe2+,Fe2+与菲洛嗪(Ferrozine)形成有色配合物,通过测定吸光度计算出甲醛的含量。某学习小组类比此原理设计如下装置测定新装修居室内空气中甲醛的含量(夹持装置略去)。
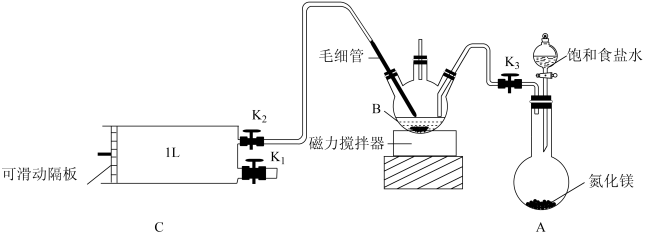
已知:甲醛和银氨溶液反应生成单质银和CO2,氮化镁与水反应放出NH3,毛细管内径不超过1mm。
请回答下列问题:
(1)A装置中反应的化学方程式为_______ ,用饱和食盐水代替水制备NH3的原因是_______ 。
(2)B中装有AgNO3溶液,仪器B的名称为_______ 。
(3)银氨溶液的制备。关闭K1、K2,打开K3,打开_______ ,使饱和食盐水慢慢滴入圆底烧瓶中,当观察到B中_______ ,停止通NH3。
(4)室内空气中甲醛含量的测定。
①用热水浴加热B,打开K1,将滑动隔板慢慢由最右端抽到最左端,吸入1L室内空气,关闭K1;后续操作是_______ ;再重复上述操作3次。毛细管的作用是_______ 。
②向上述B中充分反应后的溶液中加入稀硫酸调节溶液pH=1,再加入足量Fe2(SO4)3溶液,充分反应后立即加入菲洛嗪,Fe2+与菲洛嗪形成有色物质,在562nm处测定吸光度,测得生成Fe2+1.12mg,空气中甲醛的含量为_______ mg·L-1。

已知:甲醛和银氨溶液反应生成单质银和CO2,氮化镁与水反应放出NH3,毛细管内径不超过1mm。
请回答下列问题:
(1)A装置中反应的化学方程式为
(2)B中装有AgNO3溶液,仪器B的名称为
(3)银氨溶液的制备。关闭K1、K2,打开K3,打开
(4)室内空气中甲醛含量的测定。
①用热水浴加热B,打开K1,将滑动隔板慢慢由最右端抽到最左端,吸入1L室内空气,关闭K1;后续操作是
②向上述B中充分反应后的溶液中加入稀硫酸调节溶液pH=1,再加入足量Fe2(SO4)3溶液,充分反应后立即加入菲洛嗪,Fe2+与菲洛嗪形成有色物质,在562nm处测定吸光度,测得生成Fe2+1.12mg,空气中甲醛的含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】I.实验室用下图装置制取并研究SO2的性质。
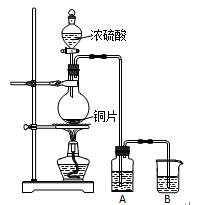
完成下列填空:
(1)圆底烧瓶中反应的化学方程式为_____________________________________ 。
(2)若A中盛放品红溶液,可以验证的SO2性质是______________ 。若要验证SO2的还原性,A中应盛放_________ 溶液。B中应盛放_________ 溶液。
II.为测定反应后的溶液中残留的硫酸浓度,实验小组进行如下探究。
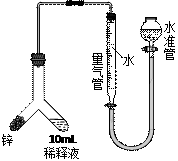
(3)甲组:取1 mL反应液加水稀释至100 mL,再取10 mL稀释液与足量锌粒用下图装置进行测定。在读取反应前后量气管中液面读数时应先调节水准管与量气管中液面等高,这样操作的目的是________ 。
实验测得反应生成的氢气体积为22.4 mL(已换算到标准状况),计算原反应液中残留的硫酸浓度为______ mol/L。
(4)乙组:欲通过加入足量的BaCl2溶液,测定生成的BaSO4沉淀质量来达到实验目的。该设计思路不可行,理由是_______________________________ 。

完成下列填空:
(1)圆底烧瓶中反应的化学方程式为
(2)若A中盛放品红溶液,可以验证的SO2性质是
II.为测定反应后的溶液中残留的硫酸浓度,实验小组进行如下探究。
(3)甲组:取1 mL反应液加水稀释至100 mL,再取10 mL稀释液与足量锌粒用下图装置进行测定。在读取反应前后量气管中液面读数时应先调节水准管与量气管中液面等高,这样操作的目的是
实验测得反应生成的氢气体积为22.4 mL(已换算到标准状况),计算原反应液中残留的硫酸浓度为

(4)乙组:欲通过加入足量的BaCl2溶液,测定生成的BaSO4沉淀质量来达到实验目的。该设计思路不可行,理由是
您最近一年使用:0次



