T℃时,某化学兴趣小组将1.0mL0.015mol/LKMnO4和1.5mol/LH2SO4的混合溶液与1.0mL0.15mol/L乙醛(CH3CHO)溶液混合后,得到c( )随时间变化的关系如图,已知反应原理为
)随时间变化的关系如图,已知反应原理为 +CH3CHO+H+→Mn2++CH3COOH+H2O(未配平)。下列说法正确的是
+CH3CHO+H+→Mn2++CH3COOH+H2O(未配平)。下列说法正确的是
 )随时间变化的关系如图,已知反应原理为
)随时间变化的关系如图,已知反应原理为 +CH3CHO+H+→Mn2++CH3COOH+H2O(未配平)。下列说法正确的是
+CH3CHO+H+→Mn2++CH3COOH+H2O(未配平)。下列说法正确的是
| A.可用浓盐酸和KMnO4配制成酸性KMnO4溶液 |
B.30.0~50.0s内, 的平均速率为0.54mol/(L·h) 的平均速率为0.54mol/(L·h) |
| C.0~30s的平均反应速率大于30~50s的原因是0~30s内生成物的浓度更小 |
D.该实验中反应的离子方程式为2 +5CH3CHO+6H+=2Mn2++5CH3COOH+3H2O +5CH3CHO+6H+=2Mn2++5CH3COOH+3H2O |
更新时间:2024-05-11 16:10:06
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】Wacker反应是利用Pd等催化烯烃氧化,其机理如下图:
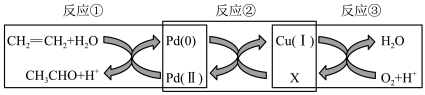
| A.反应①中氧化剂与还原剂的物质的量比为2∶1 |
| B.反应②中X为Cu(II) |
| C.该反应催化剂为Pd(Ⅱ)与Cu(I) |
| D.从总反应分析,该反应的原子利用率可达100% |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】因具有高能量密度的潜力,锂空气电池是改进当今储能技术的众多途径之一,锂空气电池电解法脱除煤中的含硫物质(主要是 )的原理如图所示。
)的原理如图所示。
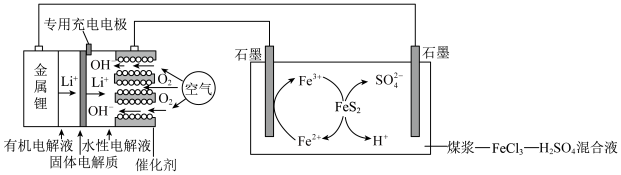
下列说法正确的是
 )的原理如图所示。
)的原理如图所示。
下列说法正确的是
A.充电时, 从阴极区移向阳极区 从阴极区移向阳极区 |
B.锂空气电池放电时,正极反应式为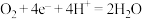 |
C.阳极石墨棒上有无色气体产生,该气体是 |
D.脱硫的化学方程式为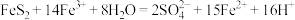 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】向体积为 的两密闭容器中各通入
的两密闭容器中各通入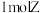 ,分别在恒温、绝热条件下发生:
,分别在恒温、绝热条件下发生: ,测得反应过程中体系压强随时间变化如图。下列说法不正确的是
,测得反应过程中体系压强随时间变化如图。下列说法不正确的是
 的两密闭容器中各通入
的两密闭容器中各通入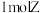 ,分别在恒温、绝热条件下发生:
,分别在恒温、绝热条件下发生: ,测得反应过程中体系压强随时间变化如图。下列说法不正确的是
,测得反应过程中体系压强随时间变化如图。下列说法不正确的是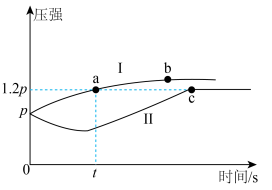
| A.曲线Ⅱ对应绝热条件 | B.曲线I、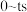 内: 内: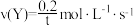 |
C.转化率: | D.平衡常数: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某反应物的浓度是1.0mol/L,经过20s后,它的浓度变成了0.2mol/L,在这20s内它的化学反应速率为
| A.0.01mol/(L·s) | B.0.04mol/(L·s) | C.0.08mol/(L·s) | D.0.05mol/(L·s) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列方案设计、现象和结论都正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 检验 溶液是否变质 溶液是否变质 | 取少量溶液于试管中,加入盐酸酸化的硝酸钡溶液 | 若产生白色沉淀,则说明已经变质 |
| B | 检验有机物 中的官能团 中的官能团 | 取少量该有机物于试管1中,加入新制氢氧化铜,加热;另取少量溴水于试管2中,滴加该有机物 | 若试管1产生砖红色沉淀,则证明有醛基;若试管2中溴水褪色,则证明存在碳碳双键 |
| C | 探究浓度对反应速率的影响 | 两支试管中均装有2ml0.01mol/L酸性高锰酸钾溶液,向第一支试管中加入2ml0.01mol/L的草酸溶液和3ml蒸馏水,第二支试管中加入5ml0.01mol/L的草酸溶液 | 第一支试管褪色时间比第二支试管长。说明其他条件相同时,反应物浓度越大反应速率越快 |
| D | 判断化合物组成中的化学键类型 | 将熔融状态下的HCl和NaCl进行导电性实验 | 不能导电的HCl由共价键形成;能导电的NaCl则由离子键形成 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关化学反应速率的认识正确的是( )
| A.对于任何化学反应来说,反应速率越大,反应现象就越明显 |
| B.化学反应速率是指一定时间内任何一种反应物浓度的减少或任何一种生成物浓度的增加 |
| C.选用适当的催化剂,分子运动加快,增加了碰撞频率,故反应速率增大 |
| D.增大反应物的量,化学反应速率不一定加快 |
您最近一年使用:0次

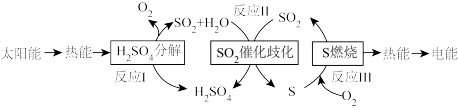
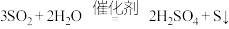
 可循环使用
可循环使用 C(g)+ D(g),在四种不同情况下的反应速率如下,其中表示反应进行得最快的是(
C(g)+ D(g),在四种不同情况下的反应速率如下,其中表示反应进行得最快的是(