利用 可实现对石膏中
可实现对石膏中 元素的脱除,涉及的主要反应如下:
元素的脱除,涉及的主要反应如下:
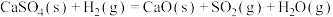
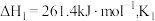

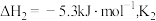
在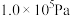 、
、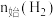 和
和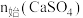 均为
均为 时,若仅考虑上述反应,平衡时各固体物质的物质的量随温度的变化关系如图所示。石膏中
时,若仅考虑上述反应,平衡时各固体物质的物质的量随温度的变化关系如图所示。石膏中 元素的脱除效果可用脱硫率
元素的脱除效果可用脱硫率 表示。下列说法
表示。下列说法不正确 的是
 可实现对石膏中
可实现对石膏中 元素的脱除,涉及的主要反应如下:
元素的脱除,涉及的主要反应如下: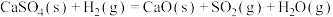
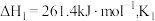

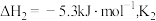
在
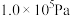 、
、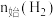 和
和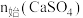 均为
均为 时,若仅考虑上述反应,平衡时各固体物质的物质的量随温度的变化关系如图所示。石膏中
时,若仅考虑上述反应,平衡时各固体物质的物质的量随温度的变化关系如图所示。石膏中 元素的脱除效果可用脱硫率
元素的脱除效果可用脱硫率 表示。下列说法
表示。下列说法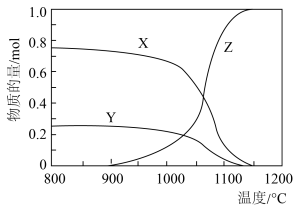
A.反应 的平衡常数 的平衡常数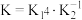 |
B.图中曲线 表示平衡时 表示平衡时 固体的物质的量随温度的变化 固体的物质的量随温度的变化 |
C.一定温度下,加入 固体或增大体系压强,均可提高平衡时的脱硫率 固体或增大体系压强,均可提高平衡时的脱硫率 |
D.其他条件不变,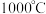 下, 下,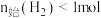 时, 时,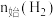 越多,平衡时的脱硫率越高 越多,平衡时的脱硫率越高 |
2024·江苏·二模 查看更多[3]
更新时间:2024-06-01 22:37:28
|
相似题推荐
多选题
|
较难
(0.4)
【推荐1】金属M的盐 ,溶液中存在平衡:
,溶液中存在平衡: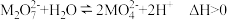 。分别在
。分别在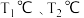 恒温条件下,向
恒温条件下,向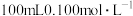 的
的 溶液中加入等量
溶液中加入等量 固体,持续搅拌下用
固体,持续搅拌下用 传感器连续测量溶液的
传感器连续测量溶液的 ,得到实验图象,下列说法错误的是
,得到实验图象,下列说法错误的是
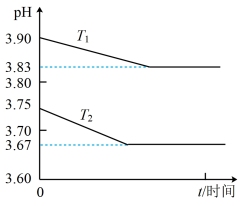
 ,溶液中存在平衡:
,溶液中存在平衡: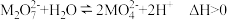 。分别在
。分别在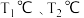 恒温条件下,向
恒温条件下,向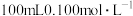 的
的 溶液中加入等量
溶液中加入等量 固体,持续搅拌下用
固体,持续搅拌下用 传感器连续测量溶液的
传感器连续测量溶液的 ,得到实验图象,下列说法错误的是
,得到实验图象,下列说法错误的是
A. |
B. 时平衡常数的数量级是 时平衡常数的数量级是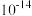 |
C.溶液中存在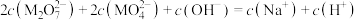 |
D. 温度下,加入 温度下,加入 ,固体再次达到平衡后, ,固体再次达到平衡后,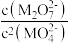 减小 减小 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐2】温度为T℃,压强为1.01×106Pa的条件下,某密闭容器内,下列反应达到化学平衡:A(g)+B(g) 3C(?),测得此时c(A)=0.022mol·L-1;压缩容器使压强增大到2.02×106Pa,第二次达到平衡时,测得c(A)=0.05mol·L-1;若继续压缩容器,使压强增大到4.04×106Pa,第三次达到平衡时,测得c(A)=0.075mol·L-1;则下列关于C物质状态的推测正确的是
3C(?),测得此时c(A)=0.022mol·L-1;压缩容器使压强增大到2.02×106Pa,第二次达到平衡时,测得c(A)=0.05mol·L-1;若继续压缩容器,使压强增大到4.04×106Pa,第三次达到平衡时,测得c(A)=0.075mol·L-1;则下列关于C物质状态的推测正确的是
 3C(?),测得此时c(A)=0.022mol·L-1;压缩容器使压强增大到2.02×106Pa,第二次达到平衡时,测得c(A)=0.05mol·L-1;若继续压缩容器,使压强增大到4.04×106Pa,第三次达到平衡时,测得c(A)=0.075mol·L-1;则下列关于C物质状态的推测正确的是
3C(?),测得此时c(A)=0.022mol·L-1;压缩容器使压强增大到2.02×106Pa,第二次达到平衡时,测得c(A)=0.05mol·L-1;若继续压缩容器,使压强增大到4.04×106Pa,第三次达到平衡时,测得c(A)=0.075mol·L-1;则下列关于C物质状态的推测正确的是| A.C为非气态 | B.C为气态 |
| C.第二次达到平衡时C为气态 | D.第三次达到平衡时C为非气态 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐1】在①、②、③容积不等的恒容密闭容器中,均充入0.lmolCO和0.2molH2,在催化剂的作用下发生反应:CO(g)+2H2(g)  CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:
CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:
下列说法正确的是
 CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示:
CH3OH(g)。测得三个容器中平衡混合物中CH3OH的体积分数随温度的变化如图所示: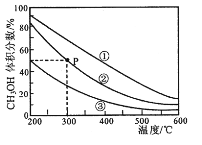
下列说法正确的是
| A.该反应的正反应为放热反应 |
| B.三个容器容积:①>②>③ |
| C.在P点,CO转化率为75% |
| D.在P点,向容器②中再充入CO、H2 及 CH3OH 各 0.025mol,此时 v(CO)正<v (CO)逆 |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐2】在起始时向 恒容密闭容器中加入
恒容密闭容器中加入 、
、 及
及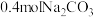 ,发生反应:
,发生反应: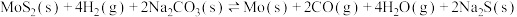 ,测得平衡时气体体积分数与温度的关系如图所示(固体物质所占体积忽略不计),下列说法正确的是
,测得平衡时气体体积分数与温度的关系如图所示(固体物质所占体积忽略不计),下列说法正确的是

 恒容密闭容器中加入
恒容密闭容器中加入 、
、 及
及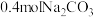 ,发生反应:
,发生反应: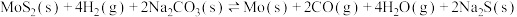 ,测得平衡时气体体积分数与温度的关系如图所示(固体物质所占体积忽略不计),下列说法正确的是
,测得平衡时气体体积分数与温度的关系如图所示(固体物质所占体积忽略不计),下列说法正确的是
| A.该反应的正反应为放热反应 |
B. 点与 点与 点的压强之比为 点的压强之比为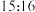 |
C. 点与 点与 点 点 的转化率之比为 的转化率之比为 |
D.若保持 点条件不变,再充入 点条件不变,再充入 、 、 及 及 各 各 ,则达平衡前v(正)<v(逆) ,则达平衡前v(正)<v(逆) |
您最近一年使用:0次
多选题
|
较难
(0.4)
名校
【推荐3】在四个恒容密闭容器中按左下表相应量充入气体,发生2N2O(g)  2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O平衡转化率如右下图所示:
2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O平衡转化率如右下图所示:
下列说法正确的是
 2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O平衡转化率如右下图所示:
2N2(g)+O2(g),容器Ⅰ、Ⅱ、Ⅲ中N2O平衡转化率如右下图所示:| 容器 | 容积/L | 起始物质的量/mol |  | ||
| N2O | N2 | O2 | |||
| Ⅰ | V1 | 0.1 | 0 | 0 | |
| Ⅱ | 1.0 | 0.1 | 0 | 0 | |
| Ⅲ | V3 | 0.1 | 0 | 0 | |
| Ⅳ | 1.0 | 0.06 | 0.06 | 0.04 | |
| A.该反应的正反应放热 |
| B.相同温度下反应时,平均反应速率:v(Ⅰ)>v(Ⅲ) |
| C.图中A、B、C三点处容器内总压强:P(Ⅰ)A<P(Ⅱ)B<P(Ⅲ)C |
| D.容器Ⅳ在470℃进行反应时,起始速率:v(N2O)正>v(N2O)逆 |
您最近一年使用:0次
多选题
|
较难
(0.4)
【推荐1】CO2催化重整CH4的反应:(Ⅰ)CH4(g)+CO2(g)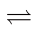 2CO(g)+2H2(g);ΔH1,
2CO(g)+2H2(g);ΔH1,
主要副反应:(Ⅱ)H2(g)+CO2(g)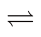 CO(g)+H2O(g);ΔH2>0,
CO(g)+H2O(g);ΔH2>0,
(Ⅲ)4H2(g)+CO2(g) CH4(g)+2H2O(g);ΔH3<0。
CH4(g)+2H2O(g);ΔH3<0。
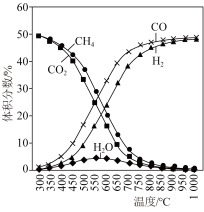
在恒容反应器中按体积分数V(CH4)∶V(CO2)=50%∶50%充入气体,加入催化剂,测得反应器中平衡时各物质的体积分数与温度的关系如图所示。下列说法正确的是( )
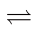 2CO(g)+2H2(g);ΔH1,
2CO(g)+2H2(g);ΔH1,主要副反应:(Ⅱ)H2(g)+CO2(g)
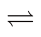 CO(g)+H2O(g);ΔH2>0,
CO(g)+H2O(g);ΔH2>0,(Ⅲ)4H2(g)+CO2(g)
 CH4(g)+2H2O(g);ΔH3<0。
CH4(g)+2H2O(g);ΔH3<0。在恒容反应器中按体积分数V(CH4)∶V(CO2)=50%∶50%充入气体,加入催化剂,测得反应器中平衡时各物质的体积分数与温度的关系如图所示。下列说法正确的是( )

| A.ΔH1=2ΔH2-ΔH3<0 |
| B.其他条件不变,适当增大起始时V(CH4)∶V(CO2),可抑制副反应(Ⅱ)、(Ⅲ)的进行 |
| C.300~580℃时,H2O的体积分数不断增大,是由于反应(Ⅲ)生成H2O的量大于反应(Ⅱ)消耗的量 |
| D.T℃时,在2.0L容器中加入2mol CH4、2mol CO2以及催化剂进行重整反应,测得CO2的平衡转化率为75%,则反应(Ⅰ)的平衡常数小于81 |
您最近一年使用:0次
【推荐2】T℃时,在恒容密闭容器中通入CH3OCH3,发生反应:CH3OCH3(g) CO(g)+H2(g)+CH4(g),测得容器内初始压强为41.6kPa,反应过程中反应速率v(CH3OCH3)、时间t与CH3OCH3分压p(CH3OCH3)的关系如图所示。下列说法正确的是
CO(g)+H2(g)+CH4(g),测得容器内初始压强为41.6kPa,反应过程中反应速率v(CH3OCH3)、时间t与CH3OCH3分压p(CH3OCH3)的关系如图所示。下列说法正确的是

 CO(g)+H2(g)+CH4(g),测得容器内初始压强为41.6kPa,反应过程中反应速率v(CH3OCH3)、时间t与CH3OCH3分压p(CH3OCH3)的关系如图所示。下列说法正确的是
CO(g)+H2(g)+CH4(g),测得容器内初始压强为41.6kPa,反应过程中反应速率v(CH3OCH3)、时间t与CH3OCH3分压p(CH3OCH3)的关系如图所示。下列说法正确的是
| A.t=400s时,CH3OCH3的转化率为0.16 |
| B.该温度下,要缩短达到平衡所需的时间,只可以使用催化剂 |
| C.平衡时,测得体系的总压强121.6 kPa,则该反应的平衡常数Kp=4000 |
| D.反应速率满足v(CH3OCH3)=k·p(CH3OCH3),t=400s时,v(CH3OCH3)=0.0154 kPa·s-1 |
您最近一年使用:0次
多选题
|
较难
(0.4)
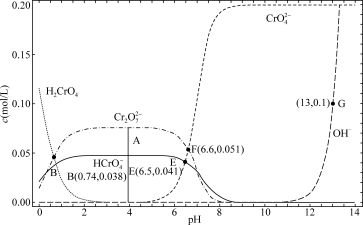
【推荐3】某温度下,改变
 溶液的pH时,各种含铬元素微粒及
溶液的pH时,各种含铬元素微粒及 浓度变化如图所示(已知
浓度变化如图所示(已知 是二元酸),下列说法中正确的是
是二元酸),下列说法中正确的是

 溶液的pH时,各种含铬元素微粒及
溶液的pH时,各种含铬元素微粒及 浓度变化如图所示(已知
浓度变化如图所示(已知 是二元酸),下列说法中正确的是
是二元酸),下列说法中正确的是
A.溶液中存在平衡 ,该温度下此反应的平衡常数 ,该温度下此反应的平衡常数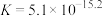 |
B.该温度下的中性溶液的 |
C.向10 mL   溶液中滴入几滴 溶液中滴入几滴  溶液,溶液橙色变浅 溶液,溶液橙色变浅 |
D.B点溶液中存在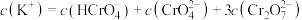 |
您最近一年使用:0次

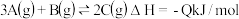 。在3个密闭容器中,按下列方式投入反应物:Ⅰ
。在3个密闭容器中,按下列方式投入反应物:Ⅰ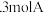 、1molB; Ⅱ
、1molB; Ⅱ 、2molB; Ⅲ
、2molB; Ⅲ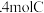 。则在保持恒温恒容反应达到平衡时,下列选项正确的是
。则在保持恒温恒容反应达到平衡时,下列选项正确的是

