铁元素在人体健康和新材料研发中有重要的应用。
I.在血液中,以 为中心的配位化合物铁卟啉是血红蛋白的重要组成部分,可用于输送
为中心的配位化合物铁卟啉是血红蛋白的重要组成部分,可用于输送 ,下图为载氧后的血红蛋白分子示意图:
,下图为载氧后的血红蛋白分子示意图:_________ 。
(2)载氧时,血红蛋白分子中 脱去配位的
脱去配位的 并与
并与 配位;若人体吸入CO,则CO占据配位点,血红蛋白失去携氧功能。由此推测,与
配位;若人体吸入CO,则CO占据配位点,血红蛋白失去携氧功能。由此推测,与 配位能力最强的是
配位能力最强的是_________ (填字母)。
a. b.
b. c.CO
c.CO
(3)一种最简单的卟啉环结构如图:_________ 。
②比较C和N的电负性大小,并从原子结构角度说明理由:_________ 。
③该卟啉分子在酸性环境中配位能力会减弱,原因是_________ 。
Ⅱ. 可用于制备优良铁磁体材料。下图是一种铁磁体化合物的立方晶胞,其边长为a pm。
可用于制备优良铁磁体材料。下图是一种铁磁体化合物的立方晶胞,其边长为a pm。 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。
(4)该晶体的密度是_________  。
。
(5)距离F最近的Cs的个数为_________ 。
I.在血液中,以
 为中心的配位化合物铁卟啉是血红蛋白的重要组成部分,可用于输送
为中心的配位化合物铁卟啉是血红蛋白的重要组成部分,可用于输送 ,下图为载氧后的血红蛋白分子示意图:
,下图为载氧后的血红蛋白分子示意图: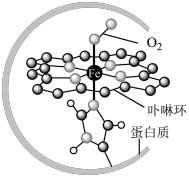
(2)载氧时,血红蛋白分子中
 脱去配位的
脱去配位的 并与
并与 配位;若人体吸入CO,则CO占据配位点,血红蛋白失去携氧功能。由此推测,与
配位;若人体吸入CO,则CO占据配位点,血红蛋白失去携氧功能。由此推测,与 配位能力最强的是
配位能力最强的是a.
 b.
b. c.CO
c.CO (3)一种最简单的卟啉环结构如图:
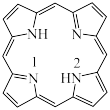
②比较C和N的电负性大小,并从原子结构角度说明理由:
③该卟啉分子在酸性环境中配位能力会减弱,原因是
Ⅱ.
 可用于制备优良铁磁体材料。下图是一种铁磁体化合物的立方晶胞,其边长为a pm。
可用于制备优良铁磁体材料。下图是一种铁磁体化合物的立方晶胞,其边长为a pm。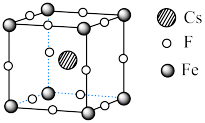
 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。(4)该晶体的密度是
 。
。(5)距离F最近的Cs的个数为
2024·北京海淀·二模 查看更多[3]
北京市海淀区2023-2024学年高三下学期期末练习(二模)化学试题天津市耀华中学2024届高三下学期第二次模拟化学试题(已下线)期末押题卷01-【好题汇编】备战2023-2024学年高二化学下学期期末真题分类汇编(上海专用)
更新时间:2024-05-11 20:32:58
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】材料是人类进步的基石,深入认识物质的结构有助于进一步开发新的材料。回答下列问题:
(1)按照杂化轨道理论,基态B原子的价电子先激发,再杂化成键形成BCl3。杂化前,处于激发态的B原子的价电子轨道表示式为_______ ( 选填标号)。
(2)已知:第四周期中3d轨道上没有未成对电子的过渡元素离子的水合离子为无色。下列离子形成的水合离子为无色的是_______。
(3)K3[Fe(CN)6]中所含元素电负性由大到小的顺序为_______ ,lmol K3[Fe(CN)6]含有_______ molσ键;Ti3+能形成化合物[TiCl(H2O)5]Cl2·H2O,该化合物中Ti3+的配位数为_______ 。
(4)Ni(CO)4常温下呈液态,其分子空间构型为正四面体。解释其易溶于CCl4、苯等有机溶剂的原因:_______ 。
(5)纯水电离产生H3O+、OH-,研究发现在某些水溶液中还存在 、
、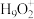 等微粒。
等微粒。
①H2O分子的键角小于H3O+离子的键角,原因是_______ 。
②画出 可能的一种结构式
可能的一种结构式_______ 。
(6)TiO2通过氮掺杂反应生成TiO2-xNy,表示如图。
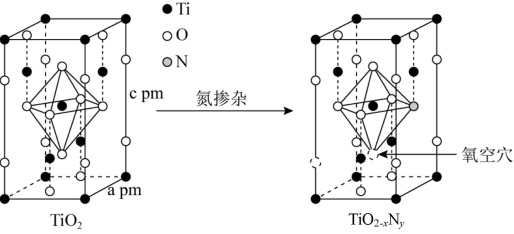
①立方晶系TiO2晶胞参数如图甲所示,若用NA表示阿伏加德罗常数,其晶体的密度为_______ g/cm3。
②图乙的结构可用化学式TiO2-xNy表示,其中x=_______ 。
(1)按照杂化轨道理论,基态B原子的价电子先激发,再杂化成键形成BCl3。杂化前,处于激发态的B原子的价电子轨道表示式为_______ ( 选填标号)。
A.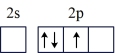 | B.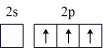 |
C.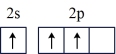 | D.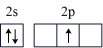 |
| A.Sc3+ | B.Cr3+ | C.Fe3+ | D.Zn2+ |
(4)Ni(CO)4常温下呈液态,其分子空间构型为正四面体。解释其易溶于CCl4、苯等有机溶剂的原因:
(5)纯水电离产生H3O+、OH-,研究发现在某些水溶液中还存在
 、
、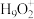 等微粒。
等微粒。①H2O分子的键角小于H3O+离子的键角,原因是
②画出
 可能的一种结构式
可能的一种结构式(6)TiO2通过氮掺杂反应生成TiO2-xNy,表示如图。

①立方晶系TiO2晶胞参数如图甲所示,若用NA表示阿伏加德罗常数,其晶体的密度为
②图乙的结构可用化学式TiO2-xNy表示,其中x=
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
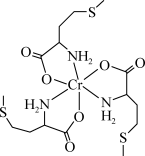
【推荐2】蛋氨酸铬(Ⅲ)配合物是一种治疗Ⅱ型糖尿病的药物,其结构简式如图所示,请回答下列问题:___________ 。
(2)基态 原子的价层电子排布式是
原子的价层电子排布式是___________ 。金属离子外层未排满的d轨道可以存取电子,降低活化能,使分解反应容易发生。根据该原理,下列金属离子能催化双氧水分解的是___________ 。(填写序号)
A. B.
B. C.
C.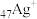 D.
D.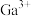
(3)蛋氨酸铬(Ⅲ)配合物的中心铬离子的配位数为___________ ,氮原子的杂化方式为___________ 。
(4)化学式为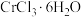 的化合物有三种结构,分别呈紫罗兰色、暗绿色、亮绿色,且
的化合物有三种结构,分别呈紫罗兰色、暗绿色、亮绿色,且 的配位数均为6,将它们配制成等体积等物质的量浓度的溶液,分别加入足量
的配位数均为6,将它们配制成等体积等物质的量浓度的溶液,分别加入足量 溶液,依次所得
溶液,依次所得 沉淀的物质的量之比为
沉淀的物质的量之比为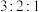 ,则呈亮绿色的配合物,其配离子可表示为
,则呈亮绿色的配合物,其配离子可表示为___________ 。 分子与
分子与 形成配位键后
形成配位键后 键角
键角___________ (填“变大”“变小”或“不变”)。
(5)氮化铬的晶体结构类型与氯化钠相似,其晶胞结构如图所示。已知氮化铬的晶体密度为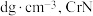 摩尔质量为
摩尔质量为 为阿伏加德罗常数的值,则立方体晶胞的边长为
为阿伏加德罗常数的值,则立方体晶胞的边长为___________  (
( ,列出表达式)。
,列出表达式)。
(2)基态
 原子的价层电子排布式是
原子的价层电子排布式是A.
 B.
B. C.
C.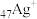 D.
D.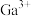
(3)蛋氨酸铬(Ⅲ)配合物的中心铬离子的配位数为
(4)化学式为
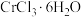 的化合物有三种结构,分别呈紫罗兰色、暗绿色、亮绿色,且
的化合物有三种结构,分别呈紫罗兰色、暗绿色、亮绿色,且 的配位数均为6,将它们配制成等体积等物质的量浓度的溶液,分别加入足量
的配位数均为6,将它们配制成等体积等物质的量浓度的溶液,分别加入足量 溶液,依次所得
溶液,依次所得 沉淀的物质的量之比为
沉淀的物质的量之比为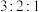 ,则呈亮绿色的配合物,其配离子可表示为
,则呈亮绿色的配合物,其配离子可表示为 分子与
分子与 形成配位键后
形成配位键后 键角
键角(5)氮化铬的晶体结构类型与氯化钠相似,其晶胞结构如图所示。已知氮化铬的晶体密度为
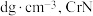 摩尔质量为
摩尔质量为 为阿伏加德罗常数的值,则立方体晶胞的边长为
为阿伏加德罗常数的值,则立方体晶胞的边长为 (
( ,列出表达式)。
,列出表达式)。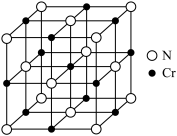
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐3】以红土镍矿(主要成分是 ,含
,含 (等)为原料制备硝酸镍的流程如图所示:
(等)为原料制备硝酸镍的流程如图所示:

注: 为
为 和
和 的混合气体。回答下列问题:
的混合气体。回答下列问题:
(1)基态镍原子价电子排布式为_______ 。
(2)“除铁铝”阶段需要先用 溶液将
溶液将 氧化为
氧化为 。
。 属于
属于_______ (“极性”或“非极性”)分子。
(3)“除镁钙”阶段为加入 除尽
除尽 ,除
,除 后的滤液中
后的滤液中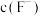 至少应为
至少应为_______  [当溶液中某离子浓度小于
[当溶液中某离子浓度小于 时,可认为该离子沉淀完全。已知该实验条件下
时,可认为该离子沉淀完全。已知该实验条件下 ,
, ]。
]。
(4)“净化液电解”阶段,析镍过程中存在竞争反应,该竞争反应的电极反应式为_______ 。
(5)工业制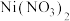 成品时,先用硝酸将
成品时,先用硝酸将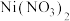 溶液酸化至
溶液酸化至 ,再经减压蒸发浓缩,然后冷却结晶、离心分离。其中“减压蒸发”的目的是
,再经减压蒸发浓缩,然后冷却结晶、离心分离。其中“减压蒸发”的目的是_______ (任答两点)。
(6)工业上用 溶液吸收
溶液吸收 制备硝酸钠,其流程如图所示:
制备硝酸钠,其流程如图所示:
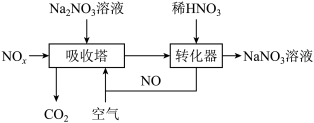
①吸收塔得到 、
、 混合溶液。键角:
混合溶液。键角:
_______  (填“>”、“=”或“<”),
(填“>”、“=”或“<”), 、N、O三种元素中电负性最大的是
、N、O三种元素中电负性最大的是_______ (填元素符号)。
②写出转化器中发生反应的化学方程式:_______ 。
 ,含
,含 (等)为原料制备硝酸镍的流程如图所示:
(等)为原料制备硝酸镍的流程如图所示:
注:
 为
为 和
和 的混合气体。回答下列问题:
的混合气体。回答下列问题:(1)基态镍原子价电子排布式为
(2)“除铁铝”阶段需要先用
 溶液将
溶液将 氧化为
氧化为 。
。 属于
属于(3)“除镁钙”阶段为加入
 除尽
除尽 ,除
,除 后的滤液中
后的滤液中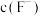 至少应为
至少应为 [当溶液中某离子浓度小于
[当溶液中某离子浓度小于 时,可认为该离子沉淀完全。已知该实验条件下
时,可认为该离子沉淀完全。已知该实验条件下 ,
, ]。
]。(4)“净化液电解”阶段,析镍过程中存在竞争反应,该竞争反应的电极反应式为
(5)工业制
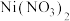 成品时,先用硝酸将
成品时,先用硝酸将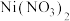 溶液酸化至
溶液酸化至 ,再经减压蒸发浓缩,然后冷却结晶、离心分离。其中“减压蒸发”的目的是
,再经减压蒸发浓缩,然后冷却结晶、离心分离。其中“减压蒸发”的目的是(6)工业上用
 溶液吸收
溶液吸收 制备硝酸钠,其流程如图所示:
制备硝酸钠,其流程如图所示:
①吸收塔得到
 、
、 混合溶液。键角:
混合溶液。键角:
 (填“>”、“=”或“<”),
(填“>”、“=”或“<”), 、N、O三种元素中电负性最大的是
、N、O三种元素中电负性最大的是②写出转化器中发生反应的化学方程式:
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐1】I.铬单质硬度大,耐腐蚀,是重要的合金材料。
(1)基态铬原子的价电子轨道表示式为_______ ;CrO2Cl2常温下为深红色液体,能与CCl4互溶,据此判断CrO2Cl2的晶体类型属于_______ 。
(2)配合物CrCl3·6H2O的配位数为6,它有三种不同组成、不同颜色的固体,其中一种为浅绿色固体,该固体与足量硝酸银溶液反应时,0.5mol固体可生成1mol氯化银沉淀,则这种浅绿色固体的配体个数比(Cl-:H2O)为_______ 。
II.砷化镓为第三代半导体材料,晶胞结构如图所示:

(3)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的化学方程式为_______ 。
(4)AsH3分子的立体构型为_______ ,其中As原子的杂化方式是_______ 。1个(CH3)3Ga分子中含有_______ 个σ键,砷的第一电离能_______ (填“>”或“<”)镓的第一电离能。
(5)砷化镓晶体中砷和镓的最近原子核间距为a nm,砷化镓的摩尔质量为bg·mol-1,阿伏伽德罗常数值为NA,则砷化镓晶体的密度表达式是_______ g·cm-3.
(1)基态铬原子的价电子轨道表示式为
(2)配合物CrCl3·6H2O的配位数为6,它有三种不同组成、不同颜色的固体,其中一种为浅绿色固体,该固体与足量硝酸银溶液反应时,0.5mol固体可生成1mol氯化银沉淀,则这种浅绿色固体的配体个数比(Cl-:H2O)为
II.砷化镓为第三代半导体材料,晶胞结构如图所示:

(3)砷化镓可由(CH3)3Ga和AsH3在700℃下反应制得,反应的化学方程式为
(4)AsH3分子的立体构型为
(5)砷化镓晶体中砷和镓的最近原子核间距为a nm,砷化镓的摩尔质量为bg·mol-1,阿伏伽德罗常数值为NA,则砷化镓晶体的密度表达式是
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】锌、铁、铜及其化合物在生活、生产中有着广泛应用。回答下列问题:
(1)基态 Fe3+的核外电子排布式为__________ 。在第四周期过渡元素中,基态原子未成对电子数最多的元素为 ________ (用元素符号表示)。
(2)一水合甘氨酸锌[(H2NCH2COO)2Zn·H2O]是一种饲料添加剂,该化合物中所涉及的 第二周期元素的第一电离能由大到小的顺序是_________ (用元素符号表示);
(3) Fe3+可与噻吩(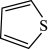 )和吡咯(
)和吡咯(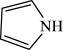 )形成配位化合物。噻吩、吡咯是类似于苯的芳香化合物,环中的五个原子形成了大π键。噻吩中C原子和S原子的杂化分式分别为:
)形成配位化合物。噻吩、吡咯是类似于苯的芳香化合物,环中的五个原子形成了大π键。噻吩中C原子和S原子的杂化分式分别为:__________ 。噻吩难溶于水,吡咯能溶于水,原因为:___________ 。
(4)磷酸铁(FePO4)可用于制造磷酸铁锂电池材料,PO 的空间构型
的空间构型 _________ 。
(5) 某种铜的氯化物晶体结构如图所示。此晶体中铜原子的配位数是_________ ;设晶胞参数为 a nm,则该铜的氯化物晶体的密度为 _________ g·cm-3。(用含 a 和 NA的式子表示,NA为阿伏加德罗常数)

(1)基态 Fe3+的核外电子排布式为
(2)一水合甘氨酸锌[(H2NCH2COO)2Zn·H2O]是一种饲料添加剂,该化合物中所涉及的 第二周期元素的第一电离能由大到小的顺序是
(3) Fe3+可与噻吩(
 )和吡咯(
)和吡咯( )形成配位化合物。噻吩、吡咯是类似于苯的芳香化合物,环中的五个原子形成了大π键。噻吩中C原子和S原子的杂化分式分别为:
)形成配位化合物。噻吩、吡咯是类似于苯的芳香化合物,环中的五个原子形成了大π键。噻吩中C原子和S原子的杂化分式分别为:(4)磷酸铁(FePO4)可用于制造磷酸铁锂电池材料,PO
 的空间构型
的空间构型 (5) 某种铜的氯化物晶体结构如图所示。此晶体中铜原子的配位数是

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】硼原子有3个价电子,但有4个价轨道,这种价电子数少于价轨道数的原子称作缺电子原子。因此,硼的一些化合物表现出缺电子特征。回答下列问题:
(1)BF3与NH3可通过___________ 键形成氨合三氟化硼(BF3·NH3),在该键中由___________ 原子提供空轨道。
(2)硼酸分子结构简式可写为B(OH)3,其晶体为层型片状结构,容易在层与层之间裂解,这是因为在平面层内硼酸分子之间通过___________ 结合,而层与层之间通过___________ 结合。
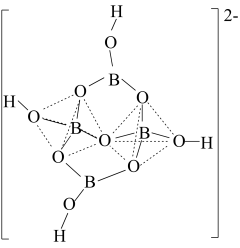
(3)硼砂是硼含氧酸的重要钠盐,其阴离子的结构如图所示,其中B原子的杂化方式为___________ 。硼砂晶体中结晶水与硼的物质的量比为2:1,硼砂的化学式为___________ 。
(4)固态硼化物可用作耐火材料、火箭外壳和涡轮机的叶片等,在超导领域也有重要应用潜质。如图为一种金属钙硼化物的立方晶胞,该化合物的化学式为___________ ,钙原子的配位数为___________ 。若由硼原子组成的正八面体棱长为apm,连接两个八面体的B—B键长为bpm,该物质的密度为___________ g·cm-3(列表达式)。
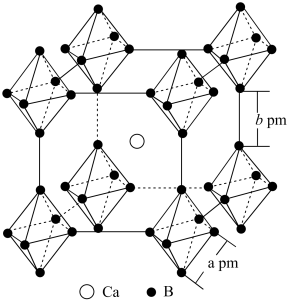
(1)BF3与NH3可通过
(2)硼酸分子结构简式可写为B(OH)3,其晶体为层型片状结构,容易在层与层之间裂解,这是因为在平面层内硼酸分子之间通过
(3)硼砂是硼含氧酸的重要钠盐,其阴离子的结构如图所示,其中B原子的杂化方式为

(4)固态硼化物可用作耐火材料、火箭外壳和涡轮机的叶片等,在超导领域也有重要应用潜质。如图为一种金属钙硼化物的立方晶胞,该化合物的化学式为

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】硼族元素可形成许多结构和性质特殊的化合物。回答下列问题
(1)基态Ga原子的电子排布式为___________ 。
(2)常温下,F2与硼单质反应生成BF3,BF3为缺电子结构,通入水中产生三种酸分别为HBF4、HF和___________ (填化学式)。NF3和NF3BF3中F-N-F的键角大小是NF3___________ NF3BF3(填“>”、“<”或“=”)。
(3)一定条件下,NH4F、NaF和NaAlO2反应生成NH3、H2O和化合物X。X晶胞及晶胞中某一原子的俯视投影如图所示。___________ 。
②X晶体内含有的作用力有___________ (填字母)。
a.配位键 b.离子键 c.氢键 d.金属键
(4)解释H2N-NH2,HO-OH,H3C-CH3中,N-N,O-O,C-C的键能O-O<N-N<C-C___________ 。
(1)基态Ga原子的电子排布式为
(2)常温下,F2与硼单质反应生成BF3,BF3为缺电子结构,通入水中产生三种酸分别为HBF4、HF和
(3)一定条件下,NH4F、NaF和NaAlO2反应生成NH3、H2O和化合物X。X晶胞及晶胞中某一原子的俯视投影如图所示。
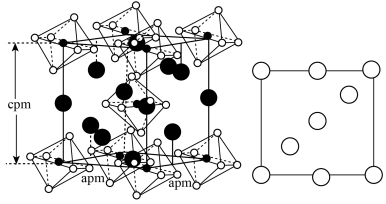
②X晶体内含有的作用力有
a.配位键 b.离子键 c.氢键 d.金属键
(4)解释H2N-NH2,HO-OH,H3C-CH3中,N-N,O-O,C-C的键能O-O<N-N<C-C
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐2】氮元素可以形成许多化合物,在我们生活生产中有广泛的应用。
(1)与NF3分子互为等电子体的分子为________ 。
(2)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构见图甲。
写出Fe3+的基态电子排布式________ 。
写出该反应的化学方程式:______________ 。
(3)维生素B4结构如图乙,则1mol维生素B4分子中含有σ键的数目为______ mol。
(4)配合物丙的结构见图,丙中含有__________ (填序号);
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
丙中碳原子的杂化方式有______________ 。
(1)与NF3分子互为等电子体的分子为
(2)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构见图甲。
写出Fe3+的基态电子排布式
写出该反应的化学方程式:
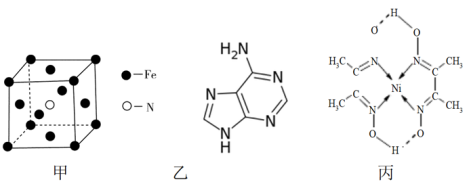
(3)维生素B4结构如图乙,则1mol维生素B4分子中含有σ键的数目为
(4)配合物丙的结构见图,丙中含有
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
丙中碳原子的杂化方式有
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】因瓦合金俗称殷钢,是一种镍铁合金,由于其膨胀系数极小,又称不变合金,适合做测量元件。回答下列问题:
 基态镍原子的价电子轨道表达式为
基态镍原子的价电子轨道表达式为____ ;铁的基态原子核外未成对电子数为___ 个。
 丁二酮肟
丁二酮肟 分子式为
分子式为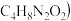 所含的碳、氮、氧三种元素中第一电离能最大的是
所含的碳、氮、氧三种元素中第一电离能最大的是_____  填元素符号
填元素符号 。在稀氨水介质中,
。在稀氨水介质中, 与丁二酮肟
与丁二酮肟 分子式为
分子式为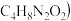 反应可生成鲜红色沉淀,其分子结构如图所示,该结构中碳原子的杂化方式为
反应可生成鲜红色沉淀,其分子结构如图所示,该结构中碳原子的杂化方式为_______ ;该结构中除含极性键、非极性键、配位键外,还含有__________ 。
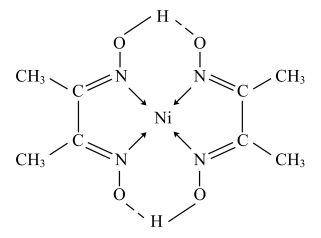
 铁、镍易与CO作用形成羰基配合物
铁、镍易与CO作用形成羰基配合物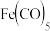 、
、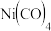 。1个
。1个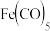 分子中含有
分子中含有 键数目为
键数目为_______ ;已知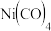 分子为正四面体构型,下列溶剂能够溶解
分子为正四面体构型,下列溶剂能够溶解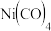 的是
的是_______  填写字母
填写字母 。
。
A.四氯化碳 苯
苯  水
水  液氨
液氨
 经查氯化亚铁的熔点为
经查氯化亚铁的熔点为 ,沸点为
,沸点为 ;而氯化铁的熔点为
;而氯化铁的熔点为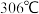 ,沸点为
,沸点为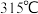 。二者熔沸点差异较大的原因是
。二者熔沸点差异较大的原因是___________ 。
 晶体中,
晶体中,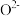 的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的
的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的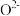 围成的正四面体空隙和3、6、7、8、9、12的
围成的正四面体空隙和3、6、7、8、9、12的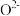 围成的正八面体空隙;
围成的正八面体空隙;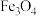 中有一半的
中有一半的 填充在正四面体空隙中,另一半
填充在正四面体空隙中,另一半 和
和 填充在正八面体空隙中。则
填充在正八面体空隙中。则 晶体中,正四面体空隙数与
晶体中,正四面体空隙数与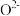 数之比为
数之比为_______ 。 晶体密度为
晶体密度为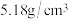 ,请计算
,请计算
_______ 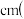 写出计算表达式即可
写出计算表达式即可 。
。

 基态镍原子的价电子轨道表达式为
基态镍原子的价电子轨道表达式为 丁二酮肟
丁二酮肟 分子式为
分子式为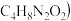 所含的碳、氮、氧三种元素中第一电离能最大的是
所含的碳、氮、氧三种元素中第一电离能最大的是 填元素符号
填元素符号 。在稀氨水介质中,
。在稀氨水介质中, 与丁二酮肟
与丁二酮肟 分子式为
分子式为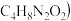 反应可生成鲜红色沉淀,其分子结构如图所示,该结构中碳原子的杂化方式为
反应可生成鲜红色沉淀,其分子结构如图所示,该结构中碳原子的杂化方式为
 铁、镍易与CO作用形成羰基配合物
铁、镍易与CO作用形成羰基配合物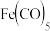 、
、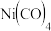 。1个
。1个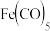 分子中含有
分子中含有 键数目为
键数目为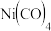 分子为正四面体构型,下列溶剂能够溶解
分子为正四面体构型,下列溶剂能够溶解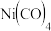 的是
的是 填写字母
填写字母 。
。 A.四氯化碳
 苯
苯 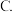 水
水  液氨
液氨  经查氯化亚铁的熔点为
经查氯化亚铁的熔点为 ,沸点为
,沸点为 ;而氯化铁的熔点为
;而氯化铁的熔点为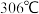 ,沸点为
,沸点为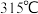 。二者熔沸点差异较大的原因是
。二者熔沸点差异较大的原因是 晶体中,
晶体中,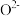 的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的
的重复排列方式如图所示,该排列方式中存在着由如1、3、6、7的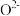 围成的正四面体空隙和3、6、7、8、9、12的
围成的正四面体空隙和3、6、7、8、9、12的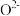 围成的正八面体空隙;
围成的正八面体空隙;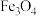 中有一半的
中有一半的 填充在正四面体空隙中,另一半
填充在正四面体空隙中,另一半 和
和 填充在正八面体空隙中。则
填充在正八面体空隙中。则 晶体中,正四面体空隙数与
晶体中,正四面体空隙数与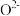 数之比为
数之比为 晶体密度为
晶体密度为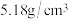 ,请计算
,请计算
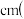 写出计算表达式即可
写出计算表达式即可 。
。 
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐1】碳及其化合物的资源化利用在生产、生活中具有重要的意义。回答下列问题:
I.汽车尾气的处理:2CO(g)+2NO(g) 2CO2(g)+N2(g) △H=-620.4kJ•mol-1。该反应的反应历程及反应物和生成物的相对能量如图所示:
2CO2(g)+N2(g) △H=-620.4kJ•mol-1。该反应的反应历程及反应物和生成物的相对能量如图所示:
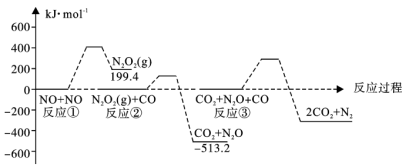
(1)反应______ (填“①”“②”或“③”)是该反应的决速步骤。
(2)反应③的焓变△H=______ kJ•mol-1。
II.向一恒容密闭容器中,充入1molCO气体和一定量的NO气体发生反应:2CO(g)+2NO(g) 2CO2(g)+N2(g),如图是3种投料比[n(CO):n(NO)]分别为2∶1、1∶1、1∶2时,反应温度对CO平衡转化率的影响曲线。
2CO2(g)+N2(g),如图是3种投料比[n(CO):n(NO)]分别为2∶1、1∶1、1∶2时,反应温度对CO平衡转化率的影响曲线。
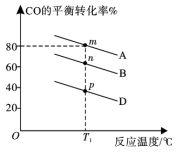
(3)图中表示投料比为2∶1的曲线是______ 。
(4)m点NO的逆反应速率_____ n点NO的正反应速率(填“>”“<”或“=”)。
(5)已知T1条件下,投料比为1∶2时,起始容器内气体的总压强为3MPa,则T1℃时该反应的平衡常数Kp=______ (MPa)-1(保留两位小数,以分压表示,气体分压=总压×物质的量分数);p点时,再向容器中充入NO和CO2,使二者分压均增大为原来的2倍,达到平衡时CO的转化率_______ (填“增大”“减小”或“不变”)。
III.利用光电催化将CO2还原为CO是很有前景的研究方向,CsPbBr3是一种重要光电池材料,其晶胞模型如图a所示,为更清晰地表示晶胞中原子所在的位置,常将立体晶胞结构转化为平面投影图,例如沿CsPbBr3晶胞的c轴将原子投影到ab平面,即可用图b表示。
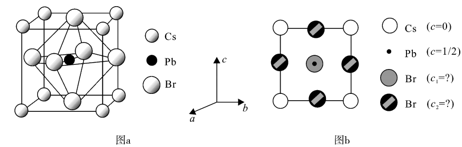
(6)图b中c1=______ ,c2=______ ;晶胞参数为apm,CsPbBr3的密度为______ g•cm-3 (设NA表示阿伏加德罗常数的值)。
I.汽车尾气的处理:2CO(g)+2NO(g)
 2CO2(g)+N2(g) △H=-620.4kJ•mol-1。该反应的反应历程及反应物和生成物的相对能量如图所示:
2CO2(g)+N2(g) △H=-620.4kJ•mol-1。该反应的反应历程及反应物和生成物的相对能量如图所示:
(1)反应
(2)反应③的焓变△H=
II.向一恒容密闭容器中,充入1molCO气体和一定量的NO气体发生反应:2CO(g)+2NO(g)
 2CO2(g)+N2(g),如图是3种投料比[n(CO):n(NO)]分别为2∶1、1∶1、1∶2时,反应温度对CO平衡转化率的影响曲线。
2CO2(g)+N2(g),如图是3种投料比[n(CO):n(NO)]分别为2∶1、1∶1、1∶2时,反应温度对CO平衡转化率的影响曲线。
(3)图中表示投料比为2∶1的曲线是
(4)m点NO的逆反应速率
(5)已知T1条件下,投料比为1∶2时,起始容器内气体的总压强为3MPa,则T1℃时该反应的平衡常数Kp=
III.利用光电催化将CO2还原为CO是很有前景的研究方向,CsPbBr3是一种重要光电池材料,其晶胞模型如图a所示,为更清晰地表示晶胞中原子所在的位置,常将立体晶胞结构转化为平面投影图,例如沿CsPbBr3晶胞的c轴将原子投影到ab平面,即可用图b表示。

(6)图b中c1=
您最近一年使用:0次
【推荐2】铋酸钠( )是一种可测定锰的强氧化剂。由辉铋矿(主要成分为
)是一种可测定锰的强氧化剂。由辉铋矿(主要成分为 ,含
,含 、
、 、
、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下:
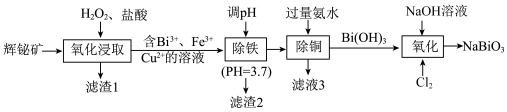
已知:① 易水解,
易水解, 难溶于冷水,与热水反应,
难溶于冷水,与热水反应, 不溶于水。
不溶于水。
②“氧化浸取”时,硫元素转化为硫单质。
③常温下,有关金属离子开始沉淀和沉淀完全的 如表:
如表:
回答下列问题:
(1)基态 的
的 电子轨道表示式为
电子轨道表示式为____________ 。“滤渣1”的主要成分为_____________ (填化学式)。
(2)“氧化浸取”过程中,需要控制温度不超过40℃的原因是____________ , 发生反应的化学方程式为
发生反应的化学方程式为____________ 。
(3)已知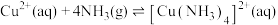 ,
, 中配体的空间结构为
中配体的空间结构为_____________ ,键角:
______  (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是_____________ 。
(4)“氧化”过程发生反应的离子方程式为____________ 。
(5)取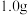 制得的
制得的 产品,加入足量稀硫酸和
产品,加入足量稀硫酸和 稀溶液,发生反应:
稀溶液,发生反应: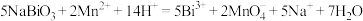 ,完全反应后再用
,完全反应后再用 的
的 标准溶液滴定生成的
标准溶液滴定生成的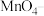 ,当溶液紫红色恰好褪去时,消耗
,当溶液紫红色恰好褪去时,消耗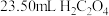 标准溶液,则产品的纯度为
标准溶液,则产品的纯度为___________________ %。
(6)我国科学家对新型二维半导体芯片材料——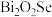 的研究取得了突破性进展。
的研究取得了突破性进展。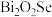 的晶胞结构中
的晶胞结构中 的位置如图所示(略去
的位置如图所示(略去 、
、 ),已知晶胞为竖直的长方体,高为
),已知晶胞为竖直的长方体,高为 ,晶体密度为
,晶体密度为 。设
。设 为阿伏加德罗常数的值,则晶胞底边边长
为阿伏加德罗常数的值,则晶胞底边边长
_______________ (填含 、
、 、
、 的计算式,不必化简)。
的计算式,不必化简)。

 )是一种可测定锰的强氧化剂。由辉铋矿(主要成分为
)是一种可测定锰的强氧化剂。由辉铋矿(主要成分为 ,含
,含 、
、 、
、 等杂质)制备
等杂质)制备 的工艺流程如下:
的工艺流程如下:
已知:①
 易水解,
易水解, 难溶于冷水,与热水反应,
难溶于冷水,与热水反应, 不溶于水。
不溶于水。②“氧化浸取”时,硫元素转化为硫单质。
③常温下,有关金属离子开始沉淀和沉淀完全的
 如表:
如表:| 金属离子 |  |  |  |  |
开始沉淀的 | 7.6 | 2.7 | 4.8 | 4.5 |
沉淀完全的 | 9.6 | 3.7 | 6.4 | 5.5 |
(1)基态
 的
的 电子轨道表示式为
电子轨道表示式为(2)“氧化浸取”过程中,需要控制温度不超过40℃的原因是
 发生反应的化学方程式为
发生反应的化学方程式为(3)已知
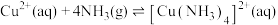 ,
, 中配体的空间结构为
中配体的空间结构为
 (填“>”、“<”或“=”),原因是
(填“>”、“<”或“=”),原因是(4)“氧化”过程发生反应的离子方程式为
(5)取
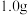 制得的
制得的 产品,加入足量稀硫酸和
产品,加入足量稀硫酸和 稀溶液,发生反应:
稀溶液,发生反应: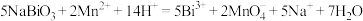 ,完全反应后再用
,完全反应后再用 的
的 标准溶液滴定生成的
标准溶液滴定生成的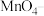 ,当溶液紫红色恰好褪去时,消耗
,当溶液紫红色恰好褪去时,消耗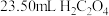 标准溶液,则产品的纯度为
标准溶液,则产品的纯度为(6)我国科学家对新型二维半导体芯片材料——
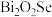 的研究取得了突破性进展。
的研究取得了突破性进展。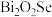 的晶胞结构中
的晶胞结构中 的位置如图所示(略去
的位置如图所示(略去 、
、 ),已知晶胞为竖直的长方体,高为
),已知晶胞为竖直的长方体,高为 ,晶体密度为
,晶体密度为 。设
。设 为阿伏加德罗常数的值,则晶胞底边边长
为阿伏加德罗常数的值,则晶胞底边边长
 、
、 、
、 的计算式,不必化简)。
的计算式,不必化简)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
【推荐3】砷是生命的第七元素,可形成多种重要的化合物。回答下列问题:
(1)基态砷原子N电子层中的成对电子与单电子的数量比为_______ 。As的第一电离能比Se大的原因是_______ 。
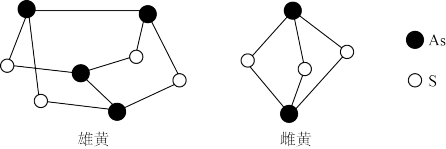
(2)雄黄(As4S4)和雌黄(As2S3)在自然界中共生,是提取砷的主要矿物原料,其结构如下图所示, 雄黄与
雄黄与 反应生成
反应生成 ,转移
,转移 电子,则另一种产物为
电子,则另一种产物为_______ 。雌黄中 的杂化方式为
的杂化方式为_______ 。
(3)亚砷酸(H3AsO3)可以用来治疗白血病,为三元弱酸,试推测 的空间构型为
的空间构型为_______ 。
(4)砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料。其晶胞结构如下图所示。晶体中As原子周围与其距离最近的As原子的个数为_______ ,若As原子的半径为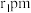 ,
, 原子的半径为
原子的半径为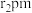 ,则最近的两个As原子的距离为
,则最近的两个As原子的距离为_______ pm。

(1)基态砷原子N电子层中的成对电子与单电子的数量比为
(2)雄黄(As4S4)和雌黄(As2S3)在自然界中共生,是提取砷的主要矿物原料,其结构如下图所示,
 雄黄与
雄黄与 反应生成
反应生成 ,转移
,转移 电子,则另一种产物为
电子,则另一种产物为 的杂化方式为
的杂化方式为
(3)亚砷酸(H3AsO3)可以用来治疗白血病,为三元弱酸,试推测
 的空间构型为
的空间构型为(4)砷化镓(GaAs)是优良的半导体材料,可用于制作微型激光器或太阳能电池的材料。其晶胞结构如下图所示。晶体中As原子周围与其距离最近的As原子的个数为
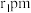 ,
, 原子的半径为
原子的半径为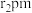 ,则最近的两个As原子的距离为
,则最近的两个As原子的距离为
您最近一年使用:0次



