氮元素可以形成许多化合物,在我们生活生产中有广泛的应用。
(1)与NF3分子互为等电子体的分子为________ 。
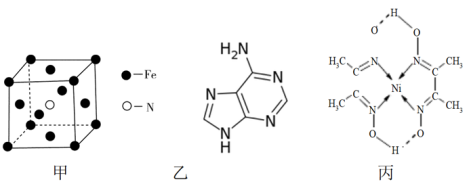
(2)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构见图甲。
写出Fe3+的基态电子排布式________ 。
写出该反应的化学方程式:______________ 。
(3)维生素B4结构如图乙,则1mol维生素B4分子中含有σ键的数目为______ mol。
(4)配合物丙的结构见图,丙中含有__________ (填序号);
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
丙中碳原子的杂化方式有______________ 。
(1)与NF3分子互为等电子体的分子为
(2)铁和氨气在640℃可发生置换反应,产物之一的晶胞结构见图甲。
写出Fe3+的基态电子排布式
写出该反应的化学方程式:
(3)维生素B4结构如图乙,则1mol维生素B4分子中含有σ键的数目为
(4)配合物丙的结构见图,丙中含有
a.极性共价键 b.非极性共价键 c.配位键 d.氢键
丙中碳原子的杂化方式有
更新时间:2017-04-30 21:05:44
|
相似题推荐
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】在人类文明的历程中,许多物质发挥过重要作用,如铁、硝酸钾、青霉素、聚乙烯、二氧化硅、富勒烯、高碘酸等。
(1)结合事实判断CO和N2相对活泼的是___________ ,试用下表中的键能数据解释其相对活泼的原因:___________ 。
(2)元素铜与镍的第二电离能分别为ICu=1958kJ·mol–1、INi=1753kJ·mol-1,ICu>INi的原因是___________ 。
(3)已知高碘酸有两种形式,化学式分别为H5IO6(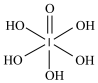 )和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6
)和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6___________ (填“>”“<”或“=”)HIO4。其原因___________
(4))KNO3中NO 的空间构型为
的空间构型为___________ ,写出与NO 互为等电子体的另一种阴离子的化学式:
互为等电子体的另一种阴离子的化学式:___________ 。
(5)已知固态HF、H2O、NH3的氢键结构和键能如下,请解释H2O、HF、NH3沸点依次降低的原因___________ 。
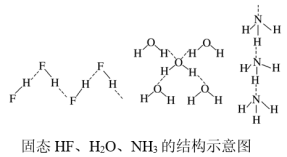
(6)富勒烯(C60)的结构如图所示,该物质能与氯气反应形成C60Cl10分子,1molC60Cl10分子中含有碳碳单键的数目为___________ 。

(1)结合事实判断CO和N2相对活泼的是
| CO | C-O | C=O | C≡O |
| 键能(kJ·mol-1) | 357.7 | 798.9 | 1071.9 |
| N2 | N—N | N=N | N≡N |
| 键能(kJ·mol-1) | 154.8 | 418.4 | 941.7 |
(3)已知高碘酸有两种形式,化学式分别为H5IO6(
 )和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6
)和HIO4,前者为五元酸,后者为一元酸。请比较二者酸性强弱:H5IO6(4))KNO3中NO
 的空间构型为
的空间构型为 互为等电子体的另一种阴离子的化学式:
互为等电子体的另一种阴离子的化学式:(5)已知固态HF、H2O、NH3的氢键结构和键能如下,请解释H2O、HF、NH3沸点依次降低的原因

| 物质 | 氢键X—H…Y | 键能/kJ·mol-1 |
| (HF)n | F—H…F | 28.1 |
| 冰 | O—H…O | 18.8 |
| (NH3)n | N—H…N | 5.4 |

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】自然界中存在大量的金属元素,其中钠、镁、铝、铁、铜等在工农业生产中有着广泛的应用。回答下列问题:
(1)CuSO4和Cu(NO3)2中阳离子核外电子排布式为__________ ,N、O、S元素的原子对键合电子吸引力最大的是___________ 。
(2)在硫酸铜溶液中加入过量KCN能生成配离子[Cu(CN)4]2-,1mol CN−中含有的π键的数目为__________ 。与CN−互为等电子体的离子或分子有__________ (写出一种即可)。
(3)[Cu(NH3)4]2+中,提供孤对电子的是___________ 。Cu(NH3)2Cl2有两种同分异构体,其中一种可溶于水,则此种化合物是___________ (填“极性”或“非极性”)分子,由此推知[Cu(NH)4]2+的空间构型是___________ 。(填“平面正方形”或“正四面体”)
(4)NH3中N原子的杂化方式是___________ ,硫元素对应的含氧酸酸性是H2SO4强于H2SO3,其原因为___________ 。
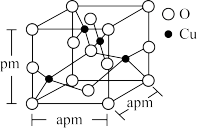
(5)铜的一种氧化物晶体结构如图所示,该氧化物的化学式是___________ 。若该晶体结构为长方体,其参数如图,阿伏加 德罗常数为NA,则该氧化物的密度为___________ g/cm3。
(1)CuSO4和Cu(NO3)2中阳离子核外电子排布式为
(2)在硫酸铜溶液中加入过量KCN能生成配离子[Cu(CN)4]2-,1mol CN−中含有的π键的数目为
(3)[Cu(NH3)4]2+中,提供孤对电子的是
(4)NH3中N原子的杂化方式是
(5)铜的一种氧化物晶体结构如图所示,该氧化物的化学式是

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐3】磷、碳、氢、氧等非金属及其化合物用途广泛。回答下列问题:
(1)白磷(P4)在氯气中燃烧可生成PCl3和PCl5。
①31 g白磷(P4)中含有化学键的数目为_______ 。(用NA表示阿伏伽德罗常数的值)
②形成PCl5时,P原子的一个3s电子激发入3d轨道后参与成键,该激发态的价电子排布式为_______ 。
③研究表明,在加压条件下PCl5于148℃液化时能发生与水类似的自耦电离,形成一种能导电的熔体,其电离方程式为_______ ,产生的阳离子的空间结构为_______ 。
(2)分子中的大π键可用符号 表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为  )。一种观点认为,苯酚羟基中的O原子是sp2杂化则苯酚中的大π键可表示为
)。一种观点认为,苯酚羟基中的O原子是sp2杂化则苯酚中的大π键可表示为_______ ,一定在同一平面上的原子有_______ 个;乙醇显中性而苯酚显酸性的原因是:在大π键中氧的p电子云向苯环转移,_______ 。
(3)可溶性普鲁士蓝晶体属立方晶系,晶胞棱长为a pm,铁-氰骨架组成的小立方体中,Fe粒子在顶点,CN—在棱上,两端均与Fe相连,立方体中心空隙可容纳K+,如图所示(CN—在图中省略)。
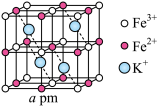
①该化合物的化学式为_______ 。
②若所有铁粒子均视为等径小球,则K+与Fe2+之间最近距离为_______ pm;该晶体的密度为_______ g•cm-3(阿伏加德罗常数为NA)
(1)白磷(P4)在氯气中燃烧可生成PCl3和PCl5。
①31 g白磷(P4)中含有化学键的数目为
②形成PCl5时,P原子的一个3s电子激发入3d轨道后参与成键,该激发态的价电子排布式为
③研究表明,在加压条件下PCl5于148℃液化时能发生与水类似的自耦电离,形成一种能导电的熔体,其电离方程式为
(2)分子中的大π键可用符号
 表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为
表示,其中m代表参与形成大π键的原子数,n代表参与形成大键的电子数(如苯分子中的大π键可表示为  )。一种观点认为,苯酚羟基中的O原子是sp2杂化则苯酚中的大π键可表示为
)。一种观点认为,苯酚羟基中的O原子是sp2杂化则苯酚中的大π键可表示为(3)可溶性普鲁士蓝晶体属立方晶系,晶胞棱长为a pm,铁-氰骨架组成的小立方体中,Fe粒子在顶点,CN—在棱上,两端均与Fe相连,立方体中心空隙可容纳K+,如图所示(CN—在图中省略)。

①该化合物的化学式为
②若所有铁粒子均视为等径小球,则K+与Fe2+之间最近距离为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】形形色色的物质,构成了我们这个五彩缤纷的世界。世上万物,神奇莫测,常常超乎人们按“常理"的想象。学习物质结构和性质的知识,能使你想象的翅膀变得更加有力。
(1)基态Ga原子的简化核外电子排布式是____ ,原子核外电子占据最高能级的电子云轮廓图为____ 。
(2)硒的含氧酸有H2SeO3、H2SeO4。酸性:H2SeO3____ H2SeO4(填“>”“<”或“=”)。SeO 的空间构型是
的空间构型是____ 。
(3)NaN3是汽车安全气囊中的主要化学成分,其阴离子的立体构型为____ 。写出和该阴离子互为等电子体的一种分子的结构式____ 。
(4)钙和铁都是第四周期元素,且原子的最外层电子数相同,铁的熔沸点远高于钙,其原因是____ 。
(5)配体中配位原子提供孤电子对的能力与元素的电负性有关,SCN—的结构式可以表示为[S=C=N]—或[S-C≡N]—,SCN-与Fe3+、Au+和Hg2+等离子能形成配离子,N、C、S的电负性依次为3.0、2.5和2.5。SCN—中提供孤电子对的原子可能是_____ 。
(6)某离子晶体XY2的晶胞结构如图所示。

①晶体中在每个X周围与它最近且距离相等的X共有____ 个。
②设该晶体的摩尔质量为Mg•mol-1,晶胞的密度为ρg•cm-3,阿伏加德罗常数为NA,则晶体中两个最近的X间的距离为____ cm。
(1)基态Ga原子的简化核外电子排布式是
(2)硒的含氧酸有H2SeO3、H2SeO4。酸性:H2SeO3
 的空间构型是
的空间构型是(3)NaN3是汽车安全气囊中的主要化学成分,其阴离子的立体构型为
(4)钙和铁都是第四周期元素,且原子的最外层电子数相同,铁的熔沸点远高于钙,其原因是
(5)配体中配位原子提供孤电子对的能力与元素的电负性有关,SCN—的结构式可以表示为[S=C=N]—或[S-C≡N]—,SCN-与Fe3+、Au+和Hg2+等离子能形成配离子,N、C、S的电负性依次为3.0、2.5和2.5。SCN—中提供孤电子对的原子可能是
(6)某离子晶体XY2的晶胞结构如图所示。

①晶体中在每个X周围与它最近且距离相等的X共有
②设该晶体的摩尔质量为Mg•mol-1,晶胞的密度为ρg•cm-3,阿伏加德罗常数为NA,则晶体中两个最近的X间的距离为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】中国海军航母建设正在有计划、有步骤地向前推进,第一艘国产航母目前正在进行海试。建造航母需要大量的新型材料。航母的龙骨要耐冲击,航母的甲板要耐高温,航母的外壳要耐腐蚀。
(1)镍铬钢抗腐蚀性能强, 的核外电子排布式为
的核外电子排布式为___________ ,铬元素在周期表中___________ 区。
(2)航母甲板涂有一层耐高温的材料—聚硅氧烷,其结构如图所示,其中C原子杂化方式为___________ 杂化。
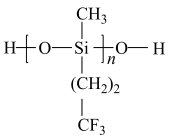
(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是___________ (填元素符号)。
②根据价层电子对互斥理论,预测 的空间构型为
的空间构型为 ___________ 形,写出一个与 互为等电子体的微粒
互为等电子体的微粒___________ 。
(4)海底金属软泥是在海洋底覆盖着的一层红棕色沉积物,蕴藏着大量的资源,含有硅、铁、锰、锌等元素。如图是从铁氧体离子晶体 中取出的能体现其晶体结构的一个立方体,则晶体中的氧离子是否构成了面心立方最密堆积
中取出的能体现其晶体结构的一个立方体,则晶体中的氧离子是否构成了面心立方最密堆积___________ (填“是”或“否”);该立方体是不是 的晶胞
的晶胞___________ (填“是”或“否”);立方体中铁离子处于氧离子围成的___________ (填空间结构)空隙。
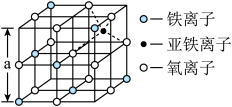
(5)已知单质铁有如图所示的三种堆积方式的晶胞结构:
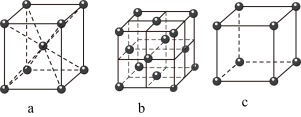
①晶胞a属于___________ 堆积;
②用含有 的式子表示出晶胞b的空间利用率
的式子表示出晶胞b的空间利用率___________ ;
③若晶胞c的密度为 ,则铁的原子半径r=
,则铁的原子半径r=___________ cm。(用含 、
、 的式子表示,
的式子表示, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
(1)镍铬钢抗腐蚀性能强,
 的核外电子排布式为
的核外电子排布式为(2)航母甲板涂有一层耐高温的材料—聚硅氧烷,其结构如图所示,其中C原子杂化方式为

(3)海洋是元素的摇篮,海水中含有大量卤族元素。
①根据下表数据判断:最有可能生成较稳定的单核阳离子的卤素原子是
| 氟 | 氯 | 溴 | 碘 | |
| 第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
 的空间构型为
的空间构型为  互为等电子体的微粒
互为等电子体的微粒(4)海底金属软泥是在海洋底覆盖着的一层红棕色沉积物,蕴藏着大量的资源,含有硅、铁、锰、锌等元素。如图是从铁氧体离子晶体
 中取出的能体现其晶体结构的一个立方体,则晶体中的氧离子是否构成了面心立方最密堆积
中取出的能体现其晶体结构的一个立方体,则晶体中的氧离子是否构成了面心立方最密堆积 的晶胞
的晶胞
(5)已知单质铁有如图所示的三种堆积方式的晶胞结构:

①晶胞a属于
②用含有
 的式子表示出晶胞b的空间利用率
的式子表示出晶胞b的空间利用率③若晶胞c的密度为
 ,则铁的原子半径r=
,则铁的原子半径r= 、
、 的式子表示,
的式子表示, 表示阿伏加德罗常数的值)。
表示阿伏加德罗常数的值)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐3】含氮物质在工业上应用非常广泛。将单质钡(Ba)、铼(Re)以一定比例混合,于特制容器中加热,依次通入N2、O2可制得某黑色晶体,该晶体晶胞如图所示,含有多个由Ba(+2)、Re(+4)、O(-2)和N(-3)组成的八面体与平面三角形,括号中为其化合价。
(1)基态Ba原子的简化电子排布式为___________ ,N、O、Ba简单氢化物的沸点由高到低的顺序为___________ (填化学式)。
(2)NO 中N原子的杂化方式为
中N原子的杂化方式为___________ ,下列离子或分子与 互为等电子体的是
互为等电子体的是___________ (填标号)。
a.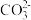 b.
b. c.SO3 d.
c.SO3 d.
(3)苯胺(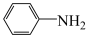 )中N原子与苯环形成p-π共轭,
)中N原子与苯环形成p-π共轭, 、
、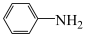 、
、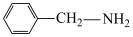 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是___________ 。
(4)该晶体中含有的八面体和平面三角形的个数比为___________ ,晶体的化学式为___________ 。
(5)晶胞参数为apm、apm、cpm, ,
,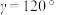 ,该晶体的密度为
,该晶体的密度为___________ g·cm-1(写出表达式)。

(1)基态Ba原子的简化电子排布式为
(2)NO
 中N原子的杂化方式为
中N原子的杂化方式为 互为等电子体的是
互为等电子体的是a.
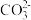 b.
b. c.SO3 d.
c.SO3 d.
(3)苯胺(
 )中N原子与苯环形成p-π共轭,
)中N原子与苯环形成p-π共轭, 、
、 、
、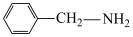 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是(4)该晶体中含有的八面体和平面三角形的个数比为
(5)晶胞参数为apm、apm、cpm,
 ,
,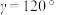 ,该晶体的密度为
,该晶体的密度为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐1】锰及其化合物在化学实验室和化工生产应用非常广泛,回答下列问题:
(1)乙酰丙酮锰(III)是一种广泛用于苯酚类化合物氧化偶联的试剂,Me表示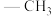 ,中心离子为
,中心离子为 离子,其结构如图所示。
离子,其结构如图所示。_______ ,该物质中不同杂化方式的碳原子数之比为_______ ,中心离子 填充在
填充在_______ 空隙中(填“四面体”或“八面体”)。
(2)从原子结构角度分析,基态原子中,Mn的第三电离能大于Fe的第三电离能的原因是_______ 。
(3) 能形成如图所示大π键,而羧基酸性随大π键电子云密度的增大而减弱,则
能形成如图所示大π键,而羧基酸性随大π键电子云密度的增大而减弱,则 、
、 、
、 酸性从强到弱顺序是
酸性从强到弱顺序是_______ 。 的顺式结构为
的顺式结构为_______ 分子(填“极性”、“非极性”)。 围成的八面体空隙中,形成无限螺旋链的络离子,同一条链内原子作用很强,其形成晶胞结构沿对角线的投影如图a所示,晶胞俯视图如图b所示,晶胞参数为
围成的八面体空隙中,形成无限螺旋链的络离子,同一条链内原子作用很强,其形成晶胞结构沿对角线的投影如图a所示,晶胞俯视图如图b所示,晶胞参数为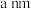 、
、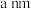 和
和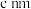 ,则该晶胞所带电荷为
,则该晶胞所带电荷为_______ 。阿伏加德罗常数的值为 ,该晶体的密度为
,该晶体的密度为_______  (用含
(用含 、a、c的式子表示)。
、a、c的式子表示)。
(1)乙酰丙酮锰(III)是一种广泛用于苯酚类化合物氧化偶联的试剂,Me表示
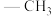 ,中心离子为
,中心离子为 离子,其结构如图所示。
离子,其结构如图所示。
 填充在
填充在(2)从原子结构角度分析,基态原子中,Mn的第三电离能大于Fe的第三电离能的原因是
(3)
 能形成如图所示大π键,而羧基酸性随大π键电子云密度的增大而减弱,则
能形成如图所示大π键,而羧基酸性随大π键电子云密度的增大而减弱,则 、
、 、
、 酸性从强到弱顺序是
酸性从强到弱顺序是 的顺式结构为
的顺式结构为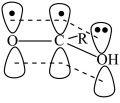
 围成的八面体空隙中,形成无限螺旋链的络离子,同一条链内原子作用很强,其形成晶胞结构沿对角线的投影如图a所示,晶胞俯视图如图b所示,晶胞参数为
围成的八面体空隙中,形成无限螺旋链的络离子,同一条链内原子作用很强,其形成晶胞结构沿对角线的投影如图a所示,晶胞俯视图如图b所示,晶胞参数为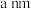 、
、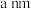 和
和 ,则该晶胞所带电荷为
,则该晶胞所带电荷为 ,该晶体的密度为
,该晶体的密度为 (用含
(用含 、a、c的式子表示)。
、a、c的式子表示)。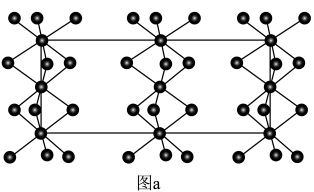

您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
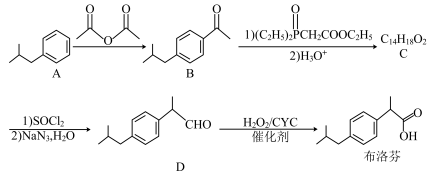
【推荐2】布洛芬是一种抗炎药,具有解热镇痛作用。一种合成布洛芬的方法如下:
已知: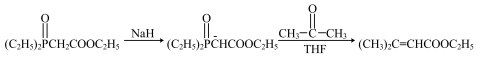
(1)D分子中采取 杂化与
杂化与 杂化的碳原子的数目之比为
杂化的碳原子的数目之比为___________ 。
(2)A→B的反应类型为___________ 。
(3)C的结构简式为___________ 。
(4)布洛芬的一种同分异构体同时满足下列条件,其结构简式为___________ 。
①能发生银镜反应和水解反应。
②核磁共振氢谱有4个吸收峰。
(5)补充完整下列合成路线流程图(括号内写反应物和反应条件,方框中写结构简式):____________


已知:
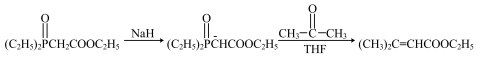
(1)D分子中采取
 杂化与
杂化与 杂化的碳原子的数目之比为
杂化的碳原子的数目之比为(2)A→B的反应类型为
(3)C的结构简式为
(4)布洛芬的一种同分异构体同时满足下列条件,其结构简式为
①能发生银镜反应和水解反应。
②核磁共振氢谱有4个吸收峰。
(5)补充完整下列合成路线流程图(括号内写反应物和反应条件,方框中写结构简式):

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
【推荐3】Ⅰ.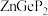 和
和 都是非线性光学晶体材料,在激光技术方面有广泛用途。回答下列问题:
都是非线性光学晶体材料,在激光技术方面有广泛用途。回答下列问题:
(1)基态氧原子核外电子有_______ 种不同的空间运动状态;基态 原子的价电子排布式为
原子的价电子排布式为_______ 。
(2)O、P、K、Zn中电负性最小的为_______ 。
(3) 、
、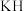 熔点由高到低的顺序为
熔点由高到低的顺序为_______ ,原因是_______ 。
(4) 可与
可与 结合生成
结合生成 ,水中
,水中 的键角比
的键角比 中的
中的_______ (填“大”或“小”)。 是常用的氧化剂,其分子结构如图1所示。
是常用的氧化剂,其分子结构如图1所示。 能与水混溶,却不溶于
能与水混溶,却不溶于 的原因是
的原因是_______ 。

(5)将纯液态 冷却到
冷却到 时,能凝固得到一种螺旋状单链结构的固体,其结构如图2所示,此固态SO3中S原子的杂化轨道类型是
时,能凝固得到一种螺旋状单链结构的固体,其结构如图2所示,此固态SO3中S原子的杂化轨道类型是_______ 。

Ⅱ.铁、铜和镉是三种过渡金属元素。回答下列问题:
(6) 比
比 稳定,试从原子结构角度解释原因
稳定,试从原子结构角度解释原因_______ 。
(7)新制的 能够溶解于过量浓
能够溶解于过量浓 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为_______ 。
(8)镉晶胞如图3所示。已知:NA是阿伏加德罗常数的值,晶体密度为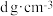 。在该晶胞中两个镉原子最近核间距
。在该晶胞中两个镉原子最近核间距
_______  (用含NA、
(用含NA、 的代数式表示);镉晶胞中原子空间利用率为
的代数式表示);镉晶胞中原子空间利用率为_______ (用含 的代数式表示)。
的代数式表示)。

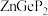 和
和 都是非线性光学晶体材料,在激光技术方面有广泛用途。回答下列问题:
都是非线性光学晶体材料,在激光技术方面有广泛用途。回答下列问题:(1)基态氧原子核外电子有
 原子的价电子排布式为
原子的价电子排布式为(2)O、P、K、Zn中电负性最小的为
(3)
 、
、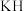 熔点由高到低的顺序为
熔点由高到低的顺序为(4)
 可与
可与 结合生成
结合生成 ,水中
,水中 的键角比
的键角比 中的
中的 是常用的氧化剂,其分子结构如图1所示。
是常用的氧化剂,其分子结构如图1所示。 能与水混溶,却不溶于
能与水混溶,却不溶于 的原因是
的原因是
(5)将纯液态
 冷却到
冷却到 时,能凝固得到一种螺旋状单链结构的固体,其结构如图2所示,此固态SO3中S原子的杂化轨道类型是
时,能凝固得到一种螺旋状单链结构的固体,其结构如图2所示,此固态SO3中S原子的杂化轨道类型是
Ⅱ.铁、铜和镉是三种过渡金属元素。回答下列问题:
(6)
 比
比 稳定,试从原子结构角度解释原因
稳定,试从原子结构角度解释原因(7)新制的
 能够溶解于过量浓
能够溶解于过量浓 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为(8)镉晶胞如图3所示。已知:NA是阿伏加德罗常数的值,晶体密度为
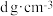 。在该晶胞中两个镉原子最近核间距
。在该晶胞中两个镉原子最近核间距
 (用含NA、
(用含NA、 的代数式表示);镉晶胞中原子空间利用率为
的代数式表示);镉晶胞中原子空间利用率为 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐1】 均是铬的重要化合物,回答下列问题:
均是铬的重要化合物,回答下列问题:
(1)基态 原子有
原子有___________ 种能量不同的电子,价电子排布式为___________ 。
(2)已知电子亲和能(E)是基态的气态原子得到电子变为气态阴离子所放出的能量, ,氧的第一电子亲和能
,氧的第一电子亲和能 为
为___________  ;
; ,其原因是
,其原因是___________ 。
(3)雷氏盐的化学式为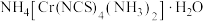 。
。
①H、C、N、O四种元素的电负性由大到小的顺序为___________ 。
②雷氏盐中所含化学键类型___________ 。
A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
③配体之一 分子的立体构型为
分子的立体构型为___________ ,与配体 互为等电子体的分子和离子有
互为等电子体的分子和离子有___________ (各写1种)。
(4)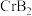 的晶体密度为
的晶体密度为 ,晶体结构(如图)为六棱柱,底边边长为
,晶体结构(如图)为六棱柱,底边边长为 ,高为
,高为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则
,则
___________ (列出计算式)。

 均是铬的重要化合物,回答下列问题:
均是铬的重要化合物,回答下列问题:(1)基态
 原子有
原子有(2)已知电子亲和能(E)是基态的气态原子得到电子变为气态阴离子所放出的能量,
 ,氧的第一电子亲和能
,氧的第一电子亲和能 为
为 ;
; ,其原因是
,其原因是(3)雷氏盐的化学式为
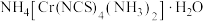 。
。①H、C、N、O四种元素的电负性由大到小的顺序为
②雷氏盐中所含化学键类型
A.离子键 B.共价键 C.配位键 D.金属键 E.氢键
③配体之一
 分子的立体构型为
分子的立体构型为 互为等电子体的分子和离子有
互为等电子体的分子和离子有(4)
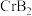 的晶体密度为
的晶体密度为 ,晶体结构(如图)为六棱柱,底边边长为
,晶体结构(如图)为六棱柱,底边边长为 ,高为
,高为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则
,则

您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
名校
解题方法
【推荐2】Fe、Co、Ni均为第Ⅷ族元素,它们的化合物在生产、生活中有着广泛的应用。
(1)基态Co原子的价电子排布式为_______ ,Co2+核外3d能级上有_____ 对成对电子。
(2)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是________ 。1 mol配离子中所含σ键的数目为________ ,配位体N3-中心原子的杂化类型为________ 。
(3)Co2+在水溶液中以[Co(H2O)6]2+存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+,其原因是_________________________________________________ 。
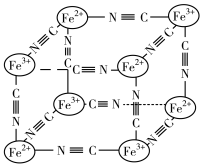
(4)某蓝色晶体晶体结构如图,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的体心上。据此可知该晶体的化学式为________ ,立方体中Fe2+间连接起来形成的空间构型是________ 。K+空缺率(体心中没有K+的占总体心的百分比)为_____________ 。
(5)NiO的晶胞结构如图甲所示,其中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为________ 。
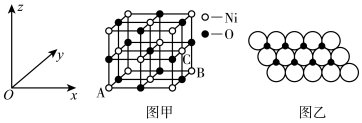
(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图乙),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为________ g(用含a、NA的代数式表示)。
(1)基态Co原子的价电子排布式为
(2)Co3+的一种配离子[Co(N3)(NH3)5]2+中,Co3+的配位数是
(3)Co2+在水溶液中以[Co(H2O)6]2+存在。向含Co2+的溶液中加入过量氨水可生成更稳定的[Co(NH3)6]2+,其原因是
(4)某蓝色晶体晶体结构如图,Fe2+、Fe3+分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个CN-,K+位于立方体的体心上。据此可知该晶体的化学式为

(5)NiO的晶胞结构如图甲所示,其中原子坐标参数A为(0,0,0),B为(1,1,0),则C原子坐标参数为

(6)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图乙),已知O2-的半径为a pm,每平方米面积上分散的该晶体的质量为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】硫酸锆 ,是制取原子能级锆及其它锆化合物的中间原料,并大量用作皮革鞣剂、羊毛处理剂、催化剂等。下面是以锆英砂(主要成分为
,是制取原子能级锆及其它锆化合物的中间原料,并大量用作皮革鞣剂、羊毛处理剂、催化剂等。下面是以锆英砂(主要成分为 ,伴有杂质
,伴有杂质 )为原料,利用碱熔法再进行酸浸制备硫酸锆的工艺过程。
)为原料,利用碱熔法再进行酸浸制备硫酸锆的工艺过程。

已知:① 、
、 、
、 均易溶于水,难溶于酒精及其他有机溶剂
均易溶于水,难溶于酒精及其他有机溶剂
②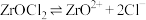 ;
;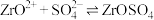
③
(1)步骤1中用到的仪器有泥三角、______ (填“铁”或“瓷”)坩埚、坩埚钳等。
(2)下列说法正确的是______。
(3)如图装置,经过一系列操作完成操作2中的抽滤和洗涤。

请选择合适的编号,按正确的操作顺序补充完整:______ 。
开抽气泵→a→d→b→______→______→______→______→b→e→关抽气泵。
a.转移固液混合物; b.确认抽干; c.加浓盐酸洗涤;
d.关闭活塞A; e.打开活塞A; f.加无水乙醇洗涤
(4)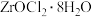 洗涤后,在800℃下灼烧可得一种压电陶瓷原料
洗涤后,在800℃下灼烧可得一种压电陶瓷原料 ,写出该灼烧过程的化学方程式
,写出该灼烧过程的化学方程式______ 。
(5)实验室可以用络合滴定法测定锆含量。已知: 与二甲酚橙生成红色络合物,
与二甲酚橙生成红色络合物, 能与EDTA(乙二胺四乙酸,结构:
能与EDTA(乙二胺四乙酸,结构: )发生络合反应(1∶1)生成无色络合物,且络合能力更强。
)发生络合反应(1∶1)生成无色络合物,且络合能力更强。

①EDTA是常见的六齿配体,与 络合的原子可能是EDTA中的
络合的原子可能是EDTA中的______ 原子(填元素符号)。
②产品中锆的含量是______ (用含c、V、m的代数式表达)
③下列有关上述滴定操作的说法正确的是______ 。

A.滴定管活塞涂凡士林:用手指蘸取少量凡士林涂抹一薄层在活塞a、b处(如图)的四周,平行插入活塞槽中,然后朝同一个方向转动
B.接近滴定终点时适当减慢滴加速度,必要时采用半滴操作
C.读数时可将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
D.第一次滴定时若测得消耗标准液体积小于5.00mL,则第二次滴定时可在稀释待测液后重新滴定来减小误差
 ,是制取原子能级锆及其它锆化合物的中间原料,并大量用作皮革鞣剂、羊毛处理剂、催化剂等。下面是以锆英砂(主要成分为
,是制取原子能级锆及其它锆化合物的中间原料,并大量用作皮革鞣剂、羊毛处理剂、催化剂等。下面是以锆英砂(主要成分为 ,伴有杂质
,伴有杂质 )为原料,利用碱熔法再进行酸浸制备硫酸锆的工艺过程。
)为原料,利用碱熔法再进行酸浸制备硫酸锆的工艺过程。
已知:①
 、
、 、
、 均易溶于水,难溶于酒精及其他有机溶剂
均易溶于水,难溶于酒精及其他有机溶剂②
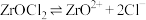 ;
;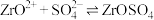
③

(1)步骤1中用到的仪器有泥三角、
(2)下列说法正确的是______。
A.副产物1为 、副产物2为NaCl、副产物3为HClO 、副产物2为NaCl、副产物3为HClO |
B.步骤3加入HCl作用是与 反应生成 反应生成 ,还能降低 ,还能降低 的溶解度 的溶解度 |
| C.操作1为蒸发结晶、趁热过滤;操作2为重结晶 |
D.制备的 溶于水后溶液呈酸性 溶于水后溶液呈酸性 |
(3)如图装置,经过一系列操作完成操作2中的抽滤和洗涤。

请选择合适的编号,按正确的操作顺序补充完整:
开抽气泵→a→d→b→______→______→______→______→b→e→关抽气泵。
a.转移固液混合物; b.确认抽干; c.加浓盐酸洗涤;
d.关闭活塞A; e.打开活塞A; f.加无水乙醇洗涤
(4)
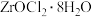 洗涤后,在800℃下灼烧可得一种压电陶瓷原料
洗涤后,在800℃下灼烧可得一种压电陶瓷原料 ,写出该灼烧过程的化学方程式
,写出该灼烧过程的化学方程式(5)实验室可以用络合滴定法测定锆含量。已知:
 与二甲酚橙生成红色络合物,
与二甲酚橙生成红色络合物, 能与EDTA(乙二胺四乙酸,结构:
能与EDTA(乙二胺四乙酸,结构: )发生络合反应(1∶1)生成无色络合物,且络合能力更强。
)发生络合反应(1∶1)生成无色络合物,且络合能力更强。
①EDTA是常见的六齿配体,与
 络合的原子可能是EDTA中的
络合的原子可能是EDTA中的②产品中锆的含量是
③下列有关上述滴定操作的说法正确的是

A.滴定管活塞涂凡士林:用手指蘸取少量凡士林涂抹一薄层在活塞a、b处(如图)的四周,平行插入活塞槽中,然后朝同一个方向转动
B.接近滴定终点时适当减慢滴加速度,必要时采用半滴操作
C.读数时可将滴定管从架上取下,捏住管上端无刻度处,使滴定管保持垂直
D.第一次滴定时若测得消耗标准液体积小于5.00mL,则第二次滴定时可在稀释待测液后重新滴定来减小误差
您最近一年使用:0次



