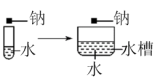
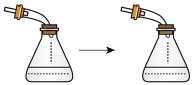
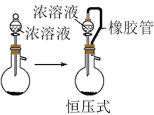
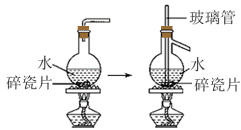
下列实验方案能达到相应实验目的的是
| 选项 | 实验方案 | 实验目的 |
| A | 室温下,用pH试纸分别测定浓度均为 的NaClO和 的NaClO和 溶液的pH 溶液的pH | 比较HClO和 的酸性强弱 的酸性强弱 |
| B | 配制 溶液时,先将 溶液时,先将 溶于适量浓盐酸中,再用蒸馏水稀释到所需浓度,最后在试剂瓶中加入少量铜粉 溶于适量浓盐酸中,再用蒸馏水稀释到所需浓度,最后在试剂瓶中加入少量铜粉 | 抑制 水解,并防止 水解,并防止 被氧化 被氧化 |
| C | 将稀硝酸与 反应产生的气体先通入饱和 反应产生的气体先通入饱和 溶液中,再通入 溶液中,再通入 溶液中 溶液中 | 验证非金属性:N>C>Si |
| D | 取等体积不同浓度的NaClO溶液,分别加入等体积等浓度的 溶液中,对比现象 溶液中,对比现象 | 探究浓度对化学反应速率的影响 |
| A.A | B.B | C.C | D.D |
更新时间:2024-05-29 20:53:51
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】密闭容器中反应CO(g)+H2O(g)⇌CO2(g)+H2(g)+Q(Q>0)达到平衡。其他条件不变时,不能使正反应速率加快的措施是
| A.通入水蒸气 | B.缩小容器体积 | C.分离出CO2 | D.升高温度 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】在体积相同,物质的量浓度相等的HCl溶液和CH3COOH溶液中分别加入足量Mg粉,产生H2的体积(同温同压下测定)的变化图示正确的是
A. | B. | C. | D. |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】化学平衡常数是表明化学反应限度的一个特征值,由下表中的数据不能 得出的结论是
| 弱酸 | HCOOH | HCN |  |
| 电离平衡常数(25℃) | 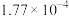 |  |   |
A. |
B. |
C. |
D.等浓度的HCOONa溶液和NaCN溶液中, |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法正确的是
A. 在水溶液中只电离,不水解 在水溶液中只电离,不水解 |
| B.硝酸钠溶液水解之后呈中性 |
| C.可溶性的铝盐都能发生水解反应 |
| D.可溶性的钾盐都不发生水解反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列有关叙述中,能说明非金属元素M比N的非金属性强的是
| A.非金属单质N能从M的化合物中置换出非金属单质M |
| B.M 原子比N原子容易得到电子 |
| C.气态氢化物水溶液的酸性HmM>HnN |
| D.氧化物水化物的酸性HmMOx>HnNOy |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】化学家Seidel指出Si与NaOH溶液的反应,首先是Si与OH-反应,生成SiO44-,然后SiO44-迅速水解生成H4 SiO4,下列有关说法正确的是。
| A.原硅酸钠(Na4SiO4)能迅速水解,且水解后呈碱性,故Na4SiO4为弱电解质 |
| B.石英玻璃、普通玻璃、陶瓷及水泥均属于硅酸盐产品 |
| C.2HCl +Na2SiO3 = H2SiO3↓+2NaCl说明Cl 的非金属性大于Si |
| D.半导体工业所说的“从沙滩到家庭”是指:将二氧化硅制成晶体硅 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】下列有关实验能达到相应实验目的的是( )
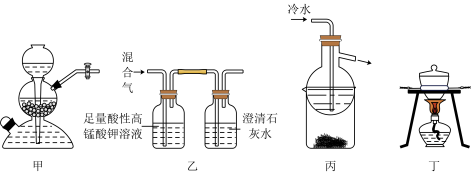
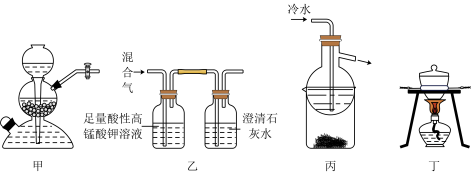
| A.甲装置可用于二氧化锰与浓盐酸反应制备氯气 |
| B.乙装置可用于检验SO2气体中混有的CO2气体 |
| C.丙装置可用于分离烧杯中的I2和NH4Cl |
| D.丁装置可用于由硫酸铜溶液获得硫酸铜晶体 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】某同学结合所学知识探究Na2O2与H2能否反应,设计装置如下,下列说法正确的是()

| A.若D中无水硫酸铜变蓝,则说明Na2O2与H2反应生成水 |
| B.装置B中盛放浓硫酸,目的是除去A中挥发出来的少量水蒸气 |
| C.装置C加热前,用试管在干燥管管口处收集气体点燃,通过声音判断气体纯度 |
| D.装置A也可直接用于二氧化锰与浓盐酸反应制取氯气 |
您最近一年使用:0次

 ,如图为速率ν(N2)变化图象,则横坐标不可能是
,如图为速率ν(N2)变化图象,则横坐标不可能是
 ,下列说法中一定正确的是
,下列说法中一定正确的是