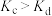已知催化剂 对吸热反应
对吸热反应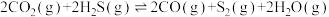 具有高选择性,通过理论计算得到反应的主要路径如下图所示,下列说法错误的是
具有高选择性,通过理论计算得到反应的主要路径如下图所示,下列说法错误的是
 对吸热反应
对吸热反应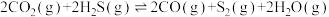 具有高选择性,通过理论计算得到反应的主要路径如下图所示,下列说法错误的是
具有高选择性,通过理论计算得到反应的主要路径如下图所示,下列说法错误的是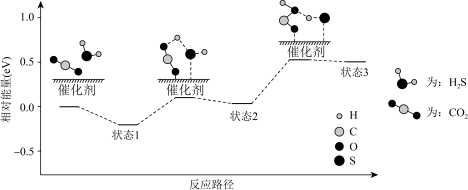
A.加入催化剂 ,会加快该反应的化学反应速率 ,会加快该反应的化学反应速率 |
B.反应过程中当 和 和 的浓度比不变的时候,该反应达到了化学平衡状态 的浓度比不变的时候,该反应达到了化学平衡状态 |
C.状态2可表示为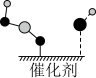 |
| D.若将该反应生成物中水的状态改成液态,那么反应前后的能量变化数值偏大 |
更新时间:2024-05-18 13:00:01
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】 是一种特别的共轭体系。在高温条件下
是一种特别的共轭体系。在高温条件下 可以由
可以由 分子经过5步氢提取和闭环脱氢反应生成。其中第一步过程的反应机理和能量变化如下:
分子经过5步氢提取和闭环脱氢反应生成。其中第一步过程的反应机理和能量变化如下:
 是一种特别的共轭体系。在高温条件下
是一种特别的共轭体系。在高温条件下 可以由
可以由 分子经过5步氢提取和闭环脱氢反应生成。其中第一步过程的反应机理和能量变化如下:
分子经过5步氢提取和闭环脱氢反应生成。其中第一步过程的反应机理和能量变化如下: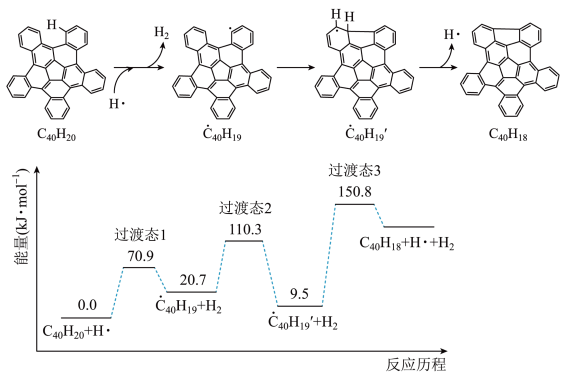
| A.反应过程中有极性键的断裂和形成 |
| B.图示历程中的基元反应,速率最慢的是第3步 |
C. 制备的总反应方程式为: 制备的总反应方程式为: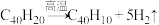 |
D.从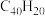 的结构分析, 的结构分析, 结构中五元环和六元环结构的数目分别为6、10 结构中五元环和六元环结构的数目分别为6、10 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】含Ru(钌)化合物可催化 转化为甲酸,其反应机理如图所示。
转化为甲酸,其反应机理如图所示。
 转化为甲酸,其反应机理如图所示。
转化为甲酸,其反应机理如图所示。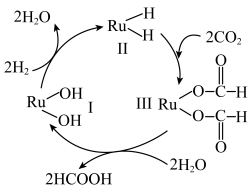
| A.1mol物质Ⅰ转化为物质Ⅱ时,反应过程中转移4mol电子 |
| B.物质Ⅱ→Ⅲ过程中,Ru元素化合价保持不变 |
| C.整个过程中,有非极性键的断裂与形成 |
| D.反应结束后,体系中水的量增多 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下表中针对可逆反应的平衡状态进行的操作所引起的变化分析正确的是
| 反应 | 操作 | 分析 | |
| A | 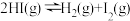 | 恒压容器,向平衡体系中充入HI | 体系中气体颜色加深 |
| B | 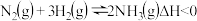 | 恒容容器,使平衡体系升温 | 体系总压降低 |
| C | 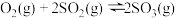 | 使用合适催化剂 | 可提高SO2的平衡转化率 |
| D | 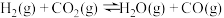 | 密闭容器,压缩体积 | 正反应速率增大 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
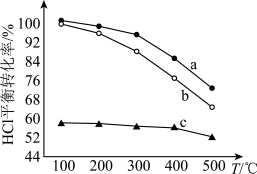
【推荐2】直接氧化法制取 Cl2的原理是:4HCl(g)+O2(g)  2Cl2(g)+2H2O(g) ,下图为进料浓度比 c(HCl) ∶c(O2)不同时 HCl 平衡转化率随温度变化的关系,有关说法正确的是
2Cl2(g)+2H2O(g) ,下图为进料浓度比 c(HCl) ∶c(O2)不同时 HCl 平衡转化率随温度变化的关系,有关说法正确的是
 2Cl2(g)+2H2O(g) ,下图为进料浓度比 c(HCl) ∶c(O2)不同时 HCl 平衡转化率随温度变化的关系,有关说法正确的是
2Cl2(g)+2H2O(g) ,下图为进料浓度比 c(HCl) ∶c(O2)不同时 HCl 平衡转化率随温度变化的关系,有关说法正确的是
| A.该反应为吸热反应 |
| B.K(300℃)<K(400℃) |
| C.进料浓度比c(HCl)∶c(O2)最大的是c线 |
| D.升温、加压、加催化剂均能提高 Cl2的平衡产率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定温度下在一定体积的密闭容器中,下列叙述能作为可逆反应A(g)+3B(g)  2C(g)达到平衡状态标志的是
2C(g)达到平衡状态标志的是
①C的生成速率与C的消耗速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④C的物质的量不再变化
⑤混合气体的总压强不再变化
⑥混合气体的总物质的量不再变化
⑦单位时间消耗a mol A,同时生成3a mol B
⑧A、B、C的分子数之比为1∶3∶2
 2C(g)达到平衡状态标志的是
2C(g)达到平衡状态标志的是 ①C的生成速率与C的消耗速率相等
②单位时间内生成a mol A,同时生成3a mol B
③A、B、C的浓度不再变化
④C的物质的量不再变化
⑤混合气体的总压强不再变化
⑥混合气体的总物质的量不再变化
⑦单位时间消耗a mol A,同时生成3a mol B
⑧A、B、C的分子数之比为1∶3∶2
| A.①③④⑤⑥⑦ | B.①③④⑤⑥⑧ | C.①③④⑥⑧ | D.①③④⑤⑧ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】在一定温度下的恒容密闭容器中,当下列哪些物理量不再发生变化时,表明下述反应:A(s)+2B(g) C(g)+D(g)已达到平衡状态
C(g)+D(g)已达到平衡状态
①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④气体的总物质的量 ⑤混合气体总质量
 C(g)+D(g)已达到平衡状态
C(g)+D(g)已达到平衡状态①混合气体的压强 ②混合气体的密度 ③B的物质的量浓度 ④气体的总物质的量 ⑤混合气体总质量
| A.②③⑤ | B.①②③ | C.②③④ | D.①③④⑤ |
您最近一年使用:0次

 可解离出氯原子,氯原子破坏臭氧层的原理如图所示。下列说法正确的是
可解离出氯原子,氯原子破坏臭氧层的原理如图所示。下列说法正确的是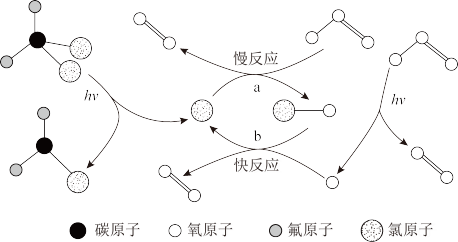
 的活化能低于反应
的活化能低于反应 的活化能
的活化能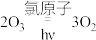
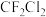 分子的空间构型是正四面体形
分子的空间构型是正四面体形
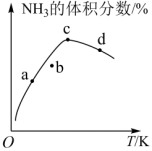
 ,将
,将 和
和 按一定比例通入恒温恒压的密闭容器中,反应相同时间后,
按一定比例通入恒温恒压的密闭容器中,反应相同时间后, 的体积分数随温度的变化关系如图所示。下列说法正确的是
的体积分数随温度的变化关系如图所示。下列说法正确的是