某学生做浓硫酸性质的实验:在一支试管中放入一块很小的铜片,再加入2mL浓硫酸,然后把试管固定在铁架台上。把一小条蘸有品红溶液的滤纸放入带有单孔橡皮塞的玻璃管中。塞紧试管口,在玻璃管口处缠放一团蘸有Na2CO3溶液的棉花。加热试管,观察现象。
回答下列问题:

(1)写出试管中发生反应的化学方程式____________________ 。
(2)试管中的液体反应一段时间后,b处滤纸条的变化为_______________ ,待试管中反应停止后,给玻璃管放有蘸过品红溶液的滤纸处微微加热,滤纸条的变化为_____________ 。
(3)蘸有Na2CO3溶液的棉花团作用是__________ 。
(4)硫酸型酸雨的形成过程可用下列反应中的__________ 来表示。
A.
B.
C.
回答下列问题:

(1)写出试管中发生反应的化学方程式
(2)试管中的液体反应一段时间后,b处滤纸条的变化为
(3)蘸有Na2CO3溶液的棉花团作用是
(4)硫酸型酸雨的形成过程可用下列反应中的
A.

B.

C.

更新时间:2016-12-09 07:40:25
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】中华人民共和国国家标准(GB2760-2011)规定葡萄酒中: 最大使用量为
最大使用量为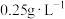 。某兴趣小组用下图装置(夹持装置略)收集某葡萄酒中的
。某兴趣小组用下图装置(夹持装置略)收集某葡萄酒中的 ,并对其含量进行测定。
,并对其含量进行测定。
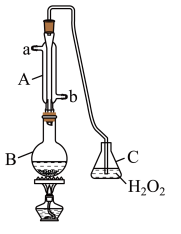
(1)B中加入300.00mL葡萄酒和适量盐酸,加热使 全部逸出并与C中的
全部逸出并与C中的 完全反应,其化学方程式为
完全反应,其化学方程式为______ 。
(2)除去C中过量的 ,然后用
,然后用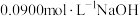 标准溶液进行滴定,若滴定终点时溶液的
标准溶液进行滴定,若滴定终点时溶液的 ,则选择的指示剂为
,则选择的指示剂为______ ;若用50 mL滴定管进行实验,当滴定管中的液面在刻度“10”处,则管内液体的体积(填序号)______
①=10 mL ②=40 mL ③<10 mL ④>40 mL
(3)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中: 含量为
含量为______  。该测定结果比实际值偏高,原因是
。该测定结果比实际值偏高,原因是______ 。
(4)若锥形瓶C中用足量水吸收 ,并改用淀粉试液作指示剂,用
,并改用淀粉试液作指示剂,用 标准
标准 溶液进行滴定(反应的化学方程式为
溶液进行滴定(反应的化学方程式为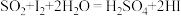 ),判断滴定终点的现象为
),判断滴定终点的现象为______ 。
若消耗标准 溶液25.00 mL,则该葡萄酒中
溶液25.00 mL,则该葡萄酒中 含量为
含量为______  。
。
 最大使用量为
最大使用量为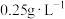 。某兴趣小组用下图装置(夹持装置略)收集某葡萄酒中的
。某兴趣小组用下图装置(夹持装置略)收集某葡萄酒中的 ,并对其含量进行测定。
,并对其含量进行测定。
(1)B中加入300.00mL葡萄酒和适量盐酸,加热使
 全部逸出并与C中的
全部逸出并与C中的 完全反应,其化学方程式为
完全反应,其化学方程式为(2)除去C中过量的
 ,然后用
,然后用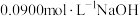 标准溶液进行滴定,若滴定终点时溶液的
标准溶液进行滴定,若滴定终点时溶液的 ,则选择的指示剂为
,则选择的指示剂为①=10 mL ②=40 mL ③<10 mL ④>40 mL
(3)滴定至终点时,消耗NaOH溶液25.00 mL,该葡萄酒中:
 含量为
含量为 。该测定结果比实际值偏高,原因是
。该测定结果比实际值偏高,原因是(4)若锥形瓶C中用足量水吸收
 ,并改用淀粉试液作指示剂,用
,并改用淀粉试液作指示剂,用 标准
标准 溶液进行滴定(反应的化学方程式为
溶液进行滴定(反应的化学方程式为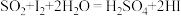 ),判断滴定终点的现象为
),判断滴定终点的现象为若消耗标准
 溶液25.00 mL,则该葡萄酒中
溶液25.00 mL,则该葡萄酒中 含量为
含量为 。
。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】甲、乙两同学为探究SO2与可溶性钡的强酸盐能否反应生成白色BaSO3沉淀,用下图所示装置进行实验(夹持装置和A中加热装置已略,气密性已检验)。
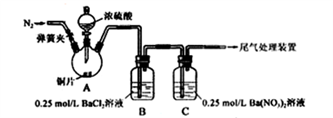
实验操作和现象:
(1)A中反应的化学方程式是_________________ ;
(2)C中生成白色沉淀的离子方程式为__________________ ;
(3)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。为证实各自的观点,在原实验基础上,甲、乙两同学分别作了如下实验:甲在原有操作之前通N2,一段时间,B中产生大量白色沉淀。乙在A、B间增加盛放饱和NaHSO3溶液的洗气瓶,B中有少量白色沉淀。产生少量沉淀的原因是_____________ 。
(4)结合(3)中两同学的实验现象。你认为原实验B中产生大量白色沉淀的主要原因是_____________ 。

实验操作和现象:
| 操作 | 现象 |
| 关闭弹簧夹,滴加一定量浓硫酸,加热 | A中有白雾生成,铜片表面产生气泡 B中有气泡冒出,产生大量白色沉淀 C中产生白色沉淀,液面上方略显浅棕色并逐渐消失 |
| 打开弹簧夹,通入N2,停止加热,一段时间后关闭 | |
| 从B、C中分别取少量白色沉淀,加稀盐酸 | 均未发现白色沉淀溶解 |
(2)C中生成白色沉淀的离子方程式为
(3)分析B中不溶于稀盐酸的沉淀产生的原因,甲认为是空气参与反应,乙认为是白雾参与反应。为证实各自的观点,在原实验基础上,甲、乙两同学分别作了如下实验:甲在原有操作之前通N2,一段时间,B中产生大量白色沉淀。乙在A、B间增加盛放饱和NaHSO3溶液的洗气瓶,B中有少量白色沉淀。产生少量沉淀的原因是
(4)结合(3)中两同学的实验现象。你认为原实验B中产生大量白色沉淀的主要原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
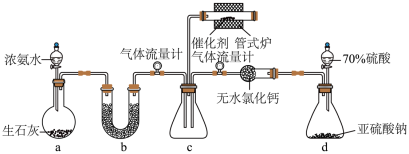
【推荐3】某兴趣小组设计实验模拟探究氨气催化还原焦炉煤气中的SO2,装置如图。
(1)装置a中盛装生石灰的仪器名称为___________ 。
(2)装置d中发生反应的化学方程式为___________ 。
(3)装置b中应盛装的药品为___________(填标号)。
(4)管式炉中反应一段时间后,催化剂表面开始有淡黄色固体生成,反应为 。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。
。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。
过程Ⅰ:
过程Ⅱ: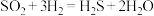
过程Ⅲ:___________ 。
(1)装置a中盛装生石灰的仪器名称为
(2)装置d中发生反应的化学方程式为
(3)装置b中应盛装的药品为___________(填标号)。
A.无水 | B.无水 | C.浓硫酸 | D.碱石灰 |
(4)管式炉中反应一段时间后,催化剂表面开始有淡黄色固体生成,反应为
 。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。
。可以用一组化学方程式表示其反应进程,补充过程Ⅲ的化学方程式。过程Ⅰ:

过程Ⅱ:
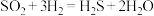
过程Ⅲ:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
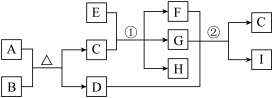
【推荐1】有关物质的转化关系如下图所示(部分物质和条件已略去)。A、C是常见的强酸,B是黄色非金属单质;E是紫红色金属单质,G是最常见的无色液体;D、F、I是常见的气体,D为红棕色,D与I组成元素相同,且相对分子质量相差16。
(1)G的化学式为________ 。
(2)反应①的化学方程式为_____________________________ 。
(3)E与A的浓溶液反应的离子方程式为_________________________________ 。
(4)反应②的化学方程式为_____________________________________ 。
(1)G的化学式为
(2)反应①的化学方程式为
(3)E与A的浓溶液反应的离子方程式为
(4)反应②的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】探究碳、硅元素的非金属性的相对强弱,根据要求完成下列各小题
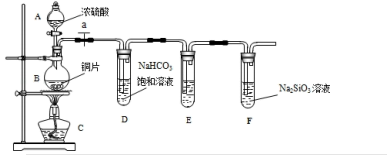
(1)实验装置: 填写所示仪器名称A__________
(2)问题探究:(已知酸性强弱:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是_________ .装置E中足量酸性KMnO4溶液的作用是________ ;
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是_______ ;
③试管D中发生反应的离子方程式是_________ 。

(1)实验装置: 填写所示仪器名称A
(2)问题探究:(已知酸性强弱:亚硫酸>碳酸)
①铜与浓硫酸反应的化学方程式是
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是
③试管D中发生反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】硫酸和硝酸都是重要的化工原料,具有广泛的用途。
(1)蔗糖中加入浓硫酸后,蔗糖变黑且体积膨胀,同时有刺激性气味的气体产生。该变化过程中体现了浓硫酸的___________ ,产生气体的化学方程式为___________ 。
(2)某同学进行有关铜的化学性质的实验,如图所示:
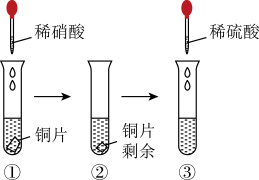
实验①可观察到的现象为___________ (尽可能描述完整);实验③中铜片逐渐溶解至消失,该同学认为铜与稀硫酸和稀硝酸均能反应,这种看法___________ (填“合理”或“不合理”)
(3)如图所示,A是能使湿润的红色石蕊试纸变蓝的气体;C、D均为空气的主要成分;E是一种有毒气体能与血红蛋白结合,反应Ⅱ在三元催化器催化作用下常用于汽车尾气的转化。
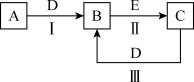
①写出实验室制A的化学方程式:___________ 。A在生产生活中有广泛的用途,写出其中的一个用途:___________ 。
②写出反应Ⅰ的化学方程式___________ ;
③写出反应Ⅱ的化学方程式___________ 。
(1)蔗糖中加入浓硫酸后,蔗糖变黑且体积膨胀,同时有刺激性气味的气体产生。该变化过程中体现了浓硫酸的
(2)某同学进行有关铜的化学性质的实验,如图所示:

实验①可观察到的现象为
(3)如图所示,A是能使湿润的红色石蕊试纸变蓝的气体;C、D均为空气的主要成分;E是一种有毒气体能与血红蛋白结合,反应Ⅱ在三元催化器催化作用下常用于汽车尾气的转化。

①写出实验室制A的化学方程式:
②写出反应Ⅰ的化学方程式
③写出反应Ⅱ的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】硝基苯是重要的化工原料,用途广泛。制备反应如下:
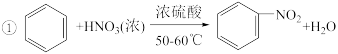
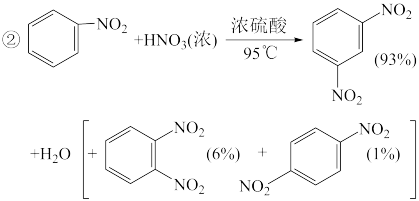
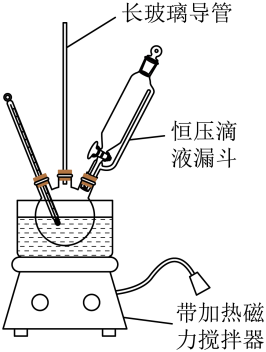
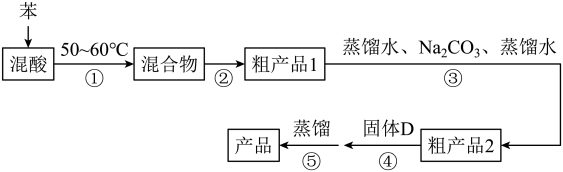
组装如右上图反应装置。 制备、提纯硝基苯流程如下:
可能用到的有关数据列表如下:
请回答下列问题:
(1)配制混酸应在烧杯中先加入__ ;实验装置中长玻璃管最好用________ 代替(填仪器名称);恒压滴液漏斗的优点是__________________ 。
(2)反应温度控制在50~60 ℃的原因是______________ ;反应结束后产物在___ 层(填“上”或者“下”),步骤②分离混酸和产品的操作名称是_____ 。
(3)用Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?_____________ 。
(4)固体D的名称为_____ 。
(5)用铁粉、稀盐酸与硝基苯(用Ph-NO2表示 )反应可生成染料中间体苯胺(Ph-NH2),其反应的化学方程式为______________________________________ 。
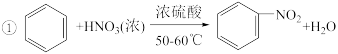


组装如右上图反应装置。 制备、提纯硝基苯流程如下:

可能用到的有关数据列表如下:
| 物 质 | 熔点/℃ | 沸点/℃ | 密度(20 ℃)/g · cm-3 | 溶解性 |
| 苯 | 5.5 | 80 | 0.88 | 微溶于水 |
| 硝基苯 | 5.7 | 210.9 | 1.205 | 难溶于水 |
| 浓硝酸 | — | 83 | 1.4 | 易溶于水 |
| 浓硫酸 | — | 338 | 1.84 | 易溶于水 |
(1)配制混酸应在烧杯中先加入
(2)反应温度控制在50~60 ℃的原因是
(3)用Na2CO3溶液洗涤之后再用蒸馏水洗涤时,怎样验证液体已洗净?
(4)固体D的名称为
(5)用铁粉、稀盐酸与硝基苯(用Ph-NO2表示 )反应可生成染料中间体苯胺(Ph-NH2),其反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】EDTA(乙二胺四乙酸)是螯合剂的代表物(沸点为116~117.2℃),可用于制备EDTAFeNa·3H2O等。实验室制备EDTA的实验步骤如下:
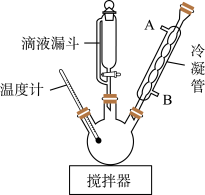
步骤1:在三口烧瓶中加入22.5 g ClCH2COOH、45 mL H2O搅拌至溶解;在不断搅拌下,将含22 g NaOH、60 mL H2O、6.6 g H2NCH2CH2NH2的盐酸盐所配成的溶液,从滴液漏斗中不断滴加到三口烧瓶中。
步骤2:加料完毕后,升温到102~106 ℃并保温,调节并保持 pH约为9,搅拌2 h。
步骤3:加入活性炭,搅拌、静置、过滤。
步骤4:滤液用盐酸酸化至pH=1,放置、结晶、过滤、洗涤、干燥,制得EDTA。
(1)图中冷凝管装置的作用是_____ ,水从接口_____ (填标号)通入。
(2)步骤3中加入活性炭的目的是_____ ;测定溶液pH的方法是_____ 。
(3)步骤4中“洗涤”时,能说明已洗涤完全的方法是_____ 。
(4)请补充完整由EDTA、NaHCO3、FeCl3·6H2O为原料制备EDTAFeNa·3H2O的实验方案(已知EDTANa4+FeCl3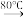 EDTAFeNa + 3NaCl):向250mL烧杯中依次加入160 mL蒸馏水、23 g EDTA,搅拌至完全溶解,
EDTAFeNa + 3NaCl):向250mL烧杯中依次加入160 mL蒸馏水、23 g EDTA,搅拌至完全溶解,_____ ,再分次加入21.6 g FeCl3·6H2O,保温20 min,调pH小于5,冷却、抽滤、洗涤、干燥得EDTAFeNa·3H2O(实验中须使用 的试剂为:NaHCO3,用量为26.8 g)。

步骤1:在三口烧瓶中加入22.5 g ClCH2COOH、45 mL H2O搅拌至溶解;在不断搅拌下,将含22 g NaOH、60 mL H2O、6.6 g H2NCH2CH2NH2的盐酸盐所配成的溶液,从滴液漏斗中不断滴加到三口烧瓶中。
步骤2:加料完毕后,升温到102~106 ℃并保温,调节并保持 pH约为9,搅拌2 h。
步骤3:加入活性炭,搅拌、静置、过滤。
步骤4:滤液用盐酸酸化至pH=1,放置、结晶、过滤、洗涤、干燥,制得EDTA。
(1)图中冷凝管装置的作用是
(2)步骤3中加入活性炭的目的是
(3)步骤4中“洗涤”时,能说明已洗涤完全的方法是
(4)请补充完整由EDTA、NaHCO3、FeCl3·6H2O为原料制备EDTAFeNa·3H2O的实验方案(已知EDTANa4+FeCl3
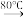 EDTAFeNa + 3NaCl):向250mL烧杯中依次加入160 mL蒸馏水、23 g EDTA,搅拌至完全溶解,
EDTAFeNa + 3NaCl):向250mL烧杯中依次加入160 mL蒸馏水、23 g EDTA,搅拌至完全溶解,
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
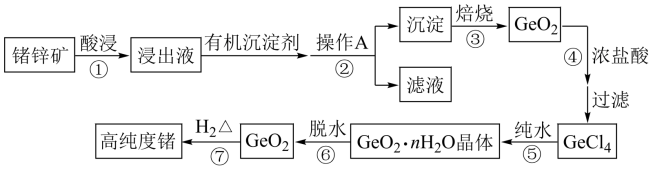
【推荐3】1871年门捷列夫最早预言了类硅元素锗,锗元素在元素周期表中与硅元素同族,并位于硅的下一周期。1886年德国化学家温克勒发现和分离了锗元素,并以其祖国的名字命名为“Ge”。锗是重要的的半导体材料,其有机化合物在治疗癌症方面有着独特的功效。
已知:①丹宁是一种有机沉淀剂,可与四价锗络合形成沉淀:
②GeCl4易水解,在浓盐酸中溶解度低。
(1)锗元素的原子序数为:___________ ;锗元素在元素周期表中的位置是:_____________ 。
(2)GeCl4的结构与SiCl4相似,写出GeCl4的电子式:_______________ 。
(3)简述步骤①中提高酸浸效率的措施____________ 、_____________ (写两种)。
(4)步骤②操作A是___________ (填操作名称)。
(5)步骤③中的物质在___________ (填仪器名称)中加热。
(6)步骤④不选用稀盐酸,而选用浓盐酸的原因可能是__________ 、________ (写出两点)。
(7)写出步骤⑤的化学方程式________________ 。
写出步骤⑦的化学方程式________________ 。
(8)请写出一种证明步骤⑦反应完全的操作方法__________________ 。
已知:①丹宁是一种有机沉淀剂,可与四价锗络合形成沉淀:
②GeCl4易水解,在浓盐酸中溶解度低。

(1)锗元素的原子序数为:
(2)GeCl4的结构与SiCl4相似,写出GeCl4的电子式:
(3)简述步骤①中提高酸浸效率的措施
(4)步骤②操作A是
(5)步骤③中的物质在
(6)步骤④不选用稀盐酸,而选用浓盐酸的原因可能是
(7)写出步骤⑤的化学方程式
写出步骤⑦的化学方程式
(8)请写出一种证明步骤⑦反应完全的操作方法
您最近一年使用:0次



