市售一次电池品种很多,碱性锌锰电池在日常生活中用量很大。回收废旧锌锰电池并进行重新处理,可以获得MnO2及其他副产品,其工艺流程如下:
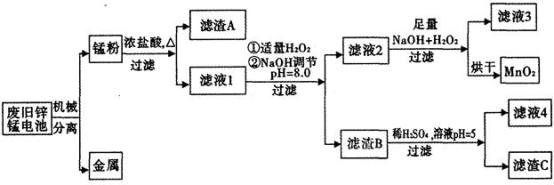
已知:“锰粉”的主要成分有MnO2、Zn(OH)2、MnOOH、碳粉,还含有少量铁盐和亚铁盐。常温下,生成氢氧化物沉淀的pH如下表:
(1)加入NaOH溶液调节pH=8.0,目的是______________________________ ;计算常温下Zn(OH)2的溶度积常数Ksp[Zn(OH)2]=____________________ 。
(2)写出滤液2中的Mn2+变成MnO2的离子方程式_______________________________ 。
(3)写出滤渣B与稀硫酸在pH=5时反应的化学方程式______________________________ 。
(4)工艺中还可以将滤液4进行_____________ 、_____________ 、_____________ 、洗涤得到含结晶水的硫酸盐晶体。
(5)MnO2常用来制取KMnO4。在一定条件下将MnO2氧化为K2MnO4,然后用铁作阴极、铂作阳极电解K2MnO4溶液得到KMnO4。电解K2MnO4溶液的总反应方程式为______________________ 。

已知:“锰粉”的主要成分有MnO2、Zn(OH)2、MnOOH、碳粉,还含有少量铁盐和亚铁盐。常温下,生成氢氧化物沉淀的pH如下表:
| 物质 | Fe(OH)3 | Fe(OH)2 | Zn(OH)2 | Mn(OH)2 / Mn(OH)3 |
| 开始沉淀pH | 2.7 | 7.6 | 5.7 | 8.3 |
| 完全沉淀pH (c≤1.0×10-5mol/L) | 3.7 | 9.6 | 8.0 | 8.8 |
(1)加入NaOH溶液调节pH=8.0,目的是
(2)写出滤液2中的Mn2+变成MnO2的离子方程式
(3)写出滤渣B与稀硫酸在pH=5时反应的化学方程式
(4)工艺中还可以将滤液4进行
(5)MnO2常用来制取KMnO4。在一定条件下将MnO2氧化为K2MnO4,然后用铁作阴极、铂作阳极电解K2MnO4溶液得到KMnO4。电解K2MnO4溶液的总反应方程式为
更新时间:2015-07-15 16:41:23
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】全球对锂资源的需求不断增长,“盐湖提锂”越来越受到重视。某兴趣小组取盐湖水进行浓缩和初步除杂后,得到浓缩卤水(含有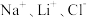 和少量
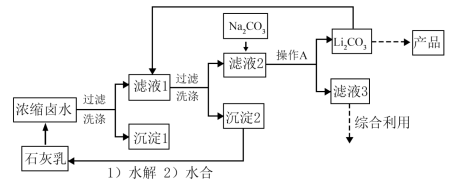
和少量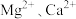 ),并设计了以下流程通过制备碳酸锂来提取锂。
),并设计了以下流程通过制备碳酸锂来提取锂。
 时相关物质的参数如下:
时相关物质的参数如下:  的溶解度:
的溶解度:
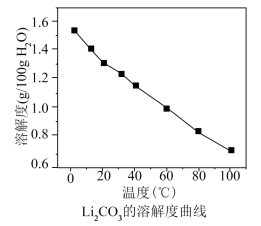
回答下列问题:
(1)“沉淀1”为_______ 。
(2)向“滤液1”中加入适量固体 的目的是
的目的是_______ 。
(3)为提高 的析出量和纯度,“操作A”依次为
的析出量和纯度,“操作A”依次为_______ 、_______ 、洗涤。
(4)有同学建议用“侯氏制碱法”的原理制备 。查阅资料后,发现文献对常温下的
。查阅资料后,发现文献对常温下的 有不同的描述:①是白色固体;②尚未从溶液中分离出来。为探究
有不同的描述:①是白色固体;②尚未从溶液中分离出来。为探究 的性质,将饱和
的性质,将饱和 溶液与饱和
溶液与饱和 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。有关反应的离子方程式为
溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。有关反应的离子方程式为_______ 。
(5)他们结合(4)的探究结果,拟将原流程中向“滤液2”加入 改为通入
改为通入 。这一改动能否达到相同的效果,作出你的判断并给出理由
。这一改动能否达到相同的效果,作出你的判断并给出理由_______ 。
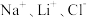 和少量
和少量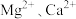 ),并设计了以下流程通过制备碳酸锂来提取锂。
),并设计了以下流程通过制备碳酸锂来提取锂。
 时相关物质的参数如下:
时相关物质的参数如下:  的溶解度:
的溶解度: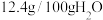
| 化合物 |  |  |  |  |
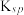 |  | 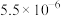 | 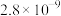 | 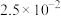 |

回答下列问题:
(1)“沉淀1”为
(2)向“滤液1”中加入适量固体
 的目的是
的目的是(3)为提高
 的析出量和纯度,“操作A”依次为
的析出量和纯度,“操作A”依次为(4)有同学建议用“侯氏制碱法”的原理制备
 。查阅资料后,发现文献对常温下的
。查阅资料后,发现文献对常温下的 有不同的描述:①是白色固体;②尚未从溶液中分离出来。为探究
有不同的描述:①是白色固体;②尚未从溶液中分离出来。为探究 的性质,将饱和
的性质,将饱和 溶液与饱和
溶液与饱和 溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。有关反应的离子方程式为
溶液等体积混合,起初无明显变化,随后溶液变浑浊并伴有气泡冒出,最终生成白色沉淀。有关反应的离子方程式为(5)他们结合(4)的探究结果,拟将原流程中向“滤液2”加入
 改为通入
改为通入 。这一改动能否达到相同的效果,作出你的判断并给出理由
。这一改动能否达到相同的效果,作出你的判断并给出理由
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】以软锰矿粉(含MnO2及少量Fe、Al、Si、Ca、Mg等的氧化物)为原料制备电池级MnO2。
(1)浸取。将一定量软锰矿粉与Na2SO3、H2SO4溶液中的一种配成悬浊液,加入三颈瓶中(如图)。70℃下通过分液漏斗缓慢滴加另一种溶液,充分反应,过滤。滴液漏斗中的溶液是_______ ;MnO2转化为Mn2+的离子方程式为_______ 。 =
=_____ [Ksp(MgF2)=5×10-11,Ksp(CaF2)=5×10-9]
(3)写出基态Mn核外价层电子排布式___________ 。
(4)制备MnCO3。在搅拌下向100mL1mol/LMnSO4溶液中缓慢滴加1mol/LNH4HCO3溶液,过滤、洗涤、干燥,得到MnCO3固体。需加入NH4HCO3溶液的体积约为_______ 。
(1)浸取。将一定量软锰矿粉与Na2SO3、H2SO4溶液中的一种配成悬浊液,加入三颈瓶中(如图)。70℃下通过分液漏斗缓慢滴加另一种溶液,充分反应,过滤。滴液漏斗中的溶液是
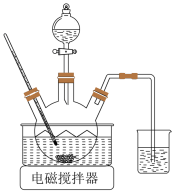
 =
=(3)写出基态Mn核外价层电子排布式
(4)制备MnCO3。在搅拌下向100mL1mol/LMnSO4溶液中缓慢滴加1mol/LNH4HCO3溶液,过滤、洗涤、干燥,得到MnCO3固体。需加入NH4HCO3溶液的体积约为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】高氯酸钾( )是一种微溶于水的白色粉末,具有强氧化性,常用于烟花制作。其制备的工业流程如下图所示。
)是一种微溶于水的白色粉末,具有强氧化性,常用于烟花制作。其制备的工业流程如下图所示。
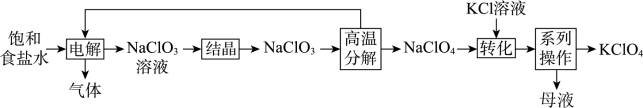
回答下列问题:
(1)“电解”步骤中,电解槽内宜使用_______ (填“阴”或“阳”)离子交换膜,产生的气体主要是_______ 。
(2)“结晶”步骤中,采用缓慢结晶的目的是_______ 。
(3)“高温分解”的化学方程式为_______ 。
(4)已知相关物质的溶解度如下表所示:
①试计算20℃时高氯酸钾的
_______ (保留2位有效数字)。
②“转化”发生反应的离子方程式为_______ 。
(5)“母液”中溶质成分是_______ (填化学式)。
 )是一种微溶于水的白色粉末,具有强氧化性,常用于烟花制作。其制备的工业流程如下图所示。
)是一种微溶于水的白色粉末,具有强氧化性,常用于烟花制作。其制备的工业流程如下图所示。
回答下列问题:
(1)“电解”步骤中,电解槽内宜使用
(2)“结晶”步骤中,采用缓慢结晶的目的是
(3)“高温分解”的化学方程式为
(4)已知相关物质的溶解度如下表所示:
温度/℃ 溶解度/g 物质 | 0 | 10 | 20 | 30 | 40 |
 | 0.76 | 1.06 | 1.68 | 2.56 | 3.73 |
| KCl | 28 | 31.2 | 34.2 | 37.2 | 40.1 |
 | 167 | 183 | 201 | 222 | 245 |

②“转化”发生反应的离子方程式为
(5)“母液”中溶质成分是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】叶蛇纹石是一种富镁硅酸盐矿物[主要成分为Mg6(Si4O10)(OH)8,还含有Al2O3、Fe2O3、FeO等杂质],利用该矿物生产铁红(Fe2O3)和碱式碳酸镁的工艺流程如图所示:
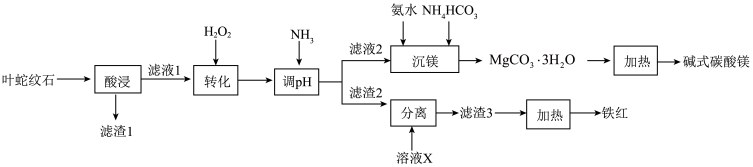
回答下列问题:
(1)“转化”步骤中,温度不能过高的原因是_______ 。“转化”时反应的离子方程式为_______ 。
(2)滤渣2的成分为_______ 。
(3)X通常选用_______ (填化学式)。
(4)“沉镁”步骤中氨水加入的量不能太多,否则MgCO3·H2O的产率会降低,其原因是_______ 。
(5)取9.1g碱式碳酸镁[xMgCO3·yMg(OH)2·zH2O],高温分解后,测得生成3.3gCO2、4.0gMgO,化学式中z=_______ 写出由MgCO3·3H2O生成产品的化学方程式:_______ 。
(6)碱式碳酸镁常用作新型阻燃剂,试分析碱式碳酸镁能够阻燃的原因:_______ 。(写出两点即可)。

回答下列问题:
(1)“转化”步骤中,温度不能过高的原因是
(2)滤渣2的成分为
(3)X通常选用
(4)“沉镁”步骤中氨水加入的量不能太多,否则MgCO3·H2O的产率会降低,其原因是
(5)取9.1g碱式碳酸镁[xMgCO3·yMg(OH)2·zH2O],高温分解后,测得生成3.3gCO2、4.0gMgO,化学式中z=
(6)碱式碳酸镁常用作新型阻燃剂,试分析碱式碳酸镁能够阻燃的原因:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐2】某化学实验室产生的废液中含有 ,
, ,
, 三种金属离子,实验室设计如下方案对废液进行处理,以回收金属并制得氧化铁,保护环境。回答下列问题:
三种金属离子,实验室设计如下方案对废液进行处理,以回收金属并制得氧化铁,保护环境。回答下列问题:
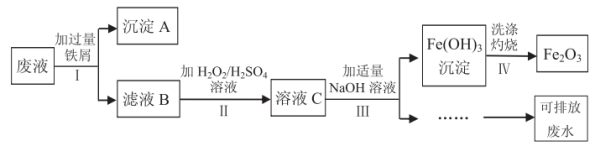
(1)步骤Ⅰ中分离溶液和沉淀的操作是___________ 。
(2)沉淀A中含有的金属单质是铁、___________ (填名称)。
(3)步骤Ⅱ中加入 溶液从浅绿色变为黄色,发生反应的离子方程式为
溶液从浅绿色变为黄色,发生反应的离子方程式为___________ 。
(4)请设计实验方案检验步骤Ⅲ中 是否沉淀完全
是否沉淀完全___________ 。
(5)“可排放废水”中含有的主要离子是___________ (填离子符号)。
 ,
, ,
, 三种金属离子,实验室设计如下方案对废液进行处理,以回收金属并制得氧化铁,保护环境。回答下列问题:
三种金属离子,实验室设计如下方案对废液进行处理,以回收金属并制得氧化铁,保护环境。回答下列问题:
(1)步骤Ⅰ中分离溶液和沉淀的操作是
(2)沉淀A中含有的金属单质是铁、
(3)步骤Ⅱ中加入
 溶液从浅绿色变为黄色,发生反应的离子方程式为
溶液从浅绿色变为黄色,发生反应的离子方程式为(4)请设计实验方案检验步骤Ⅲ中
 是否沉淀完全
是否沉淀完全(5)“可排放废水”中含有的主要离子是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】二氧化氯(ClO2)是一种高效消毒灭菌剂,可有效灭活病毒,但其稳定性较差,故常采用H2O2和NaOH混合溶液将其吸收转化为NaClO2保存。现利用如图装置及试剂制备NaClO2。
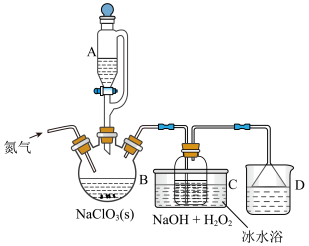
已知:①ClO2的熔点为-59℃,沸点为11℃;稳定性较差,易分解,体积分数大于10%时可能爆炸;ClO2极易溶于水,且在碱性环境中发生反应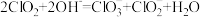 。
。
②高于60℃时NaClO2分解成NaClO3和NaCl。
回答下列问题:
(1)将一定量NaClO3与Na2SO3、H2SO4溶液中的一种配成悬浊液,加入到三颈烧瓶中,通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤。滴液漏斗中的溶液是_______ 。
(2)B为ClO2的发生装置,生成ClO2的离子方程式为_______ 。
(3)实验过程中通入N2的目的是_______ ;实验室可用饱和NaNO2溶液、NH4Cl溶液加入制取N2,化学方程式为_______ 。
(4)装置C中NaOH不能过量的原因是_______ 。
(5)NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出晶体是NaClO2。从NaClO2溶液中获得NaClO2固体的操作:_______ (须使用的试剂:无水乙醇)。

已知:①ClO2的熔点为-59℃,沸点为11℃;稳定性较差,易分解,体积分数大于10%时可能爆炸;ClO2极易溶于水,且在碱性环境中发生反应
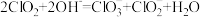 。
。②高于60℃时NaClO2分解成NaClO3和NaCl。
回答下列问题:
(1)将一定量NaClO3与Na2SO3、H2SO4溶液中的一种配成悬浊液,加入到三颈烧瓶中,通过滴液漏斗缓慢滴加另一种溶液,充分反应,过滤。滴液漏斗中的溶液是
(2)B为ClO2的发生装置,生成ClO2的离子方程式为
(3)实验过程中通入N2的目的是
(4)装置C中NaOH不能过量的原因是
(5)NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2·3H2O,高于38℃时析出晶体是NaClO2。从NaClO2溶液中获得NaClO2固体的操作:
您最近一年使用:0次



