10. 氮气化学性质很稳定,可以通过氮的固定将空气中的氮气转化氮的化合物。氮的化合物可用于进一步合成化肥、炸药以及合成树脂等。
(1)写出氮分子的电子式______________。
(2)人工合成氨反应为N
2(g)+3H
2(g)

2NH
3(g) △H=-92.4kJ/mol,在一定条件下的恒容密闭容器中,该反应达到平衡,要提高N
2的转化率,可以采取的措施是________(填序号)。
| A.分离出NH3 |
| B.加入催化剂 |
| C.升高温度 |
| D.增加N2的浓度 |
E.增加H
2的浓度
(3)氨的接触氧化制取硝酸的过程中,900℃时,氨氧化反应阶段可能发生的反应有
编号
| 热化学方程式
| 平衡常数
|
Ⅰ
| 4NH3(g)+5O2(g) 4NO(g)+6H2O (g) △H1 4NO(g)+6H2O (g) △H1
| K1=1×1053
|
Ⅱ
| 4NH3(g)+3O2(g) 2N2(g)+6H2O (g) △H2 2N2(g)+6H2O (g) △H2
| K2=1×1065
|
Ⅲ
| 2NO(g) N2(g)+O2(g) △H3 N2(g)+O2(g) △H3
| K3
|
反应Ⅲ的△H
3=____________(用△H
1、△H
2表示);反应Ⅱ的平衡常数的表达式K
2=__________;
该温度下K
3的计算结果为__________。
(4)催化反硝法可用于治理水中硝酸盐的污染。催化反硝法中,H
2能将NO
3-还原为N
2。25℃时,反应进行10min,溶液的pH由7变为12。反应的离子方程式为____________________________;其平均反应速率为v(NO
3-)______________mol/(L•min)。
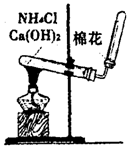
(5)实验室用下图所示装置制取NH
3。若将收集NH
3的试管改为集气瓶且瓶口向上排空气法收集NH
3,并确保不污染环境,请画出其气体收集装置和尾气吸收装置,标出所用试剂(自选)名称。