在容积为1 L的密闭容器中,进行如下反应:
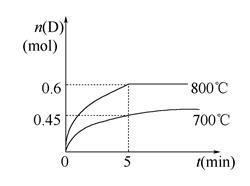
A(g)+2B(g) C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。
C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。
请回答下列问题:
(1) 700℃时,0~5min内,以B表示的平均反应速率为___________ 。
(2) 能判断反应达到化学平衡状态的依据是__________ 。
A.容器中压强不变 B.混合气体中c(A)不变
C.v正(B)=2v逆(D) D.c(A)=c(C)
(3) 若最初加入1.0 mol A和2.2 mol B,利用图中数据计算在800℃时的平衡常数K=__________ ,该反应为__________ 反应(填“吸热”或“放热”)。
(4) 800℃时,某时刻测得体系中物质的量浓度如下:c(A)=0.06 mol/L,c(B)=0.50 mol/L,c(C)=0.20 mol/L,c(D)=0.018 mol/L,则此时该反应__________ (填“向正方向进行”、“向逆方向进行”或“处于平衡状态”)。
A(g)+2B(g)
 C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。
C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。
请回答下列问题:
(1) 700℃时,0~5min内,以B表示的平均反应速率为
(2) 能判断反应达到化学平衡状态的依据是
A.容器中压强不变 B.混合气体中c(A)不变
C.v正(B)=2v逆(D) D.c(A)=c(C)
(3) 若最初加入1.0 mol A和2.2 mol B,利用图中数据计算在800℃时的平衡常数K=
(4) 800℃时,某时刻测得体系中物质的量浓度如下:c(A)=0.06 mol/L,c(B)=0.50 mol/L,c(C)=0.20 mol/L,c(D)=0.018 mol/L,则此时该反应
13-14高二上·陕西西安·期中 查看更多[4]
(已下线)2013-2014学年陕西省西安市一中高二上学期期中考试化学试卷2015届山东省桓台县第二中学高三1月检测化学试卷2016届山东省桓台第二中学高三上学期期中测试化学试卷(已下线)【南昌新东方】江西省九江一中2014-2015学年高二上学期期中化学试卷
更新时间:2016-01-08 16:50:29
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】研究NO2、SO2、CO等大气污染气体的处理具有重要意义。
I. 利用反应:6NO2+8NH3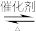 7N2+12H2O处理NO2。
7N2+12H2O处理NO2。
II. 一定条件下NO2与SO2可发生反应,方程式:NO2(g)+SO2(g)⇌ SO3(g)+NO(g) −Q。
III. CO可用于合成甲醇,反应方程式为:CO(g) + 2H2(g)⇌CH3OH(g) 。
(1)对于I中的反应,120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min时,平均反应速率υ(NO2) =_______________ 。
(2)对于II中的反应,将NO2与SO2以体积比1:2置于密闭容器中反应,下列能说明反应达到平衡状态的是_____________ (选填编号)。
a. 体系压强保持不变 b. 混合气体颜色保持不变
c. NO2和SO3的体积比保持不变 d. 混合气体的平均相对分子质量保持不变
(3)如果II中反应的平衡常数K值变大,该反应___________ (选填编号)。
a.一定向正反应方向移动 b. 平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d. 平衡移动时,逆反应速率先增大后减小
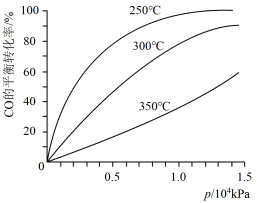
(4)对于III中的反应,CO在不同温度下的平衡转化率与压强的关系如右图示。该反应是_______ 反应(填“放热”或“吸热”)。实际生产条件控制在250℃、1.3×104 kPa左右,简述选择此压强的理由:________________________ 。
I. 利用反应:6NO2+8NH3
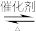 7N2+12H2O处理NO2。
7N2+12H2O处理NO2。II. 一定条件下NO2与SO2可发生反应,方程式:NO2(g)+SO2(g)⇌ SO3(g)+NO(g) −Q。
III. CO可用于合成甲醇,反应方程式为:CO(g) + 2H2(g)⇌CH3OH(g) 。
(1)对于I中的反应,120℃时,该反应在一容积为2L的容器内反应,20min时达到平衡,10min时电子转移了1.2mol,则0~10min时,平均反应速率υ(NO2) =
(2)对于II中的反应,将NO2与SO2以体积比1:2置于密闭容器中反应,下列能说明反应达到平衡状态的是
a. 体系压强保持不变 b. 混合气体颜色保持不变
c. NO2和SO3的体积比保持不变 d. 混合气体的平均相对分子质量保持不变
(3)如果II中反应的平衡常数K值变大,该反应
a.一定向正反应方向移动 b. 平衡移动时,正反应速率先减小后增大
c.一定向逆反应方向移动 d. 平衡移动时,逆反应速率先增大后减小
(4)对于III中的反应,CO在不同温度下的平衡转化率与压强的关系如右图示。该反应是

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】某温度时,在0.5L密闭容器中,某一可逆反应的A、B气体物质的量随时间变化的曲线如图所示,由图中数据分析可得:
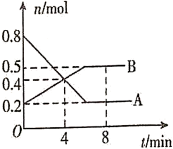
(1)该反应的化学方程式为___ 。
(2)若降低温度,则该反应的正反应速率___ (填“加快”“减慢”或“不变”,下同),逆反应速率___ 。
(3)第4min时,正、逆反应速率的大小关系为v正__ v逆(填“>”“<”或“=”)。
(4)0~4min内,用B的浓度变化来表示该反应的平均反应速率为___ mol/(L·min)。
(5)反应达到平衡,此时体系内压强与开始时的压强之比为___ 。

(1)该反应的化学方程式为
(2)若降低温度,则该反应的正反应速率
(3)第4min时,正、逆反应速率的大小关系为v正
(4)0~4min内,用B的浓度变化来表示该反应的平均反应速率为
(5)反应达到平衡,此时体系内压强与开始时的压强之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】利用元素的化合价推测物质的性质是化学研究的重要手段。如图是硫元素的常见化合价与部分物质类别的对应关系:
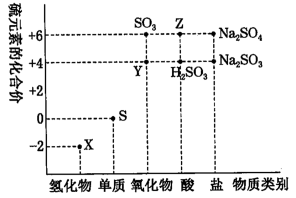
(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有___________ (填化学式)。
(2)将X与Y混合,可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为___________ 。
(3) Z的浓溶液与铜单质在一定条件 下可以发生化学反应,该反应的化学方程式为___________ 。
(4) Na2S2O3是重要的化工原料。从氧化还原反应的角度分析, 下列制备Na2S2O3的方案理论上可行的
是___________ (填字母)。
a.Na2S+S b. Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+ Na2SO4
(5) 2SO2(g) +O2(g) 2SO3(g),是工业制硫酸的主要反应之一,研究该反应的速率和限度有着重要的现实意义。一定条件下, 在2L的密闭容器中加入4molSO2(g)、6molO2(g)和 2molSO3(g),在2min末达到平衡,测得n(SO3)=4mol。
2SO3(g),是工业制硫酸的主要反应之一,研究该反应的速率和限度有着重要的现实意义。一定条件下, 在2L的密闭容器中加入4molSO2(g)、6molO2(g)和 2molSO3(g),在2min末达到平衡,测得n(SO3)=4mol。
①0~2min时间段的化学反应速率为v(SO2)=___________ 。
②2min末c(O2)=___________ mol/L。
③关于2SO2(g) +O2(g) 2SO3(g)反应,下列说法正确的是
2SO3(g)反应,下列说法正确的是 ___________ 。
A.增大氧气的浓度可提高反应速率
B.升高温度可提高反应速率
C.使用催化剂能显著增大反应速率
D.通入过量的氧气可以实现SO2的完全转化

(1)从硫元素化合价变化的角度分析,图中既有氧化性又有还原性的化合物有
(2)将X与Y混合,可生成淡黄色固体,该反应中氧化剂与还原剂的物质的量之比为
(3) Z的浓溶液与铜单质在一定条件 下可以发生化学反应,该反应的化学方程式为
(4) Na2S2O3是重要的化工原料。从氧化还原反应的角度分析, 下列制备Na2S2O3的方案理论上可行的
是
a.Na2S+S b. Na2SO3+S c.SO2+Na2SO4 d.Na2SO3+ Na2SO4
(5) 2SO2(g) +O2(g)
 2SO3(g),是工业制硫酸的主要反应之一,研究该反应的速率和限度有着重要的现实意义。一定条件下, 在2L的密闭容器中加入4molSO2(g)、6molO2(g)和 2molSO3(g),在2min末达到平衡,测得n(SO3)=4mol。
2SO3(g),是工业制硫酸的主要反应之一,研究该反应的速率和限度有着重要的现实意义。一定条件下, 在2L的密闭容器中加入4molSO2(g)、6molO2(g)和 2molSO3(g),在2min末达到平衡,测得n(SO3)=4mol。①0~2min时间段的化学反应速率为v(SO2)=
②2min末c(O2)=
③关于2SO2(g) +O2(g)
 2SO3(g)反应,下列说法正确的是
2SO3(g)反应,下列说法正确的是 A.增大氧气的浓度可提高反应速率
B.升高温度可提高反应速率
C.使用催化剂能显著增大反应速率
D.通入过量的氧气可以实现SO2的完全转化
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致:N2(g)+O2(g)⇌2NO(g)ΔH>0,已知该反应在2404℃,平衡常数K=6.4×10-4。请回答:
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟时达平衡O2的物质的量为0.5mol,则5分钟内N2的反应速率为___________ ,N2的转化率是___________ 。
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志是___________。
(3)将N2、O2的混合气体充入恒温恒容密闭容器中,下图变化趋势正确的是______ (填字母序号)。
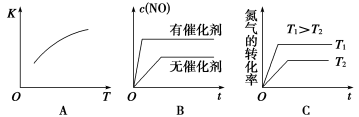
(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数________ (填“变大”、“变小”或“不变”)
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应___________ (填“处于化学平衡状态”、“向正反应方向进行”或“向逆反应方向进行”),理由是___________ 。
(1)某温度下,向2L的密闭容器中充入N2和O2各1mol,5分钟时达平衡O2的物质的量为0.5mol,则5分钟内N2的反应速率为
(2)假定该反应是在恒容条件下进行,判断该反应达到平衡的标志是___________。
| A.消耗1molN2同时生成1molO2 | B.混合气体密度不变 |
| C.混合气体平均相对分子质量不变 | D.2v正(N2)=v逆(NO) |

(4)向恒温恒容的密闭容器中充入等物质的量的N2和O2,达到平衡状态后再向其中充入一定量NO,重新达到化学平衡状态。与原平衡状态相比,此时平衡混合气中NO的体积分数
(5)该温度下,某时刻测得容器内N2、O2、NO的浓度分别为2.5×10-1mol/L、4.0×10-2mol/L和3.0×10-3mol/L,此时反应
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
(1)该反应的化学方程式为____________________ ;
(2)反应开始至2min,以气体Z表示的平均反应速率为______________________ ;
(3)平衡时容器内混合气体密度比起始时__________ (填“变大”,“变小”或“相等”下同),混合气体的平均相对分子质量比起始时___________ ;
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:
n(X)=n(Y)=2n(Z),则原混合气体中a:b=___________ 。
(5)在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的反应速率之比等于化学计量数之比
(Ⅰ)一定能证明2SO2(g)+O2(g) 2SO3(g)达到平衡状态的是
2SO3(g)达到平衡状态的是_______ (填序号,下同)。
(Ⅱ)一定能证明I2(g)+H2(g) 2HI(g)达到平衡状态的是
2HI(g)达到平衡状态的是 _________ 。
(Ⅲ)一定能证明A(s)+2B(g) C(g)+D(g)达到平衡状态的是
C(g)+D(g)达到平衡状态的是________ 。
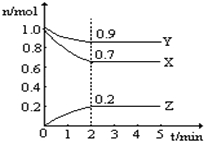
(1)该反应的化学方程式为
(2)反应开始至2min,以气体Z表示的平均反应速率为
(3)平衡时容器内混合气体密度比起始时
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:
n(X)=n(Y)=2n(Z),则原混合气体中a:b=
(5)在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的反应速率之比等于化学计量数之比
(Ⅰ)一定能证明2SO2(g)+O2(g)
 2SO3(g)达到平衡状态的是
2SO3(g)达到平衡状态的是(Ⅱ)一定能证明I2(g)+H2(g)
 2HI(g)达到平衡状态的是
2HI(g)达到平衡状态的是 (Ⅲ)一定能证明A(s)+2B(g)
 C(g)+D(g)达到平衡状态的是
C(g)+D(g)达到平衡状态的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】一定温度下,向容积为2L的恒容密闭容器中加入等物质的量的H2和I2,发生反应H2(g)+I2(g)⇌2HI(g) 。测得不同反应时间容器内H2的物质的量如表;
回答下列问题:
(1)0~20min内HI的平均反应速率为________ 。
(2)反应达到化学平衡状态时,I2的转化率为______ 。
(3)该条件下,能说明上述反应达到化学平衡状态的是____ 。(填标号)
A.混合气体颜色不再改变 B.容器内压强不再改变
C.H2、I2、HI三种气体体积分数不再改变 D.混合气体密度不再改变
(4)该反应在三种不同情况下的化学反应速率分别为:①v(H2)=0.02mol·L-1·s-1,②v(I2)=0.32mol·L-1·min-1,③v(HI)=0.84mol·L-1·min-1。则反应进行的速率由快到慢的顺序为____ 。
| 时间/min | 0 | 10 | 20 | 30 | 40 |
| n(H2)/mol | 1 | 0.75 | 0.65 | 0.6 | 0.6 |
回答下列问题:
(1)0~20min内HI的平均反应速率为
(2)反应达到化学平衡状态时,I2的转化率为
(3)该条件下,能说明上述反应达到化学平衡状态的是
A.混合气体颜色不再改变 B.容器内压强不再改变
C.H2、I2、HI三种气体体积分数不再改变 D.混合气体密度不再改变
(4)该反应在三种不同情况下的化学反应速率分别为:①v(H2)=0.02mol·L-1·s-1,②v(I2)=0.32mol·L-1·min-1,③v(HI)=0.84mol·L-1·min-1。则反应进行的速率由快到慢的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】脱除工业废气中的氮氧化物(主要指NO和NO2)可以净化空气、改善环境,是环境保护的重要课题。
(1)以漂粉精溶液为吸收剂可以有效脱除烟气中的NO。
①漂粉精溶液的主要成分是Ca(ClO)2,若吸收过程中,消耗的Ca(ClO)2与吸收的NO的物质的量之比为3∶4,则脱除后NO转化为_______ (填离子符号)。
②某化学兴趣小组研究不同温度下相同浓度漂粉精溶液对NO脱除率的影响,结果如图1所示。图1中,40~60 ℃区间 NO脱除率上升的原因为_______ ;60~80 ℃ 区间NO脱除率下降的原因可能为_______ (写一点即可)。

(2)以过硫酸钠(Na2S2O8)为氧化剂是一种新型除NO方法。
第一步:NO在碱性环境中被Na2S2O8氧化为NaNO2;
第二步:NaNO2继续被氧化为NaNO3,反应为NO +S2O
+S2O +2OH-⇌NO
+2OH-⇌NO +2SO
+2SO +H2O。
+H2O。
不同温度下,平衡时NO 的脱除率与过硫酸钠溶液初始浓度(指第二步反应的初始浓度)的关系如图2 所示。
的脱除率与过硫酸钠溶液初始浓度(指第二步反应的初始浓度)的关系如图2 所示。
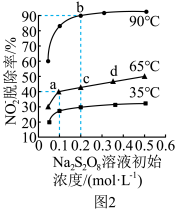
①若要平衡时NO 的脱除率至少达到90%,应选择的适宜条件是
的脱除率至少达到90%,应选择的适宜条件是_______ 。
②a、b、c三点对应平衡常数Ka、Kb、Kc的大小关系为_______ 。
③65 ℃时,NO 的初始浓度为c mol·L-1,平衡时c(OH-)=0.1 mol·L-1,该温度下第二步反应的平衡常数K=
的初始浓度为c mol·L-1,平衡时c(OH-)=0.1 mol·L-1,该温度下第二步反应的平衡常数K=_______ (用含c的代数式表示)。
(1)以漂粉精溶液为吸收剂可以有效脱除烟气中的NO。
①漂粉精溶液的主要成分是Ca(ClO)2,若吸收过程中,消耗的Ca(ClO)2与吸收的NO的物质的量之比为3∶4,则脱除后NO转化为
②某化学兴趣小组研究不同温度下相同浓度漂粉精溶液对NO脱除率的影响,结果如图1所示。图1中,40~60 ℃区间 NO脱除率上升的原因为

(2)以过硫酸钠(Na2S2O8)为氧化剂是一种新型除NO方法。
第一步:NO在碱性环境中被Na2S2O8氧化为NaNO2;
第二步:NaNO2继续被氧化为NaNO3,反应为NO
 +S2O
+S2O +2OH-⇌NO
+2OH-⇌NO +2SO
+2SO +H2O。
+H2O。不同温度下,平衡时NO
 的脱除率与过硫酸钠溶液初始浓度(指第二步反应的初始浓度)的关系如图2 所示。
的脱除率与过硫酸钠溶液初始浓度(指第二步反应的初始浓度)的关系如图2 所示。
①若要平衡时NO
 的脱除率至少达到90%,应选择的适宜条件是
的脱除率至少达到90%,应选择的适宜条件是②a、b、c三点对应平衡常数Ka、Kb、Kc的大小关系为
③65 ℃时,NO
 的初始浓度为c mol·L-1,平衡时c(OH-)=0.1 mol·L-1,该温度下第二步反应的平衡常数K=
的初始浓度为c mol·L-1,平衡时c(OH-)=0.1 mol·L-1,该温度下第二步反应的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】在密闭容器中发生下列反应:I2(g)+H2(g) 2HI(g)(正反应为放热反应)。起始时,n(H2)=a mol,n(I2)=b mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变填入相关的表格中(填“增大”“减小”或“不变”)。
2HI(g)(正反应为放热反应)。起始时,n(H2)=a mol,n(I2)=b mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变填入相关的表格中(填“增大”“减小”或“不变”)。
 2HI(g)(正反应为放热反应)。起始时,n(H2)=a mol,n(I2)=b mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变填入相关的表格中(填“增大”“减小”或“不变”)。
2HI(g)(正反应为放热反应)。起始时,n(H2)=a mol,n(I2)=b mol。只改变表中列出的条件,其他条件不变,试将化学反应速率的改变填入相关的表格中(填“增大”“减小”或“不变”)。| 编号 | 改变的条件 | 反应速率 |
| (1) | 升高温度 | |
| (2) | 加入正催化剂 | |
| (3) | 再充入a mol H2 | |
| (4) | 将容器的容积扩大到原来的2倍 | |
| (5) | 保持容积不变,通入b mol Ne |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】研究含氮元素物质的反应对生产、生活、科研等方面具有重要的意义。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼(C2H8N2)。
已知:①C2H8N2(l)+4O2(g)=2CO2(g)+N2(g)+4H2O(l) ΔH1=-2765.0kJ/mol
②2O2(g) +N2(g)=N2O4(l) ΔH2=-19.5kJ/mol
③H2O(g)= H2O(l) ΔH3=-44.0kJ/mol
则C2H8N2(l)+2N2O4(1)=3N2(g)+2CO2(g)+4H2O(g)的ΔH为_______ 。
(2)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步:I2(g)→2I(g)(快反应)
第二步:I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步:IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是_______。
(3)为避免汽车尾气中的氮氧化合物对大气的污染,需给汽车安装尾气净化装置。在净化装置中CO和NO发生反应2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH=-746.8kJ-mol-1.实验测得:v正=k正·p2(NO)·p2(CO),v逆=k逆·p(N2)·p2(CO2)。其中k正、k逆分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=物质的量分数x总压)。
N2(g)+2CO2(g) ΔH=-746.8kJ-mol-1.实验测得:v正=k正·p2(NO)·p2(CO),v逆=k逆·p(N2)·p2(CO2)。其中k正、k逆分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=物质的量分数x总压)。
①达到平衡后,仅升高温度,k正增大的倍数_______ (填“大于”“小于”或“等于”)k逆增大的倍数。
②一定温度下在刚性密闭容器中充入CO、NO和N2物质的量之比为2:2:1,压强为P0kPa。达平衡时压强为0.9P0kPa,则平衡时CO的转化率为_______ ,
_______ 。
(4)我国科技人员计算了在一定温度范围内下列反应的平衡常数Kp:
①3N2H4(1) 4NH3(g)+N2(g) ΔH1 Kp1
4NH3(g)+N2(g) ΔH1 Kp1
②4NH3(g) 2N2(g)+6H2(g) ΔH2 Kp2
2N2(g)+6H2(g) ΔH2 Kp2
绘制pKp1-T和pKp2-T的线性关系图如图所示:(已知:pKp=-1gKp)
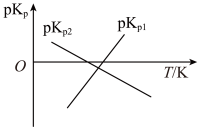
①由图可知,ΔH1_______ 0(填“>”或“<”)
②反应3N2H4(1) 3N2(g)+6H2(g)的K=
3N2(g)+6H2(g)的K=_______ (用Kp1、Kp2表示);该反应的ΔH_______ 0(填“>”或“<”)。
(1)发射“神舟十三”号的火箭推进剂为液态四氧化二氮和液态偏二甲肼(C2H8N2)。
已知:①C2H8N2(l)+4O2(g)=2CO2(g)+N2(g)+4H2O(l) ΔH1=-2765.0kJ/mol
②2O2(g) +N2(g)=N2O4(l) ΔH2=-19.5kJ/mol
③H2O(g)= H2O(l) ΔH3=-44.0kJ/mol
则C2H8N2(l)+2N2O4(1)=3N2(g)+2CO2(g)+4H2O(g)的ΔH为
(2)碘蒸气存在能大幅度提高N2O的分解速率,反应历程为:
第一步:I2(g)→2I(g)(快反应)
第二步:I(g)+N2O(g)→N2(g)+IO(g)(慢反应)
第三步:IO(g)+N2O(g)→N2(g)+O2(g)+I2(g)(快反应)
实验表明,含碘时N2O分解速率方程v=k·c(N2O)·[c(I2)]0.5(k为速率常数)。下列表述正确的是_______。
| A.N2O分解反应中,k值与碘蒸气浓度大小有关 |
| B.v(第二步的逆反应)<v(第三步反应) |
| C.IO为反应的催化剂 |
| D.第二步活化能比第三步大 |
 N2(g)+2CO2(g) ΔH=-746.8kJ-mol-1.实验测得:v正=k正·p2(NO)·p2(CO),v逆=k逆·p(N2)·p2(CO2)。其中k正、k逆分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=物质的量分数x总压)。
N2(g)+2CO2(g) ΔH=-746.8kJ-mol-1.实验测得:v正=k正·p2(NO)·p2(CO),v逆=k逆·p(N2)·p2(CO2)。其中k正、k逆分别为正、逆反应速率常数,只与温度有关;p为气体分压(分压=物质的量分数x总压)。①达到平衡后,仅升高温度,k正增大的倍数
②一定温度下在刚性密闭容器中充入CO、NO和N2物质的量之比为2:2:1,压强为P0kPa。达平衡时压强为0.9P0kPa,则平衡时CO的转化率为

(4)我国科技人员计算了在一定温度范围内下列反应的平衡常数Kp:
①3N2H4(1)
 4NH3(g)+N2(g) ΔH1 Kp1
4NH3(g)+N2(g) ΔH1 Kp1②4NH3(g)
 2N2(g)+6H2(g) ΔH2 Kp2
2N2(g)+6H2(g) ΔH2 Kp2绘制pKp1-T和pKp2-T的线性关系图如图所示:(已知:pKp=-1gKp)

①由图可知,ΔH1
②反应3N2H4(1)
 3N2(g)+6H2(g)的K=
3N2(g)+6H2(g)的K=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某兴趣小组对该反应进行了实验探究。在一定温度和催化剂的条件下,将0.1molNH3通入3L的密闭容器中进行反应(此时容器内总压为200kPa),各物质的分压随时间的变化曲线如图所示。

在该温度下,反应的标准平衡常数K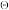 =
=___________ 。(已知:分压=总压×该组分物质的量分数,对于反应dD(g)+eE(g) gG(g)+hH(g),K
gG(g)+hH(g),K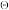 =
= ,其中p
,其中p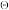 =100kPa,PG、PH、PD、PE为各组分的平衡分压)。
=100kPa,PG、PH、PD、PE为各组分的平衡分压)。

在该温度下,反应的标准平衡常数K
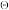 =
= gG(g)+hH(g),K
gG(g)+hH(g),K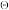 =
= ,其中p
,其中p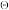 =100kPa,PG、PH、PD、PE为各组分的平衡分压)。
=100kPa,PG、PH、PD、PE为各组分的平衡分压)。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:
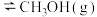
(1)下表所列数据是该反应在不同温度下的化学平衡常数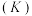
①该反应的平衡常数表达式
______________ ,
__________  填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。
。
②某温度下,将 和
和 充入2L的密闭容器中,充分反应10min后,达到平衡时测得
充入2L的密闭容器中,充分反应10min后,达到平衡时测得 ,则CO的转化率为
,则CO的转化率为____________ ,此时的温度为_________ 。
(2)向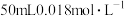 的
的 溶液中加入
溶液中加入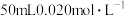 的盐酸,生成沉淀。已知该温度下AgCl的
的盐酸,生成沉淀。已知该温度下AgCl的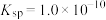 ,忽略溶液的体积变化,请计算:
,忽略溶液的体积变化,请计算:
①完全沉淀后,溶液中
________ 。
②完全沉淀后,溶液的
________ 。

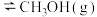
(1)下表所列数据是该反应在不同温度下的化学平衡常数
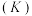
| 温度 | 250℃ | 300℃ | 350℃ |
| K |  |  |  |
①该反应的平衡常数表达式


 填“
填“ ”、“
”、“ ”或“
”或“ ”
” 。
。 ②某温度下,将
 和
和 充入2L的密闭容器中,充分反应10min后,达到平衡时测得
充入2L的密闭容器中,充分反应10min后,达到平衡时测得 ,则CO的转化率为
,则CO的转化率为(2)向
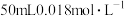 的
的 溶液中加入
溶液中加入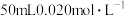 的盐酸,生成沉淀。已知该温度下AgCl的
的盐酸,生成沉淀。已知该温度下AgCl的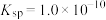 ,忽略溶液的体积变化,请计算:
,忽略溶液的体积变化,请计算:①完全沉淀后,溶液中

②完全沉淀后,溶液的

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在一固定容积的密闭容器中进行如下反应:CO2(g)+H2(g)⇌CO(g)+H2O(g)。其平衡常数K和温度t的关系如下:
(1)该反应的正反应为_______ 反应(“吸热”或“放热”);
(2)在某温度下,能判断该反应是否已经达到化学平衡状态的是:_______
(3)在850℃时,反应:CO2(g) + H2(g)⇌CO(g) + H2O(g),在该容器内各物质的浓度变化如下:
计算:3min—4min达到平衡时CO的平衡浓度c3是_______ ;CO2 (g)的转化率是_______ 。
| t℃ | 700 | 800 | 850 | 1000 | 1200 |
| K | 2.6 | 1.7 | 1.0 | 0.9 | 0.6 |
(1)该反应的正反应为
(2)在某温度下,能判断该反应是否已经达到化学平衡状态的是:_______
| A.容器中压强不变 | B.混合气体中CO浓度不变 |
| C.v(H2)正 = v(H2O)逆 | D.c(CO2) = c(CO) |
| 时间/min | CO2 (mol/L) | H2 (mol/L) | CO (mol/L) | H2 O ( mol/L) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
计算:3min—4min达到平衡时CO的平衡浓度c3是
您最近一年使用:0次



