X、Y、Z三种气体都能对大气造成污染,在工业上都可以用碱液吸收。已知X是化石燃料燃烧的产物之一,是形成酸雨的主要物质;Y是一种单质,它的水溶液具有漂白作用;Z是硝酸工业和汽车尾气中的有害物质之一,能与水反应。
请写出下列反应的化学方程式。
(1)X溶于雨水,形成酸雨_____________________ ;
(2)Y与NaOH溶液反应________________________ ;
(3)Z与水反应________________________ 。
请写出下列反应的化学方程式。
(1)X溶于雨水,形成酸雨
(2)Y与NaOH溶液反应
(3)Z与水反应
更新时间:2016-12-09 06:45:23
|
相似题推荐
填空题
|
较难
(0.4)
名校
【推荐1】某学习小组采用分类的思想,利用抽象方程式:A+H2O→B+C总结常见物质的相关知识。
(1)若A为单质:
①如果B的水溶液能刻蚀玻璃,写出刻蚀玻璃的化学方程式_____ 。
②如果金属氧化物B是磁谱仪的核心部件材料,则验证B中金属元素化合价需要的试剂有_____ 。
(2)若A为氧化物:
③如果A常作漂白剂和供氧剂,则A的电子式为_____ 。
④如果B是王水成分之一,写出实验室吸收尾气A的离子方程式_____ 。
(3)若A为氢化物:
⑤如果C为还原性单质气体,则A中化学键类型为_____ 。
(4)若A为金属氮化物:
⑥写出检验碱性气体C的实验操作_____ 。
(5)请写出A除上述类别外也符合抽象方程式条件的一个化学方程式_____ 。
(1)若A为单质:
①如果B的水溶液能刻蚀玻璃,写出刻蚀玻璃的化学方程式
②如果金属氧化物B是磁谱仪的核心部件材料,则验证B中金属元素化合价需要的试剂有
(2)若A为氧化物:
③如果A常作漂白剂和供氧剂,则A的电子式为
④如果B是王水成分之一,写出实验室吸收尾气A的离子方程式
(3)若A为氢化物:
⑤如果C为还原性单质气体,则A中化学键类型为
(4)若A为金属氮化物:
⑥写出检验碱性气体C的实验操作
(5)请写出A除上述类别外也符合抽象方程式条件的一个化学方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐2】工业或机动车尾气中的NOx会造成环境问题,可用多种方法脱除。
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含 ),获得副产品
),获得副产品 。
。
①等物质的量NO与NO2被NaOH溶液吸收,反应的离子方程式为_______ 。
②若吸收时NO与NO2比例控制不当,则吸收液经浓缩结晶、过滤得到 晶体中最有可能混有的杂质是
晶体中最有可能混有的杂质是_______ (填化学式)。排放的尾气中含量较高的氮氧化物是_______ (填化学式)。
(2)还原法:尿素水溶液热解产生的NH3可去除尾气中的NOx,流程如下:
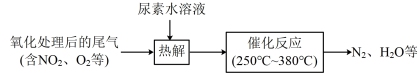
①尿素 中氮元素的化合价为
中氮元素的化合价为_______ 。
②写出“催化反应”过程中NH3还原NO2的化学方程式_______ 。
③若氧化处理后的尾气中混有SO2,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低NOx的去除率。试分析硫酸盐的产生过程_______ 。
④“催化反应”过程中需控制温度在 之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低和
之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低和_______ 。
(1)碱液吸收:NaOH溶液可吸收硝酸工业尾气(含
 ),获得副产品
),获得副产品 。
。①等物质的量NO与NO2被NaOH溶液吸收,反应的离子方程式为
②若吸收时NO与NO2比例控制不当,则吸收液经浓缩结晶、过滤得到
 晶体中最有可能混有的杂质是
晶体中最有可能混有的杂质是(2)还原法:尿素水溶液热解产生的NH3可去除尾气中的NOx,流程如下:

①尿素
 中氮元素的化合价为
中氮元素的化合价为②写出“催化反应”过程中NH3还原NO2的化学方程式
③若氧化处理后的尾气中混有SO2,此时催化剂表面会因为覆盖部分硫酸盐而导致催化剂中毒,降低NOx的去除率。试分析硫酸盐的产生过程
④“催化反应”过程中需控制温度在
 之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低和
之间。温度过高,NOx的去除率下降,其原因可能是温度过高催化剂的活性降低和
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐3】按要求回答下列问题:
(1)实验室制备氨气,下列方法中可以选用的是_______ ;
a.固态氯化铵加热分解 b.浓氨水中加入固体氢氧化钠
c.加热浓氨水 d.固态氯化铵与氢氧化钙混合加热
(2)氨的水溶液叫做氨水,用离子方程式表示氨水呈碱性的原因_______ ;
(3)NH3常用于检验氯气管道是否泄漏,写出反应的化学方程式_______ 。
(4)将57.6克的铜投入200毫升的硝酸溶液中恰好反应完全,产生标准状况下的NO2、NO共1.4 mol。
①写出刚开始反应的化学方程式_______ ;
②求硝酸的浓度_______ mol·L-1;
③将生成的气体收集在大试管中,然后倒扣在水中,写出二氧化氮与水反应的化学方程式_______ ,若往试管中通入氧气让液体充满试管,则通入氧气的物质的量_______ mol。
(1)实验室制备氨气,下列方法中可以选用的是
a.固态氯化铵加热分解 b.浓氨水中加入固体氢氧化钠
c.加热浓氨水 d.固态氯化铵与氢氧化钙混合加热
(2)氨的水溶液叫做氨水,用离子方程式表示氨水呈碱性的原因
(3)NH3常用于检验氯气管道是否泄漏,写出反应的化学方程式
(4)将57.6克的铜投入200毫升的硝酸溶液中恰好反应完全,产生标准状况下的NO2、NO共1.4 mol。
①写出刚开始反应的化学方程式
②求硝酸的浓度
③将生成的气体收集在大试管中,然后倒扣在水中,写出二氧化氮与水反应的化学方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐1】回答以下问题:
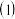 将已去除表面氧化物的铁钉
将已去除表面氧化物的铁钉 碳素钢
碳素钢 放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是
放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是 ______ .
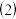 另称取已去除表面氧化物的铁钉
另称取已去除表面氧化物的铁钉 碳素钢
碳素钢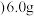 放入
放入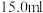 浓硫酸中,加热,充分应后得到溶液X并收集到气体Y.
浓硫酸中,加热,充分应后得到溶液X并收集到气体Y.
①甲同学认为X中除 外还可能含有
外还可能含有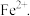 写出生成
写出生成 所有可能的离子方程式:
所有可能的离子方程式: ______ .
②乙同学取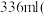 标准状况
标准状况 气体Y通入足量溴水中,发生反应的化学方程式为:
气体Y通入足量溴水中,发生反应的化学方程式为: ______ .
然后加入足量 溶液,经适当操作后得干燥固体
溶液,经适当操作后得干燥固体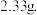 由于此推知气体Y中
由于此推知气体Y中 的体积分数为
的体积分数为 ______ .
 向100ml水中投入Na和Al共16克,充分反应后剩余金属
向100ml水中投入Na和Al共16克,充分反应后剩余金属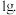 计算放出
计算放出 的体积为
的体积为 ______ 升 标准状况下
标准状况下
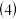 向含有
向含有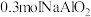 的溶液中滴加
的溶液中滴加 HCl,当生成
HCl,当生成 克沉淀时,加入盐酸的体积为
克沉淀时,加入盐酸的体积为 ______ 
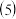 向一定量的Fe、
向一定量的Fe、 和CuO混合物投入120ml
和CuO混合物投入120ml  的硫酸溶液中,充分反应后生成896mL标准状况下的气体,得不溶物
的硫酸溶液中,充分反应后生成896mL标准状况下的气体,得不溶物 ,过滤后,向滤液中加入
,过滤后,向滤液中加入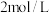 的NaOH溶液,加至40mL时开始出现沉淀,则滤液中
的NaOH溶液,加至40mL时开始出现沉淀,则滤液中 的物质的量浓度为
的物质的量浓度为 设滤液体积为
设滤液体积为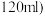
______  .
.
 将已去除表面氧化物的铁钉
将已去除表面氧化物的铁钉 碳素钢
碳素钢 放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是
放入冷浓硫酸中,10分钟后移入硫酸铜溶液中,片刻后取出观察,铁钉表面无明显变化,其原因是  另称取已去除表面氧化物的铁钉
另称取已去除表面氧化物的铁钉 碳素钢
碳素钢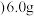 放入
放入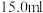 浓硫酸中,加热,充分应后得到溶液X并收集到气体Y.
浓硫酸中,加热,充分应后得到溶液X并收集到气体Y.①甲同学认为X中除
 外还可能含有
外还可能含有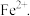 写出生成
写出生成 所有可能的离子方程式:
所有可能的离子方程式: ②乙同学取
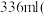 标准状况
标准状况 气体Y通入足量溴水中,发生反应的化学方程式为:
气体Y通入足量溴水中,发生反应的化学方程式为: 然后加入足量
 溶液,经适当操作后得干燥固体
溶液,经适当操作后得干燥固体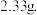 由于此推知气体Y中
由于此推知气体Y中 的体积分数为
的体积分数为  向100ml水中投入Na和Al共16克,充分反应后剩余金属
向100ml水中投入Na和Al共16克,充分反应后剩余金属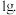 计算放出
计算放出 的体积为
的体积为  标准状况下
标准状况下
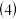 向含有
向含有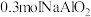 的溶液中滴加
的溶液中滴加 HCl,当生成
HCl,当生成 克沉淀时,加入盐酸的体积为
克沉淀时,加入盐酸的体积为 
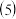 向一定量的Fe、
向一定量的Fe、 和CuO混合物投入120ml
和CuO混合物投入120ml  的硫酸溶液中,充分反应后生成896mL标准状况下的气体,得不溶物
的硫酸溶液中,充分反应后生成896mL标准状况下的气体,得不溶物 ,过滤后,向滤液中加入
,过滤后,向滤液中加入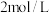 的NaOH溶液,加至40mL时开始出现沉淀,则滤液中
的NaOH溶液,加至40mL时开始出现沉淀,则滤液中 的物质的量浓度为
的物质的量浓度为 设滤液体积为
设滤液体积为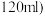
 .
.
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】为测定空气中 的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的200mL0.100mol/L的酸性
的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的200mL0.100mol/L的酸性 溶液。已知
溶液。已知 与该溶液反应的离子方程式为:
与该溶液反应的离子方程式为: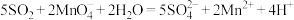 ,若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的
,若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的 可被溶液充分吸收,则该空气样品中
可被溶液充分吸收,则该空气样品中 的含量(单位为g/L)是
的含量(单位为g/L)是__________ 。
 的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的200mL0.100mol/L的酸性
的含量,某课外小组的同学将空气样品经过管道通入密闭容器中的200mL0.100mol/L的酸性 溶液。已知
溶液。已知 与该溶液反应的离子方程式为:
与该溶液反应的离子方程式为: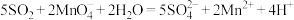 ,若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的
,若管道中空气流量为aL/min,经过bmin溶液恰好褪色,假定样品中的 可被溶液充分吸收,则该空气样品中
可被溶液充分吸收,则该空气样品中 的含量(单位为g/L)是
的含量(单位为g/L)是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】硫酸工业生产应考虑综合经济效益问题。
(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在___________ 的郊区(填选项的标号)
a. 有丰富黄铁矿资源的城市 b. 风光秀丽的旅游城市
c. 消耗硫酸甚多的工业城市 d. 人口稠密的文化、商业中心城市
(2)据测算,接触法制硫酸过程中,若反应热都未被利用,则每生产1t 98%硫酸需消耗3.6×105kJ能量。请通过计算判断,若反应:SO2(g)+1/2O2(g) ⇌SO3(g);△H=-98.3kJ·mol-1;放出的热量能在生产过程中得到充分利用,则每生产1t98%硫酸只需外界提供(或可向外界输出)__________ 千焦能量;
(3)CuFeS2是黄铁矿的另一成分,煅烧时,CuFeS2转化为CuO、Fe2O3和SO2,该反应的化学方程式为____________________ 。
(4)由硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4(由CuO与SO3在沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度不同而变化(见下表)
已知CuSO4在低于660℃时不会分解,请简要分析上表中CuSO4的质量分数随温度升高而降低的原因________________________________________ 。
(1)若从下列四个城市中选择一处新建一座硫酸厂,你认为厂址宜选在
a. 有丰富黄铁矿资源的城市 b. 风光秀丽的旅游城市
c. 消耗硫酸甚多的工业城市 d. 人口稠密的文化、商业中心城市
(2)据测算,接触法制硫酸过程中,若反应热都未被利用,则每生产1t 98%硫酸需消耗3.6×105kJ能量。请通过计算判断,若反应:SO2(g)+1/2O2(g) ⇌SO3(g);△H=-98.3kJ·mol-1;放出的热量能在生产过程中得到充分利用,则每生产1t98%硫酸只需外界提供(或可向外界输出)
(3)CuFeS2是黄铁矿的另一成分,煅烧时,CuFeS2转化为CuO、Fe2O3和SO2,该反应的化学方程式为
(4)由硫酸厂沸腾炉排出的矿渣中含有Fe2O3、CuO、CuSO4(由CuO与SO3在沸腾炉中化合而成),其中硫酸铜的质量分数随沸腾炉温度不同而变化(见下表)
| 沸腾炉温度/℃ | 600 | 620 | 640 | 660 |
| 矿渣中CuSO4的质量分数/% | 9.3 | 9.2 | 9.0 | 8.4 |
已知CuSO4在低于660℃时不会分解,请简要分析上表中CuSO4的质量分数随温度升高而降低的原因
您最近一年使用:0次



