T ℃时,在2 L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。则下列结论不正确的是( )
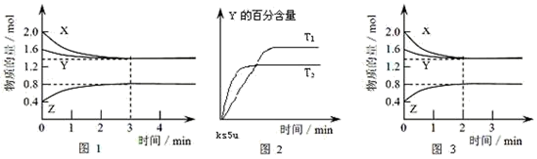

A.容器中发生的反应可表示为:3X(g)+Y(g) 2Z(g) 2Z(g) |
| B.反应进行的前3 min内,用X表示的反应速率 υ(X)=0.3mol/(L·min) |
| C.保持其他条件不变,升高温度,反应的化学平衡常数K增大 |
| D.若改变反应条件,使反应进程如图3所示,则改变的条件可能是使用了催化剂 |
2010·江苏扬州·模拟预测 查看更多[2]
更新时间:2019-01-30 18:14:09
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】一定温度下,向 2.0 L恒容密闭容器中充入1.0 mol PCl5,反应PCl5(g)⇌PCl3(g)+Cl2(g)经过一段时间后达到平衡。反应过程中测定的部分数据见下表。下列说法正确的是
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A.反应在前 50 s 的平均速率v(PCl3)=0.0032 mol·L−1·s−1 |
| B.该条件下,反应的平衡常数K=0.05 |
| C.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol·L−1,则反应的ΔH<0 |
| D.其他条件相同时,向空的容器中充入1.0 mol PCl5、0.20 mol PCl3和0.20 mol Cl2,此时 v(正)>v(逆) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列事实中,不能用勒夏特列原理解释的是
A.常温下,向 的醋酸溶液中加入醋酸钠晶体,pH增大 的醋酸溶液中加入醋酸钠晶体,pH增大 |
| B.实验室用排饱和食盐水的方法收集氯气 |
| C.工业合成氨气时,通入过量的氮气 |
D.对 的平衡体系压缩体积后,颜色变深 的平衡体系压缩体积后,颜色变深 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】活性炭还原 的反应原理为
的反应原理为 ,在密闭容器中
,在密闭容器中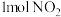 和足量
和足量 发生上述反应,反应相同时间内测得
发生上述反应,反应相同时间内测得 的生成速率与
的生成速率与 的生成速率随温度变化的关系如图1所示,维持温度不变,压缩体积,反应相同时间后测得
的生成速率随温度变化的关系如图1所示,维持温度不变,压缩体积,反应相同时间后测得 的转化率随压强的变化如图2所示:
的转化率随压强的变化如图2所示:
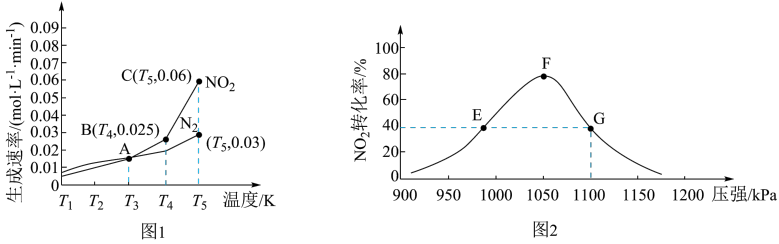
下列说法正确的是
 的反应原理为
的反应原理为 ,在密闭容器中
,在密闭容器中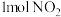 和足量
和足量 发生上述反应,反应相同时间内测得
发生上述反应,反应相同时间内测得 的生成速率与
的生成速率与 的生成速率随温度变化的关系如图1所示,维持温度不变,压缩体积,反应相同时间后测得
的生成速率随温度变化的关系如图1所示,维持温度不变,压缩体积,反应相同时间后测得 的转化率随压强的变化如图2所示:
的转化率随压强的变化如图2所示:
下列说法正确的是
| A.图1中的A、B、C三个点中只有A点达到平衡 |
B.图2中E点的 大于G点的 大于G点的 |
C.E、G两点 的浓度不同,但平衡常数相同 的浓度不同,但平衡常数相同 |
D.在恒温恒压下,向G点平衡体系中再充入一定量的 ,与原平衡相比, ,与原平衡相比, 的平衡转化率升高 的平衡转化率升高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关说法正确的是
| A.CaCO3(s) =CaO(s)+CO2(g)室温下不能自发进行,说明该反应的△H<0 |
| B.水的离子积常数Kw随着温度的升高而增大,说明水的电离是放热反应 |
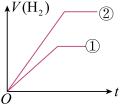
C.N2(g)+3H2(g) 2NH3(g) △H<0,其他条件不变时升高温度,反应速率V(H2)和氢气的平衡转化率均增大 2NH3(g) △H<0,其他条件不变时升高温度,反应速率V(H2)和氢气的平衡转化率均增大 |
| D.升高温度能使化学反应速率增大的主要原因是增加了反应物中活化分子的百分数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】甲烷、水蒸气催化重整是工业制备氢气的方法之一,其反应为 。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用
。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用 表示]的变化关系如图所示。
表示]的变化关系如图所示。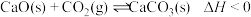 。
。
下列说法错误的是
 。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用
。在压强为p和不同温度下,平衡体系中氢气的体积分数与甲烷、水蒸气的投料比[用 表示]的变化关系如图所示。
表示]的变化关系如图所示。
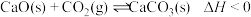 。
。下列说法错误的是
| A.该反应中正反应的活化能大于逆反应的活化能 |
B.向平衡体系中加入适量的 ,可提高氢气的产率 ,可提高氢气的产率 |
C.M点甲烷的平衡转化率为 |
D.在压强为p和600℃时,若向反应器中充入 和 和 ,平衡时氢气的体积分数小于 ,平衡时氢气的体积分数小于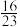 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
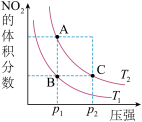
【推荐2】恒容密闭容器中,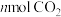 与
与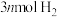 在不同温度下发生反应:
在不同温度下发生反应: ,达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示:
,达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示:
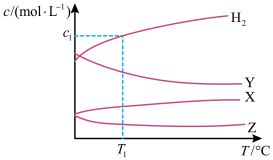
下列说法正确的是
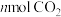 与
与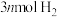 在不同温度下发生反应:
在不同温度下发生反应: ,达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示:
,达到平衡时,各组分的物质的量浓度(c)随温度(T)变化如图所示:
下列说法正确的是
| A.该反应的平衡常数随温度升高而增大 |
B.曲线Y表示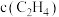 随温度的变化关系 随温度的变化关系 |
C.提高投料比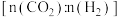 ,可提高 ,可提高 的平衡转化率 的平衡转化率 |
D.其他条件不变,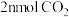 与 与 在 在 ℃下反应,达到平衡时 ℃下反应,达到平衡时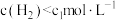 |
您最近一年使用:0次

 充入
充入 和
和 ,在一定条件下发生反应:
,在一定条件下发生反应: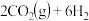
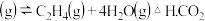 的平衡转化率
的平衡转化率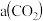 与温度的关系如图所示.下列说法正确的是
与温度的关系如图所示.下列说法正确的是
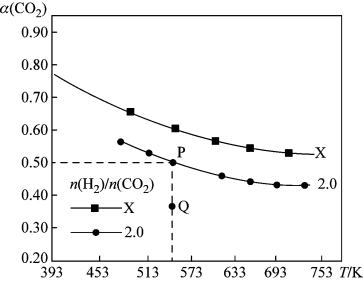
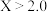 ,且Q点在氢碳比为
,且Q点在氢碳比为 时
时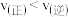
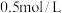 和
和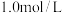 ,则可得到P点,对应温度的平衡常数的值为512
,则可得到P点,对应温度的平衡常数的值为512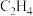 、
、 ,再次平衡后
,再次平衡后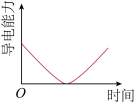
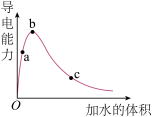
 溶液中通入少量HCl气体,溶液导电能力的变化曲线
溶液中通入少量HCl气体,溶液导电能力的变化曲线
 ,A点比B、C点颜色均深
,A点比B、C点颜色均深 的电离程度:c<a<b
的电离程度:c<a<b

