某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)硫酸铜溶液可以加快氢气生成速率的原因是_______________________ 。
(2)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是____________ 。
(3)要加快上述实验中气体产生的速率,还可采取的措施有_____________________ (答两种)。
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体。记录获得相同体积的气体所需时间。
①请完成此实验设计,其中:V1=________ ,V6=________ ,V9=______ ;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:________ 。
(1)硫酸铜溶液可以加快氢气生成速率的原因是
(2)实验室中现有Na2SO4、MgSO4、Ag2SO4、K2SO4等4种溶液,可与上述实验中CuSO4溶液起相似作用的是
(3)要加快上述实验中气体产生的速率,还可采取的措施有
(4)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体。记录获得相同体积的气体所需时间。
实验 | A | B | C | D | E | F |
| 4 mol·L-1 H2SO4/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因:
15-16高一下·河北唐山·期中 查看更多[3]
2015-2016学年河北省唐山一中高一下期中化学试卷广东省广州市北大附中为明广州实验学校2020-2021学年高一下学期期中考试化学试题(已下线)【期中复习】必刷题-【帮课堂】2021-2022学年高一化学同步精品讲义(人教版2019必修第二册)
更新时间:2016-12-09 15:28:34
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】汽车尾气中含有CO、NO等有害气体。
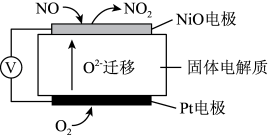
(1)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:
(提示:O2-可在此固体电解质中自由移动)___________ 反应(填“氧化”或“还原”)。
②外电路中,电子是从_________ 电极流出(填“NiO”或“Pt”)。
③Pt电极上的电极反应式为_______________________________ 。
(2)一种新型催化剂用于NO和CO的反应:2NO+2CO 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
①请将表中数据补充完整:a___________ 。
②能验证温度对化学反应速率规律的是实验____________________ (填实验序号)。
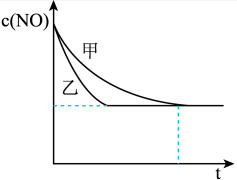
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线________________ (填“甲”或“乙”)。 2CO2+N2,
2CO2+N2,不能 说明已达到平衡状态的是________ (不定项选择);
A.容器内混合气体温度不再变化 B.容器内的气体压强保持不变
C.2v逆(NO)=v正(N2) D.容器内混合气体密度保持不变
(1)通过NO传感器可监测汽车尾气中NO的含量,其工作原理如图所示:
(提示:O2-可在此固体电解质中自由移动)
②外电路中,电子是从
③Pt电极上的电极反应式为
(2)一种新型催化剂用于NO和CO的反应:2NO+2CO
 2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。
2CO2+N2。已知增大催化剂的比表面积可提高该反应速率,为了验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分条件已经填在下表中。| 实验编号 | t(℃) | NO初始浓度 (mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| Ⅰ | 280 | 1.2×10﹣3 | 5.80×10﹣3 | 82 |
| Ⅱ | 280 | 1.2×10﹣3 | b | 124 |
| Ⅲ | 350 | a | 5.80×10﹣3 | 82 |
①请将表中数据补充完整:a
②能验证温度对化学反应速率规律的是实验
③实验Ⅰ和实验Ⅱ中,NO的物质的量浓度c(NO)随时间t的变化曲线如图所示,其中表示实验Ⅱ的是曲线
 2CO2+N2,
2CO2+N2,A.容器内混合气体温度不再变化 B.容器内的气体压强保持不变
C.2v逆(NO)=v正(N2) D.容器内混合气体密度保持不变
您最近一年使用:0次
【推荐2】磷酸锌[Zn3(PO4)2]在水中几乎不溶,其在水中的溶解度随温度的升高而降低,常用作氯化橡胶合成高分子材料的阻燃剂。工业上利用烧渣灰(主要含ZnO,还含少量FeO、Al2O3、CuO及SiO2等)为原料制取磷酸锌的工艺流程如图所示:
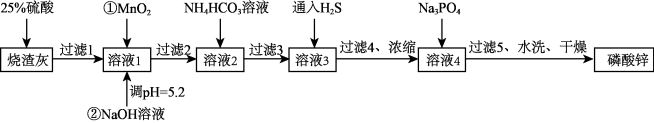
已知:Ⅰ.加入NH4HCO3溶液的目的是沉锰。
Ⅱ.几种金属离子开始沉淀与沉淀完全的pH如下表所示:
(1)用硫酸酸浸烧渣灰,为提高酸浸时锌的浸出率,可以采取的措施是_______ (填一条)。
(2)加入MnO2发生反应的离子方程式是_______ ;经过滤2得到的滤渣的主要成分是_______ (填化学式)。
(3)沉锰反应的离子方程式是_______ 。
(4)水洗时,用热水洗涤磷酸锌沉淀比用冷水洗涤损耗更少,说明原因:_______ 。
(5)通入H2S是为了除铜离子,25℃时,当通入H2S达到饱和时测得溶液的pH = 1,c(H2S)=0.1 mol·L-1,此时溶液中c(Cu2+) =6×10-17 mol·L-1,则CuS的溶度积Ksp=_______ [已知:25℃时,H2S的电离平衡常数Ka1=1×10-7,Ka2=1×10-15]。
(6)利用膜技术电解经净化的含磷酸钠的废液,可以得到所需的工业产品磷酸和氢氧化钠等,电解装置如图所示:

则M为电源的_______ (填“正极”或“负极”),d为_______ (填“阴”或“阳”)离子交换膜,电解总反应式为_______ 。

已知:Ⅰ.加入NH4HCO3溶液的目的是沉锰。
Ⅱ.几种金属离子开始沉淀与沉淀完全的pH如下表所示:
| 金属离子 | Al3+ | Fe3+ | Cu2+ | Zn2+ |
| 开始沉淀的pH | 3.0 | 2.2 | 5.4 | 6.5 |
| 沉淀完全的pH | 5.0 | 3.6 | 6.7 | 8.5 |
(2)加入MnO2发生反应的离子方程式是
(3)沉锰反应的离子方程式是
(4)水洗时,用热水洗涤磷酸锌沉淀比用冷水洗涤损耗更少,说明原因:
(5)通入H2S是为了除铜离子,25℃时,当通入H2S达到饱和时测得溶液的pH = 1,c(H2S)=0.1 mol·L-1,此时溶液中c(Cu2+) =6×10-17 mol·L-1,则CuS的溶度积Ksp=
(6)利用膜技术电解经净化的含磷酸钠的废液,可以得到所需的工业产品磷酸和氢氧化钠等,电解装置如图所示:

则M为电源的
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】精制黑钨矿的主要成分为FeWO4、MnWO4,同时还含有少量Si的化合物。工业上由黑钨矿冶炼金属钨并获取副产物的流程如图:
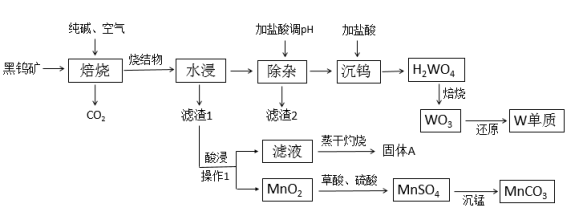
已知:①烧结物的主要成分为Fe2O3、MnO2、Na2SiO3、Na2WO4;
②上述流程中,钨的化合价只在生成钨单质的反应中发生改变;
③常温下,钨酸是难溶于水的弱酸。
请回答下列问题:
(1)为了提高黑钨矿焙烧速率,可以采取的措施是___ (写出一种即可),写出FeWO4在焙烧条件下与纯碱、空气反应的化学方程式___ 。
(2)从本题流程可以得出,同浓度的硅酸根离子比钨酸根离子结合质子能力___ (填“强”或“弱”)。
(3)“沉钨”过程,判断钨酸已完全沉淀的方法是:___ 。
(4)“操作1”用到的玻璃仪器除烧杯外还有___ ,若滤渣1用稀硫酸浸泡,则固体A主要成分的化学式为___ 。
(5)写出MnO2与硫酸、草酸(H2C2O4)溶液反应的离子方程式为___ 。
(6)工业“沉锰”过程中常选用NH4HCO3溶液作沉淀剂,若用碳酸盐代替NH4HCO3溶液可能产生其它固体杂质,该杂质可能为___ (填化学名称)。

已知:①烧结物的主要成分为Fe2O3、MnO2、Na2SiO3、Na2WO4;
②上述流程中,钨的化合价只在生成钨单质的反应中发生改变;
③常温下,钨酸是难溶于水的弱酸。
请回答下列问题:
(1)为了提高黑钨矿焙烧速率,可以采取的措施是
(2)从本题流程可以得出,同浓度的硅酸根离子比钨酸根离子结合质子能力
(3)“沉钨”过程,判断钨酸已完全沉淀的方法是:
(4)“操作1”用到的玻璃仪器除烧杯外还有
(5)写出MnO2与硫酸、草酸(H2C2O4)溶液反应的离子方程式为
(6)工业“沉锰”过程中常选用NH4HCO3溶液作沉淀剂,若用碳酸盐代替NH4HCO3溶液可能产生其它固体杂质,该杂质可能为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】化学是一门以实验为基础的科学,其中控制变量思想在探究实验中有重要应用,下列实验对影响化学反应速率的因素进行探究。
实验方案:现有0.0lmol/L酸性KMnO4溶液和0.lmol/L草酸溶液,为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
(1)请书写此过程的离子反应方程式:_____________ 。
(2)通过实验①、③可探究草酸的浓度对反应速率的影响,表中Vx=_________ mL,理由是_ 。
(3)对比实验①、②的实验现象是___________________________________ 。
(4)实验①中t min 时溶液褪色,用草酸表示的反应速率v(H2C2O4)=______________ 。
(5)甲同学在研究草酸与高锰酸钾在酸性条件下反应的影响因素时发现,草酸与酸性高锰酸钾溶液开始一段时间反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。针对上述现象,甲同学认为草酸与高锰酸钾反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是________________ 的影响。
实验方案:现有0.0lmol/L酸性KMnO4溶液和0.lmol/L草酸溶液,为探讨反应物浓度对化学反应速率的影响,设计的实验方案如下表:
| 实验 序号 | 体积V/mL | 温度/℃ | ||
| KMnO4 溶液 | 水 | H2C2O4溶液 | ||
| ① | 4.0 | 0.0 | 2.0 | 25 |
| ② | 4.0 | 0.0 | 2.0 | 60 |
| ③ | 4.0 | Vx | 1.0 | 25 |
(2)通过实验①、③可探究草酸的浓度对反应速率的影响,表中Vx=
(3)对比实验①、②的实验现象是
(4)实验①中t min 时溶液褪色,用草酸表示的反应速率v(H2C2O4)=
(5)甲同学在研究草酸与高锰酸钾在酸性条件下反应的影响因素时发现,草酸与酸性高锰酸钾溶液开始一段时间反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。针对上述现象,甲同学认为草酸与高锰酸钾反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是
您最近一年使用:0次
【推荐2】亚硝酸氯(ClNO)是有机合成中的重要试剂。亚硝酸氯可由NO与Cl2在通常条件下反应得到,化学方程式为2NO(g)+Cl2(g) 2ClNO(g)。
2ClNO(g)。
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酸氯,涉及如下反应:
①4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g) ΔH1
2NaNO3(s)+2NO(g)+Cl2(g) ΔH1
②2NO2(g)+NaCl(s) NaNO3(s)+ClNO(g) ΔH2
NaNO3(s)+ClNO(g) ΔH2
③2NO(g)+Cl2(g) 2ClNO(g) ΔH3
2ClNO(g) ΔH3
则ΔH1、ΔH2、ΔH3之间的关系为ΔH3=____________ 。
(2)已知几种化学键的键能数据如表(亚硝酸氯的结构为Cl-N=O,一氧化氮的结构为N≡O)
则2NO(g)+Cl2(g) 2ClNO(g)反应的ΔH=
2ClNO(g)反应的ΔH=_________ kJ ·mol-1
(3)T℃时,2NO(g)+Cl2(g) 2ClNO(g)的正反应速率表达式为υ正=kcn(ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为υ正=kcn(ClNO),测得速率和浓度的关系如下表:
n=__________ ;k=___________ (注明单位)。
(4)在2 L的恒容密闭容器中充入4mol NO(g)和2molCl2(g),在不同温度下测得c(ClNO)与时间的关系如图。

①由图可知T1、T2温度的速率υ1______ υ2温度T1______ T2。(填>、<或=)
②温度为T1时,能作为该反应达到平衡的标志的有__________ 。
a.气体体积保持不变 b.容器压强保持不变 c.气体颜色保持不变 d.υ(ClNO)=υ(NO) e.NO与ClNO的物质的量比值保持不变
③反应开始到10min时,Cl2的平均反应速率υ(Cl2)=_______________ 。
 2ClNO(g)。
2ClNO(g)。(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酸氯,涉及如下反应:
①4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+Cl2(g) ΔH1
2NaNO3(s)+2NO(g)+Cl2(g) ΔH1②2NO2(g)+NaCl(s)
 NaNO3(s)+ClNO(g) ΔH2
NaNO3(s)+ClNO(g) ΔH2③2NO(g)+Cl2(g)
 2ClNO(g) ΔH3
2ClNO(g) ΔH3则ΔH1、ΔH2、ΔH3之间的关系为ΔH3=
(2)已知几种化学键的键能数据如表(亚硝酸氯的结构为Cl-N=O,一氧化氮的结构为N≡O)
| 化学键 | N≡O | Cl-Cl | Cl-N | N=O |
| 键能/kJ • mol-1 | 630 | 243 | a | 607 |
则2NO(g)+Cl2(g)
 2ClNO(g)反应的ΔH=
2ClNO(g)反应的ΔH=(3)T℃时,2NO(g)+Cl2(g)
 2ClNO(g)的正反应速率表达式为υ正=kcn(ClNO),测得速率和浓度的关系如下表:
2ClNO(g)的正反应速率表达式为υ正=kcn(ClNO),测得速率和浓度的关系如下表:| 序号 | c(ClNO)/mol·L-1 | υ/mol·L-1· s-1 |
| ① | 0.30 | 3.6×10-8 |
| ② | 0.60 | 1.44×10-7 |
| ③ | 0.90 | 3.24×10-7 |
n=
(4)在2 L的恒容密闭容器中充入4mol NO(g)和2molCl2(g),在不同温度下测得c(ClNO)与时间的关系如图。

①由图可知T1、T2温度的速率υ1
②温度为T1时,能作为该反应达到平衡的标志的有
a.气体体积保持不变 b.容器压强保持不变 c.气体颜色保持不变 d.υ(ClNO)=υ(NO) e.NO与ClNO的物质的量比值保持不变
③反应开始到10min时,Cl2的平均反应速率υ(Cl2)=
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某同学进行了硫代硫酸钠与硫酸反应的有关实验,实验过程的数据记录如下(见表格),请结合表中信息,回答有关问题:
(1)该反应的化学方程式_______ 。
(2)根据你所掌握的知识判断,在上述实验中,反应速率最快的可能是______ (填实验序号)。
(3)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:
①能说明温度对该反应速率影响的组合是_____ (填实验序号,下同);
②A和B、A和C的组合比较,所研究的问题是______ ;
③B和C的组合比较,所研究的问题是______ 。
(4)教材中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较:______ 。
实验 序号 | 反应温度/℃ | 参加反应的物质 | ||||
Na2S2O3 | H2SO4 | H2O | ||||
V/mL | c/mol·L-1 | V/mL | c/mol·L-1 | V/mL | ||
A | 20 | 10 | 0.1 | 10 | 0.1 | 0 |
B | 20 | 5 | 0.1 | 10 | 0.1 | 5 |
C | 20 | 10 | 0.1 | 5 | 0.1 | 5 |
D | 40 | 5 | 0.1 | 10 | 0.1 | 5 |
(2)根据你所掌握的知识判断,在上述实验中,反应速率最快的可能是
(3)在比较某一因素对实验产生的影响时,必须排除其他因素的变动和干扰,即需要控制好与实验有关的各项反应条件,其中:
①能说明温度对该反应速率影响的组合是
②A和B、A和C的组合比较,所研究的问题是
③B和C的组合比较,所研究的问题是
(4)教材中利用了出现黄色沉淀的快慢来比较反应速率的快慢,请你分析为何不采用排水法测量单位时间内气体体积的大小进行比较:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】某研究性学习小组利用 溶液和酸性
溶液和酸性 溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
回答下列问题:
(1)通过实验A、B,可探究________ 的改变对反应速率的影响,其中
________ ,
________ ;通过实验________ (填序号)可探究出温度变化对化学反应速率的影响。
(2)若 、
、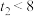 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是________ ;利用实验B中数据计算,用 的浓度变化表示的反应速率
的浓度变化表示的反应速率
_________ 。
(3)写出该反应的离子方程式______________ 。
(4)在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应较慢,溶液变色不明显;但不久突然褪色,反应明显加快。某同学认为是反应放热导致溶液温度升高所致,重做B组实验,测定反应过程中不同时间溶液的温度,结果如表:
结合实验目的与表中数据,你得出的结论是______________ 。
从影响化学反应速率的因素看,你认为还可能是______________ 的影响。若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是______________ (填字母)。
A.硫酸钾 B.水 C.二氧化锰 D.硫酸锰
 溶液和酸性
溶液和酸性 溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:
溶液之间的反应来探究“外界条件改变对化学反应速率的影响”,实验如下:实验序号 | 实验温度/K | 参加反应的物质 | 溶液颜色褪至无色时所需时间/s | ||||
|
|
| |||||
|
|
|
|
| |||
A | 293 | 2 |
| 4 |
| 0 |
|
B |
| 2 |
| 3 |
|
| 8 |
C | 313 | 2 |
|
|
| 0 |
|
(1)通过实验A、B,可探究


(2)若
 、
、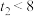 ,则由此实验可以得出的结论是
,则由此实验可以得出的结论是 的浓度变化表示的反应速率
的浓度变化表示的反应速率
(3)写出该反应的离子方程式
(4)在实验中发现高锰酸钾酸性溶液和草酸溶液反应时,开始一段时间反应较慢,溶液变色不明显;但不久突然褪色,反应明显加快。某同学认为是反应放热导致溶液温度升高所致,重做B组实验,测定反应过程中不同时间溶液的温度,结果如表:
时间/s | 0 | 2 | 4 | 6 | 8 | 10 |
温度/ | 20 | 21 | 21 |
| 22 | 22 |
从影响化学反应速率的因素看,你认为还可能是
A.硫酸钾 B.水 C.二氧化锰 D.硫酸锰
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】Ⅰ.控制变量法是化学实验的一种常用方法。下表是某学习小组研究等物质的量浓度的稀硫酸和锌反应的实验数据,分析以下数据,回答下列问题:
(1)本实验中实验2和实验3表明______________________________ 对反应速率有影响。
(2)若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快。原因是________________________________________________ 。
Ⅱ.某温度时,在5L的容器中,X、Y、Z 三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题:

(3)反应开始至2 min,Y的平均反应速率_______ mol·L-1min-1。
(4)反应开始至2 min,X的转化率________ 。
(5)写出 X、Y、Z 的反应方程式__________________________________________ 。
| 序号 | 硫酸的体积/mL | 锌的质量/g | 锌的形状 | 温度/℃ | 完全溶于酸的时间/s | 生成硫酸锌的质量/g |
| 1 | 50.0 | 2.0 | 薄片 | 25 | 100 |  |
| 2 | 50.0 | 2.0 | 颗粒 | 25 | 70 |  |
| 3 | 50.0 | 2.0 | 颗粒 | 35 | 35 | 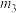 |
| 4 | 50.0 | 2.0 | 粉末 | 25 | 45 | 5.0 |
| 5 | 50.0 | 6.0 | 粉末 | 35 | 30 | 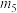 |
(2)若采用与实验1完全相同的条件,但向反应容器中滴加少量硫酸铜溶液,发现反应速率明显加快。原因是
Ⅱ.某温度时,在5L的容器中,X、Y、Z 三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题:

(3)反应开始至2 min,Y的平均反应速率
(4)反应开始至2 min,X的转化率
(5)写出 X、Y、Z 的反应方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】经研究知Cu2+对H2O2分解也具有催化作用,为比较Fe3+和Cu2+对H2O2分解的催化效果,某研究小组的同学分别设计了如图甲、乙所示的试验。回答下列问题:
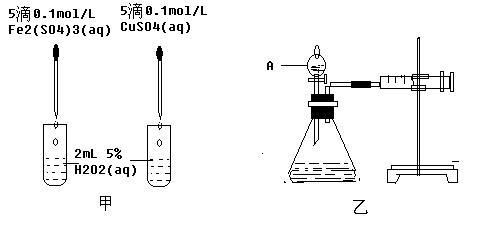
(1)定性分析:如图甲可通过观察_____ ,定性比较得出结论。写出H2O2在二氧化锰作用下发生反应的化学方程式:___________________ 。
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为_____ ,实验中需要测量的数据是_____ 。检查乙装置气密性的方法是_____ 。

(1)定性分析:如图甲可通过观察
(2)定量分析:如图乙所示,实验时均以生成40mL气体为准,其他可能影响实验的因素均已忽略。图中仪器A的名称为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】实验室研究从炼铜烟灰(主要成分为CuO、Cu2O、ZnO、PbO及其硫酸盐)中分别回收铜、锌、铅元素的流程如下。
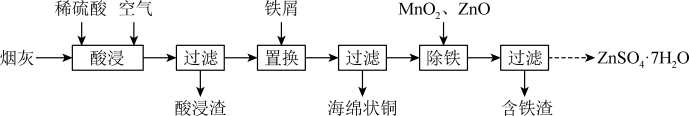
(1)酸浸过程中,金属元素均由氧化物转化为硫酸盐,其中生成CuSO4的化学方程式为:CuO + H2SO4 = CuSO4 + H2O、___________ 。
(2)铁屑加入初期,置换速率随时间延长而加快,其可能原因为:反应放热,温度升高;___________ 。铁屑完全消耗后,铜的产率随时间延长而下降,其可能原因为___________ 。
(3)已知:25 ℃时,Ksp(PbSO4)=2.5×10-8;PbSO4 + 2Cl- PbCl2 + SO
PbCl2 + SO 。一定条件下,在不同浓度的NaCl溶液中,温度对铅浸出率的影响、PbCl2的溶解度曲线分别如图-1、图-2所示。
。一定条件下,在不同浓度的NaCl溶液中,温度对铅浸出率的影响、PbCl2的溶解度曲线分别如图-1、图-2所示。
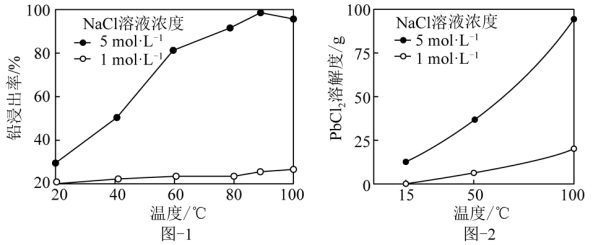
浸出后溶液循环浸取并析出PbCl2的实验结果如下表所示。
①为提高原料NaCl溶液利用率,请补充完整利用酸浸渣制备化学纯(纯度≥98.5 %)PbCl2晶体的实验方案:取一定质量的酸浸渣,___________ ,将所得晶体洗涤、干燥。(可选用的试剂:5 mol·L-1NaCl溶液,1 mol·L-1NaCl溶液,NaCl固体)
②循环一定次数后的溶液中加入适量CaCl2溶液,过滤并加水稀释至其中NaCl浓度为1 mol·L-1的目的是___________ 。

(1)酸浸过程中,金属元素均由氧化物转化为硫酸盐,其中生成CuSO4的化学方程式为:CuO + H2SO4 = CuSO4 + H2O、
(2)铁屑加入初期,置换速率随时间延长而加快,其可能原因为:反应放热,温度升高;
(3)已知:25 ℃时,Ksp(PbSO4)=2.5×10-8;PbSO4 + 2Cl-
 PbCl2 + SO
PbCl2 + SO 。一定条件下,在不同浓度的NaCl溶液中,温度对铅浸出率的影响、PbCl2的溶解度曲线分别如图-1、图-2所示。
。一定条件下,在不同浓度的NaCl溶液中,温度对铅浸出率的影响、PbCl2的溶解度曲线分别如图-1、图-2所示。
浸出后溶液循环浸取并析出PbCl2的实验结果如下表所示。
| 参数 | 循环次数 | |||
| 0 | 1 | 2 | 3 | |
| 结晶产品中PbCl2纯度/% | 99.9 | 99.3 | 98.7 | 94.3 |
②循环一定次数后的溶液中加入适量CaCl2溶液,过滤并加水稀释至其中NaCl浓度为1 mol·L-1的目的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】研究化学反应的快慢和限度具有十分重要的意义,回答下列问题:
(1)在固定体积的容器中进行反应: 。该反应为放热反应。下列一定能加快该反应速率的措施是___________。
。该反应为放热反应。下列一定能加快该反应速率的措施是___________。
(2)常温下,实验室用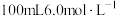 硫酸跟足量锌粉反应制取氢气。
硫酸跟足量锌粉反应制取氢气。
①为降低反应进行的速率,又不影响生成氢气的量,可向反应物中加入___________ 。(填序号)
A. 固体 B.
固体 B. 固体 C.
固体 C. 溶液 D.
溶液 D. 溶液
溶液
②向溶液中滴加少量硫酸铜溶液,反应速率加快,原因是___________ 。
(3)某温度下,在 的恒容密闭容器中,A、B、C(均为气体)三种物质的物质的量随时间的变化曲线如图所示。
的恒容密闭容器中,A、B、C(均为气体)三种物质的物质的量随时间的变化曲线如图所示。
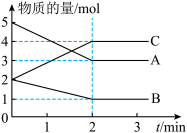
①该反应的化学方程式为___________ 。
②能说明此时反应已达到了平衡状态的是___________ (填标号)。
a.A、B、C三种物质的浓度保持不变;
b.气体A的消耗速率等于气体C的生成速率;
c.混合气体的密度不变;
d.总压强不变;
e.混合气体的平均相对分子质量不变;
f. ;
;
(1)在固定体积的容器中进行反应:
 。该反应为放热反应。下列一定能加快该反应速率的措施是___________。
。该反应为放热反应。下列一定能加快该反应速率的措施是___________。| A.降温 | B.充入氮气 | C.充入 | D.加入催化剂 |
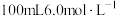 硫酸跟足量锌粉反应制取氢气。
硫酸跟足量锌粉反应制取氢气。①为降低反应进行的速率,又不影响生成氢气的量,可向反应物中加入
A.
 固体 B.
固体 B. 固体 C.
固体 C. 溶液 D.
溶液 D. 溶液
溶液②向溶液中滴加少量硫酸铜溶液,反应速率加快,原因是
(3)某温度下,在
 的恒容密闭容器中,A、B、C(均为气体)三种物质的物质的量随时间的变化曲线如图所示。
的恒容密闭容器中,A、B、C(均为气体)三种物质的物质的量随时间的变化曲线如图所示。
①该反应的化学方程式为
②能说明此时反应已达到了平衡状态的是
a.A、B、C三种物质的浓度保持不变;
b.气体A的消耗速率等于气体C的生成速率;
c.混合气体的密度不变;
d.总压强不变;
e.混合气体的平均相对分子质量不变;
f.
 ;
;
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
(1)上述实验中发生的化学反应方程式有_____________ 。
(2)硫酸铜溶液可以加快氢气生成速率的原因是__________ 。
(3)实验室中现有Na2SO4溶液、MgSO4溶液、Ag2SO4溶液、K2SO4溶液共4种溶液,其中可与上述实验中CuSO4溶液起相似作用的是_____ 。
(4) 要加快上述实验中气体产生的速率,还可采取的措施有
要加快上述实验中气体产生的速率,还可采取的措施有__________ (答两种)。
(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。
①请完成此实验设计,其中V1=________ ,V6=________ ,V9=________ 。
②该同学最后得出的结论为:当加入少量CuSO4溶液时,氢气的生成速率会大大提高,但当加入的CuSO4溶液超过一定量时,氢气的生成速率反而会下降。请分析氢气生成速率下降的主要原因______
(1)上述实验中发生的化学反应方程式有
(2)硫酸铜溶液可以加快氢气生成速率的原因是
(3)实验室中现有Na2SO4溶液、MgSO4溶液、Ag2SO4溶液、K2SO4溶液共4种溶液,其中可与上述实验中CuSO4溶液起相似作用的是
(4)
 要加快上述实验中气体产生的速率,还可采取的措施有
要加快上述实验中气体产生的速率,还可采取的措施有(5)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需的时间。
| 项目 | A | B | C | D | E | F |
| 4 mol·L-1H2SO4溶液/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL | V7 | V8 | V9 | V10 | 10 | 0 |
②该同学最后得出的结论为:当加入少量CuSO4溶液时,氢气的生成速率会大大提高,但当加入的CuSO4溶液超过一定量时,氢气的生成速率反而会下降。请分析氢气生成速率下降的主要原因
您最近一年使用:0次