A、B、C、D是四种短周期元素,E是过渡元素.A、B、C同周期,C、D同主族,A的原子结构示意图为: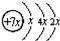 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题:
(1)写出下列元素的符号:A_____ B_____ C_____ D_____
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是_____ ,碱性最强的是_____ .
(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是_____ ,电负性最大的元素是_____ .
(4)D的氢化物比C的氢化物的沸点_____ (填“高“或“低“),原因_____
(5)E元素原子的核电荷数是_____ ,E元素在周期表的位置_____ .
(6)A、B、C最高价氧化物的晶体类型是分别是_____ 晶体、_____ 晶体、_____ 晶体
(7)画出D原子的核外电子轨道表示式_______________________ .
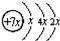 ,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题:
,B是同周期第一电离能最小的元素,C的最外层有三个未成对电子,E的外围电子排布式为3d64s2.回答下列问题:(1)写出下列元素的符号:A
(2)用化学式表示上述五种元素中最高价氧化物对应水化物酸性最强的是
(3)用元素符号表示D所在周期(除稀有气体元素外)第一电离能最大的元素是
(4)D的氢化物比C的氢化物的沸点
(5)E元素原子的核电荷数是
(6)A、B、C最高价氧化物的晶体类型是分别是
(7)画出D原子的核外电子轨道表示式
更新时间:2016-12-09 16:32:17
|
相似题推荐
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】现有六种元素A、B、C、D、E,其中A、B、C、D、E为短周期主族元素,F为第四周期元素,它们的原子序数依次增大。请根据下列相关信息,回答问题。
(1)画出A元素基态原子的核外电子排布图___________ 。
(2)B元素的电负性___________ (填“大于”“小于”或“等于”)C元素的电负性。
(3)C与D形成的化合物所含有的化学键类型为___________ 。
(4)E基态原子中能量最高的电子,其电子云在空间有___________ 个方向。
(5)基态 核外电子排布式为
核外电子排布式为___________ ,过量单质F与B的最高价氧化物对应的水化物的稀溶液完全反应生成BC气体,该反应的离子方程式为___________ 。
| A元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
B元素原子的核外 电子数比 电子数比 电子数少1 电子数少1 |
C元素基态原子 轨道有两个未成对电子 轨道有两个未成对电子 |
D元素原子的第一至第四电离能分别是: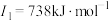 ; ; ; ;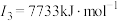 ; ;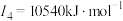 |
E原子核外所有 轨道全满或半满 轨道全满或半满 |
| F在周期表的第8纵列 |
(2)B元素的电负性
(3)C与D形成的化合物所含有的化学键类型为
(4)E基态原子中能量最高的电子,其电子云在空间有
(5)基态
 核外电子排布式为
核外电子排布式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z、Q为短周期非金属元素,R是长周期元素。X原子的电子占据2个电子层且原子中成对电子数是未成对电子数的2倍;Y的基态原子有7种不同运动状态的电子;Z元素在地壳中含量最多;Q是电负性最大的元素;R+只有三个电子层且完全充满电子。
请回答下列问题:(答题时,X、Y、Z、Q、R用所对应的元素符号表示)
(1)R的基态原子的电子排布式为________ 。
(2)X、Y、Z三种元素第一电离能从大到小顺序为_______ 。
(3)已知Y2Q2分子存在如下所示的两种结构(球棍模型,短线不一定代表单键):
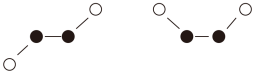
①该分子中两个Y原子之间的键型组合正确的是________ 。
A.仅1个σ键
B.1个σ键和2个π键
C.1个σ键和1个π键
D.仅2个σ键
②该分子中Y原子的杂化方式是________ 。
请回答下列问题:(答题时,X、Y、Z、Q、R用所对应的元素符号表示)
(1)R的基态原子的电子排布式为
(2)X、Y、Z三种元素第一电离能从大到小顺序为
(3)已知Y2Q2分子存在如下所示的两种结构(球棍模型,短线不一定代表单键):

①该分子中两个Y原子之间的键型组合正确的是
A.仅1个σ键
B.1个σ键和2个π键
C.1个σ键和1个π键
D.仅2个σ键
②该分子中Y原子的杂化方式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】短周期元素X、Y、Z、W的原子序数依次增大,且四种元素分别位于不同的主族,它们的单质常温下均呈气态。X、Y、W处于不同周期,且在一定条件下其单质能发生反应:X2+Y2→甲,X2+W2→乙,已知,甲、乙常温下均为气态,且两者在空气中相遇时可化合成丙。试回答下列问题:
⑴ Y和Z对应的氢化物比较稳定的是:_______________ 。(填化学式)
⑵ 化合物丙属于_____________ 晶体(填晶体类型),其水溶液显酸性,用离子方程式 表示其原因:_________________________________________ 。
⑶ X、Z可组成四原子化合物丁,丁中所含的化学键类型为:____________ 键,请说出化合物丁的一种常见用途:___________________________________ ;
⑷ X、Y组成的液态化合物Y2X4 16 g与足量丁反应生成Y2和液态水,放出QkJ的热量,写出该反应的热化学方程式 :______________________________ ;
Y2X4还可以和Z2构成清洁高效的燃料电池,若电解质溶液为NaOH溶液,则负极 的电极反应式为:________________________________________ 。
⑸ 一定条件下,取 3.4 g甲气体 置于1 L恒容的容器中,4分钟后,容器内的压强变为原来的1.2倍,且不再变化,该反应中甲气体的转化率 为:__________ 。
⑴ Y和Z对应的氢化物比较稳定的是:
⑵ 化合物丙属于
⑶ X、Z可组成四原子化合物丁,丁中所含的化学键类型为:
⑷ X、Y组成的液态化合物Y2X4 16 g与足量丁反应生成Y2和液态水,放出QkJ的热量,写出该反应的
Y2X4还可以和Z2构成清洁高效的燃料电池,若电解质溶液为NaOH溶液,则
⑸ 一定条件下,取 3.4 g
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某研究性学习小组设计了一组实验来探究元素周期律。甲同学根据元素非金属性与对应最高价含氧酸之间的关系,设计了如图1装置来一次性完成N、C、Si三种元素的非金属性强弱比较的实验研究;乙同学设计了如图2装置来验证卤族元素性质的递变规律。A、B、C三处分别是沾有NaBr溶液的棉花、湿润的淀粉KI试纸、湿润红纸。已知常温下浓盐酸与高锰酸钾能反应生成氯气。
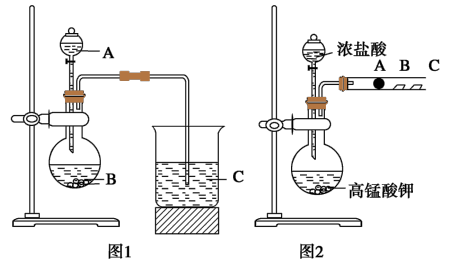
(1)图1中仪器A的名称是______________ 。甲同学实验步骤:连接仪器、______________ 、加药品、滴入试剂。
(2)①图1中烧瓶B中的盛放试剂为碳酸钙,C中盛放试剂为硅酸钠溶液,则甲同学设计实验的依据是_________________ 。
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是________________ 。
(3)图2中A处反应的离子方程式___________________ 。
(4)乙同学发现图2中B处试纸变蓝,C处红纸褪色,据此_____ (填“能”或“不能”)得出溴的非金属性强于碘,理由是__________________ 。

(1)图1中仪器A的名称是
(2)①图1中烧瓶B中的盛放试剂为碳酸钙,C中盛放试剂为硅酸钠溶液,则甲同学设计实验的依据是
②能说明碳元素的非金属性比硅元素非金属性强的实验现象是
(3)图2中A处反应的离子方程式
(4)乙同学发现图2中B处试纸变蓝,C处红纸褪色,据此
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】下表为元素周期表的一部分,请参照①-⑩在表中的位置,用相应的化学用语填空。
(1)用序号标出的10种元素中,非金属性最强元素的离子结构示意图为___________ ,②在元素周期表中的位置是___________ 。
(2)④、⑦、⑩的离子半径由大到小的顺序为___________ (用离子符号表示)
(3)由表中④、⑥元素可以组成一种淡黄色物质,请画出该物质电子式___________ ,该物质含有的化学键类型有___________ 。
(4)元素②、⑧、⑩的最高价含氧酸的酸性由强到弱的顺序是___________ (用化学式表示)
(5)⑦的单质与⑥的最高价氧化物对应水化物的水溶液反应的化学方程式为___________ 。
| ① | |||||||
| ② | ③ | ④ | ⑤ | ||||
| ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | |||
(2)④、⑦、⑩的离子半径由大到小的顺序为
(3)由表中④、⑥元素可以组成一种淡黄色物质,请画出该物质电子式
(4)元素②、⑧、⑩的最高价含氧酸的酸性由强到弱的顺序是
(5)⑦的单质与⑥的最高价氧化物对应水化物的水溶液反应的化学方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】如图是部分元素在元素周期表中位置,根据下列要求回答问题:
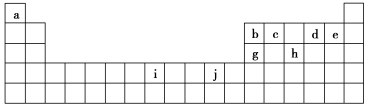
(1)下列关于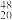 Ca、
Ca、 Bk(锫)、
Bk(锫)、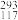 Ts和
Ts和 Ts的说法中不正确的是_______(填序号,下同)。
Ts的说法中不正确的是_______(填序号,下同)。
(2)根据元素周期表结构推知,117号元素在周期表中的位置是_______。
(3)117号元素Ts属于_______ (填“金属元素”或“非金属元素”),它的气态氢化物稳定性比砹的气态氢化物稳定性_______ (填“强”或“弱”);它的最高价氧化物的化学式为_______ 。
(4)下列关于上述元素及其化合物的判断正确的是_______。

(1)下列关于
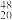 Ca、
Ca、 Bk(锫)、
Bk(锫)、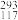 Ts和
Ts和 Ts的说法中不正确的是_______(填序号,下同)。
Ts的说法中不正确的是_______(填序号,下同)。| A.117号元素的相对原子质量为293.5 | B.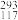 Ts和 Ts和 Ts互为同位素 Ts互为同位素 |
C.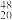 Ca、 Ca、 Bk表示两种原子、两种元素 Bk表示两种原子、两种元素 | D.上述元素都位于长周期中 |
| A.第七周期第IVA族 | B.第七周期第VIIA族 |
| C.第六周期第IVA族 | D.第六周期第VIIA族 |
(4)下列关于上述元素及其化合物的判断正确的是_______。
A.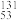 I、 I、 Cs和 Cs和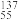 Cs放射性元素变成其他元素,发生了化学变化 Cs放射性元素变成其他元素,发生了化学变化 |
| B.he3分子和ha3分子结构相同 |
| C.j元素与d元素组成化合物的颜色相同 |
D.加碘食盐中“碘”不是碘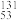 I I |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】在周期表中1~36号元素之间的A、B、C、D、E五种元素,它们的原子序数依次增大,已知A与其余四种元素既不同周期也不同主族,B的一种核素在考古时常用来鉴定一些文物的年代,C元素原子的最外层有3个自旋方向相同的未成对电子,D原子核外电子有8种不同的运动状态,E元素在第四周期,E元素位于周期表的ds区,其基态原子最外能层只有一个电子。
(1)写出基态E原子的简化电子排布式_______ ,C的单质的电子式_______ 。
(2)A与B形成的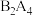 分子中,σ键和π键的个数比为
分子中,σ键和π键的个数比为_______ ,分子中B原子的杂化类型为_______ 。
(3)A与C形成 型分子,实验室制取
型分子,实验室制取 的化学方程式为
的化学方程式为_______ 。C的最高价氧化物的水化物与 所形成的盐呈酸性的原因
所形成的盐呈酸性的原因_______ (用离子方程式表示)
(4)B、C、D三种元素第一电离能由大到小的顺序为_______ (用元素符号表示)。
(5)已知D、E能形成一种化合物,其晶胞的结构如图所示,与D配位的E所形成的空间结构为_______ ,若该晶胞的棱长为apm,阿伏加德罗常数的数值为NA,则该晶体的密度为_______  (用含a、NA的符号表示)。
(用含a、NA的符号表示)。

(1)写出基态E原子的简化电子排布式
(2)A与B形成的
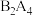 分子中,σ键和π键的个数比为
分子中,σ键和π键的个数比为(3)A与C形成
 型分子,实验室制取
型分子,实验室制取 的化学方程式为
的化学方程式为 所形成的盐呈酸性的原因
所形成的盐呈酸性的原因(4)B、C、D三种元素第一电离能由大到小的顺序为
(5)已知D、E能形成一种化合物,其晶胞的结构如图所示,与D配位的E所形成的空间结构为
 (用含a、NA的符号表示)。
(用含a、NA的符号表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】LED灯是一种环保的光源,在相同照明效果下比传统光源节能80%以上。目前市售LED晶片材质基本以砷化镓、磷化铝镓钢(AlGaInP)、氮化铟镓( InGaN)为主,砷化镓的晶胞结构如图。回答下列问题:
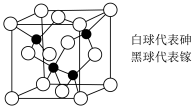
(1)砷的基态原子的电子排布式是___________ 。
(2)磷和砷是同一族的元素,第一电离能:磷___________ (填“>”“<”或“=”,下同)砷,它们形成的氢化物的沸点:PH3___________ AsH3,原因是______________________ 。
(3)AsH3是无色、稍有大蒜味的气体。AsH3中砷原子的杂化轨道方式为___________ ,AsH3的空间结构为___________ 。
(4)砷元素的常见化合价有+3和+5,它们对应的含氧酸有H3AsO3和H3AsO4两种,其中H3AsO4的酸性比H3AsO3的酸性强,从物质结构与性质的关系来看,H3AsO4的酸性比H3AsO3的酸性强的原因是_________________________________ 。
(5)此晶胞中所含的砷原子的个数为___________ ,砷化镓的化学式为___________ 。

(1)砷的基态原子的电子排布式是
(2)磷和砷是同一族的元素,第一电离能:磷
(3)AsH3是无色、稍有大蒜味的气体。AsH3中砷原子的杂化轨道方式为
(4)砷元素的常见化合价有+3和+5,它们对应的含氧酸有H3AsO3和H3AsO4两种,其中H3AsO4的酸性比H3AsO3的酸性强,从物质结构与性质的关系来看,H3AsO4的酸性比H3AsO3的酸性强的原因是
(5)此晶胞中所含的砷原子的个数为
您最近一年使用:0次
【推荐3】“张亭栋研究小组”受民间中医启发,发现As2O3对白血病有明显的治疗作用。氮(N)、磷(P)、砷(As)为第VA族元素,该族元素的化合物在研究和生产中有着许多重要用途。
(1)N原子的价电子排布式为___ ,N、P、As原子的第一电离能由大到小的顺序为___ 。
(2)NH3的沸点比AsH3的沸点高,原因是_____ 。
(3)立方氮化硼晶体(BN),是一种超硬材料,有优异的耐磨性,其晶胞如图所示。
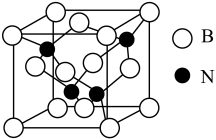
立方氮化硼是____ 晶体,晶体中N原子的杂化轨道类型为___ ,B原子的配位数为______ 。
(4)若立方氮化硼晶胞的边长为362 pm,则立方氮化硼的密度为____ g/cm3(只要求列算式,不必计算出数值,阿伏伽德罗常数的值为NA)。
(1)N原子的价电子排布式为
(2)NH3的沸点比AsH3的沸点高,原因是
(3)立方氮化硼晶体(BN),是一种超硬材料,有优异的耐磨性,其晶胞如图所示。

立方氮化硼是
(4)若立方氮化硼晶胞的边长为362 pm,则立方氮化硼的密度为
您最近一年使用:0次
【推荐1】(1)现有下列物质:①金刚石 ②干冰 ③晶体硅 ④二氧化硅晶体 ⑤氯化铵⑥氖⑦金属锌。通过非极性键形成原子晶体的是_____ ;属于分子晶体,且分子为直线形的是______ ;由单原子分子构成的分子晶体是_______ ;含有极性键的离子化合物是_______ ;能导电且为金属晶体的是_______ 。
(2)NH3在水中的溶解度是常见气体中最大的。下列因素与NH3的水溶性没有关系的是_____ (填序号)
a.NH3和H2O都是极性分子
b.NH3是一种易液化的气体
c.NH3溶于水建立了如下平衡:NH3+H2O⇌NH3•H2O⇌NH +OH-
+OH-
d.NH3在水中易形成氢键
(3)在①苯 ②CH3OH ③HCHO ④CS2 ⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有____ (填序号),CS2分子的立体构型是______ ,CO2与CS2相比,_______ (填化学式)的熔点较高。
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4,呈正四面体构型,易溶于下列物质中的_____ (填序号)
A.水 B.CCl4 C.C6H6 D.NiSO4溶液
(5)有下列四种无机含氧酸:① H3PO4 ② HClO ③ H3BO3 ④ HClO2根据无机含氧酸的酸性规律,将以上四种无机含氧酸按酸性相近两两组成一组,它们是____ ;_____ 。(填序号)
(2)NH3在水中的溶解度是常见气体中最大的。下列因素与NH3的水溶性没有关系的是
a.NH3和H2O都是极性分子
b.NH3是一种易液化的气体
c.NH3溶于水建立了如下平衡:NH3+H2O⇌NH3•H2O⇌NH
 +OH-
+OH-d.NH3在水中易形成氢键
(3)在①苯 ②CH3OH ③HCHO ④CS2 ⑤CCl4五种有机溶剂中,碳原子采取sp2杂化的分子有
(4)金属镍粉在CO气流中轻微加热,生成无色挥发性液体Ni(CO)4,呈正四面体构型,易溶于下列物质中的
A.水 B.CCl4 C.C6H6 D.NiSO4溶液
(5)有下列四种无机含氧酸:① H3PO4 ② HClO ③ H3BO3 ④ HClO2根据无机含氧酸的酸性规律,将以上四种无机含氧酸按酸性相近两两组成一组,它们是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】FeOOH为一种不溶于水的黄色固体。某学校以 废料(含少量
废料(含少量 、FeO等)为原料制备FeOOH,流程如图所示。
、FeO等)为原料制备FeOOH,流程如图所示。

回答以下问题:
(1)为提高“酸浸”的速率,可采取的措施有_______ (填一种即可)。
(2)“废渣”的主要成分可用于_______ (填一种即可)。
(3)“酸浸”时_______ (填“能”或“不能”)使用稀 ,原因是
,原因是_______ 。
(4)“试剂X”可使用_______ (填化学式,填一种即可)。
(5)从“滤液2”中获得晶体的一种方法是:_______ 、过滤、洗涤。
(6)由 转化为FeOOH的离子方程式是
转化为FeOOH的离子方程式是_______ 。
(7)研究晶体性质对工业流程的探究十分重要,该学校的化学社团欲探究A、B、C(均为单质或化合物)三种由H、C、Na、Cl元素组成的晶体。他们对上述物质进行相关实验,数据如下:
根据以上实验数据,填写表格:
 废料(含少量
废料(含少量 、FeO等)为原料制备FeOOH,流程如图所示。
、FeO等)为原料制备FeOOH,流程如图所示。
回答以下问题:
(1)为提高“酸浸”的速率,可采取的措施有
(2)“废渣”的主要成分可用于
(3)“酸浸”时
 ,原因是
,原因是(4)“试剂X”可使用
(5)从“滤液2”中获得晶体的一种方法是:
(6)由
 转化为FeOOH的离子方程式是
转化为FeOOH的离子方程式是(7)研究晶体性质对工业流程的探究十分重要,该学校的化学社团欲探究A、B、C(均为单质或化合物)三种由H、C、Na、Cl元素组成的晶体。他们对上述物质进行相关实验,数据如下:
| 熔点/℃ | 硬度 | 水溶性 | 导电性 | 水溶液与 反应 反应 | |
| A | 811 | 较大 | 易溶 | 水溶液或熔融时导电 | 白色沉淀 |
| B | 3550 | 很大 | 不溶 | 不导电 | 不反应 |
| C | -114.2 | 很小 | 易溶 | 液态不导电 | 白色沉淀 |
| 化学式 | 晶体类型 | 微粒间作用力 | |
| A | |||
| B | |||
| C |
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】2022年北京冬季奥运会场馆使用了大量不锈钢材质,不锈钢属于合金钢,其基体是铁碳合金,常用的不锈钢中含铬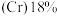 、含镍
、含镍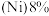 。回答下列问题:
。回答下列问题:
(1)不锈钢所属的晶体类型为_______ 。
(2)铁系元素能与 形成
形成 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点
为浅黄色液体,沸点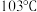 ,则该晶体的晶体类型为
,则该晶体的晶体类型为_______ 晶体, 中含有的化学键类型包括
中含有的化学键类型包括_______ (填字母)。
A.氢键 B.离子键 C.配位键 D.极性共价键 E.金属键 F.范德华力
(3)氧元素与 可形成低价态氧化物
可形成低价态氧化物 。
。
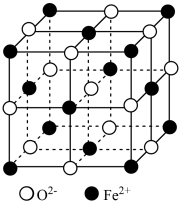
① 立方晶胞结构如图所示,则单位晶胞内
立方晶胞结构如图所示,则单位晶胞内 的个数为
的个数为_______ ;与 紧邻的所有
紧邻的所有 构成的几何构型为
构成的几何构型为_______ 。
②若 与
与 之间最近距离为
之间最近距离为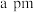 ,则该晶体的密度计算式为
,则该晶体的密度计算式为_______  。(用含
。(用含 的代数式表示,
的代数式表示, 代表阿伏加德罗常数的值)
代表阿伏加德罗常数的值)
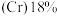 、含镍
、含镍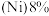 。回答下列问题:
。回答下列问题:(1)不锈钢所属的晶体类型为
(2)铁系元素能与
 形成
形成 等金属羰基化合物。已知室温时
等金属羰基化合物。已知室温时 为浅黄色液体,沸点
为浅黄色液体,沸点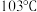 ,则该晶体的晶体类型为
,则该晶体的晶体类型为 中含有的化学键类型包括
中含有的化学键类型包括A.氢键 B.离子键 C.配位键 D.极性共价键 E.金属键 F.范德华力
(3)氧元素与
 可形成低价态氧化物
可形成低价态氧化物 。
。
①
 立方晶胞结构如图所示,则单位晶胞内
立方晶胞结构如图所示,则单位晶胞内 的个数为
的个数为 紧邻的所有
紧邻的所有 构成的几何构型为
构成的几何构型为②若
 与
与 之间最近距离为
之间最近距离为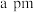 ,则该晶体的密度计算式为
,则该晶体的密度计算式为 。(用含
。(用含 的代数式表示,
的代数式表示, 代表阿伏加德罗常数的值)
代表阿伏加德罗常数的值)
您最近一年使用:0次



