某化学兴趣小组在一次实验探究中发现,向草酸溶液中逐滴加入酸性高锰酸钾溶液时,溶液褪色先慢后快,即反应速率由小变大。小组成员为此“异常”现象展开讨论,猜想造成这种现象的最可能原因有两种,并为此设计实验进行探究验证。
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:……。
【实验目的】探究草酸与高锰酸钾反应的速率变化“异常”原因
【实验用品】仪器:试管、胶头滴管、量筒、药匙、玻璃棒等;
试剂:0.1mol/L H2C2O4溶液、0.05mol/L KMnO4(硫酸酸化)溶液等。
请你根据该兴趣小组的实验探究设计思路,补充完整所缺内容。
(1)草酸(H2C2O4,弱酸)与酸性KMnO4溶液反应的离子方程式为______________
(2)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是_______________
(3)猜想Ⅱ可是:___________________
要设计实验验证猜想Ⅱ,进行该实验还要补充一种试剂及一种仪器,分别是_______________
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容_____________ 。
猜想Ⅰ:此反应过程放热,温度升高,反应速率加快;
猜想Ⅱ:……。
【实验目的】探究草酸与高锰酸钾反应的速率变化“异常”原因
【实验用品】仪器:试管、胶头滴管、量筒、药匙、玻璃棒等;
试剂:0.1mol/L H2C2O4溶液、0.05mol/L KMnO4(硫酸酸化)溶液等。
请你根据该兴趣小组的实验探究设计思路,补充完整所缺内容。
(1)草酸(H2C2O4,弱酸)与酸性KMnO4溶液反应的离子方程式为
(2)要完成对猜想Ⅰ的实验验证,至少还需要一种实验仪器是
(3)猜想Ⅱ可是:
要设计实验验证猜想Ⅱ,进行该实验还要补充一种试剂及一种仪器,分别是
(4)基于猜想Ⅱ成立,设计方案进行实验,请完成以下实验记录表内容
| 试管A | 试管B | |
| 加入试剂 | ||
| 实验现象(褪色时间) | ||
| 结论 | 猜想Ⅱ正确 | |
更新时间:2016-12-09 17:27:42
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验是化学研究的一种重要手段,请完成以下实验的探究与分析。
I.化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式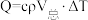 计算获得。
计算获得。
(1)配制0.50 NaOH溶液。
NaOH溶液。
①若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体___________ g。
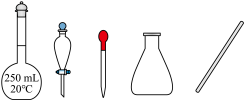
②实验中所需的玻璃仪器有烧杯、量筒和___________ 。(从下图中选择,写出名称)
(2)测定热量:将浓度为 的酸溶液和
的酸溶液和 的碱溶液各20mL进行反应。测得反应前后体系的温度值,实验结果见下表。(c和
的碱溶液各20mL进行反应。测得反应前后体系的温度值,实验结果见下表。(c和 分别取
分别取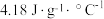 和
和 ,下同)。
,下同)。
①温度:b___________ c(填“>”“<”或“=”),理由是___________ 。
②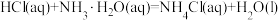 的
的
___________ 。
Ⅱ.碘及其化合物在人类活动中占有重要地位。“大象牙膏”实验中,将H2O2、KI和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:
第一步:H2O2+I-=H2O+IO-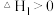 慢反应
慢反应
第二步:H2O2+IO-=O2+I-+H2O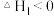 快反应
快反应
(3)该反应的决速步骤为___________ ,总反应方程式为___________ 。
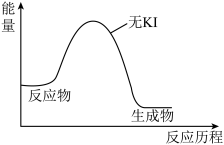
(4)在答题卡的图中画出有KI参与的两步反应的能量历程图___________ 。
I.化学反应常伴随热效应。某些反应(如中和反应)的热量变化,其数值Q可通过量热装置测量反应前后体系温度变化,用公式
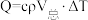 计算获得。
计算获得。(1)配制0.50
 NaOH溶液。
NaOH溶液。①若实验中大约要使用245mLNaOH溶液,至少需要称量NaOH固体
②实验中所需的玻璃仪器有烧杯、量筒和

(2)测定热量:将浓度为
 的酸溶液和
的酸溶液和 的碱溶液各20mL进行反应。测得反应前后体系的温度值,实验结果见下表。(c和
的碱溶液各20mL进行反应。测得反应前后体系的温度值,实验结果见下表。(c和 分别取
分别取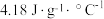 和
和 ,下同)。
,下同)。| 序号 | 体系温度/℃ | ||
| 反应试剂 | 反应前 | 反应后 | |
| i | HCl+NaOH | a | b |
| ii | HCl+NH₃·H₂O | a | c |
②
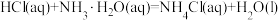 的
的
Ⅱ.碘及其化合物在人类活动中占有重要地位。“大象牙膏”实验中,将H2O2、KI和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:
第一步:H2O2+I-=H2O+IO-
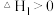 慢反应
慢反应第二步:H2O2+IO-=O2+I-+H2O
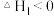 快反应
快反应(3)该反应的决速步骤为
(4)在答题卡的图中画出有KI参与的两步反应的能量历程图

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】研究碳氧化物、氮氧化物反应的特征及机理,对处理该类化合物的污染问题具有重要意义。回答下列问题:
(1)已知: 的燃烧热
的燃烧热 kJ·mol
kJ·mol ,
, 的燃烧热
的燃烧热 kJ⋅mol
kJ⋅mol ,
,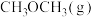 的燃烧热
的燃烧热 kJ⋅mol
kJ⋅mol ,
,
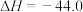 kJ⋅mol
kJ⋅mol 。则
。则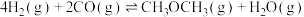

______ kJ⋅mol 。
。
(2)在恒温恒压条件下,向密闭容器中充入4.0 mol 和2.0 mol
和2.0 mol  ,发生反应
,发生反应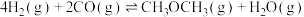 ,起始时体系压强为p,平衡时
,起始时体系压强为p,平衡时 的转化率为50%。达到平衡时,
的转化率为50%。达到平衡时,
______ ,平衡常数 (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。
(3)氮的氧化物与悬浮在大气中的海盐粒子相互作用,发生反应: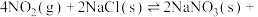
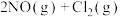 ,该反应的正反应需在低温条件下才能自发进行,则该反应的活化能:
,该反应的正反应需在低温条件下才能自发进行,则该反应的活化能: (正)
(正)_____ (填“>”或“<”) (逆)。
(逆)。
(4)CO还原NO的反应: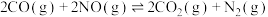

①实验测得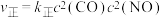 ,
,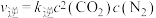 (
( ,
, 是速率常数,只与温度有关)。则升高温度,
是速率常数,只与温度有关)。则升高温度,
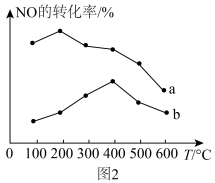
______ (填“增大”“减小”或“不变”),将 随温度变化的曲线
随温度变化的曲线______ 表示在图1中。______ 。_______ (填“正向移动”“逆向移动”或“不移动”)。
(1)已知:
 的燃烧热
的燃烧热 kJ·mol
kJ·mol ,
, 的燃烧热
的燃烧热 kJ⋅mol
kJ⋅mol ,
,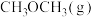 的燃烧热
的燃烧热 kJ⋅mol
kJ⋅mol ,
,
 kJ⋅mol
kJ⋅mol 。则
。则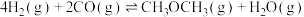

 。
。(2)在恒温恒压条件下,向密闭容器中充入4.0 mol
 和2.0 mol
和2.0 mol  ,发生反应
,发生反应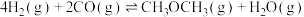 ,起始时体系压强为p,平衡时
,起始时体系压强为p,平衡时 的转化率为50%。达到平衡时,
的转化率为50%。达到平衡时,
 (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。(3)氮的氧化物与悬浮在大气中的海盐粒子相互作用,发生反应:
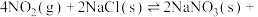
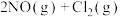 ,该反应的正反应需在低温条件下才能自发进行,则该反应的活化能:
,该反应的正反应需在低温条件下才能自发进行,则该反应的活化能: (正)
(正) (逆)。
(逆)。(4)CO还原NO的反应:
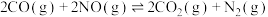

①实验测得
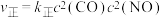 ,
,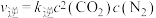 (
( ,
, 是速率常数,只与温度有关)。则升高温度,
是速率常数,只与温度有关)。则升高温度,
 随温度变化的曲线
随温度变化的曲线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某研究性学习小组设计了一组实验探究影响化学反应速率的因素。按要求回答下列问题:
(1)甲同学在a、b、c三只烧杯里分别加入50mL水,再分别滴加几滴酚酞试液,依次加入大小相近的锂、钠、钾块,观察现象。反应最快最剧烈的烧杯是_______ (填字母)。这说明对不同化学反应,影响其反应速率快慢的主要因素是_______ 。
(2)用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,实验过程中 气体标准状况下的体积[
气体标准状况下的体积[ ]与时间(t/min)的关系如图甲所示。根据图象分析,该反应过程中化学反应速率随时间变化的曲线可能是
]与时间(t/min)的关系如图甲所示。根据图象分析,该反应过程中化学反应速率随时间变化的曲线可能是_______ (填字母)。


(3)如果将生成的气体通入 溶液中(装置如图乙)从而比较碳和硅的非金属性的强弱,则b溶液是
溶液中(装置如图乙)从而比较碳和硅的非金属性的强弱,则b溶液是_______ ,c溶液是_______ 。为了能快速观察到明显现象可以采取的措施是_______ 。

(1)甲同学在a、b、c三只烧杯里分别加入50mL水,再分别滴加几滴酚酞试液,依次加入大小相近的锂、钠、钾块,观察现象。反应最快最剧烈的烧杯是
(2)用纯净的碳酸钙与稀盐酸反应制取二氧化碳气体,实验过程中
 气体标准状况下的体积[
气体标准状况下的体积[ ]与时间(t/min)的关系如图甲所示。根据图象分析,该反应过程中化学反应速率随时间变化的曲线可能是
]与时间(t/min)的关系如图甲所示。根据图象分析,该反应过程中化学反应速率随时间变化的曲线可能是

(3)如果将生成的气体通入
 溶液中(装置如图乙)从而比较碳和硅的非金属性的强弱,则b溶液是
溶液中(装置如图乙)从而比较碳和硅的非金属性的强弱,则b溶液是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学小组利用酸性KMnO4与草酸(H2C2O4)反应,设计以下实验探究化学反应快慢的影响因素。
实验用品:0.04 mol/L KMnO4溶液、0.2 mol/L H2C2O4溶液、0.36 mol/L稀硫酸、蒸馏水、MnSO4溶液、5mL量筒、胶头滴管、井穴板、细玻璃棒及秒表等
实验内容及记录:
回答下列问题:
(1)写出酸性KMnO4与草酸反应的离子方程式___________ 。
(2)V1=___________ mL,V2=___________ mL,理由是___________ 。
(3)欲探究温度对反应速率的影响,应选择的实验是___________ (填编号)。
(4)为验证“Mn2+对该反应有催化作用”,该小组同学用如图装置进行了实验④和⑤,其中实验所用酸性KMnO4溶液由0.36 mol/L稀硫酸与0.04 mol/L KMnO4溶液溶液以体积比1∶1混合所得。
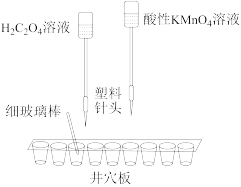
实验④:向一个井穴中滴入10滴0.2 mol/L H2C2O4溶液,逐滴加入酸性KMnO4溶液,并记录各滴加入后的褪色时间。
实验⑤:向三个井穴中分别滴加10滴0.2 mol/L H2C2O4溶液,依次滴加1、2、3滴 溶液和3、2、1滴蒸馏水,搅拌均匀,再各滴加1滴酸性KMnO4溶液,并记录褪色时间及混合体系颜色变化。
溶液和3、2、1滴蒸馏水,搅拌均匀,再各滴加1滴酸性KMnO4溶液,并记录褪色时间及混合体系颜色变化。
实验记录如下:
已知:MnO2为难溶于水的褐色固体;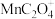 溶液呈红色,不稳定,会缓慢分解为Mn2+和CO2。
溶液呈红色,不稳定,会缓慢分解为Mn2+和CO2。
i.实验④中第5滴出现褐色沉淀可能的原因是___________ (用离子方程式表示)。
ii.实验④和⑤的现象验证了“ 对该反应有催化作用”,催化过程如下:
对该反应有催化作用”,催化过程如下:
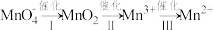
实验⑤中催化剂用量增加,褪色时间却略有延长,说明催化剂过量易催化到“催化过程”的第___________ 步,反应过程出现红色的原因是___________ 。
实验用品:0.04 mol/L KMnO4溶液、0.2 mol/L H2C2O4溶液、0.36 mol/L稀硫酸、蒸馏水、MnSO4溶液、5mL量筒、胶头滴管、井穴板、细玻璃棒及秒表等
实验内容及记录:
| 实验编号 | 试管中所加试剂及用量/mL | 温度/℃ | 紫色褪去所需时间/min | |||
| H2C2O4溶液 | KMnO4溶液 | 稀硫酸 | 蒸馏水 | |||
| ① | 2.0 | 1.0 | 1.0 | 2.0 | 20 | 4.1 |
| ② | 3.0 | 1.0 | 1.0 | V1 | 20 | 3.7 |
| ③ | V2 | 1.0 | 1.0 | 2.0 | 80 | t |
(1)写出酸性KMnO4与草酸反应的离子方程式
(2)V1=
(3)欲探究温度对反应速率的影响,应选择的实验是
(4)为验证“Mn2+对该反应有催化作用”,该小组同学用如图装置进行了实验④和⑤,其中实验所用酸性KMnO4溶液由0.36 mol/L稀硫酸与0.04 mol/L KMnO4溶液溶液以体积比1∶1混合所得。

实验④:向一个井穴中滴入10滴0.2 mol/L H2C2O4溶液,逐滴加入酸性KMnO4溶液,并记录各滴加入后的褪色时间。
实验⑤:向三个井穴中分别滴加10滴0.2 mol/L H2C2O4溶液,依次滴加1、2、3滴
 溶液和3、2、1滴蒸馏水,搅拌均匀,再各滴加1滴酸性KMnO4溶液,并记录褪色时间及混合体系颜色变化。
溶液和3、2、1滴蒸馏水,搅拌均匀,再各滴加1滴酸性KMnO4溶液,并记录褪色时间及混合体系颜色变化。实验记录如下:
| 实验④ | KMnO4溶液 | 第1滴 | 第2滴 | 第3滴 | 第4滴 | 第5滴 |
| 紫色褪去所需时间/s | 100 | 20 | 10 | 5 | 出现褐色沉淀 | |
| 实验⑤ | MnSO4溶液 | 1滴 | 2滴 | 3滴 | 体系颜色变化:红色→浅红色→无色 | |
| 蒸馏水 | 3滴 | 2滴 | 1滴 | |||
| 紫色褪去所需时间/s | 12 | 16 | 16 | |||
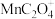 溶液呈红色,不稳定,会缓慢分解为Mn2+和CO2。
溶液呈红色,不稳定,会缓慢分解为Mn2+和CO2。i.实验④中第5滴出现褐色沉淀可能的原因是
ii.实验④和⑤的现象验证了“
 对该反应有催化作用”,催化过程如下:
对该反应有催化作用”,催化过程如下: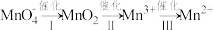
实验⑤中催化剂用量增加,褪色时间却略有延长,说明催化剂过量易催化到“催化过程”的第
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】SNCR-SCR是一种新型的烟气脱硝技术(除去烟气中的NOx),其流程如下:

该方法中主要反应的热化学方程式为:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g) ΔH=-1646 kJ/mol,如图所示,反应温度会直接影响SNCR技术的脱硝效率。
4N2(g)+6H2O(g) ΔH=-1646 kJ/mol,如图所示,反应温度会直接影响SNCR技术的脱硝效率。

回答下列问题:
(1)SNCR技术脱硝的最佳温度选择925℃的理由是_______________________ 。
(2)SNCR与SCR技术相比,SNCR技术的反应温度较高,其原因是________________ ;
但当烟气温度高于1000℃时,SNCR脱硝效率明显降低,其原因可能是___________ 。

该方法中主要反应的热化学方程式为:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g) ΔH=-1646 kJ/mol,如图所示,反应温度会直接影响SNCR技术的脱硝效率。
4N2(g)+6H2O(g) ΔH=-1646 kJ/mol,如图所示,反应温度会直接影响SNCR技术的脱硝效率。
回答下列问题:
(1)SNCR技术脱硝的最佳温度选择925℃的理由是
(2)SNCR与SCR技术相比,SNCR技术的反应温度较高,其原因是
但当烟气温度高于1000℃时,SNCR脱硝效率明显降低,其原因可能是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】NOx储存还原技术法(NSR)利用催化剂消除汽车尾气中的NOx,具有不需要额外添加还原剂、结构简单等优点,适用于轻型柴油机车和汽油机车。
(1)已知:
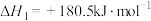

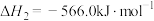
则NSR技术工作原理的热化学方程式: △H3=
△H3=_________ 。
(2)在一定温度下,向 恒容密闭容器中充入等物质的量的
恒容密闭容器中充入等物质的量的 和
和 模拟NSR反应反应过程中c(NO)隨时间变化的曲线如下图所示。
模拟NSR反应反应过程中c(NO)隨时间变化的曲线如下图所示。

①曲线a和b中,表示在该温度下使用NSR催化技术的是曲线_________ (填“a”或“b”)。
②曲线b中前10min内CO的平均反应速率v(CO)=_________ mol·L-1·min-1,此温度下该反应的平衡常数K=_________ L/mol。
③在一恒温恒容的密闭容器中发生反应,下列说法能说明该反应达到化学平衡状态的是_________ (填字母)。
A.体系的压强保持不变 B.混合气体的密度保持不变
C. D.CO2的浓度保持不变
D.CO2的浓度保持不变
④若保持其他条件不变,15min时将容器的体积压缩至1L,20min时反应重新达到平衡,NO的物质的量浓度对应的点可能是点_________ (填“A、B、C、D或E”)。
(3)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氨氧化物脱除技术。下图是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应的温度分别为_________ 。

(1)已知:

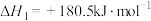

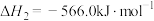
则NSR技术工作原理的热化学方程式:
 △H3=
△H3=(2)在一定温度下,向
 恒容密闭容器中充入等物质的量的
恒容密闭容器中充入等物质的量的 和
和 模拟NSR反应反应过程中c(NO)隨时间变化的曲线如下图所示。
模拟NSR反应反应过程中c(NO)隨时间变化的曲线如下图所示。
①曲线a和b中,表示在该温度下使用NSR催化技术的是曲线
②曲线b中前10min内CO的平均反应速率v(CO)=
③在一恒温恒容的密闭容器中发生反应,下列说法能说明该反应达到化学平衡状态的是
A.体系的压强保持不变 B.混合气体的密度保持不变
C.
 D.CO2的浓度保持不变
D.CO2的浓度保持不变④若保持其他条件不变,15min时将容器的体积压缩至1L,20min时反应重新达到平衡,NO的物质的量浓度对应的点可能是点
(3)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氨氧化物脱除技术。下图是不同催化剂Mn和Cr在不同温度下对应的脱氮率,由图可知工业使用的最佳催化剂和相应的温度分别为

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】晶体硅是信息科学和能源科学中的一种重要材料,以下是工业上制取纯硅的方法。

已知:在一定条件下可发生反应:Si(s)+3HCl(g)⇌SiHCl3(g)+H2(g)现在实验室模拟工业上粗硅提纯的过程,已知:SiCl4沸点57.7℃、SiHCl3沸点33.0℃。
(1)现用如下装置进行模拟反应②的过程。实验室制HCl的反应原理为:2NaCl(s)+H2SO4(浓) 2HCl↑+Na2SO4
2HCl↑+Na2SO4

A中是HCl的发生装置,你认为应选择下图哪套装置___ (填装置的字母);

(2)已知液态粗品SiHCl3中含有杂质SiCl4,则流程中操作①为___ (填操作名称),下列不是该操作所需的仪器是___ (填装置序号字母);
a.冷凝管 b.圆底烧瓶 c.蒸馏烧瓶 d.分液漏斗 e.温度计 f.接受器
(3)用SiHCl3与H2反应制备纯硅的装置如图:

①按图示组装好仪器后,下列实验步骤的正确顺序为____ (填字母)
A.打开甲装置分液漏斗旋塞滴加稀硫酸,则生成H2;
B.向装置中添加药品;
C.停止通H2;
D.检查装置气密性;
E.停止向丙装置滴加SiHCl3,并停止加热相应装置;
F.打开丙装置分液漏斗旋塞滴加SiHCl3,并加热相应装置;
步骤c中需要加热的装置为___ (填装置序号“甲”、“乙”、“丙”、“丁”)
②该套装置的设计缺陷是___ 。

已知:在一定条件下可发生反应:Si(s)+3HCl(g)⇌SiHCl3(g)+H2(g)现在实验室模拟工业上粗硅提纯的过程,已知:SiCl4沸点57.7℃、SiHCl3沸点33.0℃。
(1)现用如下装置进行模拟反应②的过程。实验室制HCl的反应原理为:2NaCl(s)+H2SO4(浓)
 2HCl↑+Na2SO4
2HCl↑+Na2SO4
A中是HCl的发生装置,你认为应选择下图哪套装置

(2)已知液态粗品SiHCl3中含有杂质SiCl4,则流程中操作①为
a.冷凝管 b.圆底烧瓶 c.蒸馏烧瓶 d.分液漏斗 e.温度计 f.接受器
(3)用SiHCl3与H2反应制备纯硅的装置如图:

①按图示组装好仪器后,下列实验步骤的正确顺序为
A.打开甲装置分液漏斗旋塞滴加稀硫酸,则生成H2;
B.向装置中添加药品;
C.停止通H2;
D.检查装置气密性;
E.停止向丙装置滴加SiHCl3,并停止加热相应装置;
F.打开丙装置分液漏斗旋塞滴加SiHCl3,并加热相应装置;
步骤c中需要加热的装置为
②该套装置的设计缺陷是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】下面是两位同学设计的证明碳酸钠样品中含有氯化钠的实验方案。
甲:取样品少许加入试管中,加入适量的蒸馏水使之溶解,配成溶液,然后加入AgNO3溶液,看是否有白色沉淀生成。
乙:取样品少许加入试管中,加入适量的自来水使之溶解,配成溶液,然后滴加稀硝酸酸化的AgNO3溶液,看是否有白色沉淀生成。
(1)两个方案均有不合理之处,请指出:
甲___ 。
乙___ 。
(2)合理的实验方案为___ 。
甲:取样品少许加入试管中,加入适量的蒸馏水使之溶解,配成溶液,然后加入AgNO3溶液,看是否有白色沉淀生成。
乙:取样品少许加入试管中,加入适量的自来水使之溶解,配成溶液,然后滴加稀硝酸酸化的AgNO3溶液,看是否有白色沉淀生成。
(1)两个方案均有不合理之处,请指出:
甲
乙
(2)合理的实验方案为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】(1)以前实验室制备纯碱(Na2CO3)的主要步骤为:将饱和NaCl溶液倒入烧杯加热,控制30~35℃,搅拌下分批加入研细的NH4HCO3固体,加料完毕,保温30分钟,静置、过滤得NaHCO3晶体。用少量蒸馏水洗涤除去杂质、抽干,转入蒸发皿中灼烧得Na2CO3固体。四种盐在不同温度下的溶解度表 (g/100g水)
①反应控制在30~35℃,是因为高于35℃NH4HCO3会分解,低于30℃则反应速率降低,为控制此温度范围,通常采取的加热方法为________________ ;
②加料完毕,保温30分钟,目的____________________________ ;
③静置后只析出NaHCO3晶体的原因______________________________ ;
④过滤所得母液中含有NaHCO3、NaCl 、NH4Cl、NH4HCO3,加入适当试剂并作进一步处理,使______ (填化学式)循环使用,回收得到NH4Cl晶体。
(2)我国科学家侯德榜改革国外的纯碱生产工艺,使其更加先进,被称为侯德榜制碱法,生产流程为:

⑤ 沉淀池中反应的化学方程式:____________________________________ ;
⑥检验产品碳酸钠中是否含有氯化钠的操作方法为:________________________ 。
⑦循环(I)中应该加入或通入物质的化学式为_____________ 。
| 温度 溶解度 | 0℃ | 10℃ | 20℃ | 30℃ | 40℃ | 50℃ | 60℃ | 100℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 39.8 |
| NH4HCO3 | 11.9 | 15.8 | 21.0 | 27.0 | — | — | — | — |
| NaHCO3 | 6.9 | 8.1 | 9.6 | 11.1 | 12.7 | 14.5 | 16.4 | — |
| NH4Cl | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.3 | 77.3 |
①反应控制在30~35℃,是因为高于35℃NH4HCO3会分解,低于30℃则反应速率降低,为控制此温度范围,通常采取的加热方法为
②加料完毕,保温30分钟,目的
③静置后只析出NaHCO3晶体的原因
④过滤所得母液中含有NaHCO3、NaCl 、NH4Cl、NH4HCO3,加入适当试剂并作进一步处理,使
(2)我国科学家侯德榜改革国外的纯碱生产工艺,使其更加先进,被称为侯德榜制碱法,生产流程为:

⑤ 沉淀池中反应的化学方程式:
⑥检验产品碳酸钠中是否含有氯化钠的操作方法为:
⑦循环(I)中应该加入或通入物质的化学式为
您最近一年使用:0次



