常温时,用0.1000mol/ LNaOH溶液滴定25.00mL0.1000mol/L某一元酸HX溶液,滴定过程中pH变化曲线如图所示。下列说法正确的是
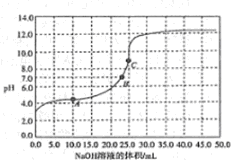
| A.HX为强酸 |
| B.在A点,c(HX)>c(X-)>c(Na+)>c(H+)>c(OH-) |
| C.在B点,两者恰好完全反应 |
| D.在C点.c(X-)+ c(HX)=0.1mol/L |
更新时间:2017-04-11 13:35:45
|
相似题推荐
单选题
|
较难
(0.4)
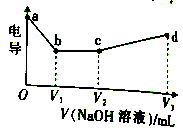
【推荐1】25℃时,向盛有50 mL pH=2的HA溶液的绝热容器 中加入pH=13的NaOH溶液,实验测得加入NaOH溶液的体积(V)与所得混合溶液的温度(T)的关系如下图所示。下列叙述正确的是

| A.HA溶液的物质的量浓度为0.01 mol·L-1 |
| B.b→c的过程中,温度降低的原因是溶液中发生了吸热反应 |
| C.a→b的过程中,混合溶液中可能存在:c(A-)=c(Na+) |
| D.25℃时,HA的电离常数K约为1.25×10-2 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列实验能达到预期实验目的的是
| 实验 | 实验目的 |
| A.测定等物质的量浓度的CH3COONa和 Na2S溶液pH | 比较CH3COOH和H2S的酸性强弱 |
B. | 测定盐酸的浓度 |
C. | 测定中和热 |
| D.先用酚酞,后用甲基橙作指示剂,用标准盐酸滴定0.1 mol/L的Na2CO3溶液 | 证明 CO32—水解分两步 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】常温下,向20mL0.lmol•L-1(CH3)2NH•H2O(一水合二甲胺)溶液中滴加0.1mol•L-1盐酸,滴定曲线如图甲所示,含C微粒的物质的量分数σ随pH变化如图乙所示。下列说法错误的是( )
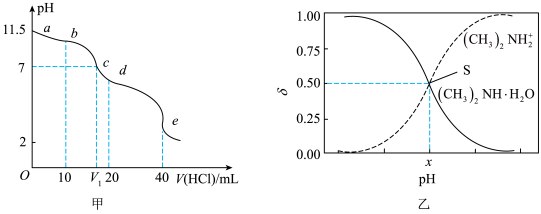

| A.e点时,溶液中c(Cl-)=2c[(CH3)2NH•H2O]+2c[(CH3)2NH2+] |
| B.S点对应溶液的pH约为11.5 |
| C.常温下(CH3)2NH•H2O的电离常数为1×10-4 |
| D.d点时,溶液中c(H+)=c(OH-)+c[(CH3)2NH•H2O] |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列说法正确的是
A.常温时,某物质的溶液中由水电离出的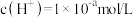 ,若 ,若 时,则该溶液的pH一定为 时,则该溶液的pH一定为 |
B.某温度时水的离子积常数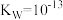 ,若将此温度下 ,若将此温度下 的NaOH溶液aL与 的NaOH溶液aL与 的稀硫酸bL混合,若所得混合液 的稀硫酸bL混合,若所得混合液 ,则 ,则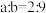 |
C.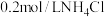 溶液和 溶液和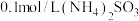 溶液中, 溶液中, 前者较大 前者较大 |
| D.浓度均为0.1mol/L的NaCl溶液和NaF溶液中,离子总浓度后者较大 |
您最近一年使用:0次

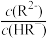 或
或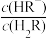 ,pY=-lg Y,题中涉及浓度的单位为mol•L-1。下列叙述错误的是
,pY=-lg Y,题中涉及浓度的单位为mol•L-1。下列叙述错误的是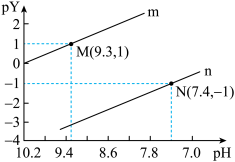
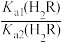 =103.9
=103.9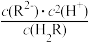 保持不变
保持不变

