元素及其化合物的应用研究是目前科学研究的前沿之一。试回答下列问题:
(1)原子序数小于36的过渡元素A和B,在周期表中位于同一族,且原子序数B比A多1,基态B原子中含有三个未成对电子。请写出B元素在周期表中的位置为______ ,属于___ 区元素,A2+在基态时价电子排布图为__________________ 。
(2)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。水分子中心原子价层电子对数为____ ,二氧化碳的VSEPR模型为______ ,苯分子中碳原子的杂化类型为________ 。
(3)Co3+有多种配合物,如Co(CN)63-、Co(NH3)4Cl2+ 等。铑(Rh)与钴属于同族元素,某些性质相似。现有铑的某盐组成为CsRh(SO4)2·4H2O,易溶解于水,向其水溶液中加入一定浓度的BaCl2溶液,无沉淀生成。该盐中铑离子的配位数为____ 。请写出该盐溶解于水后的电离方程式:_________________________________ 。
(1)原子序数小于36的过渡元素A和B,在周期表中位于同一族,且原子序数B比A多1,基态B原子中含有三个未成对电子。请写出B元素在周期表中的位置为
(2)二氧化钛作光催化剂能将居室污染物甲醛、苯等有害气体可转化为二氧化碳和水,达到无害化。水分子中心原子价层电子对数为
(3)Co3+有多种配合物,如Co(CN)63-、Co(NH3)4Cl2+ 等。铑(Rh)与钴属于同族元素,某些性质相似。现有铑的某盐组成为CsRh(SO4)2·4H2O,易溶解于水,向其水溶液中加入一定浓度的BaCl2溶液,无沉淀生成。该盐中铑离子的配位数为
更新时间:2017-04-20 13:55:45
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有六种元素,其中A、B、C、D为短周期主族元素,E、F为第四周期元素,它们的原子序数依次增大。
(1)画出A基态原子的核外电子排布图___________ 。
(2)C的基态原子的核外电子排布图 ,该同学所画的电子排布图违背
,该同学所画的电子排布图违背___________ 。
(3)D的基态原子中能量最高的电子,其电子云在空间有___________ 个方向,原子轨道呈___________ 形。
(4)写出C原子的电子排布式___________ ;写出E原子的电子简化排布式___________ 。
(5)请写出F元素价电子排布式___________ 。
(6)写出微粒的核外电子排布式:28Ni___________ ;26Fe3+___________ ;
| A元素原子的核外p电子数比s电子数少3 |
| B元素形成的物质种类繁多,其形成的一种固体单质工业上常用作切割工具 |
| C元素基态原子p轨道有3个未成对电子 |
| D原子核外所有p轨道全满或半满 |
| E在该周期中未成对电子数最多 |
| F能形成红色(或砖红色)和黑色的两种氧化物 |
(1)画出A基态原子的核外电子排布图
(2)C的基态原子的核外电子排布图
 ,该同学所画的电子排布图违背
,该同学所画的电子排布图违背(3)D的基态原子中能量最高的电子,其电子云在空间有
(4)写出C原子的电子排布式
(5)请写出F元素价电子排布式
(6)写出微粒的核外电子排布式:28Ni
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】依据原子结构知识回答下列问题。
(1)硅原子核外电子的运动状态有_____ 种。
(2)非金属性:S小于O。试用一个实验事实说明_____ 。
(3)一定温度下,对于可逆反应N2(g)+3H2(g) 2NH3(g)(正反应放热)的下列叙述,不能说明反应已达化学平衡状态的是_____。
2NH3(g)(正反应放热)的下列叙述,不能说明反应已达化学平衡状态的是_____。
(4)画出Fe3+的结构示意图_____ ;写出Mn2+的轨道表示式:_____ ;写出32号元素的元素符号及其价层电子排布式:_____ 。
(1)硅原子核外电子的运动状态有
(2)非金属性:S小于O。试用一个实验事实说明
(3)一定温度下,对于可逆反应N2(g)+3H2(g)
 2NH3(g)(正反应放热)的下列叙述,不能说明反应已达化学平衡状态的是_____。
2NH3(g)(正反应放热)的下列叙述,不能说明反应已达化学平衡状态的是_____。| A.单位时间内断裂amolN≡N键,同时断裂6amolN—H键 |
| B.NH3的生成速率与H2的生成速率之比为2∶3 |
| C.恒压容器内混合气体的总物质的量不再变化 |
| D.恒容容器内混合气体的密度不再变化 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】锌的化学性质与铝相似,工业上有较高的利用价值。某含锌废催化剂中锌以氧化物的形式存在,还含有镍、铁、铅等元素杂质,采用“氨浸除杂蒸发煅烧”新工艺生产高纯碱式碳酸锌,达到了废物综合利用的目的,工艺流程如图,请回答下列问题。
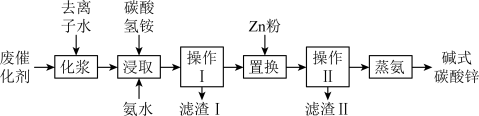
已知:“浸取”步骤后生成了锌氨配合物和镍氨配合物进行后续生产。
(1)Zn2+的价电子排布图____ ;金属配合物的结构和稳定性常用18e-经验规则预测,即中心体的价电子数加配体提供的电子数等于18,请试写出“浸取”后锌元素的存在微粒形式____ 。(填化学式)
(2)“浸取”步骤中,废催化剂中含锌物质的反应方程式为____ 。
(3)“浸取”中锌的浸出率对本工艺至关重要,图一、图二是锌浸出率分别受温度、氨水与碳酸氢铵比(氮元素浓度固定)的影响。请分析:

①图一中适宜选择的温度为42℃左右。温度不宜过高的原因是____ 。
②图二中随着氨水与碳酸氢铵比的增大,锌的浸出率先增大后减小,然后再增大。当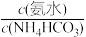 <0.75时,溶液pH值较低,试判断锌的存在形式为
<0.75时,溶液pH值较低,试判断锌的存在形式为____ ;当0.75<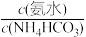 <1时,溶液pH值升高,锌的存在形式为
<1时,溶液pH值升高,锌的存在形式为____ ;当1<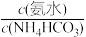 后,溶液pH值继续升高,锌的存在形式为
后,溶液pH值继续升高,锌的存在形式为___ 。
(4)滤渣II的成分为过量的Zn外,还有____ 。(填化学式)
(5)“蒸氨”操作中锌氨溶液最终以ZnCO3•2Zn(OH)2形式从溶液中析出,经过滤洗涤、干燥后得到碱式碳酸锌,其化学反应方程式为:____ 。
(6)整个过程中可以循环利用的物质为____ 。

已知:“浸取”步骤后生成了锌氨配合物和镍氨配合物进行后续生产。
(1)Zn2+的价电子排布图
(2)“浸取”步骤中,废催化剂中含锌物质的反应方程式为
(3)“浸取”中锌的浸出率对本工艺至关重要,图一、图二是锌浸出率分别受温度、氨水与碳酸氢铵比(氮元素浓度固定)的影响。请分析:

①图一中适宜选择的温度为42℃左右。温度不宜过高的原因是
②图二中随着氨水与碳酸氢铵比的增大,锌的浸出率先增大后减小,然后再增大。当
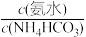 <0.75时,溶液pH值较低,试判断锌的存在形式为
<0.75时,溶液pH值较低,试判断锌的存在形式为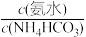 <1时,溶液pH值升高,锌的存在形式为
<1时,溶液pH值升高,锌的存在形式为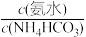 后,溶液pH值继续升高,锌的存在形式为
后,溶液pH值继续升高,锌的存在形式为(4)滤渣II的成分为过量的Zn外,还有
(5)“蒸氨”操作中锌氨溶液最终以ZnCO3•2Zn(OH)2形式从溶液中析出,经过滤洗涤、干燥后得到碱式碳酸锌,其化学反应方程式为:
(6)整个过程中可以循环利用的物质为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】储氢材料是一类能可逆地吸收和释放氢气的材料。回答下列问题
(1)多相 系储氢合金是新型储氢材料。基态
系储氢合金是新型储氢材料。基态 原子中自旋状态相反的两种电子的个数比为
原子中自旋状态相反的两种电子的个数比为_______ 。
(2)四氢铝锂( )是一种重要的储氢载体,
)是一种重要的储氢载体, 的空间构型为
的空间构型为_______ ;Li、Al、H的电负性由大到小的顺序为_______ 。
(3)氨硼烷( )是目前最具潜力的储氢材料之一,在四氢呋喃(
)是目前最具潜力的储氢材料之一,在四氢呋喃( )作溶剂的条件下可合成氨硼烷:
)作溶剂的条件下可合成氨硼烷: 。
。
① 中B的杂化轨道类型为
中B的杂化轨道类型为_______ ,H—N—H键角:
_______ 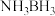 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是_______ 。
②常温下,四氢呋喃易溶于水,环戊烷难溶于水,其原因可能是_______ ;呋喃( )与氢气加成得到四氢呋喃,已知呋喃是一种具有芳香性的平面分子,分子中含有大
)与氢气加成得到四氢呋喃,已知呋喃是一种具有芳香性的平面分子,分子中含有大 键,该大
键,该大 键可表示为
键可表示为_______ (分子中的大 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数)。
键的电子数)。
(4)一种由Mg和过渡金属M组成的二元储氢材料属立方晶系,晶胞中Mg和M的原子个数比为 ,且距离Mg最近的M形成的几何图形为正四面体;晶胞在xy、xz和yz平面投影如图所示。
,且距离Mg最近的M形成的几何图形为正四面体;晶胞在xy、xz和yz平面投影如图所示。_______ 。
②该储氢材料的立方晶胞中,晶胞参数为a pm,Mg和M的原子半径分别为 pm和
pm和 pm,则Mg和M原子的空间占有率为
pm,则Mg和M原子的空间占有率为_______ 。
(1)多相
 系储氢合金是新型储氢材料。基态
系储氢合金是新型储氢材料。基态 原子中自旋状态相反的两种电子的个数比为
原子中自旋状态相反的两种电子的个数比为(2)四氢铝锂(
 )是一种重要的储氢载体,
)是一种重要的储氢载体, 的空间构型为
的空间构型为(3)氨硼烷(
 )是目前最具潜力的储氢材料之一,在四氢呋喃(
)是目前最具潜力的储氢材料之一,在四氢呋喃( )作溶剂的条件下可合成氨硼烷:
)作溶剂的条件下可合成氨硼烷: 。
。①
 中B的杂化轨道类型为
中B的杂化轨道类型为
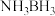 (填“>”“<”或“=”),原因是
(填“>”“<”或“=”),原因是②常温下,四氢呋喃易溶于水,环戊烷难溶于水,其原因可能是
 )与氢气加成得到四氢呋喃,已知呋喃是一种具有芳香性的平面分子,分子中含有大
)与氢气加成得到四氢呋喃,已知呋喃是一种具有芳香性的平面分子,分子中含有大 键,该大
键,该大 键可表示为
键可表示为 键可用符号
键可用符号 表示,其中m代表参与形成大
表示,其中m代表参与形成大 键的原子数,n代表参与形成大
键的原子数,n代表参与形成大 键的电子数)。
键的电子数)。(4)一种由Mg和过渡金属M组成的二元储氢材料属立方晶系,晶胞中Mg和M的原子个数比为
 ,且距离Mg最近的M形成的几何图形为正四面体;晶胞在xy、xz和yz平面投影如图所示。
,且距离Mg最近的M形成的几何图形为正四面体;晶胞在xy、xz和yz平面投影如图所示。
②该储氢材料的立方晶胞中,晶胞参数为a pm,Mg和M的原子半径分别为
 pm和
pm和 pm,则Mg和M原子的空间占有率为
pm,则Mg和M原子的空间占有率为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】已知A、B、C、D、E 为原子序数依次增大的前四周期元素。已知前四种元素的基态原子p能级都有2个单电子,E 的原子序数等于A、B、C三种元素原子序数之和。
试回答下列问题:
(1)基态E原子外围电子排布图为_________ ;其中M 能层有_____ 种能量不同的电子。
(2)从原子结构角度解释B 电负性大于D的原因是:_______________ 。
(3) 含A元素的化合物中,A 的原子间常有π键,但是含C元素的化合物中,C的原子间只能存在σ键,其主要原因是___________________ 。
(4)H2D2B8是一种具有强氧化性的二元酸(其中分子结构中有2个B原子显-1价),则H2D2B8的结构式为___________ ,分子中采取sp3杂化的B原子有______ 个。
(5)E 晶胞内粒子的堆积模型如图所示。

已知:E 晶胞的密度为ρg/cm3,NA代表阿伏伽德罗常数值,E 的相对原子质量为M。
①E 粒子的配位数为_______ 。
②E 粒子半径为_______ pm。
③E 晶胞中粒子的空间利用率φ=_____ (用含π 的式子表示)。
试回答下列问题:
(1)基态E原子外围电子排布图为
(2)从原子结构角度解释B 电负性大于D的原因是:
(3) 含A元素的化合物中,A 的原子间常有π键,但是含C元素的化合物中,C的原子间只能存在σ键,其主要原因是
(4)H2D2B8是一种具有强氧化性的二元酸(其中分子结构中有2个B原子显-1价),则H2D2B8的结构式为
(5)E 晶胞内粒子的堆积模型如图所示。

已知:E 晶胞的密度为ρg/cm3,NA代表阿伏伽德罗常数值,E 的相对原子质量为M。
①E 粒子的配位数为
②E 粒子半径为
③E 晶胞中粒子的空间利用率φ=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】 是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题:
是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题:
(1)S在元素周期表中的位置是_____ ,基态Cu的价层电子轨道表示式为_____ 。
(2)原子中运动的电子有两种相反的自旋状态,一种自旋状态用 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态S原子,其所有价电子自旋磁量子数的代数和的绝对值为
表示,称为电子的自旋磁量子数。对于基态S原子,其所有价电子自旋磁量子数的代数和的绝对值为_____ 。
(3) 形成的某种配合物A结构如图所示。
形成的某种配合物A结构如图所示。
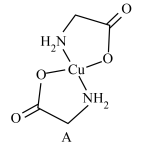
①配合物A中Cu的配位数是_____ ,已知在配合物A中与Cu相连的4个配位原子处在一个平面内,则Cu原子采用的杂化方式为_____ (填字母)。
A. B.
B. C.
C.
②A与足量稀盐酸反应时,配位键被破坏,生成 和
和_____ (写结构简式)。
(4) (相对分子质量为Mr)的晶胞结构如图所示,晶胞参数依次为anm,bnm,cnm,阿伏加德罗常数为
(相对分子质量为Mr)的晶胞结构如图所示,晶胞参数依次为anm,bnm,cnm,阿伏加德罗常数为 ,则
,则 晶体的密度为
晶体的密度为_____  (列计算式),图b为In原子沿z轴方向在x-y平面投影的位置,在图b中画出S原子沿该方向的投影位置
(列计算式),图b为In原子沿z轴方向在x-y平面投影的位置,在图b中画出S原子沿该方向的投影位置_____ (用“ ”表示S原子)。
”表示S原子)。

 是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题:
是生物医药、太阳能电池等领域的理想荧光材料。回答下列问题:(1)S在元素周期表中的位置是
(2)原子中运动的电子有两种相反的自旋状态,一种自旋状态用
 表示,与之相反的用
表示,与之相反的用 表示,称为电子的自旋磁量子数。对于基态S原子,其所有价电子自旋磁量子数的代数和的绝对值为
表示,称为电子的自旋磁量子数。对于基态S原子,其所有价电子自旋磁量子数的代数和的绝对值为(3)
 形成的某种配合物A结构如图所示。
形成的某种配合物A结构如图所示。
①配合物A中Cu的配位数是
A.
 B.
B. C.
C.
②A与足量稀盐酸反应时,配位键被破坏,生成
 和
和(4)
 (相对分子质量为Mr)的晶胞结构如图所示,晶胞参数依次为anm,bnm,cnm,阿伏加德罗常数为
(相对分子质量为Mr)的晶胞结构如图所示,晶胞参数依次为anm,bnm,cnm,阿伏加德罗常数为 ,则
,则 晶体的密度为
晶体的密度为 (列计算式),图b为In原子沿z轴方向在x-y平面投影的位置,在图b中画出S原子沿该方向的投影位置
(列计算式),图b为In原子沿z轴方向在x-y平面投影的位置,在图b中画出S原子沿该方向的投影位置 ”表示S原子)。
”表示S原子)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】我国科技工作者利用计算机技术,预测了超硬钨氮化合物( )并进行合成,这对扩充超硬材料家族以及研究硬度起源都有重要的科学意义。
)并进行合成,这对扩充超硬材料家族以及研究硬度起源都有重要的科学意义。
(1)区分 是否为晶体的最可靠的科学方法为
是否为晶体的最可靠的科学方法为_______ 。
(2)已知基态W原子的价层电子排布式为 ,则基态W原子核外最外层电子占据的能层符号是
,则基态W原子核外最外层电子占据的能层符号是_______ ;与基态 原子相比,基态W原子与基态
原子相比,基态W原子与基态 原子的未成对电子数之比为
原子的未成对电子数之比为_______ 。
(3)常见的含氮微粒有 、
、 、
、 、
、 、
、 等。
等。
① 的组成元素中,电负性最大的元素是
的组成元素中,电负性最大的元素是_______ (填元素符号,下同);第一电离能最大的元素是_______ 。
② 中心原子的杂化类型为
中心原子的杂化类型为_______ ; 的空间构型为
的空间构型为_______ 。
③已知 中存在一个大π键,可用符号
中存在一个大π键,可用符号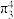 表示(3表示原子数,4表示参与形成大π键的p电子数),则一个
表示(3表示原子数,4表示参与形成大π键的p电子数),则一个 中键合电子(形成化学键的电子)的总数为
中键合电子(形成化学键的电子)的总数为_______ 。
④ 在水中的溶解性比
在水中的溶解性比 大很多,其主要原因是
大很多,其主要原因是_______ 。
(4)磷化硼(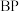 )是超硬材料家族的重要成员之一,其晶胞结构如图所示,若硼原子与磷原子最近的距离为anm,设
)是超硬材料家族的重要成员之一,其晶胞结构如图所示,若硼原子与磷原子最近的距离为anm,设 表示阿伏加德罗常数的值,则磷化硼晶体的密度为
表示阿伏加德罗常数的值,则磷化硼晶体的密度为_______  (用含a、
(用含a、 的计算式表示)。
的计算式表示)。

 )并进行合成,这对扩充超硬材料家族以及研究硬度起源都有重要的科学意义。
)并进行合成,这对扩充超硬材料家族以及研究硬度起源都有重要的科学意义。(1)区分
 是否为晶体的最可靠的科学方法为
是否为晶体的最可靠的科学方法为(2)已知基态W原子的价层电子排布式为
 ,则基态W原子核外最外层电子占据的能层符号是
,则基态W原子核外最外层电子占据的能层符号是 原子相比,基态W原子与基态
原子相比,基态W原子与基态 原子的未成对电子数之比为
原子的未成对电子数之比为(3)常见的含氮微粒有
 、
、 、
、 、
、 、
、 等。
等。①
 的组成元素中,电负性最大的元素是
的组成元素中,电负性最大的元素是②
 中心原子的杂化类型为
中心原子的杂化类型为 的空间构型为
的空间构型为③已知
 中存在一个大π键,可用符号
中存在一个大π键,可用符号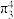 表示(3表示原子数,4表示参与形成大π键的p电子数),则一个
表示(3表示原子数,4表示参与形成大π键的p电子数),则一个 中键合电子(形成化学键的电子)的总数为
中键合电子(形成化学键的电子)的总数为④
 在水中的溶解性比
在水中的溶解性比 大很多,其主要原因是
大很多,其主要原因是(4)磷化硼(
 )是超硬材料家族的重要成员之一,其晶胞结构如图所示,若硼原子与磷原子最近的距离为anm,设
)是超硬材料家族的重要成员之一,其晶胞结构如图所示,若硼原子与磷原子最近的距离为anm,设 表示阿伏加德罗常数的值,则磷化硼晶体的密度为
表示阿伏加德罗常数的值,则磷化硼晶体的密度为 (用含a、
(用含a、 的计算式表示)。
的计算式表示)。
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】(NH4)2Fe(SO4)2·6H2O,俗名为莫尔盐,是一种重要的化工原料,可用于医药、冶金、电镀等。回答下列问题:
(1)NH 离子中N的
离子中N的_______ 轨道与H的s轨道重叠形成σ键; 的空间构型为
的空间构型为_______ ,其O-S-O的键角比 中O-S-O的键角
中O-S-O的键角_______ (填“大”或“小”)。
(2)Fe与S形成的一种化合物晶体的晶胞结构及其纵向投影如图所示,该物质的化学式为_______ 。已知:晶体密度为ρg/cm3,阿伏加德罗常数的值为NA,晶胞六棱柱底面边长为apm,则该晶胞的高c=_______ pm(列出计算式)。

(1)NH
 离子中N的
离子中N的 的空间构型为
的空间构型为 中O-S-O的键角
中O-S-O的键角(2)Fe与S形成的一种化合物晶体的晶胞结构及其纵向投影如图所示,该物质的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】钛是20世纪50年代发展起来的一种重要的结构金属,钛合金因具有强度高、耐蚀性好、耐热性高等特点而被广泛用于各个领域。回答下列问题:
(1)钛元素在元素周期表中的位置_____ 。与钛同周期且未成对电子数最多的元素,其价层电子排布图为_____ 。
(2)二氧化钛与 (光气)、
(光气)、 (二氯亚砜)等氯化试剂反应可用于制取四氯化钛。
(二氯亚砜)等氯化试剂反应可用于制取四氯化钛。
① 的空间构型为
的空间构型为_____ , 中
中 键和
键和 键的数目比为
键的数目比为_____ 。
② 是
是_____ 分子。(填“极性”或“非极性”)
(3)钛的某配合物可用于催化环烯烃聚合,其结构如下图所示:
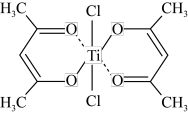
该配合物中存在的化学键有_____ (填字母)。
a.离子键 b.配位键 c.金属键 d.共价键 e.氢键
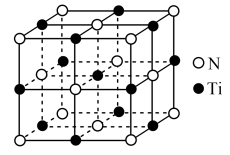
(4)氮化钛晶体的晶胞结构如图所示,该晶体结构中与 原子距离最近且相等的
原子距离最近且相等的 原子有
原子有_____ 个;若该晶胞的密度为 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞中
,则晶胞中 原子与
原子与 原子的最近距离为
原子的最近距离为_____  。(用含
。(用含 、
、 的代数式表示,
的代数式表示, 的相对原子质量48)
的相对原子质量48)
(5)在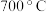 左右,将
左右,将 通过二氧化钛和炭粉的混合物可生成
通过二氧化钛和炭粉的混合物可生成 和一种含碳元素的气体,写出该反应的化学方程式
和一种含碳元素的气体,写出该反应的化学方程式_____ 。
(1)钛元素在元素周期表中的位置
(2)二氧化钛与
 (光气)、
(光气)、 (二氯亚砜)等氯化试剂反应可用于制取四氯化钛。
(二氯亚砜)等氯化试剂反应可用于制取四氯化钛。①
 的空间构型为
的空间构型为 中
中 键和
键和 键的数目比为
键的数目比为②
 是
是(3)钛的某配合物可用于催化环烯烃聚合,其结构如下图所示:

该配合物中存在的化学键有
a.离子键 b.配位键 c.金属键 d.共价键 e.氢键
(4)氮化钛晶体的晶胞结构如图所示,该晶体结构中与
 原子距离最近且相等的
原子距离最近且相等的 原子有
原子有 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 ,则晶胞中
,则晶胞中 原子与
原子与 原子的最近距离为
原子的最近距离为 。(用含
。(用含 、
、 的代数式表示,
的代数式表示, 的相对原子质量48)
的相对原子质量48)
(5)在
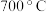 左右,将
左右,将 通过二氧化钛和炭粉的混合物可生成
通过二氧化钛和炭粉的混合物可生成 和一种含碳元素的气体,写出该反应的化学方程式
和一种含碳元素的气体,写出该反应的化学方程式
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】(1)①丙酮( )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是________ ,1mol丙酮分子中含有σ键的数目为____________ 。
②乙醇的沸点高于丙酮,这是因为__________ 。
(2)①碳的一种单质的结构如图所示。该单质的晶体类型为______ ,原子间存在的共价键类型有_______ ,碳原子的杂化轨道类型为_______________ 。

②SiCl4分子的中心原子的价层电子对数为_______ ,分子的立体构型为______ ,属于______ 分子(填“极性”或“非极性”)。
③四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图所示。

ⅰ.SiX4的沸点依F、Cl、Br、I顺序升高的原因是_____________ 。
ⅱ.结合SiX4的沸点和PbX2的熔点的变化规律,可推断:依F、Cl、Br、I顺序,PbX2中的化学键的离子性_______ 、共价性_______ 。(填“增强”“不变”或“减弱”)
(3)[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2-+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
①1 mol HCHO分子中含有σ键的物质的量为______ mol。
②HOCH2CN分子中碳原子轨道的杂化类型为_______ 。

③与H2O分子互为等电子体的阴离子为_______ 。
④[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为___________ 。
 )分子中碳原子轨道的杂化类型是
)分子中碳原子轨道的杂化类型是②乙醇的沸点高于丙酮,这是因为
(2)①碳的一种单质的结构如图所示。该单质的晶体类型为

②SiCl4分子的中心原子的价层电子对数为
③四卤化硅SiX4的沸点和二卤化铅PbX2的熔点如图所示。

ⅰ.SiX4的沸点依F、Cl、Br、I顺序升高的原因是
ⅱ.结合SiX4的沸点和PbX2的熔点的变化规律,可推断:依F、Cl、Br、I顺序,PbX2中的化学键的离子性
(3)[Zn(CN)4]2-在水溶液中与HCHO发生如下反应:4HCHO+[Zn(CN)4]2-+4H++4H2O=[Zn(H2O)4]2++4HOCH2CN
①1 mol HCHO分子中含有σ键的物质的量为
②HOCH2CN分子中碳原子轨道的杂化类型为

③与H2O分子互为等电子体的阴离子为
④[Zn(CN)4]2-中Zn2+与CN-的C原子形成配位键。不考虑空间构型,[Zn(CN)4]2-的结构可用示意图表示为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐2】早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成,回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过___________ 方法区分晶体、准晶体和非晶体。
(2)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是___________ 。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有___________ 个铜原子。
(3)Cu2+能与乙二胺(H2N- CH2- CH2- NH2) 形成配离子如图: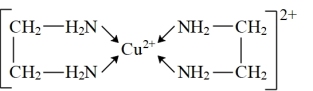 ,该配离子中含有的化学键类型有___________(填字母序号)。
,该配离子中含有的化学键类型有___________(填字母序号)。
(4)羰基铁[Fe(CO)5]可用作催化剂、汽油抗暴剂等。lmolFe(CO)5分子中含___________ molσ键。
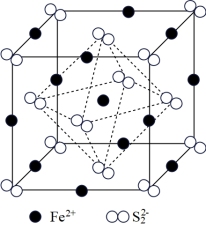
(5)FeS2晶体的晶胞如图所示。晶胞边长为a nm,FeS2的相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________ g·cm-3
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过
(2)CuO在高温时分解为O2和Cu2O,请从阳离子的结构来说明在高温时,Cu2O比CuO更稳定的原因是
(3)Cu2+能与乙二胺(H2N- CH2- CH2- NH2) 形成配离子如图:
 ,该配离子中含有的化学键类型有___________(填字母序号)。
,该配离子中含有的化学键类型有___________(填字母序号)。| A.配位键 | B.极性键 | C.离子键 | D.非极性键 |
(5)FeS2晶体的晶胞如图所示。晶胞边长为a nm,FeS2的相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】硅、铜、镓、硒等化学物质可作为制造太阳能电池板的材料。
(1)镓是ⅢA族元素,写出基态镓原子的核外电子排布式__________________ 。
(2)硒为第四周期ⅥA族元素,与其相邻的元素有砷(33号)、溴(35号),则三种元素的电负性由大到小的顺序为______________ (用元素符号表示)。
(3)SeO3分子的立体构型为____ ,与硒同主族元素的氢化物(化学式为H2R)中,沸点最低的物质化学式为____ 。
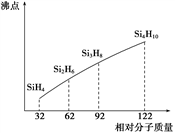
(4)硅烷(SinH2n+2)的沸点与其相对分子质量的关系如图所示,呈现这种变化的原因是____________ 。
(5)金属铜投入氨水中或投入过氧化氢溶液中均无明显现象,但投入氨水与过氧化氢的混合液中,则铜片溶解,溶液呈深蓝色,写出使溶液呈深蓝色的离子的化学式_____ 。
(6)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中金原子位于顶点,铜原子位于面心,则该合金中金原子(Au)与铜原子(Cu)个数之比为____________ ,若该晶体的晶胞边长为a pm,则该合金的密度为________________ g·cm-3(列出计算式,不要求计算结果,设阿伏伽德罗常数的值为NA)。
(1)镓是ⅢA族元素,写出基态镓原子的核外电子排布式
(2)硒为第四周期ⅥA族元素,与其相邻的元素有砷(33号)、溴(35号),则三种元素的电负性由大到小的顺序为
(3)SeO3分子的立体构型为
(4)硅烷(SinH2n+2)的沸点与其相对分子质量的关系如图所示,呈现这种变化的原因是

(5)金属铜投入氨水中或投入过氧化氢溶液中均无明显现象,但投入氨水与过氧化氢的混合液中,则铜片溶解,溶液呈深蓝色,写出使溶液呈深蓝色的离子的化学式
(6)一种铜金合金晶体具有面心立方最密堆积结构,在晶胞中金原子位于顶点,铜原子位于面心,则该合金中金原子(Au)与铜原子(Cu)个数之比为
您最近一年使用:0次



