298K时,向体积均为15.0mL,浓度均为1.00mol/L的氨水和NaHCO3溶液中分别滴加1.00mol/L的盐酸,溶液的pH与所加盐酸体积的关系如图所示。下列有关叙述正确的是
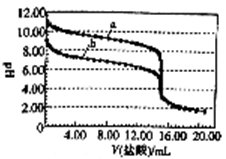
| A.曲线a是NaHCO3溶液的滴定曲线 |
| B.当V(盐酸)=4.00mL时,c(HCO3-)>c(NH4+)>c(CO32-) |
| C.当V(盐酸)=15.00mL时,c(Na+)=c(NH4+) |
| D.两个滴定过程均可选择酚酞作指示剂 |
更新时间:2017-05-12 16:49:46
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】25℃时,取浓度为0.1000mol/L的氨水20.00mL,用0.1000mol/L盐酸滴定,过程中pH随滴加溶液的体积变化关系如图所示。下列说法错误的是

| A.25℃时Kb(NH3·H2O)=10-5 |
| B.滴定过程中,水的电离程度大小是:c>b>a |
| C.本次滴定若使用酚酞试剂,会导致待测液浓度偏低 |
D.c点时溶液中离子浓度的关系是c(Cl-)>c( )>c(H+)>c(OH-) )>c(H+)>c(OH-) |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】某学生用滴定的方法测定含有少量NaCl的小苏打固体中NaHCO3的质量分数,所用标准盐酸的浓度为0.1000mol/L。关于该实验的叙述正确的是
| A.用烧杯准确配制100mL待测小苏打的溶液 |
| B.用酚酞为指示剂 |
| C.当滴至待测液变色并能将该颜色保持半分钟即为滴定终点 |
| D.盛盐酸的滴定管未用标准盐酸润洗会造成实验结果偏低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】天然水体中的H2CO3与空气中的CO2保持平衡。已知Ksp(CaCO3)=2.8×10-9,某溶洞水体中lgc(X)(X为H2CO3、HCO 、CO
、CO 或Ca2+)与pH变化的关系如图所示。下列有关溶液说法正确的是
或Ca2+)与pH变化的关系如图所示。下列有关溶液说法正确的是

 、CO
、CO 或Ca2+)与pH变化的关系如图所示。下列有关溶液说法正确的是
或Ca2+)与pH变化的关系如图所示。下列有关溶液说法正确的是
A.随pH增大,c(HCO )与c(Ca2+)的变化趋势相同 )与c(Ca2+)的变化趋势相同 |
| B.当c(Ca2+)=2.8×10-4mol•L-1时,水体的pH=6.3 |
| C.H2CO3的电离常数Ka1=10-6.3,Ka2=10-8.3 |
D.pH=7时,c(Ca2+)>c(HCO )>c(H2CO3)>c(CO )>c(H2CO3)>c(CO ) ) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】在0.1 mol·L-1的Na2CO3溶液中,下列关系正确的是
A.c(Na+)=2c(CO ) ) | B.c(OH-)=2c(H+) |
C.c(HCO )>c(H2CO3) )>c(H2CO3) | D.c(Na+)<c(CO )+c(HCO )+c(HCO ) ) |
您最近一年使用:0次





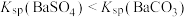

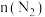 对反应的影响,H2的平衡转化率:
对反应的影响,H2的平衡转化率: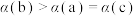
 [B(OH)4]-+H+,下列有关说法正确的是
[B(OH)4]-+H+,下列有关说法正确的是

