化学实验装置的科学设计是实验是否取得预期效果的关键。请回答下列有关实验装置的相关问题:
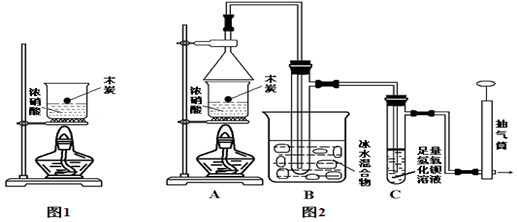
Ⅰ.下图A为“人教版”教材制备乙酸乙酯的实验装置,甲同学认为下图B装置进行酯化反应效果比A 要好,他的理由是______________________________ ;乙同学经查阅资料认为下图C装置进行酯化反应效果更好,他的理由是 ________________________________ 。

Ⅱ.某实验小组欲探究碳与浓硝酸反应的情况。甲同学设计了图1装置,认为若有红棕色气体产生就说明碳与浓硝酸发生了反应。(已知:C+4HNO3 (浓) 4NO2↑+CO2↑+2H2O)
4NO2↑+CO2↑+2H2O)
(1)甲同学的实验应该在___________ 中进行,才符合化学实验安全性的要求。
(2)乙同学认为红棕色气体不一定是碳与浓硝酸发生反应而得,所以他认为甲同学观点是错误的,他的理由是___________________________ (用化学方程式表示),为此乙同学查阅相关资料得知“0℃时四氧化二氮为液体”,从而改进了实验装置如图2所示。
(3)常温下存在:2NO2 N2O4请用平衡移动原理解释B装置的作用
N2O4请用平衡移动原理解释B装置的作用_______________________________________________________ (用文字表述)。
(4)C装置中出现的现象是_________________ ,经检测C的溶液中还含有少量氮元素,只以NO3-形式存在,写出生成该离子的离子方程式 ___________________________ 。
Ⅰ.下图A为“人教版”教材制备乙酸乙酯的实验装置,甲同学认为下图B装置进行酯化反应效果比A 要好,他的理由是

Ⅱ.某实验小组欲探究碳与浓硝酸反应的情况。甲同学设计了图1装置,认为若有红棕色气体产生就说明碳与浓硝酸发生了反应。(已知:C+4HNO3 (浓)
 4NO2↑+CO2↑+2H2O)
4NO2↑+CO2↑+2H2O)(1)甲同学的实验应该在
(2)乙同学认为红棕色气体不一定是碳与浓硝酸发生反应而得,所以他认为甲同学观点是错误的,他的理由是
(3)常温下存在:2NO2
 N2O4请用平衡移动原理解释B装置的作用
N2O4请用平衡移动原理解释B装置的作用(4)C装置中出现的现象是
更新时间:2017-05-22 22:24:16
|
相似题推荐
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】将铁粉和铜粉的均匀混合物,平均分成四等份,分别加入同浓度的稀硝酸,充分反应,在标准状况下生成NO 的体积和剩余金属的质量如下表(假设硝酸的还原产物只有NO):
试通过计算填空:
(1)硝酸的物质的量浓度为____________________ 。
(2)②中溶解了_______________ g Fe。
(3)③中溶解了_______________ g Cu。
(4)④中V=_______________ L.
| 编号 | ① | ② | ③ | ④ |
| 稀硝酸的体积/mL | 100 | 200 | 300 | 400 |
| 剩余金属的质量/g | 18.0 | 9.6 | 0 | 0 |
| NO 的体积/mL | 2240 | 4480 | 6720 | V |
(1)硝酸的物质的量浓度为
(2)②中溶解了
(3)③中溶解了
(4)④中V=
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】工业上由含铜废料(含有 、
、 、
、 等)制备硝酸铜晶体的流程如下:
等)制备硝酸铜晶体的流程如下:
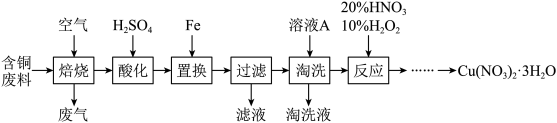
(1)“焙烧”在600℃时进行,写出 转化为
转化为 和
和 的化学方程式:
的化学方程式:________ 。
(2)“淘洗”所用的溶液A可以是________(填字母)。
(3)“反应”这一步所用 试剂是 和
和 ,反应过程中无气体生成,该反应的化学方程式:
,反应过程中无气体生成,该反应的化学方程式:________ 。
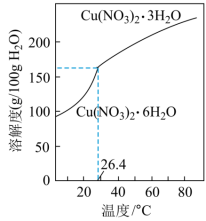
(4)根据题图分析从“反应”所得溶液中析出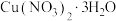 的方法是
的方法是________ 。
 、
、 、
、 等)制备硝酸铜晶体的流程如下:
等)制备硝酸铜晶体的流程如下:
(1)“焙烧”在600℃时进行,写出
 转化为
转化为 和
和 的化学方程式:
的化学方程式:(2)“淘洗”所用的溶液A可以是________(填字母)。
| A.稀硫酸 | B.浓硫酸 | C.稀硝酸 | D.浓硝酸 |
(3)“反应”这一步所用 试剂是
 和
和 ,反应过程中无气体生成,该反应的化学方程式:
,反应过程中无气体生成,该反应的化学方程式:(4)根据题图分析从“反应”所得溶液中析出
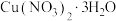 的方法是
的方法是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
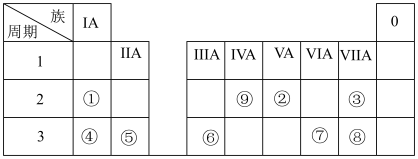
【推荐3】门捷列夫是俄国科学家,他发明的元素周期表是化学领域的重要里程碑。周期表的发明帮助人们更好地理解元素性质和变化规律。门捷列夫被誉为“现代化学之父”。_______ ,⑨最简单的气态氢化物的结构式为_______ 。
(2)写出④的最高价氧化物对应水化物和⑧的最高价氧化物对应水化物相互反应的化学方程式_______ 。
(3)③、④两种元素的简单离子半径大小关系_______ (填离子符号)。
(4)④、⑤和⑥中;金属性最强的元素是_______ (填元素符号);③和⑧两种元素形成的气态氢化物中,热稳定性强的是_______ (填化学式)。
(5)⑦、⑧中,非金属强的元素是_______ (填元素符号),请写出证明这一事实的化学方程式_______ 。
(6)②的最高价氧化物对应水化物的浓溶液与金属铜反应的化学方程式为_____ 。常温下,该浓溶液与金属铁、铝发生_____ 现象,体现该浓溶液的_______ 性。
(2)写出④的最高价氧化物对应水化物和⑧的最高价氧化物对应水化物相互反应的化学方程式
(3)③、④两种元素的简单离子半径大小关系
(4)④、⑤和⑥中;金属性最强的元素是
(5)⑦、⑧中,非金属强的元素是
(6)②的最高价氧化物对应水化物的浓溶液与金属铜反应的化学方程式为
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐1】粘合剂M的合成路线如下图所示:
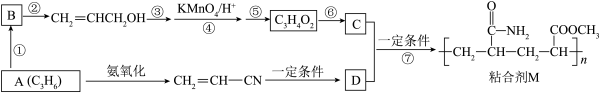
完成下列填空:
(1)写出A和B的结构简式:A______________ ;B__________ ;
(2)写出反应类型:反应⑥________________ ;反应⑦__________________ ;
(3)写出反应条件:反应②_____________ ;反应⑤____________ ;
(4)反应③和⑤的目的是________________________ ;
(5)C的具有相同官能团的同分异构体共有_________ (不含C);
(6)写出D在碱性条件下水的反应方程式______________ 。

完成下列填空:
(1)写出A和B的结构简式:A
(2)写出反应类型:反应⑥
(3)写出反应条件:反应②
(4)反应③和⑤的目的是
(5)C的具有相同官能团的同分异构体共有
(6)写出D在碱性条件下水的反应方程式
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
名校
解题方法
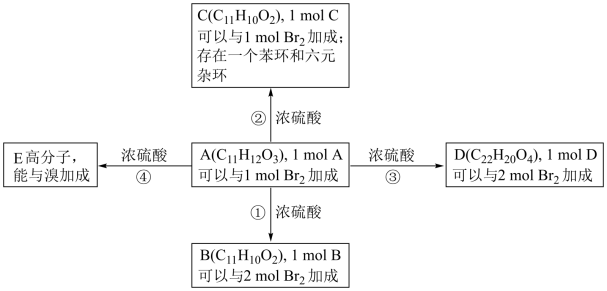
【推荐2】已知A在铜催化下被氧化的生成物不能发生银镜反应。有关A的转化关系如下:
(1)属于酯类的化合物是___________ (填代号)。
(2)①的反应类型是___________ ,理由是___________________________ 。
(3)已知A中的苯环只有一个取代基,A的结构式为___________ 。
(1)属于酯类的化合物是
(2)①的反应类型是
(3)已知A中的苯环只有一个取代基,A的结构式为
您最近一年使用:0次
解答题-有机推断题
|
较难
(0.4)
解题方法
【推荐3】某课题组以甲苯为主要原料,采用以下路线合成镇静催眠药物——苯巴比妥:
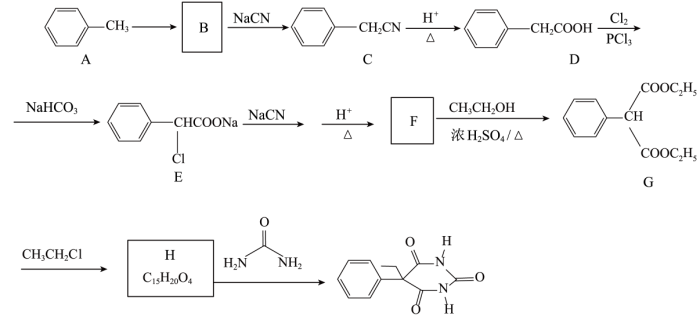
已知: 。回答下列问题:
。回答下列问题:
(1)写出H的结构简式______________________ 。H→苯巴比妥的反应类型_________________ 。
(2)写出F→G的化学方程式________________________________ 。
(3)下列说法正确的是__________ 。
a.B的核磁共振氢谱有5组峰
b.化合物E能发生取代,氧化、加成、消去等反应
c.尿素在一定条件下可水解生成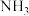 和
和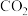
d.苯巴比妥的分子式为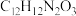
(4)F制备G时会生成副产物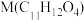 ,写出符合下列条件的M的同分异构体的结构简式:
,写出符合下列条件的M的同分异构体的结构简式: ___________________ 。
①除苯环外不含其它环状结构。且苯环上有3个取代基;
②核磁共振氢谱图显示有5种化学环境不同的氢原子;
③该物质可发生银镜反应与水解反应,且1mol该物质完全水解时需要2molNaOH。
(5)以乙醇为原料可合成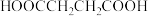 ,请设计合成路线(用流程图表示,无机试剂任选)。
,请设计合成路线(用流程图表示,无机试剂任选)。___________

已知:
 。回答下列问题:
。回答下列问题:(1)写出H的结构简式
(2)写出F→G的化学方程式
(3)下列说法正确的是
a.B的核磁共振氢谱有5组峰
b.化合物E能发生取代,氧化、加成、消去等反应
c.尿素在一定条件下可水解生成
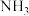 和
和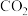
d.苯巴比妥的分子式为
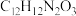
(4)F制备G时会生成副产物
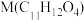 ,写出符合下列条件的M的同分异构体的结构简式:
,写出符合下列条件的M的同分异构体的结构简式: ①除苯环外不含其它环状结构。且苯环上有3个取代基;
②核磁共振氢谱图显示有5种化学环境不同的氢原子;
③该物质可发生银镜反应与水解反应,且1mol该物质完全水解时需要2molNaOH。
(5)以乙醇为原料可合成
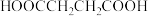 ,请设计合成路线(用流程图表示,无机试剂任选)。
,请设计合成路线(用流程图表示,无机试剂任选)。
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐1】某课外小组设计的实验室制取并提纯乙酸乙酯的方案如下所示
已知:①氯化钙可与乙醇形成CaCl2・6C2H5OH;
②有关有机物的沸点如下表所示
③2CH3CH2OH CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2O
I.制备过程:装置如图所示,A中盛有浓硫酸,B中盛有9.5mL无水乙醇和6mL冰醋酸,D中盛有饱和碳酸钠溶液。
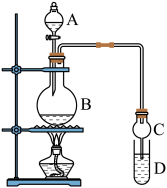
(1)实验过程中滴加大约3mL浓硫酸,B的容积最合适的是_____ (填字母代号)
A. 25 mL B 50 mL C. 250 mL D. 500 mL
(2)球形干燥管的主要作用是_______________ 。
(3)饱和碳酸钠溶液的作用是______ (填字母代号)。
A.消耗乙酸并溶解乙醇
B.碳酸钠溶液呈碱性,有利于乙酸乙酯的水解
C.加速乙酸乙酯的生成,提高其产率
D.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中的更小,有利于分层析出
II.提纯方法:
①将D中混合液进行分离。
②有机层用5mL饱和食盐水洗涤,再用5mL饱和氯化钙溶液洗涤,最后用水洗涤。有机层倒入一干燥的烧瓶中,选用合适的干燥剂干燥,得到粗产品。
③将粗产品蒸馏,收集77.1℃时的馏分,得到纯净、干燥的乙酸乙酯。
(4)第①步分离混合液时,选用的主要玻璃仪器的名称是_____________ 。
(5)第②步中用饱和食盐水洗去碳酸钠后,再用饱和氯化钙溶液洗涤,主要洗去粗产品中的______ (填物质名称)。再加入_______ (此空从下列选项中选择,四种物质均有吸水性)干燥
A.浓硫酸 B.碱石灰 C.无水硫酸钠 D.生石灰
(6)加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,一个可能的原因是_____________________________________________ 。
(7)若实验所用乙酸的质量为2.4g,乙醇的质量为2.1g,得到纯净的产品的质量为2.64g,则乙酸乙酯的产率是___________________ 。
已知:①氯化钙可与乙醇形成CaCl2・6C2H5OH;
②有关有机物的沸点如下表所示
| 试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
| 沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
 CH3CH2OCH2CH3+H2O
CH3CH2OCH2CH3+H2OI.制备过程:装置如图所示,A中盛有浓硫酸,B中盛有9.5mL无水乙醇和6mL冰醋酸,D中盛有饱和碳酸钠溶液。

(1)实验过程中滴加大约3mL浓硫酸,B的容积最合适的是
A. 25 mL B 50 mL C. 250 mL D. 500 mL
(2)球形干燥管的主要作用是
(3)饱和碳酸钠溶液的作用是
A.消耗乙酸并溶解乙醇
B.碳酸钠溶液呈碱性,有利于乙酸乙酯的水解
C.加速乙酸乙酯的生成,提高其产率
D.乙酸乙酯在饱和碳酸钠溶液中的溶解度比在水中的更小,有利于分层析出
II.提纯方法:
①将D中混合液进行分离。
②有机层用5mL饱和食盐水洗涤,再用5mL饱和氯化钙溶液洗涤,最后用水洗涤。有机层倒入一干燥的烧瓶中,选用合适的干燥剂干燥,得到粗产品。
③将粗产品蒸馏,收集77.1℃时的馏分,得到纯净、干燥的乙酸乙酯。
(4)第①步分离混合液时,选用的主要玻璃仪器的名称是
(5)第②步中用饱和食盐水洗去碳酸钠后,再用饱和氯化钙溶液洗涤,主要洗去粗产品中的
A.浓硫酸 B.碱石灰 C.无水硫酸钠 D.生石灰
(6)加热有利于提高乙酸乙酯的产率,但实验发现温度过高乙酸乙酯的产率反而降低,一个可能的原因是
(7)若实验所用乙酸的质量为2.4g,乙醇的质量为2.1g,得到纯净的产品的质量为2.64g,则乙酸乙酯的产率是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐2】苯甲酸乙酯( )的别名为安息香酸乙酯。它是一种无色透明液体,不溶于水,有芳香气味,用于配制香水、香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为:
)的别名为安息香酸乙酯。它是一种无色透明液体,不溶于水,有芳香气味,用于配制香水、香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为:
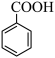 +CH3CH2OH
+CH3CH2OH
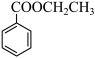 +H2O
+H2O
已知:苯甲酸在100℃会迅速升华。相关有机物的性质如表所示。
实验步骤如下:
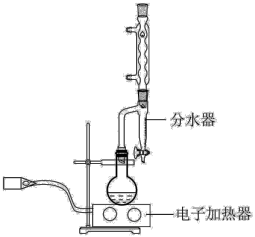
①在圆底烧瓶中加入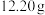 苯甲酸,
苯甲酸, 乙醇(过量),20mL环己烷以及4mL浓硫酸,混合均匀并加入沸石,按如图所示装置装好仪器,控制温度在65~70℃加热回流2h。利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
乙醇(过量),20mL环己烷以及4mL浓硫酸,混合均匀并加入沸石,按如图所示装置装好仪器,控制温度在65~70℃加热回流2h。利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
②反应结束,打开旋塞放出分水器中的液体后,关闭旋塞继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入 至溶液呈中性。用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,对滤液进行蒸馏,低温蒸出乙醚和环己烷后,继续升温,接收210~213℃的馏分。
至溶液呈中性。用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,对滤液进行蒸馏,低温蒸出乙醚和环己烷后,继续升温,接收210~213℃的馏分。
④检验合格,测得产品体积为 。
。
回答下列问题:
(1)在该实验中,圆底烧瓶的容积最适合的是________ (填序号)。
A.25mL B.50mL C.100mL D.250mL
(2)步骤①中使用分水器不断分离除去水的目的是______________ 。
(3)步骤②中应控制加热蒸馏的温度为________ (填序号)。
A.65~70℃ B.78~80℃ C.85~90℃ D.215~220℃
(4)步骤③加入 的作用是
的作用是________________________________ ;若 的加入量不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是
的加入量不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是__________________ 。
(5)关于步骤③中的萃取分液操作的叙述正确的是________ (填序号)。
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞,分液漏斗倒转过来,用力振摇
B.振摇几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.放出液体时,应打开上口玻璃塞或将玻璃塞上的凹槽对准漏斗口上的小孔
(6)计算可得本实验的产率为________ 。
 )的别名为安息香酸乙酯。它是一种无色透明液体,不溶于水,有芳香气味,用于配制香水、香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为:
)的别名为安息香酸乙酯。它是一种无色透明液体,不溶于水,有芳香气味,用于配制香水、香精和人造精油,大量用于食品工业中,也可用作有机合成中间体、溶剂等。其制备方法为: +CH3CH2OH
+CH3CH2OH
 +H2O
+H2O 已知:苯甲酸在100℃会迅速升华。相关有机物的性质如表所示。
| 名称 | 相对分子质量 | 颜色及状态 | 沸点/℃ | 密度/( ) ) |
| 苯甲酸 | 122 | 无色鳞片状或针状晶体 | 249 | 1.2659 |
| 苯甲酸乙酯 | 150 | 无色澄清液体 | 212.6 | 1.05 |
| 乙醇 | 46 | 无色澄清液体 | 78.3 | 0.7893 |
| 环己烷 | 84 | 无色澄清液体 | 80.7 | 0.78 |

①在圆底烧瓶中加入
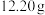 苯甲酸,
苯甲酸, 乙醇(过量),20mL环己烷以及4mL浓硫酸,混合均匀并加入沸石,按如图所示装置装好仪器,控制温度在65~70℃加热回流2h。利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。
乙醇(过量),20mL环己烷以及4mL浓硫酸,混合均匀并加入沸石,按如图所示装置装好仪器,控制温度在65~70℃加热回流2h。利用分水器不断分离除去反应生成的水,回流环己烷和乙醇。②反应结束,打开旋塞放出分水器中的液体后,关闭旋塞继续加热,至分水器中收集到的液体不再明显增加,停止加热。
③将烧瓶内反应液倒入盛有适量水的烧杯中,分批加入
 至溶液呈中性。用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,对滤液进行蒸馏,低温蒸出乙醚和环己烷后,继续升温,接收210~213℃的馏分。
至溶液呈中性。用分液漏斗分出有机层,水层用25mL乙醚萃取分液,然后合并至有机层,加入氯化钙,静置,过滤,对滤液进行蒸馏,低温蒸出乙醚和环己烷后,继续升温,接收210~213℃的馏分。④检验合格,测得产品体积为
 。
。回答下列问题:
(1)在该实验中,圆底烧瓶的容积最适合的是
A.25mL B.50mL C.100mL D.250mL
(2)步骤①中使用分水器不断分离除去水的目的是
(3)步骤②中应控制加热蒸馏的温度为
A.65~70℃ B.78~80℃ C.85~90℃ D.215~220℃
(4)步骤③加入
 的作用是
的作用是 的加入量不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是
的加入量不足,在之后蒸馏时,蒸馏烧瓶中可见到白烟生成,产生该现象的原因是(5)关于步骤③中的萃取分液操作的叙述正确的是
A.水溶液中加入乙醚,转移至分液漏斗中,塞上玻璃塞,分液漏斗倒转过来,用力振摇
B.振摇几次后需打开分液漏斗上口的玻璃塞放气
C.经几次振摇并放气后,手持分液漏斗静置待液体分层
D.放出液体时,应打开上口玻璃塞或将玻璃塞上的凹槽对准漏斗口上的小孔
(6)计算可得本实验的产率为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】“酒是陈的香”,是因为酒在储存过程中生成了有香味的乙酸乙酯。在实验室我们可以用如图所示的装置来制取乙酸乙酯。回答下列问题:
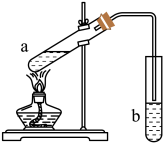
(1)写出试管a中发生的化学方程式:_____________________________________ ;
(2)试管b中的导管要在液面的稍上方,不能插入液面以下,其目的是________________ ;
(3)浓硫酸的作用为___________________________________________________ ;
(4)试管b中所盛的溶液为________________ ,其主要作用是 _________________________ 。
(5)分离乙酸乙酯、乙醇、乙酸的混合物,可按下列步骤进行:
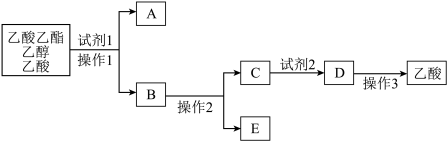
①试剂1最好选用_________________ ,
②操作1是________________ ,所用的主要仪器名称是_______________ ;
③操作2是_____________ ,试剂2最好选用_______________ ,操作3是__________ 。

(1)写出试管a中发生的化学方程式:
(2)试管b中的导管要在液面的稍上方,不能插入液面以下,其目的是
(3)浓硫酸的作用为
(4)试管b中所盛的溶液为
(5)分离乙酸乙酯、乙醇、乙酸的混合物,可按下列步骤进行:

①试剂1最好选用
②操作1是
③操作2是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
解题方法
【推荐1】为测定 溶液的浓度,甲、乙两同学设计了两个方案。完成下列填空:
溶液的浓度,甲、乙两同学设计了两个方案。完成下列填空:
I.甲方案
实验原理: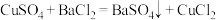
实验步骤:

已知: 受热不分解。
受热不分解。
(1)证明上述流程中灼烧后称量的质量已达恒重的依据是___________ 。
(2)步骤①的操作名称是___________ ,步骤③灼烧时盛装样品的仪器名称是___________ 。根据固体 求得
求得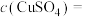
___________  。
。
II.乙方案
实验原理: ,
,
实验步骤:
①按图安装装置(夹持仪器略去);
②……
③在仪器A、B、C、D、E中加入图示的试剂;
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录;
⑤将 溶液滴入A中并搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生;
溶液滴入A中并搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生;
⑥将体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录,
⑦处理数据。
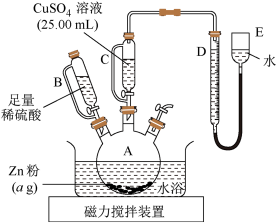
(3)步骤②的操作为___________ 。步骤⑥需保证体系恢复到室温的原因是___________ (填序号)。
a.反应热受温度影响 b.气体密度受温度影响 c.反应速率受温度影响
(4) 粉质量为
粉质量为 ,若测得
,若测得 的体积为
的体积为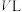 (标准状况下),则
(标准状况下),则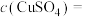
___________  (列出计算表达式,不用化简)。
(列出计算表达式,不用化简)。
(5)①若步骤⑥E管液面高于D管,未调液面即读数,则测得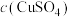
___________ (填“偏高”“偏低”或“无影响”)。
②若将恒压分液漏斗(B),改成普通分液漏斗,则测得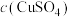
___________ (填“偏高”“偏低”或“无影响”)。
 溶液的浓度,甲、乙两同学设计了两个方案。完成下列填空:
溶液的浓度,甲、乙两同学设计了两个方案。完成下列填空:I.甲方案
实验原理:
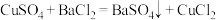
实验步骤:

已知:
 受热不分解。
受热不分解。(1)证明上述流程中灼烧后称量的质量已达恒重的依据是
(2)步骤①的操作名称是
 求得
求得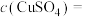
 。
。II.乙方案
实验原理:
 ,
,
实验步骤:
①按图安装装置(夹持仪器略去);
②……
③在仪器A、B、C、D、E中加入图示的试剂;
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录;
⑤将
 溶液滴入A中并搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生;
溶液滴入A中并搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生;⑥将体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录,
⑦处理数据。

(3)步骤②的操作为
a.反应热受温度影响 b.气体密度受温度影响 c.反应速率受温度影响
(4)
 粉质量为
粉质量为 ,若测得
,若测得 的体积为
的体积为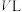 (标准状况下),则
(标准状况下),则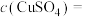
 (列出计算表达式,不用化简)。
(列出计算表达式,不用化简)。(5)①若步骤⑥E管液面高于D管,未调液面即读数,则测得
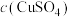
②若将恒压分液漏斗(B),改成普通分液漏斗,则测得
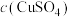
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐2】微型实验具有设计简单、节约药品等优点,某化学活动小组利用所学知识设计氯气制备和性质实验如下。回答下列问题:
I.氯气的制备:
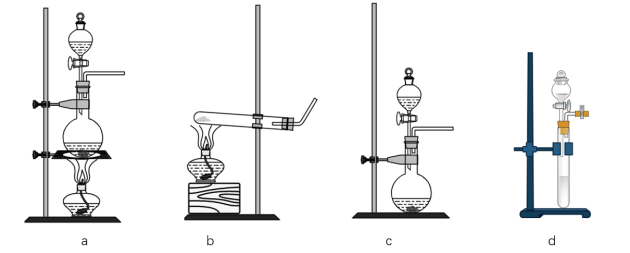
(1)若实验室用2KMn04+16HCl(浓)=2KCl+2MnCl2+5Cl+8H2O制取少量氯气,则反应的最佳装置应选用下图中____________ 。
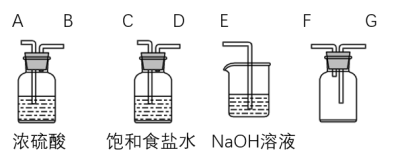
(2)利用下图装置收集纯净的氯气,其连接顺序为:发生装置
________ (按气流方向,用字母表示)。
(3)A、B两组同学分别用两种方法制取氯气,A组用含146g HCl的浓盐酸与足量的二氧化锰反应;B组用87g二氧化锰与足量的浓盐酸反应,则所得氯气的物质的量的关系为A______ B(填“>”、“<”或“=”)
Ⅱ.氯气微型实验:
(1)根据图示,完成下表
(2)仔细观察上述装置,利用该套装置_____ (填“能”或“不能”)证明溴单质的氧化性大于碘,若能应如何操作(若不能请解释为什么?)_________ 。
I.氯气的制备:
(1)若实验室用2KMn04+16HCl(浓)=2KCl+2MnCl2+5Cl+8H2O制取少量氯气,则反应的最佳装置应选用下图中
(2)利用下图装置收集纯净的氯气,其连接顺序为:发生装置

(3)A、B两组同学分别用两种方法制取氯气,A组用含146g HCl的浓盐酸与足量的二氧化锰反应;B组用87g二氧化锰与足量的浓盐酸反应,则所得氯气的物质的量的关系为A
Ⅱ.氯气微型实验:
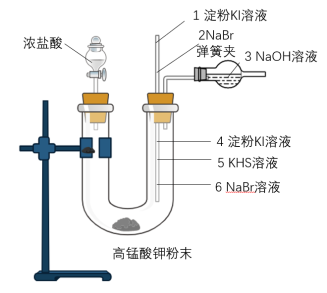
(1)根据图示,完成下表
| 位置 | 实验现象 | 解释原因 |
| 6 | 溶液变黄色 | 反应的离子方程式 |
| 5 | Cl2+HS-=2Cl-+S↓+H+ | |
| 4 | 氯气的氧化性大于碘单质 |
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐3】某实验小组探究少量Cl2和FeBr2反应的过程。
(1)配制FeBr2溶液:
ⅰ.配制50mL1.0mol/LFeBr2溶液;
ⅱ.上述溶液呈淡黄色。取少量此溶液,向其中滴入KSCN溶液,变为浅红色。
①配制50mL1.0mol/LFeBr2溶液需要的玻璃容器是________________ 。
②由ⅱ可知,此FeBr2溶液呈黄色的原因是其中含有________ ,用离子方程式解释产生其原因:_______ 。
(2)氯气和FeBr2反应实验操作及现象如下:
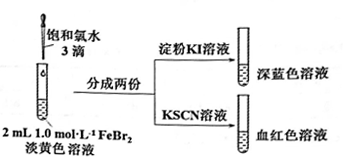
据此甲同学得出结论:少量Cl2既能和Fe2+又能和Br-发生氧化还原反应。
①Cl2和Fe2+发生反应的离子方程式是________________ 。
②乙同学认为上述实验不能证明Cl2和Br-发生反应,理由是_____________ 。
③乙同学改进实验如下:在上述FeBr2溶液中加入过量铁粉,取上清液2 mL,向其中滴加3滴饱和氯水后,再加入CCl4,振荡后静置,观察现象。乙得出结论:少量Cl2只与Fe2+反应,不与Br-反应。乙得出该结论依据的实验现象是____________________ 。
(3)丙同学继续设计实验,探究反应过程:
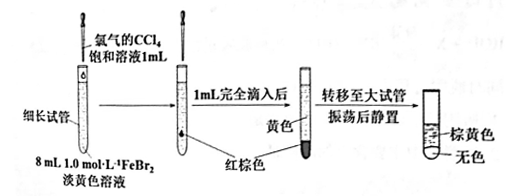
①转移到大试管前CCl4液体中呈红棕色的物质是___________ 。
②丙通过此实验可得出结论:________ 。
(1)配制FeBr2溶液:
ⅰ.配制50mL1.0mol/LFeBr2溶液;
ⅱ.上述溶液呈淡黄色。取少量此溶液,向其中滴入KSCN溶液,变为浅红色。
①配制50mL1.0mol/LFeBr2溶液需要的玻璃容器是
②由ⅱ可知,此FeBr2溶液呈黄色的原因是其中含有
(2)氯气和FeBr2反应实验操作及现象如下:

据此甲同学得出结论:少量Cl2既能和Fe2+又能和Br-发生氧化还原反应。
①Cl2和Fe2+发生反应的离子方程式是
②乙同学认为上述实验不能证明Cl2和Br-发生反应,理由是
③乙同学改进实验如下:在上述FeBr2溶液中加入过量铁粉,取上清液2 mL,向其中滴加3滴饱和氯水后,再加入CCl4,振荡后静置,观察现象。乙得出结论:少量Cl2只与Fe2+反应,不与Br-反应。乙得出该结论依据的实验现象是
(3)丙同学继续设计实验,探究反应过程:

①转移到大试管前CCl4液体中呈红棕色的物质是
②丙通过此实验可得出结论:
您最近一年使用:0次



