对于热化学方程式:SO3(g)⇌SO2(g)+1/2O2(g) △H= +98.3kJ•mol-1的描述有如下四个图象,其中正确的是(y表示SO2的含量)( )
A.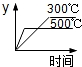 | B.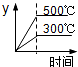 | C.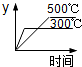 | D.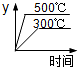 |
更新时间:2017-07-29 14:23:52
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】亚硝酰氯(NOCl)是有机合成中的重要试剂,工业上可由NO与Cl2反应制得,
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
反应I:2NO2(g)+NaCl(s) NaNO3(s)+NOCl(g)ΔH1;
NaNO3(s)+NOCl(g)ΔH1;
反应II:4NO2(g)+2NaCl(s) 2NaNO3(s)+2NO(g)+Cl2(g)ΔH2;
2NaNO3(s)+2NO(g)+Cl2(g)ΔH2;
反应III:2NO(g)+Cl2(g) 2NOCl(g)ΔH3;
2NOCl(g)ΔH3;
(2)保持恒温恒容条件,将物质的量之和为3mol的NO和Cl2以不同的氮氯比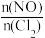 进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
(1)氮氧化物与悬浮在大气中的海盐粒子相互作用时会生成亚硝酰氯,涉及如下反应:
反应I:2NO2(g)+NaCl(s)
 NaNO3(s)+NOCl(g)ΔH1;
NaNO3(s)+NOCl(g)ΔH1;反应II:4NO2(g)+2NaCl(s)
 2NaNO3(s)+2NO(g)+Cl2(g)ΔH2;
2NaNO3(s)+2NO(g)+Cl2(g)ΔH2;反应III:2NO(g)+Cl2(g)
 2NOCl(g)ΔH3;
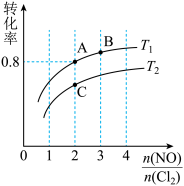
2NOCl(g)ΔH3;(2)保持恒温恒容条件,将物质的量之和为3mol的NO和Cl2以不同的氮氯比
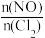 进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
进行反应,平衡时某反应物的转化率与氮氯比及不同温度的关系如图所示:
| A.上述反应焓变关系ΔH3=ΔH1-ΔH2 |
| B.图中纵坐标为物质氯气的转化率 |
| C.图中A、B、C三点对应的NOCl体积分数最大的是B |
| D.若容器容积为1L,经过10min到达A点,该时间段内反应速率v(NO)=0.08mol/(L·min) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列事实能用勒夏特列原理来解释的是(方程式中条件均省略)
A. 氧化成 氧化成 ,需要使用催化剂 ,需要使用催化剂 |
B. 左右的温度比室温更有利于合成氨反应 左右的温度比室温更有利于合成氨反应 |
C.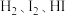 平衡混合气体加压后颜色加深 平衡混合气体加压后颜色加深 |
| D.加热氯化铜溶液,溶液颜色变为蓝绿色 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】可逆反应:L(s)+aG(g) bR(g) ΔH达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.下列判断正确的是
bR(g) ΔH达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.下列判断正确的是

 bR(g) ΔH达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.下列判断正确的是
bR(g) ΔH达到平衡时,温度和压强对该反应的影响如图所示:图中压强p1>p2,x轴表示温度,y轴表示平衡混合气中G的体积分数.下列判断正确的是
| A.ΔH<0 |
| B.增加L的物质的量,可提高G的转化率 |
| C.升高温度,G的转化率减小 |
| D.a<b |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】反应
 ,在温度为
,在温度为 、
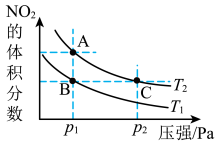
、 时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是

 ,在温度为
,在温度为 、
、 时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是
| A.A、C两点的反应速率:A>C |
| B.A、C两点气体的颜色:A深,C浅 |
C. |
| D.B、C两点气体的平均相对分子质量:B=C |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】下列叙述与图对应的是
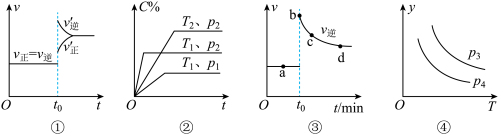

A.对于达到平衡状态的反应:N2(g)+3H2(g) 2NH3(g),图①表示在t0时刻充入了一定量的NH3,平衡逆向移动 2NH3(g),图①表示在t0时刻充入了一定量的NH3,平衡逆向移动 |
B.由图②可知,p2>p1、T1>T2满足反应:2A(g)+B(g) 2C(g) ΔH<0 2C(g) ΔH<0 |
C.图③为只改变某一条件,化学反应aA(g)+B(g) cC(g)的平衡变化图像,则图像中b、c、d三点对应的正反应速率最大的是b点 cC(g)的平衡变化图像,则图像中b、c、d三点对应的正反应速率最大的是b点 |
D.对于反应2X(g)+3Y(g) 2Z(g) ΔH<0,图④ 2Z(g) ΔH<0,图④ 轴可以表示Y的百分含量 轴可以表示Y的百分含量 |
您最近一年使用:0次

 2SO3(g)
2SO3(g)

