二氧化锆(ZrO2)是最重要的氧离子固体电解质,用于制造燃料电池、氧气含量测定仪等。可由锆英砂(主要成分为ZrSiO4,也可表示为ZrO2·SiO2;含有少量Fe2O3、Al2O3、SiO2杂质)通过如下工艺流程法制得。
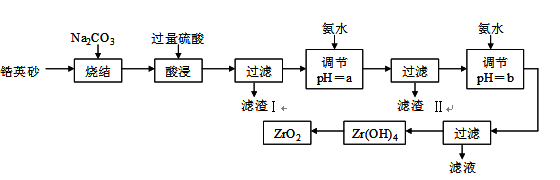
已知:①ZrO2具有两性,高温与纯碱共熔生成可溶于水的Na2ZrO3,与酸反应生成ZrO2+。②部分金属离子开始沉淀和完全沉淀的pH如下表:
请回答下列问题:
⑴烧结时ZrSiO4发生反应的化学方程式为_______________________ ;
滤渣I的化学式为______________________________ 。
⑵调节pH=a 的目的是________________________________________ ;用氨水调节pH=b后发生反应的离子方程式为______________________________________________ 。
⑶以滤渣II为主要原料制取铁红,请简述实验方法________________________ 。
⑷工业上用铝热法冶炼锆,写出以ZrO2通过铝热法制取锆的化学方程式:
________________________________________________________ 。
⑸一种新型燃料电池用掺杂Y2O3的ZrO2晶体作电解质在熔融状态下传导O2-,一极通入空气,另一极通入甲烷,写出负极的电极反应式为___________________________ 。

已知:①ZrO2具有两性,高温与纯碱共熔生成可溶于水的Na2ZrO3,与酸反应生成ZrO2+。②部分金属离子开始沉淀和完全沉淀的pH如下表:
| 金属离子 | Fe3+ | Al3+ | ZrO2+ |
| 开始沉淀的pH | 1.9 | 3.3 | 6.2 |
| 沉淀完全的pH | 3.2 | 5.2 | 8.0 |
请回答下列问题:
⑴烧结时ZrSiO4发生反应的化学方程式为
滤渣I的化学式为
⑵调节pH=a 的目的是
⑶以滤渣II为主要原料制取铁红,请简述实验方法
⑷工业上用铝热法冶炼锆,写出以ZrO2通过铝热法制取锆的化学方程式:
⑸一种新型燃料电池用掺杂Y2O3的ZrO2晶体作电解质在熔融状态下传导O2-,一极通入空气,另一极通入甲烷,写出负极的电极反应式为
更新时间:2017-09-05 21:32:09
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】氯可形成多种含氧酸盐,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
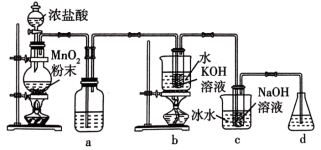
请回答下列问题:
(1)盛放浓盐酸的仪器名称是___________ ,a的作用为___________ 。
(2)b中采用的加热方式的优点为___________ ,b中反应的化学方程式为___________ 。
(3)c中采用冰水浴冷却的目的是___________ 。
(4)d中可选用试剂___________ (填标号)。
A. B.NaCl C.
B.NaCl C. D.
D.
(5)反应结束后,取出b中试管,经冷却结晶,___________ ,洗涤,干燥,得到 晶体。
晶体。
(6)取少量 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显
层显___________ 色。可知该条件下NaClO的氧化能力___________  (填“大于”或“小于”)。
(填“大于”或“小于”)。
 和NaClO,探究其氧化还原性质。
和NaClO,探究其氧化还原性质。
请回答下列问题:
(1)盛放浓盐酸的仪器名称是
(2)b中采用的加热方式的优点为
(3)c中采用冰水浴冷却的目的是
(4)d中可选用试剂
A.
 B.NaCl C.
B.NaCl C. D.
D.
(5)反应结束后,取出b中试管,经冷却结晶,
 晶体。
晶体。(6)取少量
 和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入
和NaClO溶液分别置于1号和2号试管中,滴加中性KI溶液。1号试管溶液颜色不变。2号试管溶液变为棕色,加入 振荡,静置后
振荡,静置后 层显
层显 (填“大于”或“小于”)。
(填“大于”或“小于”)。
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】从生产造影剂的含碘废液(含碘有机副产物和无机碘)中回收碘的实验步骤如图。
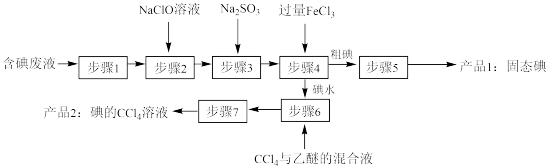
已知:①还原性: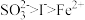 。
。
②含碘有机副产物可表示为R—I(R为有机基团)。
③ 、乙醚的沸点分别为76.8℃、34.5℃,两者可混溶。
、乙醚的沸点分别为76.8℃、34.5℃,两者可混溶。
回答下列问题:
(1)“步骤1”为检验废液中无机碘的成分,下列判断正确的是______ (填标号)。
A.向废液中加入过量 ,充分反应后加入淀粉溶液,溶液不变蓝,说明不含
,充分反应后加入淀粉溶液,溶液不变蓝,说明不含
B.向废液中加入淀粉溶液、无明显现象,再加入 溶液,溶液变蓝,说明含有
溶液,溶液变蓝,说明含有
C.废液中可能大量共存的一组离子是
(2)“步骤2”中 溶液的作用是
溶液的作用是______ ;“步骤3”的目的是______ 。
(3)“步骤4”中发生反应的离子方程式为______ 。
(4)“步骤5”为升华法精制粗碘,实验装置如图,水应从接口______ (填“a”或“b”)处通入,向含 的粗碘中加入适量
的粗碘中加入适量 可避免产品中含有
可避免产品中含有 ,这是因为
,这是因为______ (用化学方程式表示)。

(5)“步骤6”采用四氯化碳和乙醚的混合溶液萃取碘时,不同体积比萃取效果如下表所示:
选用表中的 为
为______ (填标号)时最适合,理由是______ 。
(6)“步骤7”的操作名称是______ 。

已知:①还原性:
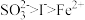 。
。②含碘有机副产物可表示为R—I(R为有机基团)。
③
 、乙醚的沸点分别为76.8℃、34.5℃,两者可混溶。
、乙醚的沸点分别为76.8℃、34.5℃,两者可混溶。回答下列问题:
(1)“步骤1”为检验废液中无机碘的成分,下列判断正确的是
A.向废液中加入过量
 ,充分反应后加入淀粉溶液,溶液不变蓝,说明不含
,充分反应后加入淀粉溶液,溶液不变蓝,说明不含
B.向废液中加入淀粉溶液、无明显现象,再加入
 溶液,溶液变蓝,说明含有
溶液,溶液变蓝,说明含有
C.废液中可能大量共存的一组离子是

(2)“步骤2”中
 溶液的作用是
溶液的作用是(3)“步骤4”中发生反应的离子方程式为
(4)“步骤5”为升华法精制粗碘,实验装置如图,水应从接口
 的粗碘中加入适量
的粗碘中加入适量 可避免产品中含有
可避免产品中含有 ,这是因为
,这是因为
(5)“步骤6”采用四氯化碳和乙醚的混合溶液萃取碘时,不同体积比萃取效果如下表所示:
| 编号 |  | 萃取1次( ) ) | 萃取2次( ) ) | 萃取3次( ) ) |
| A | 1:1 | 红 | 红 | 黄红 |
| B | 1:2.5 | 红 | 黄红 | 浅黄红 |
| C | 1:3 | 黄红 | 黄红 | 浅黄红 |
| D | 1:3.5 | 黄红 | 黄红 | 浅黄红 |
| E | 1:4 | 黄红 | 浅黄红 | 浅黄色 |
| F | 1:4.5 | 黄红 | 浅黄红 | 无色 |
 为
为(6)“步骤7”的操作名称是
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】碘及碘化钾是实验室中的常见试剂,含碘废液中碘元素通常以 、
、 、
、 和
和 中的一种或多种形式存在,回收碘具有很好的经济价值。
中的一种或多种形式存在,回收碘具有很好的经济价值。
(1)为检验某实验室酸性废液中是否含 ,现进行如下实验:取少量废液,向其中滴加淀粉溶液,溶液不变蓝。另取少量废液,
,现进行如下实验:取少量废液,向其中滴加淀粉溶液,溶液不变蓝。另取少量废液,_______ ,则溶液中含有 。请补充完整该实验方案,实验中可以选用的试剂有:
。请补充完整该实验方案,实验中可以选用的试剂有: 溶液、
溶液、 溶液、淀粉溶液、KSCN溶液、
溶液、淀粉溶液、KSCN溶液、 溶液。
溶液。
(2)一种由含 的废液制取单质碘的流程如下:
的废液制取单质碘的流程如下: 溶液,再加入
溶液,再加入 至沉淀不再增加。
至沉淀不再增加。
Ⅰ.沉碘时有CuI沉淀和 生成,写出该反应的离子方程式:
生成,写出该反应的离子方程式:_______ 。
Ⅱ.若不加入 溶液,仅加入
溶液,仅加入 也可生成CuI沉淀。沉碘时不是仅加入
也可生成CuI沉淀。沉碘时不是仅加入 的原因是
的原因是_______ 。
②氧化、蒸发的装置如图所示。_______ 。
Ⅱ.蒸发出的碘蒸气冷却后易凝固。实验过程中,若发现玻璃导管中有单质碘凝固析出,为防止堵塞,可以采取的方法是_______ 。
(3)若废液中含有 ,可以用
,可以用 进行萃取,萃取后所得有机层可以用KOH溶液进行反萃取。反萃取后所得水层中的溶质为
进行萃取,萃取后所得有机层可以用KOH溶液进行反萃取。反萃取后所得水层中的溶质为 和KI。请补充完整由反萃取后所得水层制取KI晶体的实验方案:取反萃取后所得水层,
和KI。请补充完整由反萃取后所得水层制取KI晶体的实验方案:取反萃取后所得水层,_______ 。(已知KI易溶于水;氧化性: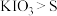 。实验中可以选用的试剂有:
。实验中可以选用的试剂有: 气体、NaOH溶液、稀硫酸)
气体、NaOH溶液、稀硫酸)
(4)某含碘废液中,碘元素以 形式存在,为测定
形式存在,为测定 的浓度,现进行如下实验:准确量取20.00mL废液,加水稀释配成100.00mL溶液,取20.00mL溶液,加入盐酸,加入足量KI晶体,以淀粉为指示剂,用0.1000
的浓度,现进行如下实验:准确量取20.00mL废液,加水稀释配成100.00mL溶液,取20.00mL溶液,加入盐酸,加入足量KI晶体,以淀粉为指示剂,用0.1000
 溶液滴定
溶液滴定 至恰好完全反应,消耗
至恰好完全反应,消耗 溶液24.00mL。已知测定过程中发生的反应为
溶液24.00mL。已知测定过程中发生的反应为 (未配平)
(未配平)  (未配平)
(未配平)
计算废液中 的物质的量浓度,并写出计算过程
的物质的量浓度,并写出计算过程______ 。
 、
、 、
、 和
和 中的一种或多种形式存在,回收碘具有很好的经济价值。
中的一种或多种形式存在,回收碘具有很好的经济价值。(1)为检验某实验室酸性废液中是否含
 ,现进行如下实验:取少量废液,向其中滴加淀粉溶液,溶液不变蓝。另取少量废液,
,现进行如下实验:取少量废液,向其中滴加淀粉溶液,溶液不变蓝。另取少量废液, 。请补充完整该实验方案,实验中可以选用的试剂有:
。请补充完整该实验方案,实验中可以选用的试剂有: 溶液、
溶液、 溶液、淀粉溶液、KSCN溶液、
溶液、淀粉溶液、KSCN溶液、 溶液。
溶液。(2)一种由含
 的废液制取单质碘的流程如下:
的废液制取单质碘的流程如下:
 溶液,再加入
溶液,再加入 至沉淀不再增加。
至沉淀不再增加。Ⅰ.沉碘时有CuI沉淀和
 生成,写出该反应的离子方程式:
生成,写出该反应的离子方程式:Ⅱ.若不加入
 溶液,仅加入
溶液,仅加入 也可生成CuI沉淀。沉碘时不是仅加入
也可生成CuI沉淀。沉碘时不是仅加入 的原因是
的原因是②氧化、蒸发的装置如图所示。
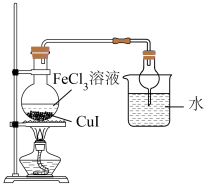
Ⅱ.蒸发出的碘蒸气冷却后易凝固。实验过程中,若发现玻璃导管中有单质碘凝固析出,为防止堵塞,可以采取的方法是
(3)若废液中含有
 ,可以用
,可以用 进行萃取,萃取后所得有机层可以用KOH溶液进行反萃取。反萃取后所得水层中的溶质为
进行萃取,萃取后所得有机层可以用KOH溶液进行反萃取。反萃取后所得水层中的溶质为 和KI。请补充完整由反萃取后所得水层制取KI晶体的实验方案:取反萃取后所得水层,
和KI。请补充完整由反萃取后所得水层制取KI晶体的实验方案:取反萃取后所得水层,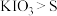 。实验中可以选用的试剂有:
。实验中可以选用的试剂有: 气体、NaOH溶液、稀硫酸)
气体、NaOH溶液、稀硫酸)(4)某含碘废液中,碘元素以
 形式存在,为测定
形式存在,为测定 的浓度,现进行如下实验:准确量取20.00mL废液,加水稀释配成100.00mL溶液,取20.00mL溶液,加入盐酸,加入足量KI晶体,以淀粉为指示剂,用0.1000
的浓度,现进行如下实验:准确量取20.00mL废液,加水稀释配成100.00mL溶液,取20.00mL溶液,加入盐酸,加入足量KI晶体,以淀粉为指示剂,用0.1000
 溶液滴定
溶液滴定 至恰好完全反应,消耗
至恰好完全反应,消耗 溶液24.00mL。已知测定过程中发生的反应为
溶液24.00mL。已知测定过程中发生的反应为 (未配平)
(未配平)  (未配平)
(未配平)计算废液中
 的物质的量浓度,并写出计算过程
的物质的量浓度,并写出计算过程
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】镁的单质及其化合物用途非常广泛。
(1)镁热还原法可制备铷、钛等金属,已知下列物理常数:
在750℃时可实现用镁还原RbCl制Rb,该反应能够发生的原因是_________________________________ (用文字和化学方程式说明)。
(2)无机抗菌剂Mg2ClO(OH)3·H2O(碱式次氯酸镁)可由MgCl2、NaOH及Cl2反应制得,该反应的化学方程式为______________________________________ 。
(3)CaC2冶镁的原理为CaC2(s)+MgO(s) CaO(s)+Mg(g)+2C(s) △H,反应达到平衡时Mg的产率随温度的变化如图所示。
CaO(s)+Mg(g)+2C(s) △H,反应达到平衡时Mg的产率随温度的变化如图所示。
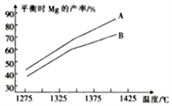
①△H__________ (填“>"或“<”,下同)0。
②已知A、B中固体总质量相等,则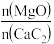 :A
:A__________ B。
(4)Mg(OH)2浆液可脱除烟气中的SO2,其脱硫效率、pH及时间的关系如图所示。
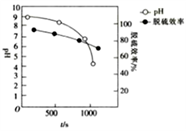
Mg(OH)2浆液脱除SO2的过程中包含的主要反应如下:
Ⅰ.Mg(OH)2+SO2=MgSO3+H2O
Ⅱ.MgSO3+SO2+H2O=Mg(HSO3)2
Ⅲ.Mg(HSO3)2+Mg(OH)2=2MgSO3+2H2O
Ⅳ.2MgSO3+O2=2MgSO4
已知:20℃时,H2SO3的电离平衡常数K1=1.54×10-2、K2=1.02×10-7;25℃时,Ksp[Mg(OH)2]=1.2×10-11,MgSO3,的溶解度为0.646g。
①脱硫过程中使浆液pH减小最显著的反应是__________ (填“Ⅰ”“Ⅱ”“Ⅲ”或“Ⅳ”)。
②约900s之后,脱硫效率明显降低,其原因是________________________ 。
(1)镁热还原法可制备铷、钛等金属,已知下列物理常数:
| Mg | Rb | RbCl | MgCl2 | |
| 熔点/℃ | 648 | 38.89 | 718 | 714 |
| 沸点/℃ | 1107 | 688 | 1390 | 1412 |
(2)无机抗菌剂Mg2ClO(OH)3·H2O(碱式次氯酸镁)可由MgCl2、NaOH及Cl2反应制得,该反应的化学方程式为
(3)CaC2冶镁的原理为CaC2(s)+MgO(s)
 CaO(s)+Mg(g)+2C(s) △H,反应达到平衡时Mg的产率随温度的变化如图所示。
CaO(s)+Mg(g)+2C(s) △H,反应达到平衡时Mg的产率随温度的变化如图所示。
①△H
②已知A、B中固体总质量相等,则
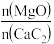 :A
:A(4)Mg(OH)2浆液可脱除烟气中的SO2,其脱硫效率、pH及时间的关系如图所示。

Mg(OH)2浆液脱除SO2的过程中包含的主要反应如下:
Ⅰ.Mg(OH)2+SO2=MgSO3+H2O
Ⅱ.MgSO3+SO2+H2O=Mg(HSO3)2
Ⅲ.Mg(HSO3)2+Mg(OH)2=2MgSO3+2H2O
Ⅳ.2MgSO3+O2=2MgSO4
已知:20℃时,H2SO3的电离平衡常数K1=1.54×10-2、K2=1.02×10-7;25℃时,Ksp[Mg(OH)2]=1.2×10-11,MgSO3,的溶解度为0.646g。
①脱硫过程中使浆液pH减小最显著的反应是
②约900s之后,脱硫效率明显降低,其原因是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】工业合成氨是人类科学技术的一项重大突破,我国目前氨的生产能力位居世界首位。其合成原理为:
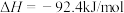
 。
。
(1)合成氨及其衍生工业是化工生产的重要门类,某工厂用下图流程合成氨及其含氮产物:
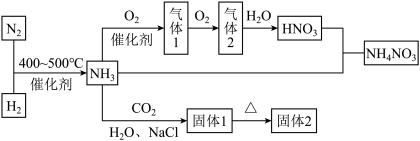
上流程中气体2为___________ ,在饱和 溶液中先通入过量
溶液中先通入过量 再通入过量
再通入过量 可得到固体
可得到固体___________ ;
(2)合成氨反应在常温下___________ (填“能”或“不能”)自发;
(3)在恒温恒容密闭容器中充入
 和
和
 进行合成氨的反应,下列能说明该反应已达平衡状态的是
进行合成氨的反应,下列能说明该反应已达平衡状态的是___________ ;
a.断裂
 同时生成
同时生成

b.容器内压强保持不变
c.混合气体密度保持不变
d。容器内 、
、 、
、 物质的量之比为1:3:2
物质的量之比为1:3:2
e. 的百分含量保持不变
的百分含量保持不变
(4)研究表明,合成氨反应在Fe催化剂上可能通过下图机理进行(*表示催化剂表面吸附位, 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 )。
)。
(ⅰ)
(ⅱ)
(ⅲ)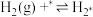
(ⅳ)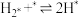
(ⅴ)
……
(…)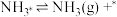
判断上述反应机理中,速率控制步骤(即速率最慢步骤)为___________ (填步骤前的标号),理由是___________ 。
(5)基于 载氮体的碳基化学链合成氨技术示反应如下:
载氮体的碳基化学链合成氨技术示反应如下:
吸氮反应:
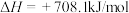
释氮反应:
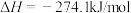
在温度为T、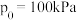 恒压条件下进行吸氮反应,平衡时氮气转化率为50%,分压平衡常数
恒压条件下进行吸氮反应,平衡时氮气转化率为50%,分压平衡常数
___________  。
。

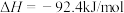
 。
。(1)合成氨及其衍生工业是化工生产的重要门类,某工厂用下图流程合成氨及其含氮产物:

上流程中气体2为
 溶液中先通入过量
溶液中先通入过量 再通入过量
再通入过量 可得到固体
可得到固体(2)合成氨反应在常温下
(3)在恒温恒容密闭容器中充入

 和
和
 进行合成氨的反应,下列能说明该反应已达平衡状态的是
进行合成氨的反应,下列能说明该反应已达平衡状态的是a.断裂

 同时生成
同时生成

b.容器内压强保持不变
c.混合气体密度保持不变
d。容器内
 、
、 、
、 物质的量之比为1:3:2
物质的量之比为1:3:2e.
 的百分含量保持不变
的百分含量保持不变(4)研究表明,合成氨反应在Fe催化剂上可能通过下图机理进行(*表示催化剂表面吸附位,
 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 )。
)。(ⅰ)

(ⅱ)

(ⅲ)
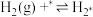
(ⅳ)
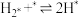
(ⅴ)

……
(…)
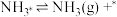
判断上述反应机理中,速率控制步骤(即速率最慢步骤)为
(5)基于
 载氮体的碳基化学链合成氨技术示反应如下:
载氮体的碳基化学链合成氨技术示反应如下:吸氮反应:

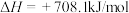
释氮反应:

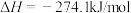
在温度为T、
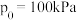 恒压条件下进行吸氮反应,平衡时氮气转化率为50%,分压平衡常数
恒压条件下进行吸氮反应,平衡时氮气转化率为50%,分压平衡常数
 。
。
您最近半年使用:0次
【推荐3】为减少 排放,科学家着眼于能源转换和再利用等问题。回答下列问题:
排放,科学家着眼于能源转换和再利用等问题。回答下列问题:
(1)我国科学家采用酞菁钴( )和锌-氮-碳(
)和锌-氮-碳( )串联催化剂,可有效地将
)串联催化剂,可有效地将 还原为甲烷。模拟装置如图1所示,串联催化剂表面反应历程如图2所示。
还原为甲烷。模拟装置如图1所示,串联催化剂表面反应历程如图2所示。
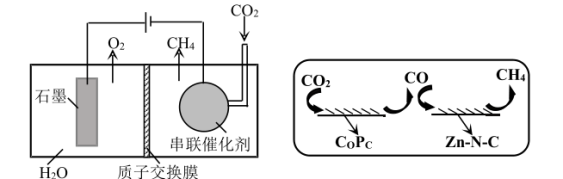
①关于该装置的说法错误的是_______ 。
A.串联催化剂表面发生的反应为: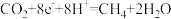
B.该串联催化装置,可将 制备
制备 的过程分解在两种活性位点上进行
的过程分解在两种活性位点上进行
C. 在
在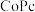 表面被氧化,生成中间产物
表面被氧化,生成中间产物
D.标准状况下,每生成 ,理论上可处理
,理论上可处理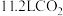
②已知: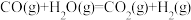 ΔH1=-akJ/mol
ΔH1=-akJ/mol
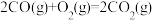 ΔH2=-bkJ/mol
ΔH2=-bkJ/mol
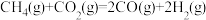 ΔH3=+ckJ/mol(a、b、c均为正值)
ΔH3=+ckJ/mol(a、b、c均为正值)
则反应 的ΔH4=
的ΔH4=_______ kJ/mol (用a、b、c表示)。
(2) 还可制取
还可制取 和水蒸气。将
和水蒸气。将 和
和 充入
充入 恒容密闭容器中,在两种不同催化剂作用下发生反应,相同时间内
恒容密闭容器中,在两种不同催化剂作用下发生反应,相同时间内 的转化率随温度变化曲线如图3所示:
的转化率随温度变化曲线如图3所示:
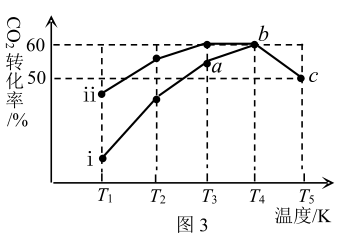
① 点时v正
点时v正_______ v逆 (填“>”“<”“=”)。
②随温度的升高, 的转化率先增大后减小,理由是
的转化率先增大后减小,理由是_______ 。
③已知c点时容器内的压强为P,在T5温度下该反应的平衡常数Kp为_______ (用含P的关系式表示)。
(3)在某催化剂作用下, 和
和 还能发生如下反应:
还能发生如下反应: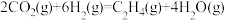 。图4所示为在体积为
。图4所示为在体积为 的恒容容器中,通入
的恒容容器中,通入 和
和 时,测得的温度对
时,测得的温度对 的平衡转化率和催化剂催化效率的影响:
的平衡转化率和催化剂催化效率的影响:
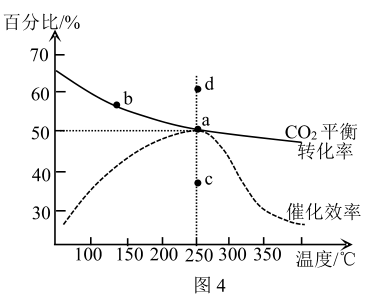
①a、b两点平衡常数的大小关系为:Ka_______ Kb (填“>”“<”)。
②如果不用催化剂,其他条件不变,则250℃时 的平衡转化率位于
的平衡转化率位于_______ 点(填“a”“c”“d”)。
 排放,科学家着眼于能源转换和再利用等问题。回答下列问题:
排放,科学家着眼于能源转换和再利用等问题。回答下列问题:(1)我国科学家采用酞菁钴(
 )和锌-氮-碳(
)和锌-氮-碳( )串联催化剂,可有效地将
)串联催化剂,可有效地将 还原为甲烷。模拟装置如图1所示,串联催化剂表面反应历程如图2所示。
还原为甲烷。模拟装置如图1所示,串联催化剂表面反应历程如图2所示。
图1 图2
①关于该装置的说法错误的是
A.串联催化剂表面发生的反应为:
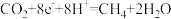
B.该串联催化装置,可将
 制备
制备 的过程分解在两种活性位点上进行
的过程分解在两种活性位点上进行C.
 在
在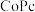 表面被氧化,生成中间产物
表面被氧化,生成中间产物
D.标准状况下,每生成
 ,理论上可处理
,理论上可处理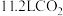
②已知:
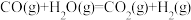 ΔH1=-akJ/mol
ΔH1=-akJ/mol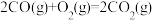 ΔH2=-bkJ/mol
ΔH2=-bkJ/mol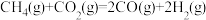 ΔH3=+ckJ/mol(a、b、c均为正值)
ΔH3=+ckJ/mol(a、b、c均为正值)则反应
 的ΔH4=
的ΔH4=(2)
 还可制取
还可制取 和水蒸气。将
和水蒸气。将 和
和 充入
充入 恒容密闭容器中,在两种不同催化剂作用下发生反应,相同时间内
恒容密闭容器中,在两种不同催化剂作用下发生反应,相同时间内 的转化率随温度变化曲线如图3所示:
的转化率随温度变化曲线如图3所示:
①
 点时v正
点时v正②随温度的升高,
 的转化率先增大后减小,理由是
的转化率先增大后减小,理由是③已知c点时容器内的压强为P,在T5温度下该反应的平衡常数Kp为
(3)在某催化剂作用下,
 和
和 还能发生如下反应:
还能发生如下反应: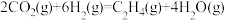 。图4所示为在体积为
。图4所示为在体积为 的恒容容器中,通入
的恒容容器中,通入 和
和 时,测得的温度对
时,测得的温度对 的平衡转化率和催化剂催化效率的影响:
的平衡转化率和催化剂催化效率的影响:
①a、b两点平衡常数的大小关系为:Ka
②如果不用催化剂,其他条件不变,则250℃时
 的平衡转化率位于
的平衡转化率位于
您最近半年使用:0次
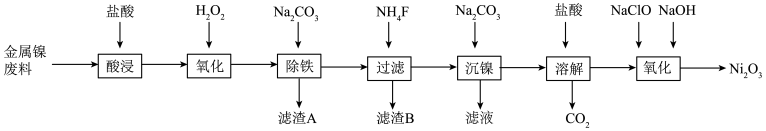
【推荐1】NiCl2是化工合成中最重要的镍源,工业上以金属镍废料(含Fe、Mg等杂质)为原料生产NiCl2,继而生产Ni2O3的工艺流程如图:
已知:①Ksp(MgF2)=7.4×10-11
②当溶液中某离子浓度小于1×10-5 mol/L时,可认为该离子已完全沉淀。
③流程中相关金属离子生成氢氧化物沉淀的pH如表所示:
(1)为了提高镍元素的浸出率,在“酸浸”时可采取的措施有_______ (写出一条即可)。
(2)加入H2O2的目的是_______ (用离子方程式表示)。
(3)“除铁”时,控制溶液pH的范围为_______ 。
(4)滤渣B的主要成分的化学式为_______ 。
(5)在“沉镍”操作中,为确保镍沉淀完全,溶液中 浓度应大于
浓度应大于_______ (已知:Ksp(NiCO3)=1.42×10-7)。
(6)“氧化”生成Ni2O3的离子方程式为_______ 。

已知:①Ksp(MgF2)=7.4×10-11
②当溶液中某离子浓度小于1×10-5 mol/L时,可认为该离子已完全沉淀。
③流程中相关金属离子生成氢氧化物沉淀的pH如表所示:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.1 | 6.5 | 7.1 |
| 沉淀完全的pH | 3.2 | 9.7 | 9.2 |
(1)为了提高镍元素的浸出率,在“酸浸”时可采取的措施有
(2)加入H2O2的目的是
(3)“除铁”时,控制溶液pH的范围为
(4)滤渣B的主要成分的化学式为
(5)在“沉镍”操作中,为确保镍沉淀完全,溶液中
 浓度应大于
浓度应大于(6)“氧化”生成Ni2O3的离子方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
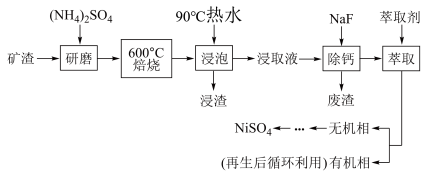
【推荐2】NiSO4主要用于电镀工业,作为电镀镍和化学镍的主要原料,也用于生产其他镍盐(如氧化镍、硫酸镍铵、碳酸镍等),从矿渣[含NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等]中回收NiSO4的工艺流程如图:
已知(NH4)2SO4在350℃分解生成NH3和H2SO4,回答下列问题:
(1)“浸渣”的成分有Fe2O3、FeO(OH)、CaSO4外,还含有___________ (写化学式)。
(2)矿渣中部分FeO焙烧时与H2SO4反应生成Fe2(SO4)3的化学方程式为___________ 。
(3)向“浸取液”中加入NaF以除去溶液中Ca2+(浓度为1.0×10-3mol•L﹣1),当溶液中c(F﹣)=2.0×10-3.5mol•L-1时,除钙率为___________ [Ksp(CaF2)=4.0×10-11]。
(4)溶剂萃取可用于对溶液中的金属离子进行富集与分离:Fe2+(水相)+2RH(有机相) FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值为
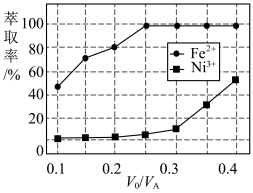
FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值为 ___________ 。在 ___________ (填“强碱性”“强酸性”或“中性”)介质中“反萃取”能使有机相再生而循环利用。
(5)以Fe、Ni为电极制取Na2FeO4的原理如图所示。通电后,在铁电极附近生成紫红色的FeO 。
。
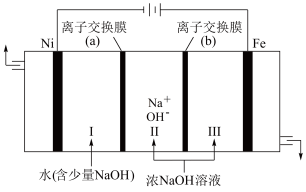
①电解时阳极的电极反应式为___________ ,离子交换膜(b)为 ___________ (填“阴”或“阳”)离子交换膜。
②向铁电极区出现的红褐色物质中加入少量的NaClO溶液,沉淀溶解。该反应的离子方程式为___________ 。

已知(NH4)2SO4在350℃分解生成NH3和H2SO4,回答下列问题:
(1)“浸渣”的成分有Fe2O3、FeO(OH)、CaSO4外,还含有
(2)矿渣中部分FeO焙烧时与H2SO4反应生成Fe2(SO4)3的化学方程式为
(3)向“浸取液”中加入NaF以除去溶液中Ca2+(浓度为1.0×10-3mol•L﹣1),当溶液中c(F﹣)=2.0×10-3.5mol•L-1时,除钙率为
(4)溶剂萃取可用于对溶液中的金属离子进行富集与分离:Fe2+(水相)+2RH(有机相)
 FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值为
FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如图所示,V0/VA的最佳取值为 
(5)以Fe、Ni为电极制取Na2FeO4的原理如图所示。通电后,在铁电极附近生成紫红色的FeO
 。
。
①电解时阳极的电极反应式为
②向铁电极区出现的红褐色物质中加入少量的NaClO溶液,沉淀溶解。该反应的离子方程式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】利用“铁脱络-化学沉淀法”回收电镀废水中镍的流程如图。

已知:①废水中镍主要以NiR2络合物形式存在,其在水溶液中存在平衡:NiR2(aq)⇌Ni2+(aq)+2R-(aq,有机配体)K=1.6×10-14。
②常温下,Ksp[Fe(OH)3]=1×10-39,Ksp[Ni(OH)2]=1.6×10-15。
③“脱络”(指NiR2转化成Ni2+)过程中,反应历程如下:
i.Fe2++H2O2=Fe3++OH-+·OH
ii.R-+·OH=OH-+·R
iii.H2O2+2·OH=O2↑+2H2O
(1)·OH的电子式为_______ ,其中氧元素的化合价为_______ 价。
(2)①根据·OH与H2O2的反应历程,分析“脱络”时加入的Fe2+的作用机制:_______ 。
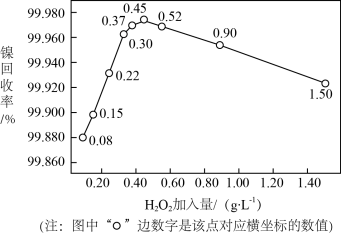
②实验测得H2O2加入量对溶液中镍回收率的影响如图所示。由图可知,当加入H2O2的量为_______ g·L-1时,镍回收效果最好;当加入H2O2的量较大时,镍回收回率下降,可能的原因是_______ 。
(3)常温下,若“脱络”后的废水中c(Ni2+)=0.01mol·L-1,“沉淀”时先加入NaOH至溶液的pH=_______ ,使Fe3+恰好沉淀完全(Fe3+浓度为10-6mol·L-1,忽略溶液体积变化),此时_______ (填“有”或“无”)Ni(OH)2沉淀生成。
(4)取100mL某电镀废水利用上述流程回收镍,得到2.325gNi(OH)2沉淀,经计算该步骤中Ni2+的回收率为99.97%;Ni(OH)2沉淀再经稀硫酸溶解、_______ 、过滤,得到NiSO4·7H2O固体的质量为6.744g。试计算100mL该电镀废水中镍转化成NiSO4·7H2O的总回收率:_______ (保留四位有效数字)。

已知:①废水中镍主要以NiR2络合物形式存在,其在水溶液中存在平衡:NiR2(aq)⇌Ni2+(aq)+2R-(aq,有机配体)K=1.6×10-14。
②常温下,Ksp[Fe(OH)3]=1×10-39,Ksp[Ni(OH)2]=1.6×10-15。
③“脱络”(指NiR2转化成Ni2+)过程中,反应历程如下:
i.Fe2++H2O2=Fe3++OH-+·OH
ii.R-+·OH=OH-+·R
iii.H2O2+2·OH=O2↑+2H2O
(1)·OH的电子式为
(2)①根据·OH与H2O2的反应历程,分析“脱络”时加入的Fe2+的作用机制:
②实验测得H2O2加入量对溶液中镍回收率的影响如图所示。由图可知,当加入H2O2的量为

(3)常温下,若“脱络”后的废水中c(Ni2+)=0.01mol·L-1,“沉淀”时先加入NaOH至溶液的pH=
(4)取100mL某电镀废水利用上述流程回收镍,得到2.325gNi(OH)2沉淀,经计算该步骤中Ni2+的回收率为99.97%;Ni(OH)2沉淀再经稀硫酸溶解、
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】高铁电池是一种新型可充电电池,与普通电池相比,该电池能较长时间保持稳定的放电电压。高铁电池的总反应式为3Zn+2K2FeO4+8H2O 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。
请回答下列问题:
(1)高铁电池的负极材料是______ 放电时负极反应式为____________________ 。
(2)放电时,正极发生________ (填“氧化”或“还原”)反应;正极反应式为______________________________ ;放电时,________ (填“正”或“负”)极附近溶液的碱性增强。
(3)充电时,阳极反应式为______________ ,阳极附近溶液的碱性________ (填“增强”“减弱”或“不变”)。
 3Zn(OH)2+2Fe(OH)3+4KOH。
3Zn(OH)2+2Fe(OH)3+4KOH。请回答下列问题:
(1)高铁电池的负极材料是
(2)放电时,正极发生
(3)充电时,阳极反应式为
您最近半年使用:0次
解答题-工业流程题
|
适中
(0.65)
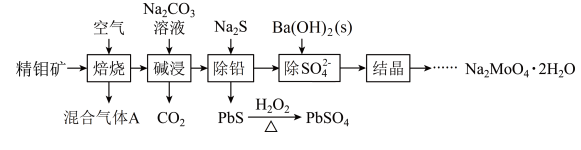
【推荐2】钼酸钠( Na2MoO4)可与重金属盐产生沉淀,是目前应用较多的一种新型水处理剂。利用精钼矿(主要成分是MoS2,含少量PbS等)来制取钼酸钠晶体的工艺流程如下图所示。
请回答下列问题:
(1)混合气A中含有一种大气污染物,其化学式为___________ 。
(2)焙烧的过程中采用如图1所示的“多层逆流焙烧”。

①多层逆流焙烧的优点是___________ (任答两点)。
②依据如图2,写出第6~12层MoO2参加反应的化学方程式___________ 。
(3)写出碱浸时发生反应的离子方程式___________ 。
(4)PbS与H2O2反应时,温度高于40℃后,反应速率反而减慢,原因是___________ 。
(5)流程图中“除SO42-”的过程中,当 BaMoO4开始沉淀时,SO42-的去除率为97.0%,已知原 Na2MoO4溶液中c(MoO42-)=0.48mol/L, c(SO42-)=0.040mol/L, Ksp(BaSO4)=1.0×10-10, 则Ksp(BaMoO4)=___________ 。(过程中溶液体积变化忽略不计)
(6)锂和二硫化钼形成的二次电池的总反应为:xLi+nMoS2 Lix(MoS2)n,则电池放电时的正极反应式是
Lix(MoS2)n,则电池放电时的正极反应式是___________ 。

请回答下列问题:
(1)混合气A中含有一种大气污染物,其化学式为
(2)焙烧的过程中采用如图1所示的“多层逆流焙烧”。

①多层逆流焙烧的优点是
②依据如图2,写出第6~12层MoO2参加反应的化学方程式
(3)写出碱浸时发生反应的离子方程式
(4)PbS与H2O2反应时,温度高于40℃后,反应速率反而减慢,原因是
(5)流程图中“除SO42-”的过程中,当 BaMoO4开始沉淀时,SO42-的去除率为97.0%,已知原 Na2MoO4溶液中c(MoO42-)=0.48mol/L, c(SO42-)=0.040mol/L, Ksp(BaSO4)=1.0×10-10, 则Ksp(BaMoO4)=
(6)锂和二硫化钼形成的二次电池的总反应为:xLi+nMoS2
 Lix(MoS2)n,则电池放电时的正极反应式是
Lix(MoS2)n,则电池放电时的正极反应式是
您最近半年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】电化学在科技、生产、社会和生活的各个发面都发挥着重要的作用。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择____ (填字母)。

a.金块 b.锌板 c.铜板 d.钠块
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图。(电极均为石墨电极)
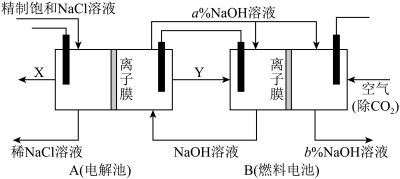
写出A装置中发生反应的离子反应方程式:____ ,分析比较图示中a%与b%的大小:a%____ b%(填“>”“<”或“=”)。
(3)写出燃料电池B中的负极的电极反应:____ 。
通过NO传感器可监测汽车尾气中NO的含量,工作原理如图所示:
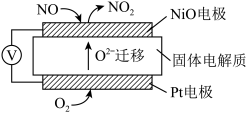
(4)Pt电极上的电极反应式为____ 。
(1)图中,为了减缓海水对钢闸门A的腐蚀,材料B可以选择

a.金块 b.锌板 c.铜板 d.钠块
(2)氯碱工业是高耗能产业,一种将电解池与燃料电池相组合的新工艺,节能超过30%,在此工艺中,物料传输和转化关系如图。(电极均为石墨电极)

写出A装置中发生反应的离子反应方程式:
(3)写出燃料电池B中的负极的电极反应:
通过NO传感器可监测汽车尾气中NO的含量,工作原理如图所示:

(4)Pt电极上的电极反应式为
您最近半年使用:0次



