X、Y、Z、W有如图所示的转化关系:
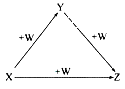
(1)若X单质的一种同素异形体是一种黑色的非金属单质,则Y转化为Z的化学方程式_________________ ,Z的晶体类型______________ 晶体。
(2)若X为一种金属的氯化物,Y是一种常见的两性氢氧化物,W为化工常用的强碱,写出Y与W反应的离子方程式_______________________ 。
(3)若X是一种活泼的金属单质,Z是一种淡黄色的化合物,Z的化学式___________ ,则Z转化为W的化学方程式________________________________________________ 。

(1)若X单质的一种同素异形体是一种黑色的非金属单质,则Y转化为Z的化学方程式
(2)若X为一种金属的氯化物,Y是一种常见的两性氢氧化物,W为化工常用的强碱,写出Y与W反应的离子方程式
(3)若X是一种活泼的金属单质,Z是一种淡黄色的化合物,Z的化学式
更新时间:2017-09-15 20:35:43
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】下列框图中的物质均为初中化学常见的物质,其中A是建筑材料的主要成分,B属于氧化物,下图是它们之间的相互转化关系。请回答:

(1)写出物质A的化学式:_____________ ;
(2)得到F溶液的操作Ⅰ的名称为:________________ ;
(3)若I是红褐色沉淀,请写出下列转化的化学方程式:
B→G:_________________ ;G + F → I:__________________ 。

(1)写出物质A的化学式:
(2)得到F溶液的操作Ⅰ的名称为:
(3)若I是红褐色沉淀,请写出下列转化的化学方程式:
B→G:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】A、B、C、D、E、F、G为原子序数依次增大的短周期主族元素。B、C、D均能与A形成10电子分子,E单质可用于野外焊接钢轨的原料,F与D同主族。
(1)D、E、F的离子半径由大到小的顺序为_______________________ (填离子符号)。
(2)F和G形成的一种化合物甲中所有原子均为8电子稳定结构,该化合物与水反应生成F单质、F的最高价含氧酸和G的氢化物,该反应的化学方程式为___________________ 。
(3)C能分别与A和D按原子个数比1:2形成化合物乙和丙,乙的结构式为__________ 。常温下,液体乙与气体丙反应生成两种无污染的物质,该反应的氧化产物与还原产物的物质的量之比为________________ 。
(4)现取100 mL1 mol/L的E的氯化物溶液,向其中加入1 mol/L NaOH溶液产生了3.9g沉淀,则加入的NaOH溶液体积可能为_________________________ mL。
(1)D、E、F的离子半径由大到小的顺序为
(2)F和G形成的一种化合物甲中所有原子均为8电子稳定结构,该化合物与水反应生成F单质、F的最高价含氧酸和G的氢化物,该反应的化学方程式为
(3)C能分别与A和D按原子个数比1:2形成化合物乙和丙,乙的结构式为
(4)现取100 mL1 mol/L的E的氯化物溶液,向其中加入1 mol/L NaOH溶液产生了3.9g沉淀,则加入的NaOH溶液体积可能为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】Ⅰ.某混合物的无色溶液中,可能含有以下离子中的若干种:K+、Ca2+、Fe3+、NH4+、Cl-、CO32-和SO42-。现每次取10.00mL进行实验:
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体448mL(标准状况下);
③第三份加入足量BaCl2溶液后,生成白色沉淀,过滤、干燥,得到固体4.30g,该固体经足量盐酸洗涤,干燥后剩余2.33g。
(1)c(CO32-)=______ mol·L−1;
(2)某同学认为该溶液中一定存在K+,浓度范围是_________________ ;
(3)根据以上实验,某离子可能存在。检验该离子是否存在的方法是___________________________ ;
(4)写出③中固体加入足量盐酸洗涤的离子方程式________________________________ 。
Ⅱ.四种物质有如下相互转化关系:

(5)若化合物A是红棕色粉末状固体,化合物B是一种既可以与强酸溶液反应又可以与强碱溶液反应的氧化物,则该反应的化学方程式为____________________ ;
(6)若甲是活泼金属,化合物B是强碱,则该反应的离子方程式为____________ ;
(7)若乙是黑色固体,化合物B是优质的耐高温材料。则该反应的化学方程式为____________________ ;
(8)若化合物A可作光导纤维材料,乙是一种重要的半导体材料。则该反应的化学方程式为____________________ 。
①第一份加入AgNO3溶液有沉淀产生;
②第二份加入足量NaOH后加热,收集到气体448mL(标准状况下);
③第三份加入足量BaCl2溶液后,生成白色沉淀,过滤、干燥,得到固体4.30g,该固体经足量盐酸洗涤,干燥后剩余2.33g。
(1)c(CO32-)=
(2)某同学认为该溶液中一定存在K+,浓度范围是
(3)根据以上实验,某离子可能存在。检验该离子是否存在的方法是
(4)写出③中固体加入足量盐酸洗涤的离子方程式
Ⅱ.四种物质有如下相互转化关系:

(5)若化合物A是红棕色粉末状固体,化合物B是一种既可以与强酸溶液反应又可以与强碱溶液反应的氧化物,则该反应的化学方程式为
(6)若甲是活泼金属,化合物B是强碱,则该反应的离子方程式为
(7)若乙是黑色固体,化合物B是优质的耐高温材料。则该反应的化学方程式为
(8)若化合物A可作光导纤维材料,乙是一种重要的半导体材料。则该反应的化学方程式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某研究性学习小组在做过氧化钠与水反应的实验时,发现过氧化钠与水反应后的溶液中滴加酚酞溶液呈现红色,但红色很快褪色,甲乙丙三位同学对此现象分别做了如下实验:
甲、因为反应后试管很热,所以可能是溶液温度过高使红色褪去;乙、因为所加水量太少,红色褪去可能是生成氢氧化钠浓度较大的影响;丙、过氧化钠具有强氧化性,生成物中氧气、过氧化氢(可能产物)等也具有强氧化性,可能是氧化漂白了红色物质。
(1)验证甲同学的推测是否正确的方法是______ 。
(2)验证乙同学的方法正确的是______ 。
(3)验证丙同学的推测是否正确的方法是______ 。
甲、因为反应后试管很热,所以可能是溶液温度过高使红色褪去;乙、因为所加水量太少,红色褪去可能是生成氢氧化钠浓度较大的影响;丙、过氧化钠具有强氧化性,生成物中氧气、过氧化氢(可能产物)等也具有强氧化性,可能是氧化漂白了红色物质。
(1)验证甲同学的推测是否正确的方法是
(2)验证乙同学的方法正确的是
(3)验证丙同学的推测是否正确的方法是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如下转化关系(其他产物及反应条件已略去,反应可以在水溶液中进行):
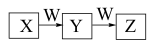
(1)若W是O2,则X不可能是________ (填代号)
a.NH3 b.Mg c.H2S d.Al
(2)若Z为淡黄色粉末,常用作呼吸面具中的供氧剂
①Z与CO2反应的化学方程式为_______ ;
②78g Z与水发生反应时转移电子的物质的量为________ mol。
(3)若X、Y、Z三种物质都含有一种金属元素,且Y为两性物质
①X溶液一步转化为Z溶液的反应离子方程式为________ ;
②将X溶液、Z溶液等体积混合,恰好完全反应,则X溶液、Z溶液的浓度之比为______ 。
(4)若X为一元强碱溶液,W是形成酸雨的主要气体。
①则Y到Z的离子方程式为________ ;
②请画出向含0.01mol X和0.01mol Y的溶液中逐滴加入0.1mol/L稀盐酸的体积和生成气体的物质的量的关系的图像___ 。
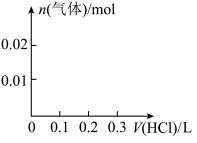
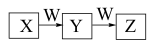
(1)若W是O2,则X不可能是
a.NH3 b.Mg c.H2S d.Al
(2)若Z为淡黄色粉末,常用作呼吸面具中的供氧剂
①Z与CO2反应的化学方程式为
②78g Z与水发生反应时转移电子的物质的量为
(3)若X、Y、Z三种物质都含有一种金属元素,且Y为两性物质
①X溶液一步转化为Z溶液的反应离子方程式为
②将X溶液、Z溶液等体积混合,恰好完全反应,则X溶液、Z溶液的浓度之比为
(4)若X为一元强碱溶液,W是形成酸雨的主要气体。
①则Y到Z的离子方程式为
②请画出向含0.01mol X和0.01mol Y的溶液中逐滴加入0.1mol/L稀盐酸的体积和生成气体的物质的量的关系的图像

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】 也是一种重要的钠的化合物。某研究性小组取用
也是一种重要的钠的化合物。某研究性小组取用 于圆底烧瓶中,并设计了如下图装置探究其强氧化性。
于圆底烧瓶中,并设计了如下图装置探究其强氧化性。

(1)原定实验计划是在分液漏斗中加入稀盐酸,则发生的化学方程式为_______ ;
(2)而由于同学的疏忽,错误地取成了浓盐酸,实验中观察到B中湿润的红色纸条褪色,说明反应中有_______ (填化学式)生成,若B中改放湿润的淀粉KI试纸,凭试纸变蓝能否证明上述结论?_______ (填“能”或“不能”),理由是_______ 。
(3)实验中,在D的集气瓶中收集到能使带火星木条复燃的无色气体,有同学认为该气体是 被浓盐酸还原所得,从氧化还原角度分析该推断是否合理?
被浓盐酸还原所得,从氧化还原角度分析该推断是否合理?_______ 。
(4)还有同学认为D的集气瓶中收集到的气体是 与浓盐酸中的水反应得到。通过实验证实
与浓盐酸中的水反应得到。通过实验证实 与干燥的HCl能反应,请完成并配平该化学方程式:
与干燥的HCl能反应,请完成并配平该化学方程式:______ 。
_______Na2O2+_______HCl=_______Cl2+_______NaCl+_______。
 也是一种重要的钠的化合物。某研究性小组取用
也是一种重要的钠的化合物。某研究性小组取用 于圆底烧瓶中,并设计了如下图装置探究其强氧化性。
于圆底烧瓶中,并设计了如下图装置探究其强氧化性。
(1)原定实验计划是在分液漏斗中加入稀盐酸,则发生的化学方程式为
(2)而由于同学的疏忽,错误地取成了浓盐酸,实验中观察到B中湿润的红色纸条褪色,说明反应中有
(3)实验中,在D的集气瓶中收集到能使带火星木条复燃的无色气体,有同学认为该气体是
 被浓盐酸还原所得,从氧化还原角度分析该推断是否合理?
被浓盐酸还原所得,从氧化还原角度分析该推断是否合理?(4)还有同学认为D的集气瓶中收集到的气体是
 与浓盐酸中的水反应得到。通过实验证实
与浓盐酸中的水反应得到。通过实验证实 与干燥的HCl能反应,请完成并配平该化学方程式:
与干燥的HCl能反应,请完成并配平该化学方程式:_______Na2O2+_______HCl=_______Cl2+_______NaCl+_______。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】现有含一定量Na2O杂质的Na2O2试样,用下图所示的实验装置通过与纯净、干燥的CO2反应来测定试样中Na2O2的纯度。
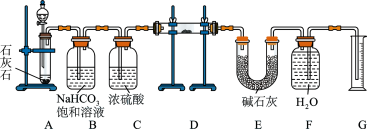
回答下列问题:
(1)按上图组装好实验装置后,首先应该进行的操作是______________ 。
(2)分液漏斗中所装试液是__________ 。
(3)装置D中发生反应的化学方程是:Na2O + CO2 = Na2CO3和____ 。
(4)E中碱石灰的作用是__________ 。
(5)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则试样中Na2O2的含量为__________ 。

回答下列问题:
(1)按上图组装好实验装置后,首先应该进行的操作是
(2)分液漏斗中所装试液是
(3)装置D中发生反应的化学方程是:Na2O + CO2 = Na2CO3和
(4)E中碱石灰的作用是
(5)若开始时测得样品的质量为2.0 g,反应结束后测得气体体积为224 mL(标准状况),则试样中Na2O2的含量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】a、b、c、d、e为五种短周期主族元素,原子序数依次递增。下图是a~e五种元素的单质及其化合物(或其溶液)的转化关系。已知A为金属单质,E为淡黄色固体,B、C、D是非金属单质,且在常温常压下都是气体,D常用于自来水的杀菌、消毒,化合物F通常状况下呈气态。请回答下列问题:

(1)d在元素周期表中的位置位于___________ , 的电子式为
的电子式为___________ 。
(2)e的单质与d的最高价氧化物对应的水化物反应的化学方程式是___________ 。
(3) 可在呼吸面具中作为氧气来源,假设每人每分钟消耗
可在呼吸面具中作为氧气来源,假设每人每分钟消耗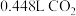 (标准状况),且所需的
(标准状况),且所需的 全部由
全部由 来提供,则某消防员工作1小时所需
来提供,则某消防员工作1小时所需 的质量为
的质量为___________ g。
(4)b、c、d元素中,原子半径由小到大的顺序是___________ (填元素符号);c、d、e元素分别形成的简单离子中离子半径最小的是___________ (填离子符号)。
(5)b和e两元素相比较,非金属性较强是___________ (填元素符号),可以证明该结论的是___________ 。
A.e的气态氢化物比b的气态氢化物稳定
B.b氧化物对应的水化物的酸性弱于e氧化物对应的水化物的酸性
C.b的简单氢化物的沸点比e的氢化物沸点低
D.b和e形成的化合物中的化合价b为正价,e为负价

(1)d在元素周期表中的位置位于
 的电子式为
的电子式为(2)e的单质与d的最高价氧化物对应的水化物反应的化学方程式是
(3)
 可在呼吸面具中作为氧气来源,假设每人每分钟消耗
可在呼吸面具中作为氧气来源,假设每人每分钟消耗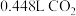 (标准状况),且所需的
(标准状况),且所需的 全部由
全部由 来提供,则某消防员工作1小时所需
来提供,则某消防员工作1小时所需 的质量为
的质量为(4)b、c、d元素中,原子半径由小到大的顺序是
(5)b和e两元素相比较,非金属性较强是
A.e的气态氢化物比b的气态氢化物稳定
B.b氧化物对应的水化物的酸性弱于e氧化物对应的水化物的酸性
C.b的简单氢化物的沸点比e的氢化物沸点低
D.b和e形成的化合物中的化合价b为正价,e为负价
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】I.下列图示中,A为一种常见的单质,B、C、D、E是含A元素的常见化合物,它们的焰色反应均为黄色。
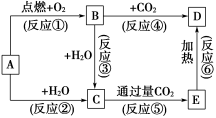
请填写下列空白:
(1)以上反应中,属于氧化还原反应的有_______ (填写编号)。
(2)写出A→C反应的离子方程式:_______ ;B→D的化学方程式:_______ 。
II.某校科学兴趣小组探究二氧化碳与过氧化钠反应是否有氧气生成;设计了下图的实验装置。B中盛有饱和碳酸氢钠溶液,E为收集氧气装置。
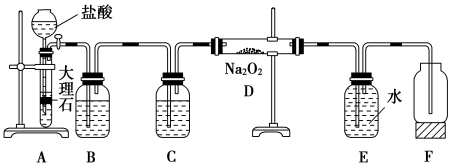
(3)装置B的作用是_______ 。

请填写下列空白:
(1)以上反应中,属于氧化还原反应的有
(2)写出A→C反应的离子方程式:
II.某校科学兴趣小组探究二氧化碳与过氧化钠反应是否有氧气生成;设计了下图的实验装置。B中盛有饱和碳酸氢钠溶液,E为收集氧气装置。

(3)装置B的作用是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
真题
名校
【推荐1】某兴趣小组用铝箔制备Al2O3、AlCl3·6H2O及明矾大晶体,具体流程如下:
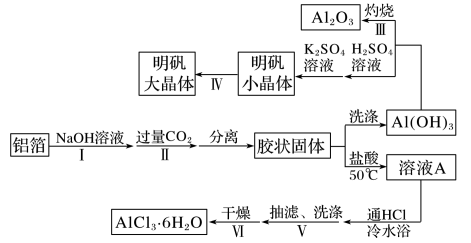
已知:AlCl3·6H2O易溶于水、乙醇及乙醚;明矾在水中的溶解度如下表。
请回答:
(1)步骤Ⅰ中的化学方程式______________________________________ 。步骤Ⅱ中生成Al(OH)3的离子方程式________________________________________ 。
(2)步骤Ⅲ,下列操作合理的是______________________ 。
A.坩埚洗净后,无需擦干,即可加入Al(OH)3灼烧
B.为了得到纯Al2O3,需灼烧至恒重
C.若用坩埚钳移动灼热的坩埚,需预热坩埚钳
D.坩埚取下后放在石棉网上冷却待用
E.为确保称量准确,灼烧后应趁热称重
(3)步骤Ⅳ,选出在培养规则明矾大晶体过程中合理的操作并排序_______________ 。
①迅速降至室温 ②用玻璃棒摩擦器壁③配制90℃的明矾饱和溶液 ④自然冷却至室温
⑤选规则明矾小晶体并悬挂在溶液中央⑥配制高于室温10~20℃的明矾饱和溶液
(4)由溶液A制备AlCl3·6H2O的装置如图:
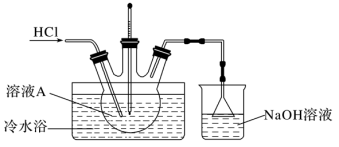
①通入HCl的作用是抑制AlCl3水解和________________ 。
②步骤Ⅴ,抽滤时,用玻璃纤维替代滤纸的理由是____________________________ ;
洗涤时,合适的洗涤剂是______________________ 。
③步骤Ⅵ,为得到纯净的AlCl3·6H2O,宜采用的干燥方式是___________________ 。

已知:AlCl3·6H2O易溶于水、乙醇及乙醚;明矾在水中的溶解度如下表。
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 90 |
| 溶解度/g | 3.00 | 3.99 | 5.90 | 8.39 | 11.7 | 24.8 | 71.0 | 109 |
(1)步骤Ⅰ中的化学方程式
(2)步骤Ⅲ,下列操作合理的是
A.坩埚洗净后,无需擦干,即可加入Al(OH)3灼烧
B.为了得到纯Al2O3,需灼烧至恒重
C.若用坩埚钳移动灼热的坩埚,需预热坩埚钳
D.坩埚取下后放在石棉网上冷却待用
E.为确保称量准确,灼烧后应趁热称重
(3)步骤Ⅳ,选出在培养规则明矾大晶体过程中合理的操作并排序
①迅速降至室温 ②用玻璃棒摩擦器壁③配制90℃的明矾饱和溶液 ④自然冷却至室温
⑤选规则明矾小晶体并悬挂在溶液中央⑥配制高于室温10~20℃的明矾饱和溶液
(4)由溶液A制备AlCl3·6H2O的装置如图:

①通入HCl的作用是抑制AlCl3水解和
②步骤Ⅴ,抽滤时,用玻璃纤维替代滤纸的理由是
洗涤时,合适的洗涤剂是
③步骤Ⅵ,为得到纯净的AlCl3·6H2O,宜采用的干燥方式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】X、Y、Z、M、W、Q、R是7种短周期元素,其原子半径及主要化合价如下:
完成下列填空:
(1)上述元素中,金属性最强的在周期表中的位置是____________________ ;X、Y、Q各自形成的简单离子中,离子半径由大到小的顺序是_______ (填离子符号)。W和R按原子个数比1∶4构成的阳离子所含的化学键是________________ 。
(2)表中所列4种第三周期元素的最高价氧化物的水化物碱性最弱的是_______ (填化学式),其电离方程式为_____________________________________ 。
(3)M与Z相比,非金属性较强的是_____________ (填元素名称),请从原子结构的角度说明理由________________________________________________ 。
(4)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应,反应方程式如下:
请配平,当有0.5molH2O2参加此反应,电子转移的个数为____________ 。
| 元素代号 | X | Y | Z | M | W | Q | R |
| 原子半径/nm | 0.186 | 0.143 | 0.104 | 0.099 | 0.070 | 0.066 | 0.032 |
| 主要化合价 | +1 | +3 | +6,﹣2 | +7,﹣1 | +5,﹣3 | ﹣2 | +1 |
(1)上述元素中,金属性最强的在周期表中的位置是
(2)表中所列4种第三周期元素的最高价氧化物的水化物碱性最弱的是
(3)M与Z相比,非金属性较强的是
(4)在稀硫酸中,KMnO4和H2O2能发生氧化还原反应,反应方程式如下:
请配平,当有0.5molH2O2参加此反应,电子转移的个数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】某混合物A,含有Al2(SO4)3、Al2O3和Fe2O3,在一定条件下可实现下图所示的变化。
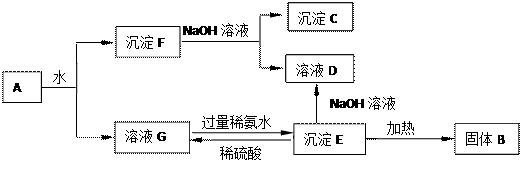
请回答下列问题。
(1)B、C、D、E 4种物质的化学式为:
B____________ 、C____________ 、D____________ 、E____________ 。
(2)沉淀F与NaOH溶液反应的离子方程式为________________________________ 。
沉淀E与稀硫酸反应的离子方程为____________________________________ 。
溶液G与过量稀氨水反应的化学方程为________________________________ 。

请回答下列问题。
(1)B、C、D、E 4种物质的化学式为:
B
(2)沉淀F与NaOH溶液反应的离子方程式为
沉淀E与稀硫酸反应的离子方程为
溶液G与过量稀氨水反应的化学方程为
您最近一年使用:0次



