高铁酸钾(K2FeO4)是一种新型、高效、多功能绿色水处理剂,比Cl2、O3、ClO2、KMnO4氧化性更强,无二次污染。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入KOH至饱和,使高铁酸钾析出。
(1)干法制备高铁酸钾的主要反应为:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①该反应中的还原剂是_______ ,该反应每生成1 mol Na2FeO4转移_____ mol电子。
②简要说明K2FeO4作为水处理剂时,在水处理过程中所起的作用:一是K2FeO4氧化性强,可以消毒杀菌;二是__________________ 。
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO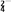 、Cl-、H2O。
、Cl-、H2O。
①写出并配平湿法制备高铁酸钾的离子反应方程式:_____________________ 。
②若反应过程中转移了0.3 mol电子,则还原产物的物质的量为________ 。
③低温下,向高铁酸钠溶液中加入KOH至饱和,可析出高铁酸钾(K2FeO4),说明了什么问题______________________ 。
(1)干法制备高铁酸钾的主要反应为:2FeSO4+6Na2O2===2Na2FeO4+2Na2O+2Na2SO4+O2↑。
①该反应中的还原剂是
②简要说明K2FeO4作为水处理剂时,在水处理过程中所起的作用:一是K2FeO4氧化性强,可以消毒杀菌;二是
(2)湿法制备高铁酸钾(K2FeO4)的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO
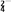 、Cl-、H2O。
、Cl-、H2O。①写出并配平湿法制备高铁酸钾的离子反应方程式:
②若反应过程中转移了0.3 mol电子,则还原产物的物质的量为
③低温下,向高铁酸钠溶液中加入KOH至饱和,可析出高铁酸钾(K2FeO4),说明了什么问题
更新时间:2017-09-26 21:04:26
|
相似题推荐
填空题
|
适中
(0.64)
【推荐1】(1)维生素C 又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C 具有______ 性。(填氧化性或还原性)
(2)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3 CO2↑。该反应的氧化剂是____ ,当16g 硫参加反应时,转移的电子数为__________ 。
(3)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。上述反应中,若有10个铝原子参与反应,则转移的电子数为__________ 个,用“双线桥法”标明反应中电子转移的方向和数目_________ 。
(2)我国古代四大发明之一的黑火药是由硫磺粉、硝酸钾和木炭粉按一定比例混合而成,爆炸时的反应为:S+2KNO3+3C=K2S+N2↑+3 CO2↑。该反应的氧化剂是
(3)饮用水中的NO3-对人类健康会产生危害,为了降低饮用水中NO3-的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将NO3-还原为N2,其化学方程式为:10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。上述反应中,若有10个铝原子参与反应,则转移的电子数为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】阅读下面科普信息,回答问题:
一个体重50kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)在Fe+4HNO3(稀)===Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了______ 性,则56g Fe参加反应时,被还原的HNO3为____ g。
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食中毒的事件,其原因是NaNO2外观和食盐相似,又有咸味,却可以把人体内的Fe2+转化为Fe3+而失去了与O2结合的能力。(已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。)根据上述反应,可判断NaNO2具有__________ 性。鉴别NaNO2和NaCl,可选用的物质有:①水 ②碘化钾淀粉试纸 ③淀粉 ④白酒 ⑤食醋,你认为必须选用的物质有______ (填序号)。
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是______ 。
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)请配平以下化学方程式______ Al+______ NaNO3+______ NaOH=______ NaAlO2+______ N2↑+______ H2O;若反应过程中转移5mol 电子,则生成标准状况下N2的体积为______ 。
一个体重50kg的健康人含铁2 g,这2g铁在人体中以Fe2+和Fe3+的形式存在。亚铁离子易被吸收,给贫血者补充铁时,应给予含亚铁离子的亚铁盐,如硫酸亚铁。服用维生素C,可使食物中的铁离子还原成亚铁离子,有利于铁的吸收。
(1)在Fe+4HNO3(稀)===Fe(NO3)3+NO↑+2H2O的反应中,HNO3表现了
(2)工业盐的主要成分是NaNO2,曾多次发生过因误食中毒的事件,其原因是NaNO2外观和食盐相似,又有咸味,却可以把人体内的Fe2+转化为Fe3+而失去了与O2结合的能力。(已知NaNO2能发生如下反应:2NaNO2+4HI=2NO↑+I2+2NaI+2H2O。)根据上述反应,可判断NaNO2具有
(3)某厂废液中,含有2%~5%的NaNO2,直接排放会造成污染,下列试剂能使NaNO2转化为不引起二次污染的N2的是
A.NaCl B.NH4Cl C.HNO3 D.浓H2SO4
(4)请配平以下化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】写出下列反应的离子方程式
(1)铜屑放入稀硫酸中不发生反应,若在稀硫酸中加入H2O2中加入,铜屑可以逐渐溶解,该反应的离子方程式:______ 。
(2)将20mL 0.5 mol/LK2SO3 溶液逐滴加入到20mL0.2 mol/LKMnO4 溶液(硫酸酸化)中,溶液恰好褪为无色。写出反应的离子方程式:______ 。
(3)用氯酸钠(NaClO3)和硫酸酸化的H2O2反应生成ClO2,请写出该反应的化学方程式。______ 。
(4)氮气的实验室制法是用氯化铵(NH4Cl)与亚硝酸钠(NaNO2)反应,同时生成氯化钠和水。写出该反应的化学方程式:______ 。
(5)二氧化硫可以使酸性高锰酸钾褪色,请写出该反应的离子方程式:______ 。
(1)铜屑放入稀硫酸中不发生反应,若在稀硫酸中加入H2O2中加入,铜屑可以逐渐溶解,该反应的离子方程式:
(2)将20mL 0.5 mol/LK2SO3 溶液逐滴加入到20mL0.2 mol/LKMnO4 溶液(硫酸酸化)中,溶液恰好褪为无色。写出反应的离子方程式:
(3)用氯酸钠(NaClO3)和硫酸酸化的H2O2反应生成ClO2,请写出该反应的化学方程式。
(4)氮气的实验室制法是用氯化铵(NH4Cl)与亚硝酸钠(NaNO2)反应,同时生成氯化钠和水。写出该反应的化学方程式:
(5)二氧化硫可以使酸性高锰酸钾褪色,请写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】已知溶液中,还原性为HSO3->I-,氧化性为IO3->I2>SO42-。在含3 mol NaHSO3的溶液中逐滴加入KIO3溶液,加入KIO3和析出I2的物质的量的关系如图所示,请回答下列问题

下列问题:
(1)a点处的氧化产物是_________ (填化学式,下同),还原产物是_______ ,a点对应的离子方程式为_____ 。
(2)当n(I2)达到最大值时,n(IO3-)对应的最小值为____ mol,此时反应的离子方程式是_____________ 。
(3)当溶液中的I-为0.4mol时,加入的KIO3为______ mol。
(4)若向100mL 1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为____________ 。

下列问题:
(1)a点处的氧化产物是
(2)当n(I2)达到最大值时,n(IO3-)对应的最小值为
(3)当溶液中的I-为0.4mol时,加入的KIO3为
(4)若向100mL 1mol/L的KIO3溶液中滴加NaHSO3溶液,反应开始时的离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】金属冶炼与处理常涉及氧化还原反应。
(1)由下列物质冶炼相应金属时采用电解法的是___________________________ 。
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2=4CuSO4+2H2O,该反应的还原剂是________ 。当1mol O2发生反应时,还原剂所失电子的物质的量为________ mol。向CuSO4溶液中加入镁条时有气体生成,该气体是________________________________________________________________________ 。
(1)由下列物质冶炼相应金属时采用电解法的是
a.Fe2O3 b.NaCl c.Cu2S d.Al2O3
(2)辉铜矿(Cu2S)可发生反应:2Cu2S+2H2SO4+5O2=4CuSO4+2H2O,该反应的还原剂是
您最近一年使用:0次
【推荐3】高铁酸钾(K2FeO4)是一种新型绿色消毒剂,其在消毒(发生氧化还原反应)后可形成Fe(OH)3胶体,常用于处理饮用水。工业上有干法与湿法两种制备高铁酸钾的方法。
(1)干法制备高铁酸钾时,先制备得到Na2FeO4,反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中,氧化剂是_______ ,氧化产物是_______ 。
(2)配平湿法制备高铁酸钾反应的离子方程式并用单线桥表示出电子转移的方向和数目:_____ 。
_______Fe(OH)3+_______ClO−+_______OH−=_______ +_______Cl−+_______H2O。
+_______Cl−+_______H2O。
(3)取少量K2FeO4溶液,滴加盐酸,有Cl2产生,该反应表明氧化性:K2FeO4_______ (填“>”或“<”)Cl2。
(1)干法制备高铁酸钾时,先制备得到Na2FeO4,反应为2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑,该反应中,氧化剂是
(2)配平湿法制备高铁酸钾反应的离子方程式并用单线桥表示出电子转移的方向和数目:
_______Fe(OH)3+_______ClO−+_______OH−=_______
 +_______Cl−+_______H2O。
+_______Cl−+_______H2O。(3)取少量K2FeO4溶液,滴加盐酸,有Cl2产生,该反应表明氧化性:K2FeO4
您最近一年使用:0次
【推荐1】重铬酸钾 和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为
和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为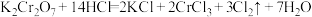 。
。
(1)浓盐酸在反应中表现出来的性质是_______ (填写编号)
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2) 是
是_______ (“氧化”或“还原”)产物;产生 ,则转移电子的物质的量为
,则转移电子的物质的量为____ mol。
(3)从铬元素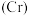 的化合价态上判断,
的化合价态上判断,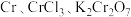 三种物质中的铬元素既表现氧化性又表现还原性的是
三种物质中的铬元素既表现氧化性又表现还原性的是_____________ (写化学式,下同)。
(4)已知氯气有毒,与水反应生成两种酸。实验室制备氯气可选用__________ 溶液进行尾气处理。
 和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为
和浓盐酸在一定温度下反应可制备黄绿色的氯气,其化学方程式为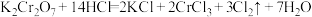 。
。(1)浓盐酸在反应中表现出来的性质是
①只有还原性 ②还原性和酸性 ③只有氧化性 ④氧化性和酸性
(2)
 是
是 ,则转移电子的物质的量为
,则转移电子的物质的量为(3)从铬元素
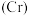 的化合价态上判断,
的化合价态上判断,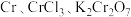 三种物质中的铬元素既表现氧化性又表现还原性的是
三种物质中的铬元素既表现氧化性又表现还原性的是(4)已知氯气有毒,与水反应生成两种酸。实验室制备氯气可选用
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有下列物质:① 溶液;②铁;③稀硫酸;④二氧化碳;⑤
溶液;②铁;③稀硫酸;④二氧化碳;⑤ 固体;⑥熔融
固体;⑥熔融 ;⑦
;⑦ 胶体;⑧蔗糖溶液。
胶体;⑧蔗糖溶液。
(1)将上述物质的序号填写在表格的空白处:
(2)某学习小组为证实 溶液和
溶液和 溶液的反应是离子反应,设计了如下实验。
溶液的反应是离子反应,设计了如下实验。
[实验原理]溶液的导电性由溶液中离子的浓度及离子电荷数决定。通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应是离子反应。
[实验装置]如图所示:
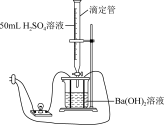
[实验过程与记录]
(3)写出下列情况发生反应的离子方程式:向 溶液中逐滴加入
溶液中逐滴加入 溶液至溶液显中性
溶液至溶液显中性___________ ,继续滴加 溶液
溶液___________ 。
(4) 可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钠(Na2FeO4)。可以通过以下两种方法制备:
可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钠(Na2FeO4)。可以通过以下两种方法制备:
①请将湿法制备高铁酸钠的离子方程式配平:______
___________ ___________
___________ ___________
___________ ___________
___________ ___________
___________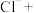 ___________
___________ 。
。
②干法制备高铁酸钠的化学方程式: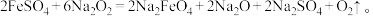 该反应中的氧化产物是
该反应中的氧化产物是___________ (填化学式)。生成 ,转移电子数目为
,转移电子数目为___________ 。
 溶液;②铁;③稀硫酸;④二氧化碳;⑤
溶液;②铁;③稀硫酸;④二氧化碳;⑤ 固体;⑥熔融
固体;⑥熔融 ;⑦
;⑦ 胶体;⑧蔗糖溶液。
胶体;⑧蔗糖溶液。(1)将上述物质的序号填写在表格的空白处:
| 分类标准 | 能导电的纯净物 | 电解质 |
| 属于该类的物质 |
 溶液和
溶液和 溶液的反应是离子反应,设计了如下实验。
溶液的反应是离子反应,设计了如下实验。[实验原理]溶液的导电性由溶液中离子的浓度及离子电荷数决定。通过观察实验现象,判断溶液中离子浓度的变化,从而证明反应是离子反应。
[实验装置]如图所示:

[实验过程与记录]
| 实验步骤 | 实验现象 | 实验结论 |
连接好装置,向烧杯中加入 的 的 溶液,逐滴滴加 溶液,逐滴滴加 的 的 溶液直至过量,边滴边振荡 溶液直至过量,边滴边振荡 | ① | ② 溶液和 溶液和 溶液的反应是离子反应 溶液的反应是离子反应 |
 溶液中逐滴加入
溶液中逐滴加入 溶液至溶液显中性
溶液至溶液显中性 溶液
溶液(4)
 可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钠(Na2FeO4)。可以通过以下两种方法制备:
可用于制备一种新型、高效、多功能绿色水处理剂高铁酸钠(Na2FeO4)。可以通过以下两种方法制备:①请将湿法制备高铁酸钠的离子方程式配平:
___________
 ___________
___________ ___________
___________ ___________
___________ ___________
___________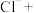 ___________
___________ 。
。②干法制备高铁酸钠的化学方程式:
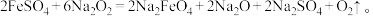 该反应中的氧化产物是
该反应中的氧化产物是 ,转移电子数目为
,转移电子数目为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】N2O、NO和NO2等氮氧化物是空气污染物,含有氮氧化物的尾气需处理后才能排放。
(1)N2O的处理:用特殊催化剂使其分解为对大气友好的气体,则N2O分解的化学方程式为____ 。
(2)NO和NO2的处理:已除去N2O的氮氧化物可用NaOH溶液吸收,主要反应为:
NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO2+NaNO3+H2O。
同一条件下,若V(NO)∶V(NO2)=5∶2的混合气体,通过足量NaOH溶液后,溶液中的溶质为____ (填化学式)。
(3)NO的处理:NO能将酸性的NaClO溶液的还原为Cl-,实验测得100mL1.2mol·L−1 NaClO可以吸收标准状况下1.792LNO气体,则反应的离子方程式为________ 。
(4)一定条件下,氨气可将氮氧化物转化为无毒气体。分析若用氨气转化NO2时,氧化产物与还原产物的质量比为________ 。
(1)N2O的处理:用特殊催化剂使其分解为对大气友好的气体,则N2O分解的化学方程式为
(2)NO和NO2的处理:已除去N2O的氮氧化物可用NaOH溶液吸收,主要反应为:
NO+NO2+2NaOH=2NaNO2+H2O;2NO2+2NaOH=NaNO2+NaNO3+H2O。
同一条件下,若V(NO)∶V(NO2)=5∶2的混合气体,通过足量NaOH溶液后,溶液中的溶质为
(3)NO的处理:NO能将酸性的NaClO溶液的还原为Cl-,实验测得100mL1.2mol·L−1 NaClO可以吸收标准状况下1.792LNO气体,则反应的离子方程式为
(4)一定条件下,氨气可将氮氧化物转化为无毒气体。分析若用氨气转化NO2时,氧化产物与还原产物的质量比为
您最近一年使用:0次
【推荐1】高铁酸钾是一种非氯高效消毒剂,主要用于饮用水处理。高铁酸钾(K2FeO4)在强碱性条件下能够稳定存在。工业上是先制得高铁酸钠,然后在低温下,向高铁酸钠溶液中加入饱和的KOH,使高铁酸钾析出。
(1)方法一:可利用固体反应物反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
①生成物Na2FeO4中铁元素的化合价为________
②该反应中的还原剂是________ ,每生成1mol Na2FeO4转移_______ mol电子。
(2)方法二:
反应:Fe(OH)3+ClO-+OH-——FeO42-+Cl-+H2O(未配平)
①配平离子反应方程式:_____ Fe(OH)3+______ ClO-+_____ OH-=_____ FeO42-+______ Cl-+________ H2O
②若反应过程中转移了3mol电子,则还原产物的物质的量为_______ mol
(3)向Na2FeO4溶液中加入适量饱和的KOH溶液,有K2FeO4析出,请写出该反应的化学方程式________
(1)方法一:可利用固体反应物反应:2FeSO4+6Na2O2=2Na2FeO4+2Na2O+2Na2SO4+O2↑
①生成物Na2FeO4中铁元素的化合价为
②该反应中的还原剂是
(2)方法二:
反应:Fe(OH)3+ClO-+OH-——FeO42-+Cl-+H2O(未配平)
①配平离子反应方程式:
②若反应过程中转移了3mol电子,则还原产物的物质的量为
(3)向Na2FeO4溶液中加入适量饱和的KOH溶液,有K2FeO4析出,请写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】(1)很多含氯物质都能做消毒剂。液氯可以用于饮用水消毒,但是消毒后的水中可能产生危害人体健康的有机氯化物。世界各国陆续开发新型自来水消毒剂,下列物质可以用于自来水消毒的有___ 。
A.Na2O2 B.ClO2 C.O3 D.O2 E.HCl
(2)84消毒液是一种常用消毒剂,其中的有效成分是___ (写出化学式)。高铁酸钠(Na2FeO4)也可以用于作自来水处理剂,高铁酸钠处理过的水中含有氢氧化铁胶体,则高铁酸钠作自来水处理剂的优点是___ 。
(3)漂白粉的质量靠它的“有效氯”衡量。有效氯是根据它同盐酸作用时产生的氯气量来计算的。写出由漂白粉的有效成分Ca(ClO)2和浓HCl发生反应制备Cl2化学方程式:___ 。
生成的微量氯气与氢碘酸反应,可以得到碘单质,反应生成的碘与Na2S2O3可以定量的进行反应:2Na2S2O3+I2=Na2S4O6+2NaI,漂白粉的有效氯= ×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为
×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为___ 。
A.Na2O2 B.ClO2 C.O3 D.O2 E.HCl
(2)84消毒液是一种常用消毒剂,其中的有效成分是
(3)漂白粉的质量靠它的“有效氯”衡量。有效氯是根据它同盐酸作用时产生的氯气量来计算的。写出由漂白粉的有效成分Ca(ClO)2和浓HCl发生反应制备Cl2化学方程式:
生成的微量氯气与氢碘酸反应,可以得到碘单质,反应生成的碘与Na2S2O3可以定量的进行反应:2Na2S2O3+I2=Na2S4O6+2NaI,漂白粉的有效氯=
 ×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为
×100%。漂白粉的有效氯一般高于30.0%,某化工厂漂白粉22.0g进行上述一系列反应进行测定,消耗硫代硫酸钠0.200mol,则其有效氯为
您最近一年使用:0次



