短周期元素 a~g 在表中的位置如右表,请回答下列问题:
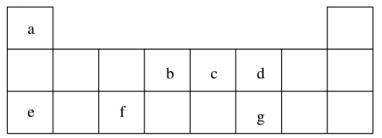
(1)d、e元素常见离子的半径由大到小的顺序为(用化学式表示)__________ ;b、c两元素非金属性较强的是(写元素符号)_________ ,写出能证明这一结论的一个化学方程式_____________ 。
(2)下列有关说法正确的是( )
A.e在 d2 中燃烧,生成e2d
B.加热熔化eda时不可用Al2O3坩埚,可用瓷坩埚
C.将 gd2 通入溴水中,溴水褪色,体现了gd2 的漂白性
D.将打磨过的 f 置于酒精灯上点燃,观察到f 熔化但未见液滴滴落
(3)上述元素可组成盐 R:ca4f(gd4)2和盐S:ca4agd4。
①相同条件下,0.1 mol·L-1盐R中 c(ca4+)_______ (填“=”、 “>”或“<”)0.1 mol·L-1盐S中c(ca4+)。
②R常用作净水剂,其原理为(用离子方程式表示)______________ 。
③向盛有 10 mL 1 mol·L-1盐S溶液的烧杯中滴加1 mol·L-1 NaOH溶液至中性,则反应后各离子浓度由大到小的排列顺序是_____________ 。
④向盛有 10 mL 1 mol·L-1盐R溶液的烧杯中滴加 1 mol·L-1NaOH溶液 32 mL后,继续滴加至35 mL,写出此时段(32 mL~35 mL)间发生的离子方程式:_____________ 。

(1)d、e元素常见离子的半径由大到小的顺序为(用化学式表示)
(2)下列有关说法正确的是
A.e在 d2 中燃烧,生成e2d
B.加热熔化eda时不可用Al2O3坩埚,可用瓷坩埚
C.将 gd2 通入溴水中,溴水褪色,体现了gd2 的漂白性
D.将打磨过的 f 置于酒精灯上点燃,观察到f 熔化但未见液滴滴落
(3)上述元素可组成盐 R:ca4f(gd4)2和盐S:ca4agd4。
①相同条件下,0.1 mol·L-1盐R中 c(ca4+)
②R常用作净水剂,其原理为(用离子方程式表示)
③向盛有 10 mL 1 mol·L-1盐S溶液的烧杯中滴加1 mol·L-1 NaOH溶液至中性,则反应后各离子浓度由大到小的排列顺序是
④向盛有 10 mL 1 mol·L-1盐R溶液的烧杯中滴加 1 mol·L-1NaOH溶液 32 mL后,继续滴加至35 mL,写出此时段(32 mL~35 mL)间发生的离子方程式:
更新时间:2017-10-21 10:54:23
|
相似题推荐
填空题
|
较难
(0.4)
【推荐1】二氧化碳又名碳酸气,具有较高的民用和工业价值,在多种领域有着广泛的应用。目前,二氧化碳在棚菜气肥、蔬菜(肉类)保鲜、生产可降解塑料等也展现良好的发展前景。二氧化碳是一种无色无味的气体,无毒、不导电并且没有可燃性。但是金属镁在点燃的条件下可以在二氧化碳气体中燃烧。其中还原产物是碳
Ⅰ.①氧化产物是___________________
②请写出化学反应方程式,并用单线桥法表示该反应的电子转移总数__________
Ⅱ.CO2气体与碱溶液反应时,用量不同其生成的产物不同。
①少量CO2通入过量的KOH溶液中,请写出离子反应方程式____________________
②取两份等物质的量浓度等体积的Ca(OH)2的溶液,一份通入过量CO2,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图所示
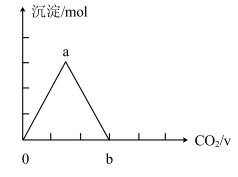
写出沉淀变化由a到b的离子方程式:________________________________
Ⅲ.另一份先加入少量的KOH固体溶解,再将过量CO2通入KOH和Ca(OH)2的混合溶液中,请绘图表示出生成沉淀的物质的量(n)和通入CO2体积(V)的关系___________ ;并写出与图②中不同曲线处对应的离子反应方程式_____________________________
Ⅰ.①氧化产物是
②请写出化学反应方程式,并用单线桥法表示该反应的电子转移总数
Ⅱ.CO2气体与碱溶液反应时,用量不同其生成的产物不同。
①少量CO2通入过量的KOH溶液中,请写出离子反应方程式
②取两份等物质的量浓度等体积的Ca(OH)2的溶液,一份通入过量CO2,生成沉淀的物质的量(n)和通入CO2体积(V)的关系如图所示

写出沉淀变化由a到b的离子方程式:
Ⅲ.另一份先加入少量的KOH固体溶解,再将过量CO2通入KOH和Ca(OH)2的混合溶液中,请绘图表示出生成沉淀的物质的量(n)和通入CO2体积(V)的关系

您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】某实验小组为探究ClO-、I2、SO42-在酸性条件下的氧化性强弱,设计实验如下:
实验①:
在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:
向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式____________________________ 。
(2)实验②中化学反应转移电子的物质的量是_______________________ 。
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是_________________ 。
实验①:
在淀粉碘化钾溶液中加入少量次氯酸钠溶液,并加入少量的稀硫酸,溶液立即变蓝;
实验②:
向实验①的溶液中加入4 mL 0.5 mol/L的亚硫酸钠溶液,蓝色恰好完全褪去。
(1)写出实验①中发生反应的离子方程式
(2)实验②中化学反应转移电子的物质的量是
(3)以上实验说明,在酸性条件下ClO-、I2、SO42-的氧化性由弱到强的顺序是
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】弱电解质有许多,如:醋酸、碳酸、氢氰酸、一水合氨、氢氧化铝、氢氧化铜等。 时,醋酸、碳酸、氢氰酸的电离平衡常数如下表:
时,醋酸、碳酸、氢氰酸的电离平衡常数如下表:
(1) 时,pH相等的三种溶液①
时,pH相等的三种溶液① 溶液、②
溶液、② 溶液、③
溶液、③ 溶液,浓度由大到小的顺序为
溶液,浓度由大到小的顺序为___________ (填序号)。
(2) 时,向
时,向 溶液中通入少量
溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为___________ 。
(3)将浓度为 的
的 与
与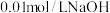 溶液等体积混合,充分反应后混合溶液中
溶液等体积混合,充分反应后混合溶液中
__________ 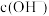 ( “大于”、 “等于”或 “小于”),结合所学知识与必要数据,解释原因:
( “大于”、 “等于”或 “小于”),结合所学知识与必要数据,解释原因:__________ 。
(4)用蒸馏水稀释 的醋酸,下列各式表示的数值随水量的增加而增大的是_____
的醋酸,下列各式表示的数值随水量的增加而增大的是_____
 时,醋酸、碳酸、氢氰酸的电离平衡常数如下表:
时,醋酸、碳酸、氢氰酸的电离平衡常数如下表:| 化学式 | 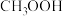 |  |  |
| 电离平衡常数 |  | 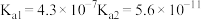 |  |
 时,pH相等的三种溶液①
时,pH相等的三种溶液① 溶液、②
溶液、② 溶液、③
溶液、③ 溶液,浓度由大到小的顺序为
溶液,浓度由大到小的顺序为(2)
 时,向
时,向 溶液中通入少量
溶液中通入少量 ,反应的离子方程式为
,反应的离子方程式为(3)将浓度为
 的
的 与
与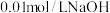 溶液等体积混合,充分反应后混合溶液中
溶液等体积混合,充分反应后混合溶液中
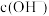 ( “大于”、 “等于”或 “小于”),结合所学知识与必要数据,解释原因:
( “大于”、 “等于”或 “小于”),结合所学知识与必要数据,解释原因:(4)用蒸馏水稀释
 的醋酸,下列各式表示的数值随水量的增加而增大的是_____
的醋酸,下列各式表示的数值随水量的增加而增大的是_____A. | B. | C.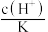 | D. |
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】物质在水中存在电离平衡、水解平衡。请根据所学知识回答:
(1)次磷酸( )是一种精细化工产品,向10mL
)是一种精细化工产品,向10mL  溶液中加入20mL等物质的量浓度的NaOH溶液后,所得的溶液中只有
溶液中加入20mL等物质的量浓度的NaOH溶液后,所得的溶液中只有 、
、 两种阴离子。
两种阴离子。
①写出 溶液与足量NaOH溶液反应后形成的正盐的化学式:
溶液与足量NaOH溶液反应后形成的正盐的化学式:___________ 。
②常温下,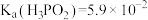 ,0.1mol/L的
,0.1mol/L的 溶液在加水稀释过程中,下列表达式的数据一定变小的是
溶液在加水稀释过程中,下列表达式的数据一定变小的是___________ (填序号)。
A. B.
B. C.
C.
(2)25℃时,HF的电离常数为 ;
; 的电离常数为
的电离常数为 ,
,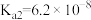 ,
, 。在
。在 溶液加入过量NaF溶液的离子反应方程式为
溶液加入过量NaF溶液的离子反应方程式为___________ 。
(3)盐碱地(含较多 、NaCl)不利于植物生长,盐碱地呈碱性的原因:
、NaCl)不利于植物生长,盐碱地呈碱性的原因:___________ (用离子方程式说明);已知25℃时,H2CO3的Ka1= 4.3×10-7,Ka2= 5×10-11 ,则当 溶液中
溶液中 时,溶液的pH=
时,溶液的pH=___________ 。
(4)某温度下,水的离子积常数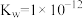 。该温度下,将pH=1的HCl溶液与pH=10的NaOH溶液混合并保持恒温,忽略混合前后溶液体积的变化。欲使混合溶液pH=3,则盐酸溶液与NaOH溶液的体积比为
。该温度下,将pH=1的HCl溶液与pH=10的NaOH溶液混合并保持恒温,忽略混合前后溶液体积的变化。欲使混合溶液pH=3,则盐酸溶液与NaOH溶液的体积比为___________ 。
(5)相同物质的量浓度的五种溶液:① 、②氨水、③
、②氨水、③ 、④
、④ 、⑤
、⑤ ,
, 由大到小顺序是
由大到小顺序是___________ (用序号表示)。
(1)次磷酸(
 )是一种精细化工产品,向10mL
)是一种精细化工产品,向10mL  溶液中加入20mL等物质的量浓度的NaOH溶液后,所得的溶液中只有
溶液中加入20mL等物质的量浓度的NaOH溶液后,所得的溶液中只有 、
、 两种阴离子。
两种阴离子。①写出
 溶液与足量NaOH溶液反应后形成的正盐的化学式:
溶液与足量NaOH溶液反应后形成的正盐的化学式:②常温下,
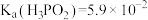 ,0.1mol/L的
,0.1mol/L的 溶液在加水稀释过程中,下列表达式的数据一定变小的是
溶液在加水稀释过程中,下列表达式的数据一定变小的是A.
 B.
B. C.
C.
(2)25℃时,HF的电离常数为
 ;
; 的电离常数为
的电离常数为 ,
,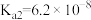 ,
, 。在
。在 溶液加入过量NaF溶液的离子反应方程式为
溶液加入过量NaF溶液的离子反应方程式为(3)盐碱地(含较多
 、NaCl)不利于植物生长,盐碱地呈碱性的原因:
、NaCl)不利于植物生长,盐碱地呈碱性的原因: 溶液中
溶液中 时,溶液的pH=
时,溶液的pH=(4)某温度下,水的离子积常数
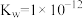 。该温度下,将pH=1的HCl溶液与pH=10的NaOH溶液混合并保持恒温,忽略混合前后溶液体积的变化。欲使混合溶液pH=3,则盐酸溶液与NaOH溶液的体积比为
。该温度下,将pH=1的HCl溶液与pH=10的NaOH溶液混合并保持恒温,忽略混合前后溶液体积的变化。欲使混合溶液pH=3,则盐酸溶液与NaOH溶液的体积比为(5)相同物质的量浓度的五种溶液:①
 、②氨水、③
、②氨水、③ 、④
、④ 、⑤
、⑤ ,
, 由大到小顺序是
由大到小顺序是
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐2】在日常生活中,为了达到更好的清洁效果,经常有人会将洁厕液(含有盐酸)与84消毒液混合使用,从而引发中毒的事故。
(1)两种日化产品的主要成分中都含有氯元素,该元素在元素周期表中的位置是_______________ 。
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式:________________________ 。
(3)洁厕液的主要成分是盐酸.下列关于卤化氢性质的比较中,错误的是________ 。
A.酸性:
B.稳定性:
C.熔点:
D.还原性:
(4)常温下,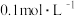 的NaClO溶液的
的NaClO溶液的 ,原因是
,原因是________________________________ (用方程式解释).常温下HClO的电离平衡常数为________ 。洁厕液与84消毒液混合后会生成有毒的氯气,写出该反应的离子方程式:____________________________ 。
(5)高铁酸钾(K2FeO4)是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产:
①在碱性条件下,利用NaClO氧化硝酸铁,制得K2FeO4,该反应的离子方程式为___________ 。
②K2FeO4与KOH反应生成 。K2FeO4在水溶液中易水解:
。K2FeO4在水溶液中易水解: ,在“提纯”K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
,在“提纯”K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用________ 溶液(填序号)。
A.水
B.NH4Cl、2-甲基-2-丙醇
C.Fe(NO3)3、2-甲基-2-丙醇
D.CH3COONa、2-甲基-2-丙醇
(6)消毒效率是单位质量物质得到的电子数,则 与NaClO两种消毒剂的消毒效率之比为
与NaClO两种消毒剂的消毒效率之比为________ 。
(1)两种日化产品的主要成分中都含有氯元素,该元素在元素周期表中的位置是
(2)84消毒液的主要成分是次氯酸钠,写出次氯酸钠的电子式:
(3)洁厕液的主要成分是盐酸.下列关于卤化氢性质的比较中,错误的是
A.酸性:

B.稳定性:

C.熔点:

D.还原性:

(4)常温下,
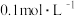 的NaClO溶液的
的NaClO溶液的 ,原因是
,原因是(5)高铁酸钾(K2FeO4)是一种高效多功能水处理剂,工业上常采用NaClO氧化法生产:
①在碱性条件下,利用NaClO氧化硝酸铁,制得K2FeO4,该反应的离子方程式为
②K2FeO4与KOH反应生成
 。K2FeO4在水溶液中易水解:
。K2FeO4在水溶液中易水解: ,在“提纯”K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用
,在“提纯”K2FeO4时采用重结晶、洗涤、低温烘干的方法,则洗涤剂最好选用A.水
B.NH4Cl、2-甲基-2-丙醇
C.Fe(NO3)3、2-甲基-2-丙醇
D.CH3COONa、2-甲基-2-丙醇
(6)消毒效率是单位质量物质得到的电子数,则
 与NaClO两种消毒剂的消毒效率之比为
与NaClO两种消毒剂的消毒效率之比为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐3】25℃时,如果取0.1 mol·L-1HA溶液与0.1 mol·L-1NaOH溶液等体积混合(混合后溶液体积的变化不计),测得混合溶液的pH=8,试回答以下问题:
(1)混合溶液的pH=8的原因_______ (用离子方程式表示);
(2)混合溶液中由水电离出的c(H+)_______ 0.1 mol·L-1 NaOH溶液中由水电离出的c(H+);(填>、<、=)
(3)将混合溶液从25 ℃升温至30 ℃,溶液中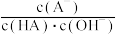 将
将 _______ (填增大或减小)
(4)求出混合液中下列算式的计算结果(填具体数字):c (HA)+c (A-)=_______ mol·L-1;
(5)若向0.1 mol·L-1HA溶液中加入少量水,溶液中 将
将_______ (填增大或减小)
(6)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,将相同温度下相同浓度的四种盐溶液:A.NH4HCO3;B.NH4A;C.(NH4)2SO4;D.NH4Cl,按pH由大到小的顺序排列_______ (填序号)
(1)混合溶液的pH=8的原因
(2)混合溶液中由水电离出的c(H+)
(3)将混合溶液从25 ℃升温至30 ℃,溶液中
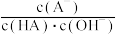 将
将 (4)求出混合液中下列算式的计算结果(填具体数字):c (HA)+c (A-)=
(5)若向0.1 mol·L-1HA溶液中加入少量水,溶液中
 将
将(6)已知NH4A溶液为中性,又知将HA溶液加到Na2CO3溶液中有气体放出,将相同温度下相同浓度的四种盐溶液:A.NH4HCO3;B.NH4A;C.(NH4)2SO4;D.NH4Cl,按pH由大到小的顺序排列
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
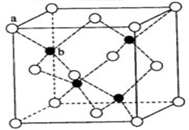
【推荐1】硫化锌荧光材料的研究从1868年法国化学家Sidot发现至今已有近150年的历史。其中立方硫化锌的晶胞如图所示。请回答下列问题:
(1)锌元素在周期表中的位于第______ 周期_____ 族, 属于_____ 区;
(2)基态锌原子的价电子排布式为_________ ;
(3)一般锌元素常表现为+2 价的原因是_____ ;
(4)立方硫化锌晶体的每个晶胞中含有_____ 个锌离子, 其配位数为_____ ;含有_____ 个硫离子,其配位数为_____ ;
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,其晶胞边长为540.0 pm,密度为_________ g·cm-3(列式并计算),a位置S2-离子与b位置Zn2+离子之间的距离为_____ pm(列式表示)。

(1)锌元素在周期表中的位于第
(2)基态锌原子的价电子排布式为
(3)一般锌元素常表现为+2 价的原因是
(4)立方硫化锌晶体的每个晶胞中含有
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛。立方ZnS晶体结构如下图所示,其晶胞边长为540.0 pm,密度为
您最近一年使用:0次
填空题
|
较难
(0.4)
【推荐2】(1)已知CuCl2溶液与乙二胺H2N-CH2CH2-NH2[常用(en)表示]作用,可形成配离子(如图所示):
请回答下列问题︰
①乙二胺分子中N原子成键时采取的杂化类型是____________ ,
乙二胺沸点高于Cl-CH2CH2-Cl的主要原因是___________________________ 。
②上述配离子中含有的化学键类型有:__________________ 。(填写代码,多选) ;
a配位键 b极性键 c非极性键 d离子键
③该配合物 [Cu(en)2]Cl2的系统命名为_______ ;其中铜离子的配位数是_______ 。
(2)下表中实线是元素周期表的部分边界,其中上边界未用实线标出。

根据信息回答下列问题:
①周期表中基态Ga原子的最外层电子排布式为__________________
②Fe元素位于周期表的_____ 区;Fe与CO易形成配合物Fe(CO)5,在Fe(CO)5中铁的化合价为____ ;
已知:原子数目和电子总数(或价电子总数)相同的粒子互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为______ 和______ (填化学式)。
③根据VSEPR理论预测ED4-离子的空间构型为_________ 。B、C、D、E原子相互化合形成的分子中,所有原子都满足最外层8电子稳定结构的化学式为____________ (写2种)。

请回答下列问题︰
①乙二胺分子中N原子成键时采取的杂化类型是
乙二胺沸点高于Cl-CH2CH2-Cl的主要原因是
②上述配离子中含有的化学键类型有:
a配位键 b极性键 c非极性键 d离子键
③该配合物 [Cu(en)2]Cl2的系统命名为
(2)下表中实线是元素周期表的部分边界,其中上边界未用实线标出。

根据信息回答下列问题:
①周期表中基态Ga原子的最外层电子排布式为
②Fe元素位于周期表的
已知:原子数目和电子总数(或价电子总数)相同的粒子互为等电子体,等电子体具有相似的结构特征。与CO分子互为等电子体的分子和离子分别为
③根据VSEPR理论预测ED4-离子的空间构型为
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
【推荐1】填写下列空格。
(1)已知拆开1molH-H键、1molCl-Cl键、1molH-Cl键分别需要吸收的能量为436.4kJ、242.7kJ、431.8kJ。则由H2和Cl2反应生成1molHCl需要_____ (填“放出”或“吸收”)____ kJ的热量。
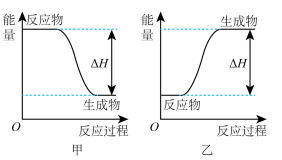
(2)H2可以在Cl2中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图_____ (填“甲”或“乙”)。
(3)已知:H2与Cl2在光照条件下会发生爆炸。同温同压下,反应H2(g)+Cl2(g)=2HCl(g)。在光照和点燃条件下的∆H_____ (填“相等”或“不相等”)。
(4)硅、磷、硫、氯元素的气态氢化物的形成条件和热稳定性如下表所示:
结合元素原子结构等知识,分析以上信息可得出的结论是:同周期非金属元素,随着元素核电荷数的递增,____________________________________ ,因此,Si、P、S、Cl非金属性依次增强。
(1)已知拆开1molH-H键、1molCl-Cl键、1molH-Cl键分别需要吸收的能量为436.4kJ、242.7kJ、431.8kJ。则由H2和Cl2反应生成1molHCl需要
(2)H2可以在Cl2中安静地燃烧。甲、乙两图中,能表示该反应能量变化的是图

(3)已知:H2与Cl2在光照条件下会发生爆炸。同温同压下,反应H2(g)+Cl2(g)=2HCl(g)。在光照和点燃条件下的∆H
(4)硅、磷、硫、氯元素的气态氢化物的形成条件和热稳定性如下表所示:
| 元素符号 | Si | P | S | Cl |
| 单质与氢气的反应 | 高温下反应 | 磷蒸气与氢气能反应 | 加热时反应 | 光照或点燃时发生爆炸而化合 |
| 气态氢化物的热稳定性 | 不稳定 | 不稳定 | 受热分解 | 稳定 |
您最近一年使用:0次
填空题
|
较难
(0.4)
名校
解题方法
【推荐2】现有a~i 9种短周期元素,它们在同期表中的位置如下,请据此回答下列问题:(请用具体的元素符号及化学用语作答)
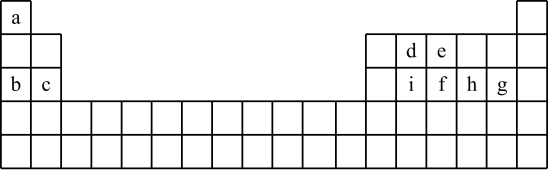
(1)a~i元素中,金属性最强的是________ ,最高价氧化物对应水化物中,酸性最强的物质是___________ 。g所在族的元素形成的氢化物中沸点最低的是____________________ 。
(2)比较b、e、g简单离子半径的大小___________________ (用离子符号作答)。
(3)写出由a~i 9种元素中的某些元素形成,且所有原子都满足最外层为8电子结构的任意两种化合物的化学式__________________ 、___________________ 。
(4)用一个化学反应方程式表示d的非金属性强于i_______________________________ 。
(5)由于在周期表中位置相近的元素性质相近,启发了人们在周期表中的一定区域内寻找新的物质。人们在周期表里金属和非金属的交界处找到了半导体材料。
①下列单质中,不能做半导体材料的物质是______ (填序号)。
A.Si B.Ge C.S
②砷(As)是e的同族元素,上比e多2个电子层,砷的一种核素含有42个中子,该核素的符号_________ ;镓(Ga)与As同周期,最外层有3个电子,Ga与As可以形成一种新型化合物半导体材料,其性能更优越。这种新型化合物化学式为____________________ 。
(6)c与a形成的化合物的电子式为___________ ,用电子式表示a与h形成a2h的过程__________________________________________ 。
(7)根据周期表对角线法则,金属Be和Al单质及化合物性质相似。试写出Be和氢氧化钠溶液反应的离子方程式_________________________________ 。

(1)a~i元素中,金属性最强的是
(2)比较b、e、g简单离子半径的大小
(3)写出由a~i 9种元素中的某些元素形成,且所有原子都满足最外层为8电子结构的任意两种化合物的化学式
(4)用一个化学反应方程式表示d的非金属性强于i
(5)由于在周期表中位置相近的元素性质相近,启发了人们在周期表中的一定区域内寻找新的物质。人们在周期表里金属和非金属的交界处找到了半导体材料。
①下列单质中,不能做半导体材料的物质是
A.Si B.Ge C.S
②砷(As)是e的同族元素,上比e多2个电子层,砷的一种核素含有42个中子,该核素的符号
(6)c与a形成的化合物的电子式为
(7)根据周期表对角线法则,金属Be和Al单质及化合物性质相似。试写出Be和氢氧化钠溶液反应的离子方程式
您最近一年使用:0次
填空题
|
较难
(0.4)
解题方法
【推荐3】2015年8月12日晚,天津滨海新区某公司仓库发生爆炸,事发仓库里存放了大量的硝酸铵、氰化钠(NaCN)、金属钠等危险化学品。回答下列问题:
(1)NaCN的电子式为:_______________________ 。
(2)金属钠属于危化品中的易燃固体,其着火时不能用水灭火,请用化学方程式解释其原因:_____________________________ 。
(3)氰化钠是一种重要的化工原料,也是剧毒危险品,皮肤伤口接触、吸入、吞食微量可中毒死亡。氰化钠易溶于水,水溶液呈强碱性。氰化钠泄漏可用双氧水或硫代硫酸钠中和。
①用离子方程式表示氰化钠水溶液呈强碱性的原因:______________________________ 。
②用双氧水处理产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,请写出该反应的化学方程式_____________________________ ;
③用硫代硫酸钠中和的离子方程式为CN-+ →A+
→A+ (已配平),A为
(已配平),A为_________ (填化学式)。
(4)CN-中C元素显+2价,N元素显﹣3价,则非金属性N_______ C(填<、=或>),请用简单的实验方法证明(要求说明简单操作、现象和结论):_______________________________________ 。
(5)0.4mol/L的NaCN和0.2mol/L的HCl等体积混合,溶液显碱性,其溶液中离子浓度大小排列顺序是_______________________________________
(1)NaCN的电子式为:
(2)金属钠属于危化品中的易燃固体,其着火时不能用水灭火,请用化学方程式解释其原因:
(3)氰化钠是一种重要的化工原料,也是剧毒危险品,皮肤伤口接触、吸入、吞食微量可中毒死亡。氰化钠易溶于水,水溶液呈强碱性。氰化钠泄漏可用双氧水或硫代硫酸钠中和。
①用离子方程式表示氰化钠水溶液呈强碱性的原因:
②用双氧水处理产生一种酸式盐和一种能使湿润的红色石蕊试纸变蓝的气体,请写出该反应的化学方程式
③用硫代硫酸钠中和的离子方程式为CN-+
 →A+
→A+ (已配平),A为
(已配平),A为(4)CN-中C元素显+2价,N元素显﹣3价,则非金属性N
(5)0.4mol/L的NaCN和0.2mol/L的HCl等体积混合,溶液显碱性,其溶液中离子浓度大小排列顺序是
您最近一年使用:0次

 是一种锂离子电池的正极材料。用
是一种锂离子电池的正极材料。用 在一定条件下可制得
在一定条件下可制得 在周期表中的位置
在周期表中的位置 时,固体残留率为
时,固体残留率为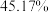 ,写出残留固体(
,写出残留固体( )的化学式
)的化学式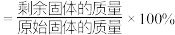 )。
)。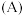 与
与 混合并在空气中煅烧,反应生成
混合并在空气中煅烧,反应生成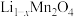 ,为测定
,为测定 的值。称取
的值。称取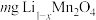 固体,经一系列化学处理,将锂全部转化为
固体,经一系列化学处理,将锂全部转化为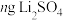 ,写出
,写出

