一定温度下,向容积为2 L的密闭容器中通入两种气体发生化学反应,反应中各物质(A、B、C、D)的物质的量变化如图所示,对该反应的推断合理的是
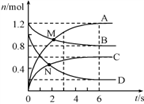

| A.M点表示v(A)=v(B) |
| B.0~6 s内,v(A)∶v(B)∶v(C)∶v(D)=3∶1∶1.5∶2 |
| C.反应进行到6 s时,各物质的物质的量浓度相等 |
| D.反应进行到6 s时,C的平均反应速率为 0.1 mol·L-1·s-1 |
17-18高二上·河南安阳·阶段练习 查看更多[3]
更新时间:2018-01-02 19:19:59
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】在25℃时,固定容积的密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表,建立平衡需要的时间为20 s,则下列说法不正确的是( )
| 物质 | X | Y | Z |
| 初始浓度/(mol·L-1) | 0.2 | 0.1 | 0.1 |
| 平衡浓度/(mol·L-1) | 0.05 | 0.05 | 0.2 |
A.反应可表示为3X+Y  2Z 2Z |
| B.建立平衡过程中,用Z表示的反应速率为v(Z)=0.005 mol·L-1·s-1 |
| C.达平衡后,X、Y浓度分别增加0.35 mol·L-1和0.15 mol·L-1,平衡正移,X的转化率变小 |
| D.若初始浓度:X为0.2 mol·L-1,Y为0.2 mol·L-1,Z为0.8mol·L-1,则v正>v逆 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】一定温度下,向容积为2 L的密闭容器中通入气体X、Y、Z,反应中各物质的物质的量变化如图所示,对该反应的推断合理的是
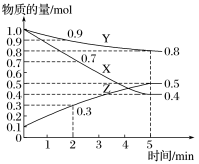

A.该反应的化学方程式为2X+Y 2Z 2Z |
| B.反应开始至2min时,Z的平均反应速率为0.1 mol·L-1·min-1 |
| C.该反应为可逆反应 |
| D.4min时,X、Z的速率相等 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】为减小 对环境的影响,在倡导“低碳”的同时,还需加强对
对环境的影响,在倡导“低碳”的同时,还需加强对 创新利用的研究.
创新利用的研究. 时,将
时,将 和
和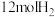 充入3L密闭容器中,发生反应
充入3L密闭容器中,发生反应 ,
,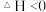 ,容器中
,容器中 的物质的量随时间变化如曲线I所示,平衡时容器内压强为仍为
的物质的量随时间变化如曲线I所示,平衡时容器内压强为仍为 ,改变某一条件重新进行上述反应,
,改变某一条件重新进行上述反应, 的物 质的量随时间变化如曲线Ⅱ所示。下列说法错误的是( )
的物 质的量随时间变化如曲线Ⅱ所示。下列说法错误的是( )

 对环境的影响,在倡导“低碳”的同时,还需加强对
对环境的影响,在倡导“低碳”的同时,还需加强对 创新利用的研究.
创新利用的研究. 时,将
时,将 和
和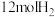 充入3L密闭容器中,发生反应
充入3L密闭容器中,发生反应 ,
,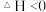 ,容器中
,容器中 的物质的量随时间变化如曲线I所示,平衡时容器内压强为仍为
的物质的量随时间变化如曲线I所示,平衡时容器内压强为仍为 ,改变某一条件重新进行上述反应,
,改变某一条件重新进行上述反应, 的物 质的量随时间变化如曲线Ⅱ所示。下列说法错误的是( )
的物 质的量随时间变化如曲线Ⅱ所示。下列说法错误的是( )
| A.曲线Ⅱ对应的条件改变是增大压强 |
B. 时,上述反应平衡常数为 时,上述反应平衡常数为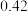 ,则 ,则 |
C.在 ,若起始时向容器中充入5 mol ,若起始时向容器中充入5 mol  、5 mol 、5 mol  、5 mol 、5 mol  和 5 mol 和 5 mol  ,则达平衡前 ,则达平衡前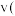 正 正 逆 逆 |
D.在 ,若起始时向容器由充入 ,若起始时向容器由充入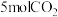 、6mol 、6mol  ,平衡时容器内压强 ,平衡时容器内压强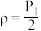 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向某密闭容器中加入 0.3 mol A、0.1 mol C 和一定量的 B 三种气体, 一定条件下发生如下反应:3A(g)  B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是
B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是

 B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是
B(g)+2C(g),各物质的浓度随时间变化如图所示[t0~t1 阶段的 c(B)变化未画出]。下列说法中正确的是
| A.若t1=15s, A 的浓度变化表示 t0~t1阶段的平均反应速率为 0.09 mol·L-1·s-1 |
B.t0~t1阶段,此过程中容器放出a kJ热量,该反应的热化学方程式为:3A(g) B(g)+2C(g) ΔH=-50a kJ·mol-1 B(g)+2C(g) ΔH=-50a kJ·mol-1 |
| C.该容器的容积为2 L,B的起始的物质的量为0.03 mol |
| D.t1时该反应达到平衡且A 的转化率为60% |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】开发CO2催化加氢可合成二甲醚。其主要反应为:
① CO2(g)+ 3H2(g) CH3OH(g) + H2O(g) ΔH1 =﹣49.01 kJ·mol−1
CH3OH(g) + H2O(g) ΔH1 =﹣49.01 kJ·mol−1
② 2CH3OH(g) CH3OCH3(g) + H2O(g) ΔH2 =﹣24.52 kJ·mol−1
CH3OCH3(g) + H2O(g) ΔH2 =﹣24.52 kJ·mol−1
合成二甲醚时还会发生副反应:
③ CO2(g)+ H2(g) CO(g) + H2O(g) ΔH3 = + 41.2 kJ·mol−1
CO(g) + H2O(g) ΔH3 = + 41.2 kJ·mol−1
其他条件相同时,反应温度对CO2平衡总转化率及反应2.5小时的CO2实际总转化率影响如图1所示;反应温度对二甲醚的平衡选择性及反应2.5小时的二甲醚实际选择性影响如图2所示。(已知:CH3OCH3的选择性= ×100%)。
×100%)。

下列说法正确的是
① CO2(g)+ 3H2(g)
 CH3OH(g) + H2O(g) ΔH1 =﹣49.01 kJ·mol−1
CH3OH(g) + H2O(g) ΔH1 =﹣49.01 kJ·mol−1② 2CH3OH(g)
 CH3OCH3(g) + H2O(g) ΔH2 =﹣24.52 kJ·mol−1
CH3OCH3(g) + H2O(g) ΔH2 =﹣24.52 kJ·mol−1合成二甲醚时还会发生副反应:
③ CO2(g)+ H2(g)
 CO(g) + H2O(g) ΔH3 = + 41.2 kJ·mol−1
CO(g) + H2O(g) ΔH3 = + 41.2 kJ·mol−1其他条件相同时,反应温度对CO2平衡总转化率及反应2.5小时的CO2实际总转化率影响如图1所示;反应温度对二甲醚的平衡选择性及反应2.5小时的二甲醚实际选择性影响如图2所示。(已知:CH3OCH3的选择性=
 ×100%)。
×100%)。
下列说法正确的是
| A.不改变反应时间和温度,增大压强或增大CO2与H2的投料比都能进一步提高CO2实际总转化率和二甲醚实际选择性 |
| B.CO2催化加氢合成二甲醚的最佳温度为240℃左右 |
| C.温度高于290℃,CO2平衡总转化率随温度升高而上升的原因为反应①进行程度大于反应③ |
| D.一定温度下,加入多孔CaO(s)或选用高效催化剂,均能提高平衡时H2的转化率 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】一定温度下,恒容密闭容器充入一定量的丙烷发生反应: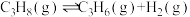
 。总压强分别为P1和P2时,上述反应在不同温度下达到平衡,测得丙烷及丙烯的物质的量分数如图所示,下列说法正确的是
。总压强分别为P1和P2时,上述反应在不同温度下达到平衡,测得丙烷及丙烯的物质的量分数如图所示,下列说法正确的是

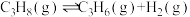
 。总压强分别为P1和P2时,上述反应在不同温度下达到平衡,测得丙烷及丙烯的物质的量分数如图所示,下列说法正确的是
。总压强分别为P1和P2时,上述反应在不同温度下达到平衡,测得丙烷及丙烯的物质的量分数如图所示,下列说法正确的是
A. | B. |
| C.Q点,丙烷的平衡转化率为33.3% | D.556℃时,反应的平衡常数为0.125 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】用活性炭还原NO2可防止空气污染,其反应原理为2C(s)+2NO2(g) N2(g)+2CO2(g)。在密闭容器中1mol NO2和足量C发生上述反应,反应相同时间内测得 NO2的生成速率与 N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内得 NO2的转化率随压强的变化如图2所示。
N2(g)+2CO2(g)。在密闭容器中1mol NO2和足量C发生上述反应,反应相同时间内测得 NO2的生成速率与 N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内得 NO2的转化率随压强的变化如图2所示。
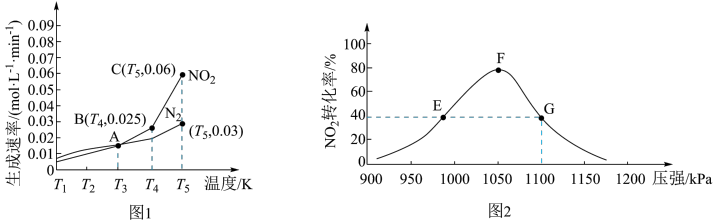
下列说法正确的是
 N2(g)+2CO2(g)。在密闭容器中1mol NO2和足量C发生上述反应,反应相同时间内测得 NO2的生成速率与 N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内得 NO2的转化率随压强的变化如图2所示。
N2(g)+2CO2(g)。在密闭容器中1mol NO2和足量C发生上述反应,反应相同时间内测得 NO2的生成速率与 N2的生成速率随温度变化的关系如图1所示;维持温度不变,反应相同时间内得 NO2的转化率随压强的变化如图2所示。 
下列说法正确的是
A.图1中的A、B、C三个点中只有A点的 正= 正= 逆 逆 |
B.图2中E点的 逆大于F点的 逆大于F点的 正 正 |
| C.图2中平衡常数K(E)=K(G),则NO2的平衡浓度c(E)=c(G) |
| D.G点时NO2的分压为550kPa |
您最近一年使用:0次


 ,某温度下在容积不变的密闭容器中通入NO和CO,不同时间NO和CO的浓度如下表.下列说法中不正确的是
,某温度下在容积不变的密闭容器中通入NO和CO,不同时间NO和CO的浓度如下表.下列说法中不正确的是


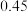

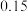

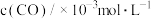
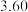

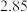
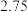





 molNO,
molNO,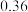 molCO,重新达平衡后CO浓度比原平衡大
molCO,重新达平衡后CO浓度比原平衡大

