(1)在标准状况下,由CO和CO2组成的混合气体6.72 L,质量为12 g。则混合气体中CO的体积分数为_________________ 。
(2)某物质A加热时按化学方程式2A = 2B+C+3D分解,产物均为气体,测得由生成物组成的混合物气体对H2的相对密度为20,则反应物A的摩尔质量为_________________ 。
(3)用质量分数为36.5%的浓盐酸(密度为1.25 g·cm-3)在容量瓶中配制240 mL1mol·L-1的稀盐酸。经计算需要_____________ mL浓盐酸。
(4)汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则生成标准状况下N2 的体积为_________________ L。
(2)某物质A加热时按化学方程式2A = 2B+C+3D分解,产物均为气体,测得由生成物组成的混合物气体对H2的相对密度为20,则反应物A的摩尔质量为
(3)用质量分数为36.5%的浓盐酸(密度为1.25 g·cm-3)在容量瓶中配制240 mL1mol·L-1的稀盐酸。经计算需要
(4)汽车剧烈碰撞时,安全气囊中发生反应10NaN3+2KNO3=K2O+5Na2O+16N2↑。若氧化产物比还原产物多1.75mol,则生成标准状况下N2 的体积为
更新时间:2018-01-17 10:17:50
|
相似题推荐
计算题
|
适中
(0.65)
【推荐1】工业上通常采用将氯气通入消石灰或石灰乳的方法制取漂白粉。消石灰要含略少于1%(质量分数)的水,因为极为干燥的消石灰是不跟氯气反应的。生产漂白粉的反应过程比较复杂,可发生如下反应:
①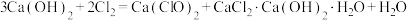 ;
;
②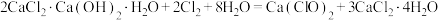 。
。
回答下列问题:
(1) 的摩尔质量为
的摩尔质量为__________ , 中质量分数最大的元素为
中质量分数最大的元素为__________ (填元素符号)。
(2)所含氢原子总数为 的
的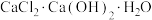 的物质的量为
的物质的量为__________ ,该化合物中Ca元素的物质的量为__________ 。
(3)反应②中,每转移 电子,此时消耗
电子,此时消耗 的体积约为
的体积约为__________ (标准状况下)。
(4)同温同压下,氯化氢与氯气两种气体的密度之比为__________ 。
①
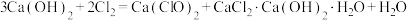 ;
;②
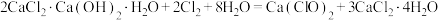 。
。回答下列问题:
(1)
 的摩尔质量为
的摩尔质量为 中质量分数最大的元素为
中质量分数最大的元素为(2)所含氢原子总数为
 的
的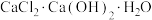 的物质的量为
的物质的量为(3)反应②中,每转移
 电子,此时消耗
电子,此时消耗 的体积约为
的体积约为(4)同温同压下,氯化氢与氯气两种气体的密度之比为
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐2】Ⅰ.(1)标准状况下,1.92 g某气体的体积为672 mL,则此气体的相对分子质量为________ 。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为______________ 。
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为________ 。
Ⅱ.在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为ρ g·cm-3,计算该溶液的浓度(用以上字母表示)。
(1)该溶液的物质的量浓度________________
(2)该溶液的质量分数_________________________
Ⅲ.有两份溶液,其中所含溶质相同,设其摩尔质量为M g·mol-1。根据下表信息,回答有关问题:
(1)取等质量两份溶液混合,则所得混合液中溶质的质量分数w3=________ 。(用以上字母表示)
(2)若有w1>w2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为w4,若ρ1>ρ2,则w3___ w4;若ρ1<ρ2,w3______ w4(填“>”“<”或“=”)。
(2)在25 ℃、101 kPa的条件下,同质量的CH4和A气体的体积之比是15∶8,则A的摩尔质量为
(3)两个相同容积的密闭容器X、Y,在25 ℃下,X中充入a g A气体,Y中充入a g CH4气体,X与Y内的压强之比是4∶11,则A的摩尔质量为
Ⅱ.在标准状况下,将aLNH3完全溶于水得到VmL氨水,溶液的密度为ρ g·cm-3,计算该溶液的浓度(用以上字母表示)。
(1)该溶液的物质的量浓度
(2)该溶液的质量分数
Ⅲ.有两份溶液,其中所含溶质相同,设其摩尔质量为M g·mol-1。根据下表信息,回答有关问题:
| 溶质的质量分数 | 溶液的密度(g·cm-3) | |
| 第一份溶液 | w1 | ρ1 |
| 第二份溶液 | w2 | ρ2 |
(1)取等质量两份溶液混合,则所得混合液中溶质的质量分数w3=
(2)若有w1>w2,取等体积的两份溶液混合,设所得混合液中溶质的质量分数为w4,若ρ1>ρ2,则w3
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】请回答下列问题:
(1)3.01×1023个CO2在标准状况下的体积约为______ L,它与_____ g H2O含有相同的氧原子数。
(2)23.75 g某+2价金属的氯化物(MCl2)中含有3.01×1023个Cl-,则MCl2的摩尔质量为______ , M的相对原子质量为________ 。
(3)某气体在同温同压下相对H2相对密度为32,则该气体的相对分子质量为__________ 。
(4)在标准状况下22.4 L由氮气和氧气组成的混合气体,其质量为30g,则其中氧气的质量为________ g。
(1)3.01×1023个CO2在标准状况下的体积约为
(2)23.75 g某+2价金属的氯化物(MCl2)中含有3.01×1023个Cl-,则MCl2的摩尔质量为
(3)某气体在同温同压下相对H2相对密度为32,则该气体的相对分子质量为
(4)在标准状况下22.4 L由氮气和氧气组成的混合气体,其质量为30g,则其中氧气的质量为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】现有14.4 g CO和CO2的混合气体,在标准状况下所占的体积约为8.96 L。回答下列问题:
(1)该混合气体中CO物质的量为________ ;CO2物质的量为_________ 。
(2)混合气体中碳原子的个数___________ 。(用NA表示阿伏加 德罗常数的值)
(3)将混合气体依次通过如图装置,最后收集在气球中。
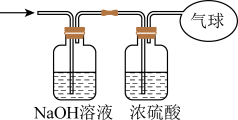
①气球中收集到的气体的摩尔质量_________ ;
②标况下气球中收集到的气体的体积为________________ ;
③气球中收集到的气体的电子总数为________ 。(用NA表示阿伏加 德罗常数的值)
(1)该混合气体中CO物质的量为
(2)混合气体中碳原子的个数
(3)将混合气体依次通过如图装置,最后收集在气球中。

①气球中收集到的气体的摩尔质量
②标况下气球中收集到的气体的体积为
③气球中收集到的气体的电子总数为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】5.1镁铝混合物放入足量氢氧化钠溶液中充分反应后,生成气体在标准状况的体积为2.24L。
计算:(请写详细的计算步骤)
(1)混合物中含有镁的质量为多少克____________ ?
(2)若反应完成后,溶液体积为50mL,则溶液中含铝化合物的物质的量浓度为多少?______
计算:(请写详细的计算步骤)
(1)混合物中含有镁的质量为多少克
(2)若反应完成后,溶液体积为50mL,则溶液中含铝化合物的物质的量浓度为多少?
您最近一年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】现有以下物质:①H2SO4;②液氨;③KOH固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥银;⑦SO2;⑧CH3COOH;⑨蔗糖;⑩苯;⑪酒精。请回答下列问题:
(1)以上物质中能导电的是_______ (填序号),以上物质中属于电解质的是_______ (填序号)。以上物质中属于非电解质的是_______ (填序号)。
(2)某物质A加热时按化学方程式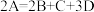 分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对
分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对 的相对密度为40,则反应物A的摩尔质量为
的相对密度为40,则反应物A的摩尔质量为_______ 。
(3)质量比为11:7:16的 、CO、
、CO、 ,它们所含分子数之比为
,它们所含分子数之比为_______ ,所含氧原子数之比为_______ 。
(4)标准状况下有①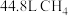 ,②
,② 个
个 分子,③
分子,③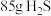 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是_______ 。(填序号)
(5)在标准状况下,用干燥的烧瓶装满一瓶氯化氢和氢气的混合气体倒置于水槽中,此时烧瓶中盐酸的物质的量浓度是_______ mol/L。(假设烧瓶内的液体不扩散出水槽)
(6)标准状况下,将V L的氨气溶于0.2L的水中,所得溶液的密度为d g·cm-3,此氨水的物质的量浓度是_______ mol/L;已知25%的氨水的密度为ρ1g/cm3,5%的氨水的密度为ρ2g/ cm3,ρ1<ρ2,若将上述两种溶液等体积混合,所得氨水的质量分数_______ 15%(填>、<或=)。
(1)以上物质中能导电的是
(2)某物质A加热时按化学方程式
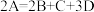 分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对
分解,产物均为气体,测得相同条件下由生成物组成的混合物气体对 的相对密度为40,则反应物A的摩尔质量为
的相对密度为40,则反应物A的摩尔质量为(3)质量比为11:7:16的
 、CO、
、CO、 ,它们所含分子数之比为
,它们所含分子数之比为(4)标准状况下有①
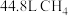 ,②
,② 个
个 分子,③
分子,③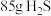 三种气体,对这三种气体的物质的量从大到小的顺序是
三种气体,对这三种气体的物质的量从大到小的顺序是(5)在标准状况下,用干燥的烧瓶装满一瓶氯化氢和氢气的混合气体倒置于水槽中,此时烧瓶中盐酸的物质的量浓度是
(6)标准状况下,将V L的氨气溶于0.2L的水中,所得溶液的密度为d g·cm-3,此氨水的物质的量浓度是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】实验室中经常需配制一定浓度的NaOH溶液,现将22.0g NaOH固体溶于水配成100.0mL溶液,其密度为1.2g.mL﹣1.
(1)该溶液中NaOH的质量分数约为 .
(2)从该溶液中取出10.0mL,其中NaOH的物质的量浓度为 ,含NaOH的物质的量为 .
(3)将取出的10.0mL溶液加水稀释到100.0mL,稀释后溶液中NaOH的物质的量浓度为 .
(1)该溶液中NaOH的质量分数约为 .
(2)从该溶液中取出10.0mL,其中NaOH的物质的量浓度为 ,含NaOH的物质的量为 .
(3)将取出的10.0mL溶液加水稀释到100.0mL,稀释后溶液中NaOH的物质的量浓度为 .
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】硫酸常用于金属表面除锈。(原理:Fe2O3+3H2SO4=Fe2(SO4)3+3H2O)
(1)把50g质量分数为98%的浓硫酸,稀释成10%的稀硫酸,需要水的质量是多少____ ?
(2)要使16gFe2O3恰好完全反应,需消耗上述10%的稀硫酸的质量是多少_____ ?
(1)把50g质量分数为98%的浓硫酸,稀释成10%的稀硫酸,需要水的质量是多少
(2)要使16gFe2O3恰好完全反应,需消耗上述10%的稀硫酸的质量是多少
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】(1)将质量比为14︰15的N2和NO混合,则混合气体中N2和NO的物质的量之比为_______________ ,氮原子和氧原子的个数比为_____________ 。
(2) 5molCO2在标准状况下所占的体积约为________________ ;所含氧原子的数目约为__________________________ 。
(3)12.4 g Na2X中含有0.4 mol Na+,则Na2X的摩尔质量是_____________ ,该物质的化学式为_____________ 。
(4)在___________ mL 0.2 mol/L NaOH溶液中含1 g溶质;配制50 mL 0.2 mol/L CuSO4溶液,需要CuSO4·5H2O_______________ g。
(2) 5molCO2在标准状况下所占的体积约为
(3)12.4 g Na2X中含有0.4 mol Na+,则Na2X的摩尔质量是
(4)在
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】将19.2g铜粉与一定量的浓硝酸反应,当铜粉完全反应时收集到气体11.2L(标准状况下)。计算:
(1)产生NO、NO2标况下的体积分别是_______ 、_______ 。
(2)所消耗硝酸的物质的量是_______ 。
(1)产生NO、NO2标况下的体积分别是
(2)所消耗硝酸的物质的量是
您最近一年使用:0次
【推荐2】回答下列问题:
(1)在一定条件下,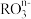 和氟气可发生如下反应
和氟气可发生如下反应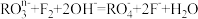 从而可知在
从而可知在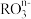 中,元素R的化合价为
中,元素R的化合价为_______ 。
(2)若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为dg/L,则此溶液的物质的量浓度为_______ mol/L。(用含V,d字母的算式表示)
(3)某学生用 和
和 组成的均匀混合物进行以下实验。(气体体积已折算成标准状况下的体积,不考虑
组成的均匀混合物进行以下实验。(气体体积已折算成标准状况下的体积,不考虑 在水中的溶解,不考虑HCl的挥发)
在水中的溶解,不考虑HCl的挥发)
实验1:取2.96g固体混合物加入质量分数为12.0%,密度为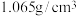 的盐酸40mL共产生672mL气体。
的盐酸40mL共产生672mL气体。
实验2:取8.88g该固体混合物逐滴加入40mL该盐酸,则产生amL的气体。
①盐酸的物质的量浓度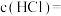
_______ (保留两位小数)。
②样品中物质的量之比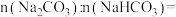
_______ 。
③a=_______ mL。
(1)在一定条件下,
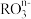 和氟气可发生如下反应
和氟气可发生如下反应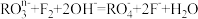 从而可知在
从而可知在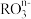 中,元素R的化合价为
中,元素R的化合价为(2)若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为dg/L,则此溶液的物质的量浓度为
(3)某学生用
 和
和 组成的均匀混合物进行以下实验。(气体体积已折算成标准状况下的体积,不考虑
组成的均匀混合物进行以下实验。(气体体积已折算成标准状况下的体积,不考虑 在水中的溶解,不考虑HCl的挥发)
在水中的溶解,不考虑HCl的挥发)实验1:取2.96g固体混合物加入质量分数为12.0%,密度为
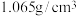 的盐酸40mL共产生672mL气体。
的盐酸40mL共产生672mL气体。实验2:取8.88g该固体混合物逐滴加入40mL该盐酸,则产生amL的气体。
①盐酸的物质的量浓度
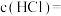
②样品中物质的量之比
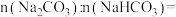
③a=
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐3】水泥是重要的建筑材料,水泥熟料的主要成分为CaO、SiO2,并含有一定量的铁、铝和镁等金属的氧化物。实验室测定水泥样品中钙的含量:先将水泥转变为草酸钙,用KMnO4标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:MnO4-+H++H2C2O4→Mn2++CO2↑+H2O。实验中称取0.400 g水泥样品,滴定时消耗了0.0500 mol·L−1的KMnO4溶液36.00 mL,则该水泥样品中钙的质量分数为______________ 。
您最近一年使用:0次



