下列说法正确的是
| A.已知反应CH4(g)+2O2(g)→CO2(g)+2H2O(1) 其△S>0 |
| B.对有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C.在滴有酚酞的Na2CO3溶液中,逐滴加入BaCl2溶液,溶液褪色 |
| D.在高温条件下,C能置换出SiO2中的Si,说明C的氧化性强于Si |
2011·吉林·一模 查看更多[1]
(已下线)2011届吉林省高考复习质量监测(理综)化学部分
更新时间:2016-12-09 01:39:20
|
相似题推荐
单选题
|
适中
(0.65)
名校
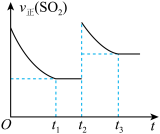
【推荐1】一定温度下,密闭容器中进行反应:2SO2(g)+O2(g) 2SO3(g))△H<0。测得v正(SO2)随反应时间(t)的变化如图所示。其中在t2时刻改变了某个条件,下列有关说法正确的是( )
2SO3(g))△H<0。测得v正(SO2)随反应时间(t)的变化如图所示。其中在t2时刻改变了某个条件,下列有关说法正确的是( )
 2SO3(g))△H<0。测得v正(SO2)随反应时间(t)的变化如图所示。其中在t2时刻改变了某个条件,下列有关说法正确的是( )
2SO3(g))△H<0。测得v正(SO2)随反应时间(t)的变化如图所示。其中在t2时刻改变了某个条件,下列有关说法正确的是( )
| A.t1时平衡常数K1小于t3时平衡常数K2 |
| B.t1时平衡混合气的M1 >t3时平衡混合气的M2 |
| C.t2时刻改变的条件可能是:升温或缩小容器体积 |
| D.t1时平衡混合气中的SO3的体积分数等于t3时平衡混合气中SO3的体积分数 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列方案设计、现象和结论均不正确的是
| 选项 | 实验目的 | 实验操作 |
| A | 探究催化剂对反应速率的影响 | 2支各盛有2mL0.1mol/L过氧化氢溶液的试管,向其中一支试管中滴加FeCl3溶液,观察实验现象 |
| B | 探究浓度对反应速率的影响 | 在锥形瓶内各盛有2g锌粒(颗粒大小基本相网),然后通过分液漏斗分别加入40mL1mol/L和40mL2mol/L的硫酸,比较两者收集10mL氢气所用的时间 |
| C | 探究浓度对反应速率的影响 | 向2支各盛有2mL1.0mol/LKMnO4酸性溶液的试管中,分别加入2mL0.1mol/LH2C2O4溶液和2mL0.2mol/LH2C2O4溶液,记录溶液褪色所需的时间 |
| D | 探究固体表面积对反应速率的影响 | 称取相同质量的块状大理石和粉末状纯碱,加入盛有浓度、体积均相同的盐酸的小烧杯中,观察实验现象 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】某密闭容器中发生如下反应:X(g)+3Y(g) 2Z(g) ΔH<0。如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
2Z(g) ΔH<0。如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
 2Z(g) ΔH<0。如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是
2Z(g) ΔH<0。如图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量。下列说法中正确的是 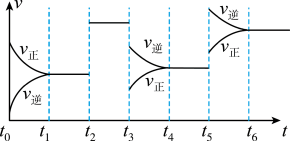
| A.t2时加入催化剂 | B.t3时降低了温度 |
| C.t5时增大了压强 | D.t4~t5时间内转化率一定最低 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
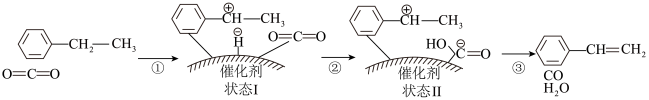
【推荐1】CO2氧化乙苯脱氢制苯乙烯的反应方程式是: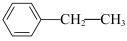 (g)+CO2(g)
(g)+CO2(g)
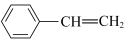 (g)+H2O(g)+CO(g),其反应历程如图所示。下列有关说法正确的是
(g)+H2O(g)+CO(g),其反应历程如图所示。下列有关说法正确的是
A.该反应的 |
B.该反应的平衡常数表达式为 ( (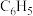 -表示苯基) -表示苯基) |
| C.催化剂表面酸性越强,苯乙烯的产率越高 |
D.过程③可能生成副产物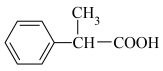 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知反应:
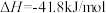 ,标准状况下,
,标准状况下,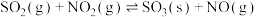
 。下列有关说法错误的是
。下列有关说法错误的是

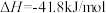 ,标准状况下,
,标准状况下,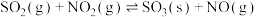
 。下列有关说法错误的是
。下列有关说法错误的是A.该反应的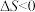 |
B.该反应的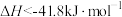 |
C.若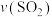 生成= 生成=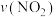 消耗,则该反应到达平衡状态 消耗,则该反应到达平衡状态 |
D.反应过程中及时分离 ,有利于废气的转化 ,有利于废气的转化 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】一定温度下,可逆反应:2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g) ∆H<0在某密闭容器中达到平衡,下列说法不正确的是。
| A.2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g) ∆S<0 |
| B.2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g),反应达到平衡,升高温度,有利于平衡逆移 |
| C.2NH3(g)+CO2(g)⇌NH4COONH2(s),若在恒温下压缩容器体积,氨基甲酸铵固体的质量增大 |
| D.2NH3(g)+CO2(g)⇌CO(NH2)2(s)+H2O(g),在密闭容器中达到平衡,混合气体的平均相对分子质量不变,则反应一定达到平衡 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,下列有关离子共存的说法中正确的是
A.某无色溶液中可能大量存在Al3+、 、Cl-、 、Cl-、 |
B.小苏打溶液中,可能大量存在I-、 、Ba2+、ClO- 、Ba2+、ClO- |
C.在水电离出H+浓度为1×10-13mol·L-1的澄清透明溶液可能大量存在Mg2+、Cu2+、 、 、 |
| D.使甲基橙呈红色的溶液中,可能大量存在Na+、K+、[Al(OH)4]-、Cl- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】25 ℃时某些弱酸的电离平衡常数如下表所示:
常温下,稀释CH3COOH、HClO两种酸时,溶液的pH随加水量变化的曲线如图所示,下列说法正确的是( )

| CH3COOH | HClO | H2CO3 |
| K(CH3COOH) =1.8×10-5 | K(HClO) =3.0×10-8 | K(H2CO3)a1=4.4×10-7 K(H2CO3)a2=4.7×10-11 |
常温下,稀释CH3COOH、HClO两种酸时,溶液的pH随加水量变化的曲线如图所示,下列说法正确的是( )

| A.相同浓度的CH3COOH和HClO的混合溶液中,各离子浓度的大小关系是: c(H+)>c(ClO-)>c(CH3COO-)>c(OH-) |
B.图象中a、c两点所处的溶液中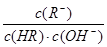 相等(HR代表CH3COOH或HClO) 相等(HR代表CH3COOH或HClO) |
| C.图象中a点酸的浓度大于b点酸的浓度 |
| D.向NaClO溶液中通入少量二氧化碳的离子方程式为:2ClO-+CO2+H2O=2HClO+CO32— |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】赖氨酸[H2N(CH2)4CH(NH2)COOH,用HR表示]是人体必需氨基酸,其盐酸盐(H3RCl2)在水溶液中存在如下平衡:H3R2+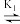 H2R+
H2R+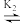 HR
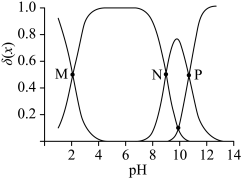
HR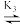 R-。向一定浓度的H3RCl2溶液中滴加NaOH溶液,溶液中H3R2+、H2R+、HR和R-的分布系数δ(x)随pH变化如图所示。.已知δ(x)=
R-。向一定浓度的H3RCl2溶液中滴加NaOH溶液,溶液中H3R2+、H2R+、HR和R-的分布系数δ(x)随pH变化如图所示。.已知δ(x)=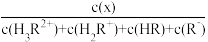 。下列表述正确的是
。下列表述正确的是
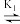 H2R+
H2R+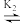 HR
HR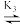 R-。向一定浓度的H3RCl2溶液中滴加NaOH溶液,溶液中H3R2+、H2R+、HR和R-的分布系数δ(x)随pH变化如图所示。.已知δ(x)=
R-。向一定浓度的H3RCl2溶液中滴加NaOH溶液,溶液中H3R2+、H2R+、HR和R-的分布系数δ(x)随pH变化如图所示。.已知δ(x)=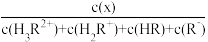 。下列表述正确的是
。下列表述正确的是
| A.已知CH3COOH的电离平衡常数Ka=1.75×10-5,则H2R+与CH3COO-不能大量共存 |
| B.N点,向溶液中加入少量NaOH溶液发生反应的离子方程式为:H2R++OH-=H2O+HR |
| C.M点,c(Na+)>c(Cl-)>c(H+)>c(OH-) |
| D.P点,c(Cl-)+c(OH-)+c(HR)=c(H2R+)+2c(H3R2+)+c(H+) |
您最近一年使用:0次



