聚合氯化铝是一种新型、高效絮凝剂和净水剂,其单体是液态的碱式氯化铝[Al2(OH)nCl6-n]。
本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为分布广、价格廉的高岭土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下:
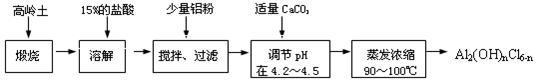
回答下列问题:
(1)“煅烧”的目的是_________________________________________ 。
(2)“溶解”过程中发生反应的离子方程式为_________________________________________________________________________________________
(3)加少量铝粉的主要作用是________________________________ 。
(4)“调节pH在4.2~4.5”的过程中,除添加必要的试剂,还需借助的实验用品是________________ ;“蒸发浓缩”需保持温度在90~100℃,控制温度的实验方法是________________________ 。
本实验采用铝盐溶液水解絮凝法制备碱式氯化铝。其制备原料为分布广、价格廉的高岭土,化学组成为:Al2O3(25%~34%)、SiO2(40%~50%)、Fe2O3(0.5%~3.0%)以及少量杂质和水分。已知氧化铝有多种不同的结构,化学性质也有差异,且一定条件下可相互转化;高岭土中的氧化铝难溶于酸。制备碱式氯化铝的实验流程如下:

回答下列问题:
(1)“煅烧”的目的是
(2)“溶解”过程中发生反应的离子方程式为
(3)加少量铝粉的主要作用是
(4)“调节pH在4.2~4.5”的过程中,除添加必要的试剂,还需借助的实验用品是
2011·广东·模拟预测 查看更多[1]
(已下线)2011届广东省高三全真高考模拟(四)(理综)化学部分
更新时间:2011-04-14 15:13:50
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】以非水溶性钾长石(K2O·Al2O3·6SiO2)为原料提取Al2O3、K2CO3等物质的流程如图。
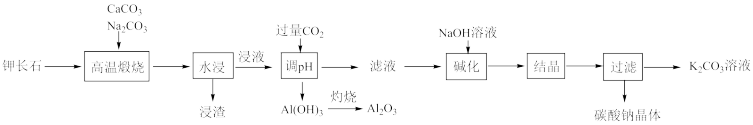
已知碳酸钠和碳酸钾的溶解度随温度的变化如表所示:
(1)在将钾长石“高温煅烧”前,需将钾长石粉碎处理,其目的是___ 。
(2)“浸液”中金属阳离子主要有___ 。
(3)“浸渣”中的主要成分可能有___ (填化学式)。
(4)“过滤”所需的玻璃仪器有___ 。
(5)写出通入过量CO2生成Al(OH)3反应的离子方程式:___ 。
(6)上述流程中可循环利用的物质为___ (填化学式)。
(7)“碱化”后获得碳酸钠晶体的方法是___ (填“降温结晶”或“蒸发结晶”)。

已知碳酸钠和碳酸钾的溶解度随温度的变化如表所示:
| 温度/℃ 溶解度/g | 0 | 10 | 20 | 30 | 40 |
| 碳酸钠 | 6.9 | 12 | 22.1 | 39 | 49 |
| 碳酸钾 | 107 | 109 | 110 | 114 | 117 |
(2)“浸液”中金属阳离子主要有
(3)“浸渣”中的主要成分可能有
(4)“过滤”所需的玻璃仪器有
(5)写出通入过量CO2生成Al(OH)3反应的离子方程式:
(6)上述流程中可循环利用的物质为
(7)“碱化”后获得碳酸钠晶体的方法是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】以含Fe2O3、FeO、SiO2、Al2O3的混合物为原料,设计两种制备铁红(Fe2O3)的方案,部分产物已略去。
【方案1 】

【方案2 】

(1)溶液A所含阳离子有_________________
(2)加入双氧水的作用是_________________
(3)固体C 的成分是_________________ (填化学式)
(4)试剂x可以选择_________________ (填序号)
a.NaOH溶液 b.氨水 c.二氧化碳 d.稀硫酸
(5)用试剂x浸取原料发生的离子方程式为_________________
【方案1 】

【方案2 】

(1)溶液A所含阳离子有
(2)加入双氧水的作用是
(3)固体C 的成分是
(4)试剂x可以选择
a.NaOH溶液 b.氨水 c.二氧化碳 d.稀硫酸
(5)用试剂x浸取原料发生的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐3】铝是一种应用广泛的金属,工业上用 和冰晶石(
和冰晶石( )混合熔融电解制得。
)混合熔融电解制得。
①铝土矿的主要成分是 和
和 等。从铝土矿中提炼
等。从铝土矿中提炼 的流程如下:
的流程如下:
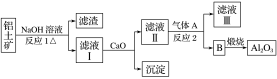
②以萤石( )和纯碱为原料制备冰晶石的流程如下:
)和纯碱为原料制备冰晶石的流程如下:
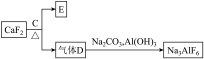
请回答下列问题:
(1)写出反应1的化学方程式____________ 。
(2)滤液1中加入 生成的沉淀是
生成的沉淀是____________ ,反应2的离子方程式为____________ (气体 过量)。
过量)。
(3) 可作为建筑材料,化合物
可作为建筑材料,化合物 是浓硫酸,请写出由
是浓硫酸,请写出由 制备冰晶石的化学方程式
制备冰晶石的化学方程式____________ 。
(4)电解氧化铝制铝时,以石墨为电极,请写出阳极的电极反应式____________ 。
 和冰晶石(
和冰晶石( )混合熔融电解制得。
)混合熔融电解制得。①铝土矿的主要成分是
 和
和 等。从铝土矿中提炼
等。从铝土矿中提炼 的流程如下:
的流程如下:
②以萤石(
 )和纯碱为原料制备冰晶石的流程如下:
)和纯碱为原料制备冰晶石的流程如下:
请回答下列问题:
(1)写出反应1的化学方程式
(2)滤液1中加入
 生成的沉淀是
生成的沉淀是 过量)。
过量)。(3)
 可作为建筑材料,化合物
可作为建筑材料,化合物 是浓硫酸,请写出由
是浓硫酸,请写出由 制备冰晶石的化学方程式
制备冰晶石的化学方程式(4)电解氧化铝制铝时,以石墨为电极,请写出阳极的电极反应式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】元素铬(Cr)在自然界主要以+3价和+6价存在。
(1)工业上利用铬铁矿(FeO·Cr2O3)冶炼铬的工艺流程如图所示:
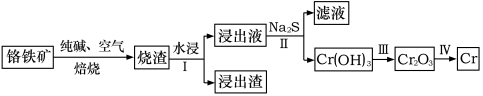
①为加快焙烧速率和提高原料的利用率,可采取的措施之一是___ 。
②“水浸Ⅰ”要获得“浸出液”的操作是____ 。已知“浸出液”的主要成分为Na2CrO4,则Cr2O3在高温焙烧时反应的化学方程式为___ 。
③若向“滤液”中加入盐酸酸化的氯化钡溶液有白色沉淀生成,则操作Ⅱ发生反应的离子方程式为___ 。
(2)含有Cr2O 的废水毒性较大,某工厂为了使废水的排放达标,进行如下处理:
的废水毒性较大,某工厂为了使废水的排放达标,进行如下处理:
Cr2O
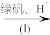 Cr3+、Fe3+
Cr3+、Fe3+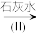 Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3
①该废水中加入绿矾(FeSO4·7H2O)和H+,发生反应的离子方程式为___ 。
②若处理后的废水中残留的c(Fe3+)=2.0×10-13mol·L-1,则残留的Cr3+的浓度为____ 。(已知:Ksp[Fe(OH)3]=4.0×10-38,Ksp[Cr(OH)3]=6.0×10-31)
(1)工业上利用铬铁矿(FeO·Cr2O3)冶炼铬的工艺流程如图所示:

①为加快焙烧速率和提高原料的利用率,可采取的措施之一是
②“水浸Ⅰ”要获得“浸出液”的操作是
③若向“滤液”中加入盐酸酸化的氯化钡溶液有白色沉淀生成,则操作Ⅱ发生反应的离子方程式为
(2)含有Cr2O
 的废水毒性较大,某工厂为了使废水的排放达标,进行如下处理:
的废水毒性较大,某工厂为了使废水的排放达标,进行如下处理:Cr2O

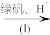 Cr3+、Fe3+
Cr3+、Fe3+ Cr(OH)3、Fe(OH)3
Cr(OH)3、Fe(OH)3①该废水中加入绿矾(FeSO4·7H2O)和H+,发生反应的离子方程式为
②若处理后的废水中残留的c(Fe3+)=2.0×10-13mol·L-1,则残留的Cr3+的浓度为
您最近一年使用:0次
【推荐2】由黏土(主要成分Al2O3·2SiO2·2H2O,含少量Fe2O3、CaO、MgO等杂质)与磷肥生产的含氟废气生产冰晶石Na3AlF6的工艺流程如下:
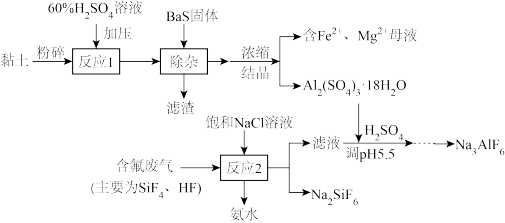
请回答下列问题:
(1) 冰晶石在电解Al2O3制铝中的作用是______ ,需定期更换石墨______ (填“阳”或“阴”)极。
(2) 不用98%硫酸进行“反应1”的可能原因是______ 。
A.不易发生离子反应,造成浸出率下降
B.反应速率太快太剧烈,造成了操作危险
C.产生较多酸性废液,也提高了原料成本
(3) 保持其他条件不变,反应1的铝浸出率在不同温度下随时间变化如图所示。“反应1”的最佳温度与时间分别是______ ℃、______ min。

(4) “除杂”步骤产生的“滤渣”中含有BaSO4、CaSO4、S等难溶物,写出产生S的离子方程式______ 。
(5) 若按“黏土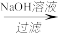 滤液
滤液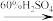 溶液
溶液 ”来制备Al2(SO4)3·18H2O,该方案的原料利用率比原方案更
”来制备Al2(SO4)3·18H2O,该方案的原料利用率比原方案更______ (填“高”或“低”)。
(6) “反应2”所得“滤液”中含氟物质主要为______ (写化学式)。
(7) 已知Ka(HF)= 6.4×10-4,Al3++ 6F- AlF
AlF 的K=1.0×1019,欲使平衡时c(AlF
的K=1.0×1019,欲使平衡时c(AlF )/c(Al3+)≥10,且调节并维持滤液pH=5.5,则其中HF平衡浓度应不低于
)/c(Al3+)≥10,且调节并维持滤液pH=5.5,则其中HF平衡浓度应不低于______ mol/L(保留2位有效数字,100.5≈ 3.2)。

请回答下列问题:
(1) 冰晶石在电解Al2O3制铝中的作用是
(2) 不用98%硫酸进行“反应1”的可能原因是
A.不易发生离子反应,造成浸出率下降
B.反应速率太快太剧烈,造成了操作危险
C.产生较多酸性废液,也提高了原料成本
(3) 保持其他条件不变,反应1的铝浸出率在不同温度下随时间变化如图所示。“反应1”的最佳温度与时间分别是

(4) “除杂”步骤产生的“滤渣”中含有BaSO4、CaSO4、S等难溶物,写出产生S的离子方程式
(5) 若按“黏土
 滤液
滤液 溶液
溶液 ”来制备Al2(SO4)3·18H2O,该方案的原料利用率比原方案更
”来制备Al2(SO4)3·18H2O,该方案的原料利用率比原方案更(6) “反应2”所得“滤液”中含氟物质主要为
(7) 已知Ka(HF)= 6.4×10-4,Al3++ 6F-
 AlF
AlF 的K=1.0×1019,欲使平衡时c(AlF
的K=1.0×1019,欲使平衡时c(AlF )/c(Al3+)≥10,且调节并维持滤液pH=5.5,则其中HF平衡浓度应不低于
)/c(Al3+)≥10,且调节并维持滤液pH=5.5,则其中HF平衡浓度应不低于
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】从废旧磷酸铁理电池的正极材料(含LiFePO4、石墨粉和铝箔等)中综合回收锂、铁和磷等的工艺流程如图所示:
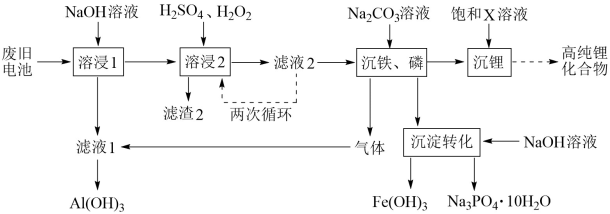
回答下列问题:
(1)“溶浸1”中铝溶解的化学方程式为________ 。
(2)完成“溶浸2”反应的离子方程式:____LiFePO4+___H2O2+____=_____Li++____+_____ +____H2O
+____H2O
__________
(3)“滤渣2”的主要成分是__________ 。
(4) “滤渣2”循环两次的目的是_______ 。
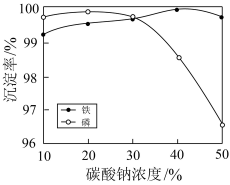
(5)“沉铁、磷”时,析出FePO4沉淀,反应的离子方程式为_______ 。实验中,铁、磷的沉淀率结果如图所示。碳酸钠浓度大于30%后,铁沉淀率仍然升高,磷沉淀率明显降低,其可能原因是_________ 。
(6)为了充分沉淀,“沉锂”时所用的X和适宜温度是_______ (填标号)。
A. NaOH 20-40℃ B. NaOH 80-100℃ C. Na2CO3 20-40℃ D. Na2CO3 60-80℃

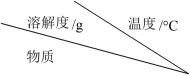 | 0 | 20 | 40 | 60 | 80 | 100 |
| LiOH | 11.9 | 12.4 | 13.2 | 14.6 | 16.6 | 19.1 |
| Li2CO3 | 1.54 | 1.33 | 1.17 | 1.01 | 0.85 | 0.72 |
回答下列问题:
(1)“溶浸1”中铝溶解的化学方程式为
(2)完成“溶浸2”反应的离子方程式:____LiFePO4+___H2O2+____=_____Li++____+_____
 +____H2O
+____H2O(3)“滤渣2”的主要成分是
(4) “滤渣2”循环两次的目的是
(5)“沉铁、磷”时,析出FePO4沉淀,反应的离子方程式为

(6)为了充分沉淀,“沉锂”时所用的X和适宜温度是
A. NaOH 20-40℃ B. NaOH 80-100℃ C. Na2CO3 20-40℃ D. Na2CO3 60-80℃
您最近一年使用:0次
【推荐1】工业上采用铁氧体法处理某总铬含量约为1600 的废水(主要成分为
的废水(主要成分为 ,pH约为4.3),同时回收含铬复合铁氧体
,pH约为4.3),同时回收含铬复合铁氧体 ,工艺流程如下:
,工艺流程如下: 是两性氢氧化物。
是两性氢氧化物。
(1)“还原”时发生反应的离子方程式为_____ 。
(2)“共沉淀”时 太小或太大均不利于除铬,原因是
太小或太大均不利于除铬,原因是_____ 。
(3)研究不同工艺对沉降分离效率的影响_____ (填“竖管”或“斜管”)沉降池。
②铁源选择:其他条件不变,使用不同亚铁盐作铁源,“共沉淀”后的沉淀高度随沉淀时间的变化关系如图乙所示,理论上应选择作_____ 铁源,理由是_____ 。
(4)“加热氧化”时,通入压缩空气的作用是①将剩余 部分氧化为
部分氧化为 ;②
;②_____ 。
(5)已知国家《污水综合排放标准》中总铬污染物排放限值为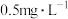 。废水经一次处理后的总铬去除率达
。废水经一次处理后的总铬去除率达 ,出水
,出水_____ (填“直接排放”或“循环处理”)。
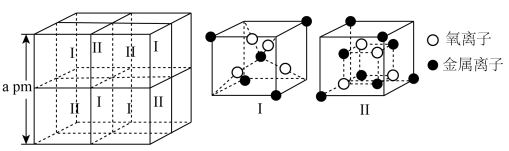
(6)含铬复合铁氧体立方晶胞如图所示。 的核外电子排布式为
的核外电子排布式为_____ 。
②铬复合铁氧体中 数目与
数目与 、
、 数目之和的比值为
数目之和的比值为_____ 。
③铬复合铁氧体的密度为_____  (用含
(用含 、
、 的式子表示)。
的式子表示)。
 的废水(主要成分为
的废水(主要成分为 ,pH约为4.3),同时回收含铬复合铁氧体
,pH约为4.3),同时回收含铬复合铁氧体 ,工艺流程如下:
,工艺流程如下:
 是两性氢氧化物。
是两性氢氧化物。(1)“还原”时发生反应的离子方程式为
(2)“共沉淀”时
 太小或太大均不利于除铬,原因是
太小或太大均不利于除铬,原因是(3)研究不同工艺对沉降分离效率的影响
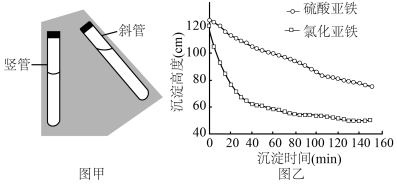
②铁源选择:其他条件不变,使用不同亚铁盐作铁源,“共沉淀”后的沉淀高度随沉淀时间的变化关系如图乙所示,理论上应选择作
(4)“加热氧化”时,通入压缩空气的作用是①将剩余
 部分氧化为
部分氧化为 ;②
;②(5)已知国家《污水综合排放标准》中总铬污染物排放限值为
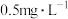 。废水经一次处理后的总铬去除率达
。废水经一次处理后的总铬去除率达 ,出水
,出水(6)含铬复合铁氧体立方晶胞如图所示。
 的核外电子排布式为
的核外电子排布式为②铬复合铁氧体中
 数目与
数目与 、
、 数目之和的比值为
数目之和的比值为③铬复合铁氧体的密度为
 (用含
(用含 、
、 的式子表示)。
的式子表示)。
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】乙酸硅是白色至米色晶体。某校同学设计实验先制备SiCl4,再由SiCl4与乙酸酐反应制备乙酸硅。已知部分物质性质如表:
回答下列问题:
Ⅰ.制备SiCl4装置(部分夹持仪器已省略)如图:
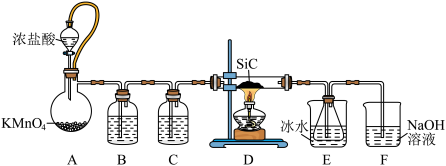
(1)装置D中发生的是置换反应,其化学方程式为_______ 。
(2)装置E用冰水浴的目的是_______ 。
(3)上述设计的装置有一处明显不妥,改进的方法是_______ 。
Ⅱ.制备(CH3COO)4Si的反应装置如图所示。
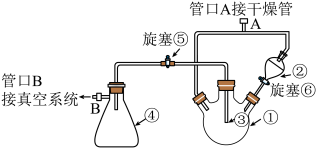
(4)仪器①的名称是_______ ,图中装置组装完毕后,首先进行的操作是_______ 。
(5)取255gSiCl4放入仪器①中,在电磁搅拌下,由分液漏斗滴入稍过量的乙酸酐,关闭旋塞⑥,反应为放热反应,反应后反应混合物带色,不久仪器①底部析出大颗粒晶体。该过程中,玻璃管③的管口必须保持在液面上方的原因是_______ 。
(6)待放置一段时间,用干冰―丙酮冷冻剂冷却,然后将③的管口插入液体中(或“插入烧瓶底部"”),再慢慢打开旋塞,小心缓慢地除去仪器①中的残留液体,接着再分两次由分液漏斗各滴入75mL左右的乙酸酐,再缓慢除去,最后得到335g精制的四乙酸硅,则四乙酸硅的产率为_______ %(保留到小数点后一位)。
| 物质 | 化学式 | 熔点 | 沸点 | 性质 |
| 乙酸硅 | (CH3COO)4Si | 110℃ | 148℃ | 白色至米色晶体 |
| 四氯化硅 | SiCl4 | -70℃ | 57.6℃ | 极易水解 |
| 乙酸酐 | (CH3CO)2O | -73℃ | 140℃ |
Ⅰ.制备SiCl4装置(部分夹持仪器已省略)如图:

(1)装置D中发生的是置换反应,其化学方程式为
(2)装置E用冰水浴的目的是
(3)上述设计的装置有一处明显不妥,改进的方法是
Ⅱ.制备(CH3COO)4Si的反应装置如图所示。

(4)仪器①的名称是
(5)取255gSiCl4放入仪器①中,在电磁搅拌下,由分液漏斗滴入稍过量的乙酸酐,关闭旋塞⑥,反应为放热反应,反应后反应混合物带色,不久仪器①底部析出大颗粒晶体。该过程中,玻璃管③的管口必须保持在液面上方的原因是
(6)待放置一段时间,用干冰―丙酮冷冻剂冷却,然后将③的管口插入液体中(或“插入烧瓶底部"”),再慢慢打开旋塞,小心缓慢地除去仪器①中的残留液体,接着再分两次由分液漏斗各滴入75mL左右的乙酸酐,再缓慢除去,最后得到335g精制的四乙酸硅,则四乙酸硅的产率为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】磷酸铁锂(LiFePO4)被认为是最有前途的锂离子电池正极材料。某企业利用富铁浸出液生成磷酸铁锂,开辟了处理硫酸亚铁废液一条新途径。其主要流程如下:
硫酸亚铁废液一条新途径.其主要流程如下:
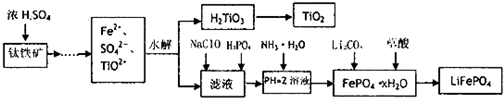
已知:H2TiO3是种难溶于水的物质。
(1)钛铁矿用浓硫酸处理之前,需要粉碎,其目的是______________________________ 。
(2)TiO2+水解生成H2TiO3的离子方程式为___________________________________ 。
(3)加入NaClO发生反应的离子方程式为______________________________________ 。
(4)在实验中,从溶液中过滤出H2TiO3后,所得滤液浑浊,应如何操作_____________ 。
(5)为测定钛铁矿中铁的含量,某同学取经浓硫酸等处理的溶液(此时钛铁矿中的铁已全部转化为二价铁离子),采取KMnO4标准液滴定Fe2+的方法:(不考虑KMnO4与其他物质反应)在滴定过程中,若未用标准液润洗滴定管,则使测定结果____ (填“偏高”、“偏低”或“无影响”),滴定终点的现象是__________________________________ 。滴定分析时,称取a g钛铁矿,处理后,用c mol/L KMnO4标准液滴定,消耗V mL,则铁元素的质量分数的表达式为____ 。
硫酸亚铁废液一条新途径.其主要流程如下:

已知:H2TiO3是种难溶于水的物质。
(1)钛铁矿用浓硫酸处理之前,需要粉碎,其目的是
(2)TiO2+水解生成H2TiO3的离子方程式为
(3)加入NaClO发生反应的离子方程式为
(4)在实验中,从溶液中过滤出H2TiO3后,所得滤液浑浊,应如何操作
(5)为测定钛铁矿中铁的含量,某同学取经浓硫酸等处理的溶液(此时钛铁矿中的铁已全部转化为二价铁离子),采取KMnO4标准液滴定Fe2+的方法:(不考虑KMnO4与其他物质反应)在滴定过程中,若未用标准液润洗滴定管,则使测定结果
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】蒸馏碘滴定法可测量中药材中二氧化硫是否超标(亚硫酸盐折算成二氧化硫)。原理是利用如图装置将亚硫酸盐转化为SO2,然后通过碘标准溶液滴定吸收液。
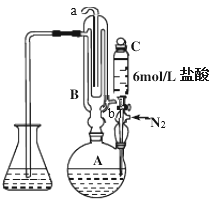
实验步骤如下:
I.SO2含量的测定
烧瓶A中加中药粉10g,加蒸馏水300 mL;锥形瓶中加蒸馏水125mL和淀粉试液1mL作为吸收液; 打开冷凝水,通氮气,滴入盐酸10mL; 加热烧瓶A并保持微沸约3min后,用0.01000mol/L 碘标准溶液一边吸收一边滴定,至终点时消耗碘标准溶液V1mL;
Ⅱ.空白实验
只加300mL蒸馏水,重复上述操作,需碘标准溶液体积为V0mL。
(1)仪器C的名称_______ 。
(2)滴入盐酸前先通氮气一段时间作用是___ ,测定过程中氮气的流速过快会导致测量结果___ 。(填“偏大”“偏小”或“不变”)
(3)①滴定过程中使用的滴定管为____ 。
A.酸式无色滴定管 B.酸式棕色滴定管
C.碱式无色滴定管 D.碱式棕色滴定管
②滴定时锥形瓶中反应的离子方程式为_______ ,滴定终点的现象是_____ 。
(4)该中药中含SO2含量为_____ mg/ kg。

实验步骤如下:
I.SO2含量的测定
烧瓶A中加中药粉10g,加蒸馏水300 mL;锥形瓶中加蒸馏水125mL和淀粉试液1mL作为吸收液; 打开冷凝水,通氮气,滴入盐酸10mL; 加热烧瓶A并保持微沸约3min后,用0.01000mol/L 碘标准溶液一边吸收一边滴定,至终点时消耗碘标准溶液V1mL;
Ⅱ.空白实验
只加300mL蒸馏水,重复上述操作,需碘标准溶液体积为V0mL。
(1)仪器C的名称
(2)滴入盐酸前先通氮气一段时间作用是
(3)①滴定过程中使用的滴定管为
A.酸式无色滴定管 B.酸式棕色滴定管
C.碱式无色滴定管 D.碱式棕色滴定管
②滴定时锥形瓶中反应的离子方程式为
(4)该中药中含SO2含量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】CoCO3可用作选矿剂、催化剂及伪装涂料的颜料。以含钴废渣(主要成分为CoO、Co2O3,还含有Al2O3、ZnO等杂质)为原料制备CoCO3的一种工艺流程如下:
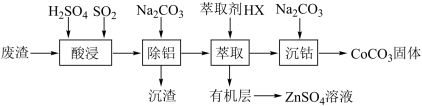
已知:①常温下,Ksp(CoCO3)=1.6×10-7
②相关金属离子[c(Mn+)=1.0mol·L-1]形成氢氧化物沉淀的pH范围如下:
(1)“酸浸”时加快溶解的方法有___________ (写出一种)。
(2)写出“酸浸”时发生氧化还原反应的化学方程式___________ 。
(3)“除铝”过程中需要调节溶液pH的范围为___________ ,形成沉渣时发生反应的离子方程式为___________ 。
(4)“沉钴”后经过滤、洗涤、干燥可得CoCO3固体,其中洗涤沉淀的方法是___________ 。
(5)当Co2+沉淀完全时[c(Co2+)≤1×10-5mol·L-1],溶液中c(CO )至少应大于
)至少应大于___________ 。
(6)在空气中煅烧CoCO3生成钴的氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴的氧化物的化学式为___________ 。

已知:①常温下,Ksp(CoCO3)=1.6×10-7
②相关金属离子[c(Mn+)=1.0mol·L-1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | 开始沉淀的pH | 沉淀完全的pH |
| Co2+ | 7.6 | 9.4 |
| Al3+ | 3.0 | 5.0 |
| Zn2+ | 5.4 | 8.0 |
(1)“酸浸”时加快溶解的方法有
(2)写出“酸浸”时发生氧化还原反应的化学方程式
(3)“除铝”过程中需要调节溶液pH的范围为
(4)“沉钴”后经过滤、洗涤、干燥可得CoCO3固体,其中洗涤沉淀的方法是
(5)当Co2+沉淀完全时[c(Co2+)≤1×10-5mol·L-1],溶液中c(CO
 )至少应大于
)至少应大于(6)在空气中煅烧CoCO3生成钴的氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为0.672L(标准状况),则该钴的氧化物的化学式为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某课外小组的同学拟用图所示装置从含碘废液(除H2O外,还有I2、I-等)中回收碘。回答下列问题:
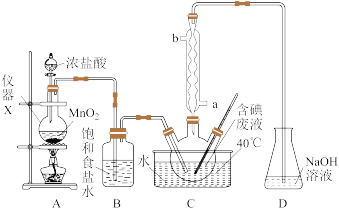
(1)装置A中发生反应的离子方程式为________ 。
(2)仪器X的名称为____ ;装置D的作用是________________ 。
(3)装置C中球形冷凝管中的冷却水从_____ (填“a”或“b”)进入,反应控制在较低温度下且保持溶液pH=2进行,其主要原因是____________________ 。
(4)三颈烧瓶中液体经过滤得粗碘,粗碘可经_______ (填操作名称)得到纯碘。

(1)装置A中发生反应的离子方程式为
(2)仪器X的名称为
(3)装置C中球形冷凝管中的冷却水从
(4)三颈烧瓶中液体经过滤得粗碘,粗碘可经
您最近一年使用:0次



