工业制玻璃时,发生的主要反应的化学方程式为: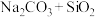

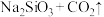
完成下列填空:
(1)钠原子核外具有______ 种不同能量的电子,钠元素在周期表中的位置为____________ 。
(2)在上述反应中,反应物和生成物的晶体类型共有_____ 种,写出气体产物的电子式_______________ 。
(3)上述物质中的非金属元素原子半径由大到小顺序为___________ (用元素符号表示),下列能判断它们的非金属性强弱的依据是:________ (选填编号)。
a. 气态氢化物的熔沸点 b. 最高价氧化物对应水化物的酸性
c. 气态氢化物的热稳定性 d. 三种元素两两形成的化合物中电子对偏向
(4)常温下,相同物质的量浓度的 和
和 溶液中,
溶液中,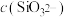
_____ 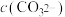 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
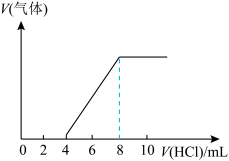
(5)向10mL一定浓度的 溶液中逐滴加入0.1mol/L的稀盐酸,加入盐酸的体积与产生气体的体积有如图关系。由此可知原
溶液中逐滴加入0.1mol/L的稀盐酸,加入盐酸的体积与产生气体的体积有如图关系。由此可知原 溶液的物质的量浓度为
溶液的物质的量浓度为__________ 。在滴入盐酸的整个过程中,溶液中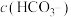 的变化情况是
的变化情况是______________ 。
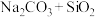

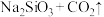
完成下列填空:
(1)钠原子核外具有
(2)在上述反应中,反应物和生成物的晶体类型共有
(3)上述物质中的非金属元素原子半径由大到小顺序为
a. 气态氢化物的熔沸点 b. 最高价氧化物对应水化物的酸性
c. 气态氢化物的热稳定性 d. 三种元素两两形成的化合物中电子对偏向
(4)常温下,相同物质的量浓度的
 和
和 溶液中,
溶液中,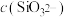
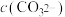 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。(5)向10mL一定浓度的
 溶液中逐滴加入0.1mol/L的稀盐酸,加入盐酸的体积与产生气体的体积有如图关系。由此可知原
溶液中逐滴加入0.1mol/L的稀盐酸,加入盐酸的体积与产生气体的体积有如图关系。由此可知原 溶液的物质的量浓度为
溶液的物质的量浓度为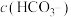 的变化情况是
的变化情况是
更新时间:2018-04-14 11:35:43
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】4gNaOH固体溶解后配制成100mL溶液,其物质的量浓度为__________ ,取出10mL该溶液,它的物质的量浓度为__________ ,将取出的10mL加水稀释至100mL,其物质的量浓度变为_________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】一定质量的铜粉恰好完全溶解于 一定浓度的硝酸中,得到
一定浓度的硝酸中,得到 和
和 的混合气体
的混合气体 (标准状况),将这些气体与
(标准状况),将这些气体与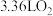 (标准状况)混合后通入
(标准状况)混合后通入 溶液,所有气体被完全吸收生成硝酸钠。计算:
溶液,所有气体被完全吸收生成硝酸钠。计算:
(1)溶解的铜粉质量是_______ g
(2)混合气体中 与
与 的物质的量之比为
的物质的量之比为_______ 。
(3)硝酸的物质的量浓度为_______ mol/L。
 一定浓度的硝酸中,得到
一定浓度的硝酸中,得到 和
和 的混合气体
的混合气体 (标准状况),将这些气体与
(标准状况),将这些气体与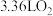 (标准状况)混合后通入
(标准状况)混合后通入 溶液,所有气体被完全吸收生成硝酸钠。计算:
溶液,所有气体被完全吸收生成硝酸钠。计算:(1)溶解的铜粉质量是
(2)混合气体中
 与
与 的物质的量之比为
的物质的量之比为(3)硝酸的物质的量浓度为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题:
(1)19g某二价金属的氯化物ACl2中含有0.4mol 离子,
离子, 的摩尔质量是
的摩尔质量是_______ ,A的相对原子质量是_______ ,A的原子结构示意图为_______ 。
(2)取1.43g 溶于水配成100mL溶液,
溶于水配成100mL溶液, 物质的量浓度为
物质的量浓度为_______ ,取出20mL该溶液用蒸馏水稀释,使 溶液物质的量浓度变为0.004mol/L,加入蒸馏水的体积(设稀释时,对溶液体积的影响忽略计)
溶液物质的量浓度变为0.004mol/L,加入蒸馏水的体积(设稀释时,对溶液体积的影响忽略计)_______ 。
(3)在标准状况下,由CO和 组成的混合气体13.44L,质量为20g。此混合气体中的C和O两种原子的物质的量之比为
组成的混合气体13.44L,质量为20g。此混合气体中的C和O两种原子的物质的量之比为_______ ,CO的质量为_______ 。
(4)室温下,某容积固定的密闭容器由可移动的活塞(忽略摩擦力)隔成A、B两室,向A室中充入 和
和 的混合气体,向B室中充入4mol空气,此时活塞的位置如下图所示:
的混合气体,向B室中充入4mol空气,此时活塞的位置如下图所示:

已知A室混合气体的质量为136g,若将A室中 与
与 的混合气体点燃引爆,恢复室温后,最终活塞停留的位置在
的混合气体点燃引爆,恢复室温后,最终活塞停留的位置在_______ (填数字)刻度,反应后容器内气体压强与反应前气体压强之比为_______ 。
(1)19g某二价金属的氯化物ACl2中含有0.4mol
 离子,
离子, 的摩尔质量是
的摩尔质量是(2)取1.43g
 溶于水配成100mL溶液,
溶于水配成100mL溶液, 物质的量浓度为
物质的量浓度为 溶液物质的量浓度变为0.004mol/L,加入蒸馏水的体积(设稀释时,对溶液体积的影响忽略计)
溶液物质的量浓度变为0.004mol/L,加入蒸馏水的体积(设稀释时,对溶液体积的影响忽略计)(3)在标准状况下,由CO和
 组成的混合气体13.44L,质量为20g。此混合气体中的C和O两种原子的物质的量之比为
组成的混合气体13.44L,质量为20g。此混合气体中的C和O两种原子的物质的量之比为(4)室温下,某容积固定的密闭容器由可移动的活塞(忽略摩擦力)隔成A、B两室,向A室中充入
 和
和 的混合气体,向B室中充入4mol空气,此时活塞的位置如下图所示:
的混合气体,向B室中充入4mol空气,此时活塞的位置如下图所示:
已知A室混合气体的质量为136g,若将A室中
 与
与 的混合气体点燃引爆,恢复室温后,最终活塞停留的位置在
的混合气体点燃引爆,恢复室温后,最终活塞停留的位置在
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】根据信息回答下列问题:
Ⅰ.(1)25℃时,将0.02 mol/L 的Ba(OH)2溶液与物质的量浓度相同的NaHSO4溶液等体积混合,所得的溶液的pH=_______ 。
(2)25 ℃时,有0.1mol·L-1的四种溶液:① HCl ② Na2CO3 ③ CH3COOH ④NaOH。上述四种溶液中,其中水的电离程度最大的是_______ ( 填序号,下同,),溶液的pH值由大到小的顺序是_______ 。
(3)向碳酸钠溶液中加入明矾会产生沉淀和气体,反应的离子方程式为:_______ 。
(4) 25 ℃某浓度的NaHCO3溶液的pH=9,则此时溶液中c(CO ):c(HCO
):c(HCO )=
)=_______ 。(已知H2CO3的电离常数:K1=4.4×10-7 ,K2=4.7×10-11.)
Ⅱ.(5)食醋是日常饮食中的一种调味剂,国家标准规定酿造食醋中醋酸含量不得低于0.035g/mL。选择酚酞作指示剂,用标准NaOH溶液可以测定食醋中醋酸的浓度,以检测白醋是否符合国家标准。某品牌白醋的醋酸浓度测定过程如图所示,回答下列问题:
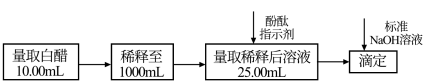
①滴定达到终点时的现象是_______ 。
②某次实验滴定开始和结束时,碱式滴定管中的液面如图所示,则所用NaOH溶液的体积为_______ mL。
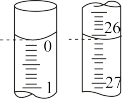
③若通过实验测得稀释后白醋的浓度为0.0600mol·L-1,则该白醋_______ (填“符合”或“不符合”)国家标准。
④下列操作中,可能使所测白醋中醋酸的浓度数值偏低的是_______ (填编号)。
A.碱式滴定管未用标准NaOH溶液润洗就直接注入标准NaOH溶液
B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥
C.滴定过程中振荡时有液滴溅出
D.读取NaOH溶液体积时,开始时仰视读数,滴定结束时俯视读数
E.碱式滴定管在滴定前有气泡,滴定后气泡消失
Ⅰ.(1)25℃时,将0.02 mol/L 的Ba(OH)2溶液与物质的量浓度相同的NaHSO4溶液等体积混合,所得的溶液的pH=
(2)25 ℃时,有0.1mol·L-1的四种溶液:① HCl ② Na2CO3 ③ CH3COOH ④NaOH。上述四种溶液中,其中水的电离程度最大的是
(3)向碳酸钠溶液中加入明矾会产生沉淀和气体,反应的离子方程式为:
(4) 25 ℃某浓度的NaHCO3溶液的pH=9,则此时溶液中c(CO
 ):c(HCO
):c(HCO )=
)=Ⅱ.(5)食醋是日常饮食中的一种调味剂,国家标准规定酿造食醋中醋酸含量不得低于0.035g/mL。选择酚酞作指示剂,用标准NaOH溶液可以测定食醋中醋酸的浓度,以检测白醋是否符合国家标准。某品牌白醋的醋酸浓度测定过程如图所示,回答下列问题:

①滴定达到终点时的现象是
②某次实验滴定开始和结束时,碱式滴定管中的液面如图所示,则所用NaOH溶液的体积为

③若通过实验测得稀释后白醋的浓度为0.0600mol·L-1,则该白醋
④下列操作中,可能使所测白醋中醋酸的浓度数值偏低的是
A.碱式滴定管未用标准NaOH溶液润洗就直接注入标准NaOH溶液
B.滴定前盛放白醋稀溶液的锥形瓶用蒸馏水洗净后没有干燥
C.滴定过程中振荡时有液滴溅出
D.读取NaOH溶液体积时,开始时仰视读数,滴定结束时俯视读数
E.碱式滴定管在滴定前有气泡,滴定后气泡消失
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】请根据所学知识回答下列问题:
(1)NaHSO3溶液中共存在7种微粒,它们是Na+、HSO 、H+、SO
、H+、SO 、H2O、
、H2O、_______ 、_______ (填微粒符号)。
(2)常温下,物质的量浓度相同的下列溶液 :
①NH4Cl ② NH4HCO3 ③(NH4)2SO4 ④ NH4HSO4
溶液中c(NH )最大的是:
)最大的是:_______ ,最小的是:_______ (填序号)
(3)常温下,物质的量浓度均为0.1mol/L的六种溶液①NaOH、②NaCl、③Na2CO3、④H2SO3、⑤CH3COONa、⑥H2SO4,pH从大到小排列顺序为_______ (填序号)
(4)常温时,AlCl3的水溶液呈酸性,原因是(用离子方程式表示):_______ 把AlCl3溶液蒸干,灼烧,最后得到的固体产物主要是_______ (填化学式)
| 酸 | 电离常数 |
| CH3COOH | K = 1.8×10 -5 |
| H2CO3 | K1= 4.3×10 -7,K2= 5.6×10 -11 |
| H2SO3 | K1=1.54×10-2 , K2=1.02×10-7 |
 、H+、SO
、H+、SO 、H2O、
、H2O、(2)常温下,物质的量浓度相同的下列溶液 :
①NH4Cl ② NH4HCO3 ③(NH4)2SO4 ④ NH4HSO4
溶液中c(NH
 )最大的是:
)最大的是:(3)常温下,物质的量浓度均为0.1mol/L的六种溶液①NaOH、②NaCl、③Na2CO3、④H2SO3、⑤CH3COONa、⑥H2SO4,pH从大到小排列顺序为
(4)常温时,AlCl3的水溶液呈酸性,原因是(用离子方程式表示):
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】回答下列问题
(1)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
①向其中加入少量KOH溶液时,发生反应的离子方程式是___________ 。
②现将 溶液和
溶液和 溶液等体积混合,得到缓冲溶液。
溶液等体积混合,得到缓冲溶液。
a.若HA为HCN,该溶液显碱性,则溶液中c(Na+)___________ c(CN-) (填“<”、“=”或“>”)。
b.若HA为 ,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是
,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是___________ 。
③若室温时,0.1mol/L的HA在水中有0.1%发生电离,则该溶液的pH为___________ ,此酸的电离平衡常数约为___________ 。
(2)25°C时, H2CO3的Ka1 =4.4 ×10-7,Ka2= 4.7 ×10-11
①试计算CO 的水解常数Kh为
的水解常数Kh为___________ ;
②若加水稀释NaHCO3溶液时,其水解程度___________ ,溶液的pH ___________ (填“增大”或“减小”);
③写出NaHCO3溶液中的电荷守恒式___________ 。
(1)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液。向其中加入少量酸或碱时,溶液的酸碱性变化不大。
①向其中加入少量KOH溶液时,发生反应的离子方程式是
②现将
 溶液和
溶液和 溶液等体积混合,得到缓冲溶液。
溶液等体积混合,得到缓冲溶液。a.若HA为HCN,该溶液显碱性,则溶液中c(Na+)
b.若HA为
 ,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是
,该溶液显酸性,则溶液中所有的离子按浓度由大到小排列的顺序是③若室温时,0.1mol/L的HA在水中有0.1%发生电离,则该溶液的pH为
(2)25°C时, H2CO3的Ka1 =4.4 ×10-7,Ka2= 4.7 ×10-11
①试计算CO
 的水解常数Kh为
的水解常数Kh为②若加水稀释NaHCO3溶液时,其水解程度
③写出NaHCO3溶液中的电荷守恒式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】按要求填空:
(1)Fe成为阳离子时首先失去_______ 轨道电子,Sm的价层电子排布式为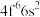 ,
, 价层电子排布式为
价层电子排布式为_______ 。
(2)Cu2+基态核外电子排布式为_______ 。
(1)Fe成为阳离子时首先失去
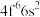 ,
, 价层电子排布式为
价层电子排布式为(2)Cu2+基态核外电子排布式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】工业上高纯硅可以通过下列反应制取:SiCl4(g)+2H2(g)⇌Si(s)+4HCl(g)﹣236kJ
(1)反应涉及的元素原子半径从大到小的排列顺序为_____ 。其中硅原子最外层有_____ 个未成对电子,有_____ 种不同运动状态的电子;
(2)反应涉及的化合物中,写出属于非极性分子的结构式:_____ ;产物中晶体硅的熔点远高HCl,原因是_____ ;
(3)氯和硫是同一周期元素,写出一个能比较氯和硫非金属性强弱的化学方程式:_____ ;
(4)在一定温度下进行上述反应,若反应容器的容积为2L,3分钟后达到平衡,测得气体质量减小8.4g,则在3分钟内H2的平均反应速率为_____ ;
(5)该反应的平衡常数表达式K=_____ ,可以通过_____ 使K增大;
(6)一定条件下,在密闭恒容器中,能表示上述反应一定达到化学平衡状态的是_____ 。
a.v逆(SiCl4)=2v正(H2)
b.固体质量保持不变
c.混合气体密度保持不变
d.c(SiCl4):c(H2):c(HCl)=1:2:4
(1)反应涉及的元素原子半径从大到小的排列顺序为
(2)反应涉及的化合物中,写出属于非极性分子的结构式:
(3)氯和硫是同一周期元素,写出一个能比较氯和硫非金属性强弱的化学方程式:
(4)在一定温度下进行上述反应,若反应容器的容积为2L,3分钟后达到平衡,测得气体质量减小8.4g,则在3分钟内H2的平均反应速率为
(5)该反应的平衡常数表达式K=
(6)一定条件下,在密闭恒容器中,能表示上述反应一定达到化学平衡状态的是
a.v逆(SiCl4)=2v正(H2)
b.固体质量保持不变
c.混合气体密度保持不变
d.c(SiCl4):c(H2):c(HCl)=1:2:4
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】Ti、Fe、Cr、Mn等均为过渡元素,在生产生活中起着不可替代的重要作用,对其单质和化合物的应用研究是目前科学研究的前沿之一。请回答下列问题:
(1)Cr元素的基态原子电子排布式为_____________________ ,比较Fe和 Mn的各级电离能后发现,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子______ (填“难”或“易”)。
(2)Cu元素处于周期表____________ 区,向盛有硫酸铜的试管里加入氨水,首先形成蓝色沉淀,继续加入氨水,沉淀溶解,此时的离子方程式为______________ ,若加入乙醇将析出____________ 色的晶体,其配离子的离子构型为_____________
(3)某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应(巨磁电阻效应)。用A、B、O表示这类特殊晶体的化学式:_____________ 。
(4)有一种蓝色晶体可表示为:[KxFey(CN)z],研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上,K+位于上述晶胞体心,且K+空缺率为50%(体心中没有K+的占总体心的百分比),其晶体中的阴离子晶胞结构如上图的图2所示,该晶体的化学式可表示为____________ 。
(1)Cr元素的基态原子电子排布式为
(2)Cu元素处于周期表
(3)某钙钛型复合氧化物(如图1),以A原子为晶胞的顶点,A位可以是Ca、Sr、Ba或Pb,当B位是V、Cr、Mn、Fe时,这种化合物具有CMR效应(巨磁电阻效应)。用A、B、O表示这类特殊晶体的化学式:

(4)有一种蓝色晶体可表示为:[KxFey(CN)z],研究表明它的结构特性是Fe2+、Fe3+分别占据立方体的顶点,自身互不相邻,而CN-位于立方体的棱上,K+位于上述晶胞体心,且K+空缺率为50%(体心中没有K+的占总体心的百分比),其晶体中的阴离子晶胞结构如上图的图2所示,该晶体的化学式可表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】请回答:
(1)标准状况下,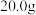 氟化氢气体的体积明显小于
氟化氢气体的体积明显小于 ,其原因是
,其原因是_______ 。
(2)碳元素的单质性质差异很大,金刚石硬度大,可用于研磨和切割;足球烯( )硬度小,是制作高级润滑剂的重要原料。两种碳单质性能差异明显的原因是
)硬度小,是制作高级润滑剂的重要原料。两种碳单质性能差异明显的原因是_______ 。
(1)标准状况下,
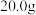 氟化氢气体的体积明显小于
氟化氢气体的体积明显小于 ,其原因是
,其原因是(2)碳元素的单质性质差异很大,金刚石硬度大,可用于研磨和切割;足球烯(
 )硬度小,是制作高级润滑剂的重要原料。两种碳单质性能差异明显的原因是
)硬度小,是制作高级润滑剂的重要原料。两种碳单质性能差异明显的原因是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下列是中学化学常见的物质
A.金刚石 B.HCl C.NaCl D.Na2SO4 E.Na2S F .He G.N2
请用序号回答(1)-(4)题:
(1)这些物质中只含共价键的是______________
(2)既含离子键又含共价键的是_______________
(3)固态时属于离子晶体的是_______________
(4)熔化时需克服共价键的是______________
(5)试写出E、G的电子式:__________ 、___________
A.金刚石 B.HCl C.NaCl D.Na2SO4 E.Na2S F .He G.N2
请用序号回答(1)-(4)题:
(1)这些物质中只含共价键的是
(2)既含离子键又含共价键的是
(3)固态时属于离子晶体的是
(4)熔化时需克服共价键的是
(5)试写出E、G的电子式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】回答下列问题:
(1)现有几组物质的熔点(℃)数据:
据此回答下列问题:
①A组属于_______ 晶体,其熔化时克服的微粒间的作用力是_______ 。
② C组中HF熔点反常是由于_______ 。
③ D组晶体可能具有的性质是_______ (填序号)。
A.硬度小 B.水溶液能导电 C.固体能导电 D.熔融状态能导电
④ D组晶体的熔点由高到低的顺序为NaCl_______ KCl(填“>”“<”“=”)
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是_______ 。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为_______ ,提供孤电子对的成键原子是_______ 。
③氨的沸点_______ (填“高于”或“低于”)膦(PH3),原因是_______ ;氨是_______ 分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______ 。
(1)现有几组物质的熔点(℃)数据:
| A组 | B组 | C组 | D组 |
| 金刚石:3 550 ℃ | Li:181 ℃ | HF:-83 ℃ | NaCl:801 ℃ |
| 硅晶体:1 410 ℃ | Na:98 ℃ | HCl:-115 ℃ | KCl:776 ℃ |
| 硼晶体:2 300 ℃ | K:64 ℃ | HBr:-89 ℃ | RbCl:718 ℃ |
| 二氧化硅:1 723 ℃ | Rb:39 ℃ | HI:-51 ℃ | CsCl:645 ℃ |
①A组属于
② C组中HF熔点反常是由于
③ D组晶体可能具有的性质是
A.硬度小 B.水溶液能导电 C.固体能导电 D.熔融状态能导电
④ D组晶体的熔点由高到低的顺序为NaCl
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为
③氨的沸点
您最近一年使用:0次



