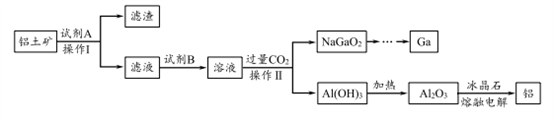
铝(熔点660℃)是一种应用广泛的金属,镓(Ga)与铝同主族,曾被称为“类铝”,其氧化物和氢氧化物均为两性化合物。工业上以铝土矿(含有Al2O3、Ga2O3、SiO2等物质)为原料提取Al2O3(熔点2045℃),并将Al2O3和冰晶石(Na3AlF6,六氟合铝酸钠)混合熔融后电解制得。回答下列问题:
(1)冶金工业上常用金属铝作还原剂冶炼钒、铬、锰等金属,写出铝与CrO3在高温下反应的化学方程式___________________ 。
(2)操作I得到滤渣的主要成分有________________ 。
(3)将0.1 mol/L AlCl3溶液和10% NH4F溶液等体积混合,充分反应后滴加氨水,无沉淀析出。则AlCl3与NH4F反应的化学方程式为________________ ;该实验所用试管及盛装NH4F溶液的试剂瓶均为塑料材质,原因是 _________________________ 。
(4)饮用水中的NO3-对人类健康会产生危害。为了降低饮用水中的NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为_________ ,此方法的缺点是处理后的水中生成了AlO2-,仍然可能对人类健康产生危害,还需对该饮用水进行一系列后续处理。已知:25℃时,Ksp[Al(OH)3]=1.3×10-33,Al(OH)3 AlO2-+H++H2O K=1.0×10-13。25℃时,若欲使上述处理的水中AlO2-浓度降低到1.0×10-6 mol/L,则应调节至pH=
AlO2-+H++H2O K=1.0×10-13。25℃时,若欲使上述处理的水中AlO2-浓度降低到1.0×10-6 mol/L,则应调节至pH=____ ,此时水中 =
=__________ 。
(5)工业上常用碳棒作电极电解熔融氧化铝的方法冶炼铝(如图所示)。
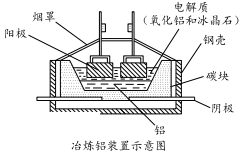
①阴极电极反应式为________________________ 。
②工业生产中,阳极材料要定期补充,其原因是:____________________ 。
(6)下列有关推理不合理的是______ 。
a.工业上可以用热还原法来制取Ga
b.酸性:Al(OH)3>Ga(OH)3
c.由最外层电子数相同可知,镓与铝的化学性质相似
d.可用GaCl3溶液、氨水和盐酸设计实验证明Ga(OH)3的两性

(1)冶金工业上常用金属铝作还原剂冶炼钒、铬、锰等金属,写出铝与CrO3在高温下反应的化学方程式
(2)操作I得到滤渣的主要成分有
(3)将0.1 mol/L AlCl3溶液和10% NH4F溶液等体积混合,充分反应后滴加氨水,无沉淀析出。则AlCl3与NH4F反应的化学方程式为
(4)饮用水中的NO3-对人类健康会产生危害。为了降低饮用水中的NO3-的浓度,有研究人员建议在碱性条件下用铝粉将NO3-还原为N2,该反应的离子方程式为
 AlO2-+H++H2O K=1.0×10-13。25℃时,若欲使上述处理的水中AlO2-浓度降低到1.0×10-6 mol/L,则应调节至pH=
AlO2-+H++H2O K=1.0×10-13。25℃时,若欲使上述处理的水中AlO2-浓度降低到1.0×10-6 mol/L,则应调节至pH= =
=(5)工业上常用碳棒作电极电解熔融氧化铝的方法冶炼铝(如图所示)。

①阴极电极反应式为
②工业生产中,阳极材料要定期补充,其原因是:
(6)下列有关推理不合理的是
a.工业上可以用热还原法来制取Ga
b.酸性:Al(OH)3>Ga(OH)3
c.由最外层电子数相同可知,镓与铝的化学性质相似
d.可用GaCl3溶液、氨水和盐酸设计实验证明Ga(OH)3的两性
更新时间:2018-04-28 10:09:16
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】用硼镁矿 主要成分为
主要成分为 ,含少量
,含少量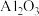 和
和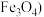 制取粗硼的工艺流程为:
制取粗硼的工艺流程为:
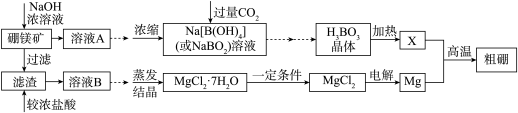
已知: 硼与铝的性质相似,也能与氢氧化钠溶液反应.
硼与铝的性质相似,也能与氢氧化钠溶液反应.
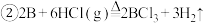
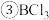 的熔点为
的熔点为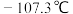 ,沸点为
,沸点为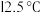 ,在潮湿空气中易形成白雾.
,在潮湿空气中易形成白雾.
I.回答下列问题:
 证明溶液B中含有铁元素的方法是
证明溶液B中含有铁元素的方法是 ______
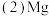 与X反应制取粗硼的化学方程式
与X反应制取粗硼的化学方程式 ______
 上图中制取
上图中制取 的“一定条件”是指
的“一定条件”是指 ______
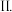 某同学设计如图所示装置制备三氯化硼.
某同学设计如图所示装置制备三氯化硼.
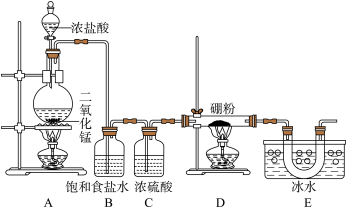
回答下列问题:
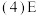 装置的作用是
装置的作用是 ______ .
 如果去掉B装置,可能的后果是
如果去掉B装置,可能的后果是 ______ .
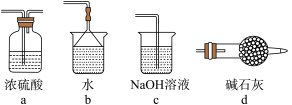
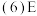 装置后面还应连接的一个装置是
装置后面还应连接的一个装置是 ______ .
 主要成分为
主要成分为 ,含少量
,含少量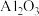 和
和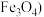 制取粗硼的工艺流程为:
制取粗硼的工艺流程为: 
已知:
 硼与铝的性质相似,也能与氢氧化钠溶液反应.
硼与铝的性质相似,也能与氢氧化钠溶液反应. 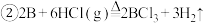
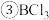 的熔点为
的熔点为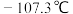 ,沸点为
,沸点为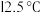 ,在潮湿空气中易形成白雾.
,在潮湿空气中易形成白雾. I.回答下列问题:
 证明溶液B中含有铁元素的方法是
证明溶液B中含有铁元素的方法是 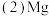 与X反应制取粗硼的化学方程式
与X反应制取粗硼的化学方程式  上图中制取
上图中制取 的“一定条件”是指
的“一定条件”是指 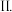 某同学设计如图所示装置制备三氯化硼.
某同学设计如图所示装置制备三氯化硼. 
回答下列问题:
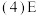 装置的作用是
装置的作用是  如果去掉B装置,可能的后果是
如果去掉B装置,可能的后果是 
 装置后面还应连接的一个装置是
装置后面还应连接的一个装置是
您最近一年使用:0次
【推荐2】铝氢化钠(NaAlH4)是重要的还原剂。以铝土矿(主要成分Al2O3,含极少量SiO2、Fe2O3等杂质)为原料制备NaAlH4的一种流程如图:
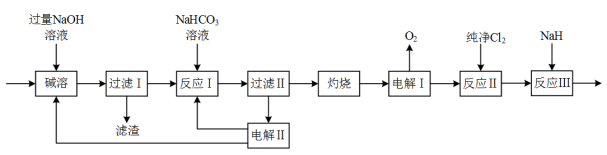
已知:“碱溶”中SiO2转化成难溶的Na2Al2Si2O8
(1)过滤Ⅰ所得滤液的主要成分为___________ (填化学式)。
(2)过滤Ⅱ所得滤液的主要成分为___________ (填化学式)。
(3)过滤Ⅱ到灼烧之间还应有的步骤是___________ 。
(4)电解Ⅰ的化学方程式为___________ 。
(5)反应Ⅲ的化学方程式为___________ 。
(6)过滤Ⅰ所得滤渣主要成分有Na2Al2Si2O8和Fe2O3,可以采用如图流程进行分离:

①滤渣溶于盐酸所得的固体物质可能为___________ (填化学式)。
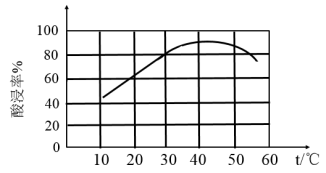
②滤渣溶于盐酸的“酸浸率”与温度关系如图所示,试解释温度过高,“酸浸率”降低的原因___________ 。

已知:“碱溶”中SiO2转化成难溶的Na2Al2Si2O8
(1)过滤Ⅰ所得滤液的主要成分为
(2)过滤Ⅱ所得滤液的主要成分为
(3)过滤Ⅱ到灼烧之间还应有的步骤是
(4)电解Ⅰ的化学方程式为
(5)反应Ⅲ的化学方程式为
(6)过滤Ⅰ所得滤渣主要成分有Na2Al2Si2O8和Fe2O3,可以采用如图流程进行分离:

①滤渣溶于盐酸所得的固体物质可能为
②滤渣溶于盐酸的“酸浸率”与温度关系如图所示,试解释温度过高,“酸浸率”降低的原因

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】NH4Al(SO4)2是食品加工中最为快捷的食品添加剂,用于焙烤食品,工业上常用铝土矿(主要成分为Al2O3和少量SiO2、Fe2O3杂质)生产铵明矾晶体NH4Al(SO4)2•12H2O,其工艺流程图如下:
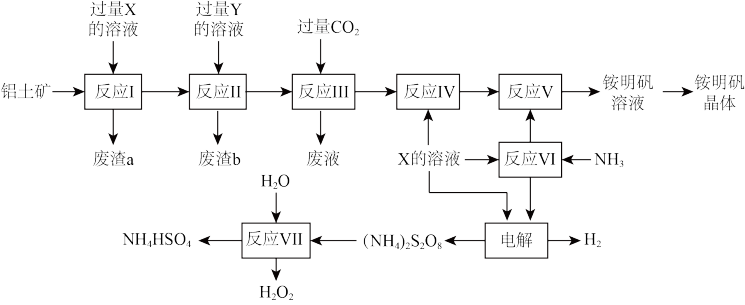
(1)废渣a、b 的成分分别是_______________ 、_______________ 。(写化学式)
(2)流程图中X的化学式为_______________ 。
(3)反应Ⅲ的离子方程式为________________ ,从铵明矾溶液中获得铵明矾晶体的操作依次为__________ (填操作名称)、冷却结晶、过滤洗涤。
(4)反应Ⅶ的化学方程式为___________________ 。
(5)向硫酸铝铵溶液中逐滴加入氢氧化钡溶液,不可能发生的离子反应是_____________ 。(填选项字母)

(1)废渣a、b 的成分分别是
(2)流程图中X的化学式为
(3)反应Ⅲ的离子方程式为
(4)反应Ⅶ的化学方程式为
(5)向硫酸铝铵溶液中逐滴加入氢氧化钡溶液,不可能发生的离子反应是
A.NH4+ + SO + Ba2+ + OH—= BaSO4↓ + NH3·H2O + Ba2+ + OH—= BaSO4↓ + NH3·H2O |
B.2Al3+ + 3SO + 3Ba2+ + 6OH—= 3BaSO4↓ + 2Al(OH)3↓ + 3Ba2+ + 6OH—= 3BaSO4↓ + 2Al(OH)3↓ |
C.Al3+ + 2SO + 2Ba2+ + 4OH—= 2BaSO4↓ + AlO + 2Ba2+ + 4OH—= 2BaSO4↓ + AlO + 2H2O + 2H2O |
D.NH + Al3+ + 2SO + Al3+ + 2SO + 2Ba2+ + 4OH—= 2BaSO4↓ + Al(OH)3↓ + NH3·H2O + 2Ba2+ + 4OH—= 2BaSO4↓ + Al(OH)3↓ + NH3·H2O |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】与氨气相关的化学变化是氮循环和转化的重要一环,对生产、生活有重要的价值。
1.下图转化途径中属于“固氮”的是___________。
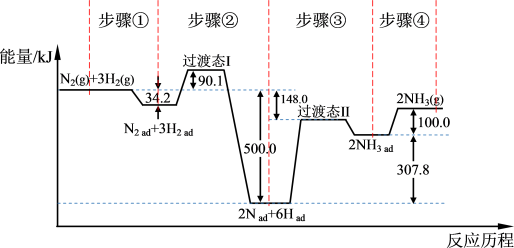
合成氨是目前转化空气中氮最有效的工业方法,其反应历程和能量变化的简图如下:(图中ad表示物质吸附在催化剂表面时的状态) 的
的
___________  ,对总反应速率影响较大的是步骤
,对总反应速率影响较大的是步骤___________ 。(填写编号)3.若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是___________。
4.氨是极具前景的氢能载体和性能卓越的“零碳”燃料,利用 的燃烧反应
的燃烧反应 能设计成燃料电池,其工作原理如图所示。电极
能设计成燃料电池,其工作原理如图所示。电极 为
为___________ (选填“正”或“负”)极;电极 的电极反应式为
的电极反应式为___________ ;当正负极共消耗3.136L(标准状况)气体时,通过负载的电子数为___________ 个。 等离子的废液,为了对废液进行处理,某同学采用硫化物沉淀法处理
等离子的废液,为了对废液进行处理,某同学采用硫化物沉淀法处理 。
。
已知:常温下
5.常温下,调节 溶液的
溶液的 ,比较溶液中含硫微粒浓度的大小
,比较溶液中含硫微粒浓度的大小___________ 。
6.常温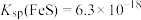 ,下列说法正确的是___________。
,下列说法正确的是___________。
1.下图转化途径中属于“固氮”的是___________。
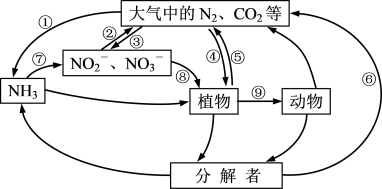
| A.④⑤⑥ | B.①③④ | C.①⑤⑦ | D.②⑧⑨ |
 的
的
 ,对总反应速率影响较大的是步骤
,对总反应速率影响较大的是步骤| A.升高温度,使单位体积内活化分子百分数增加 |
| B.增加反应物的浓度,使单位体积内活化分子百分数增加 |
| C.使用催化剂,能降低反应活化能,使单位体积内活化分子数增加 |
| D.增大压强,能降低反应的活化能,使单位体积内活化分子数增加 |
 的燃烧反应
的燃烧反应 能设计成燃料电池,其工作原理如图所示。电极
能设计成燃料电池,其工作原理如图所示。电极 为
为 的电极反应式为
的电极反应式为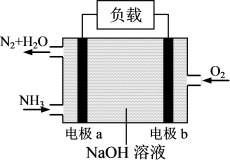
 等离子的废液,为了对废液进行处理,某同学采用硫化物沉淀法处理
等离子的废液,为了对废液进行处理,某同学采用硫化物沉淀法处理 。
。已知:常温下

5.常温下,调节
 溶液的
溶液的 ,比较溶液中含硫微粒浓度的大小
,比较溶液中含硫微粒浓度的大小6.常温
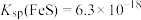 ,下列说法正确的是___________。
,下列说法正确的是___________。A.常温下, 的溶解度大于FeS 的溶解度大于FeS |
B.反应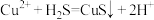 不能发生 不能发生 |
C.除去废液中的 ,可选用 ,可选用 作沉淀剂 作沉淀剂 |
D.常温下,向饱和 溶液中加入少量 溶液中加入少量 固体后, 固体后,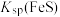 减小 减小 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
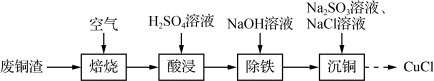
【推荐2】以工业废铜渣(主要含CuO,还含有CuS、Fe2O3等)为原料制备CuCl,并测定其纯度。其制备过程可表示为
(1)焙烧。将废铜渣放在空气中加热至300℃充分焙烧,反应中CuS转化成CuO,其反应的化学方程式为_______ 。
(2)酸浸。将焙烧后的产物与一定浓度的硫酸溶液放入反应器中,以一定的速率搅拌进行反应。在该过程中,还可以提高铜元素浸出效率的措施是_______ 。
(3)除铁。酸浸后,测得溶液中c(Fe3+)=0.1 mol·L-1,c(Cu2+)=2 mol·L-1.向其中滴加NaOH溶液调节溶液pH除去Fe3+,则需调节溶液pH范围为____ 。已知:Fe3+完全沉淀后其浓度应小于1×10-6 mol·L-1。
(4)沉铜。除铁后,过滤,向滤液中加入Na2SO3溶液、NaCl溶液, 搅拌下充分反应,过滤,洗涤,干燥得到CuCl。
①得到CuCl沉淀的离子方程式为_______ 。
②相同条件下,CuCl沉淀率随 的变化如下图所示。
的变化如下图所示。 大于2.5,CuCl沉淀率几乎不变的原因
大于2.5,CuCl沉淀率几乎不变的原因_______ 。
(1)焙烧。将废铜渣放在空气中加热至300℃充分焙烧,反应中CuS转化成CuO,其反应的化学方程式为
(2)酸浸。将焙烧后的产物与一定浓度的硫酸溶液放入反应器中,以一定的速率搅拌进行反应。在该过程中,还可以提高铜元素浸出效率的措施是
(3)除铁。酸浸后,测得溶液中c(Fe3+)=0.1 mol·L-1,c(Cu2+)=2 mol·L-1.向其中滴加NaOH溶液调节溶液pH除去Fe3+,则需调节溶液pH范围为
(4)沉铜。除铁后,过滤,向滤液中加入Na2SO3溶液、NaCl溶液, 搅拌下充分反应,过滤,洗涤,干燥得到CuCl。
①得到CuCl沉淀的离子方程式为
②相同条件下,CuCl沉淀率随
 的变化如下图所示。
的变化如下图所示。 大于2.5,CuCl沉淀率几乎不变的原因
大于2.5,CuCl沉淀率几乎不变的原因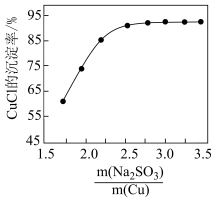
您最近一年使用:0次
【推荐3】碱式碳酸锰[Mn2(OH)2CO3]一种不溶于水的固体,是制造其他含锰化合物的原料。工业上以方锰矿(主要成分为MnO,还含有少量的Fe3O4、Al2O3、CaO、SiO2)为原料制备碱式碳酸锰。
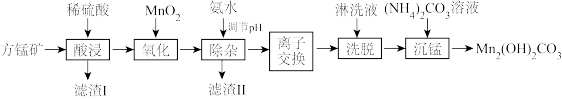
25℃时,相关物质的Ksp如下表:
回答下列问题:
(1)“酸浸”时,滤渣I的成分是_______ (填化学式)。
(2)“氧化”时,该反应的离子方程式为_______ 。
(3)“除杂”时,使用氨水的目的是将Fe3+和Al3+转化为沉淀而除去,则调节溶液的pH≥_______ :若Al3+沉淀完全时,则溶液中Fe3+的物质的量浓度为_______ mol·L-1,(通常认为溶液中的离子浓度≤1×10-5mol·L-1沉淀完全)
(4)“离子交换”和“洗脱”时,发生反应:Mn2++2HR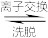 MnR2+2H+(HR是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应呈
MnR2+2H+(HR是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应呈_______ (填“酸”、“碱”或“中”)性。
(5)“沉锰”时,反应的离子方程式为_______ ,过滤、洗涤、干燥,得到Mn2(OH)2CO3,确保洗涤干净的操作是_______ 。
(6)为测定产品中锰的含量,取ag样品于烧杯中,加水溶解,加入足量的稀硫酸溶解,滴加过量的0.1000 mol·L-1(NH4)2S2O8溶液将锰元素转化为MnO ,充分反应后加热一段时间,冷却将烧杯中的溶液全部转移至250mL容量瓶中。取25.00mL于锥形瓶中,用0.1000mol·L-1FeSO4标准溶液滴定,达滴定终点时,消耗FeSO4溶液的体积为VmL。
,充分反应后加热一段时间,冷却将烧杯中的溶液全部转移至250mL容量瓶中。取25.00mL于锥形瓶中,用0.1000mol·L-1FeSO4标准溶液滴定,达滴定终点时,消耗FeSO4溶液的体积为VmL。
①滴定终点的现象是_______ 。
②该产品中锰的质量分数为_______ 。(用含a、V的式子表示)。

25℃时,相关物质的Ksp如下表:
| 物质 | Mn(OH)2 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Ca(OH)2 |
| Ksp | 2×10-13 | 5×10-17 | 3×10-39 | 1×10-32 | 6×10-6 |
(1)“酸浸”时,滤渣I的成分是
(2)“氧化”时,该反应的离子方程式为
(3)“除杂”时,使用氨水的目的是将Fe3+和Al3+转化为沉淀而除去,则调节溶液的pH≥
(4)“离子交换”和“洗脱”时,发生反应:Mn2++2HR
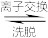 MnR2+2H+(HR是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应呈
MnR2+2H+(HR是氢型交换树脂)。洗脱为了提高“洗脱”效率,淋洗液应呈(5)“沉锰”时,反应的离子方程式为
(6)为测定产品中锰的含量,取ag样品于烧杯中,加水溶解,加入足量的稀硫酸溶解,滴加过量的0.1000 mol·L-1(NH4)2S2O8溶液将锰元素转化为MnO
 ,充分反应后加热一段时间,冷却将烧杯中的溶液全部转移至250mL容量瓶中。取25.00mL于锥形瓶中,用0.1000mol·L-1FeSO4标准溶液滴定,达滴定终点时,消耗FeSO4溶液的体积为VmL。
,充分反应后加热一段时间,冷却将烧杯中的溶液全部转移至250mL容量瓶中。取25.00mL于锥形瓶中,用0.1000mol·L-1FeSO4标准溶液滴定,达滴定终点时,消耗FeSO4溶液的体积为VmL。①滴定终点的现象是
②该产品中锰的质量分数为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】对下图中两极加以必要的联接并填空:
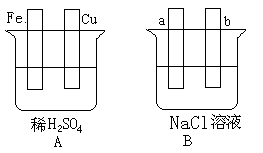
(1)在A图中,请加以必要联接 ,使铜片上冒H2气泡。________
Fe片的电极反应式:________________ ,溶液中SO42-向____ (填“铁”或“铜”)片迁移。
(2)在B图中,请加以必要联接, 使b极析出Cl2。总反应方程式:___________________ 。
(3)若将A、B串联(a接Cu,b接Fe),则a极析出的物质是____________ 。若导线中有0.2mol的电子通过, 则Fe片质量减少________ , 同时a电极产生的气体在标准状况下的体积为__________ 。

(1)在A图中,
Fe片的电极反应式:
(2)在B图中,
(3)若将A、B串联(a接Cu,b接Fe),则a极析出的物质是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】钛白粉(TiO2)是重要的白色颜料,LiFePO4是锂离子电池的正极材料。实验室模拟利用钛铁矿(主要成分为FeTiO3和少量Fe2O3、CaO、SiO2)进行钛白粉和LiFePO4的联合生产工艺如图所示:
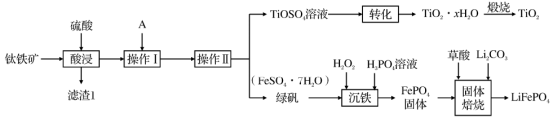
回答下列问题:
(1)LiFePO4中Fe的化合价是___________ 。
(2)“酸浸”中发生的反应较多,请写出FeTiO3发生反应的化学方程式___________ ;“滤渣1”的主要成分有___________ 。
(3)“操作I”加入过量A物质的主要目的是:___________ 。硫酸亚铁晶体易被氧化,其溶解度如表所示,由表中信息可知,“操作II”包括:真空加热浓缩、___________ 、过滤、洗涤。
(4)取170.0 g TiO2·xH2O经煅烧至恒重后固体质量为80.0 g,则x=___________ 。
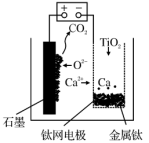
(5)可利用TiO2通过下述方法制备金属钛:用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制取金属钛。阳极反应式是___________ ,制备前后CaO的物质的量___________ (选填“减小”“不变”或“增大”)。

回答下列问题:
(1)LiFePO4中Fe的化合价是
(2)“酸浸”中发生的反应较多,请写出FeTiO3发生反应的化学方程式
(3)“操作I”加入过量A物质的主要目的是:
| 温度/℃ | 0 | 10 | 30 | 50 | 56.7 | 60 | 64 | 70 | 80 | 90 |
| 溶解度/g | 14.0 | 17.0 | 25.0 | 33.0 | 35.2 | 35.3 | 35.6 | 33.0 | 30.5 | 27 |
| 析出晶体 | FeSO4·7H2O | FeSO4·4H2O | FeSO4·H2O | |||||||
(4)取170.0 g TiO2·xH2O经煅烧至恒重后固体质量为80.0 g,则x=
(5)可利用TiO2通过下述方法制备金属钛:用如图所示装置(熔融CaF2-CaO作电解质)获得金属钙,并用钙还原TiO2制取金属钛。阳极反应式是

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】重金属元素铬的毒性较大,含铬废水需经处理达标后才能排放。
Ⅰ.某工业废水中主要含有Cr3+,同时还含有少量的Fe2+、Fe3+、Al3+、Ca2+和Mg2+等,且酸性较强。为回收利用,通常采用如下流程处理:

注:常温下,部分阳离子以氢氧化物形式完全沉淀时所需的pH,如下表:
(1)氧化过程中可代替H2O2加入的试剂是________ (填字母,下同)。
A.Na2O2 B.HNO3 C.FeCl3 D.KMnO4
(2)加入NaOH溶液调整溶液pH=8时,除去的离子是________ ;
已知钠离子交换树脂的原理:Mn++nNaR―→MRn+nNa+,此步操作被交换除去的杂质离子是____________ 。
A.Fe3+ B.Al3+ C.Ca2+ D.Mg2+
(3)还原过程在酸性条件下进行,每消耗0.8 mol Cr2O 转移4.8 mol e-,该反应离子方程式为
转移4.8 mol e-,该反应离子方程式为________________________________________________________________________ 。
Ⅱ.酸性条件下,六价铬主要以Cr2O 形式存在,工业上常用电解法处理含Cr2O
形式存在,工业上常用电解法处理含Cr2O 的废水,该法用Fe作电极电解含Cr2O
的废水,该法用Fe作电极电解含Cr2O 的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3溶液。
的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3溶液。
(1)电解时能否用Cu电极来代替Fe电极?________ (填“能”或“不能”),理由是_____________ 。
(2)常温下,Cr(OH)3的溶度积Ksp=1×10-20,假设溶液的c(Cr3+)=0.01mol/L,当pH应为______ 时开始生成沉淀。
Ⅰ.某工业废水中主要含有Cr3+,同时还含有少量的Fe2+、Fe3+、Al3+、Ca2+和Mg2+等,且酸性较强。为回收利用,通常采用如下流程处理:

注:常温下,部分阳离子以氢氧化物形式完全沉淀时所需的pH,如下表:
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Mg(OH)2 | Al(OH)3 | Cr(OH)3 |
| pH | 3.7 | 9.6 | 11.1 | 8 | 9 |
A.Na2O2 B.HNO3 C.FeCl3 D.KMnO4
(2)加入NaOH溶液调整溶液pH=8时,除去的离子是
已知钠离子交换树脂的原理:Mn++nNaR―→MRn+nNa+,此步操作被交换除去的杂质离子是
A.Fe3+ B.Al3+ C.Ca2+ D.Mg2+
(3)还原过程在酸性条件下进行,每消耗0.8 mol Cr2O
 转移4.8 mol e-,该反应离子方程式为
转移4.8 mol e-,该反应离子方程式为Ⅱ.酸性条件下,六价铬主要以Cr2O
 形式存在,工业上常用电解法处理含Cr2O
形式存在,工业上常用电解法处理含Cr2O 的废水,该法用Fe作电极电解含Cr2O
的废水,该法用Fe作电极电解含Cr2O 的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3溶液。
的酸性废水,随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3溶液。(1)电解时能否用Cu电极来代替Fe电极?
(2)常温下,Cr(OH)3的溶度积Ksp=1×10-20,假设溶液的c(Cr3+)=0.01mol/L,当pH应为
您最近一年使用:0次
【推荐1】我国力争于2030年前做到碳达峰,2060年前实现碳中和。资源化利用碳氧化合物能有效减少CO2排放,实现自然界中的碳循环。
(1)以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
Ⅰ.CO2(g)+C2H6(g)=C2H4(g)+H2O(g)+CO(g) △H=+177kJ·mol-l(主反应)
Ⅱ.C2H6(g)=CH4(g)+H2(g)+C(s) △H=+9kJ·mol-l(副反应)
反应Ⅰ的反应历程可分为如下两步:
ⅰ.C2H6(g)=C2H4(g)+H2(g) △H1
ⅱ.H2(g)+CO2(g)=H2O(g)+CO(g) △H2=+41kJ·mol-l
①△H1=____ 。
②相比于提高c(C2H6),提高c(CO2)对反应Ⅰ速率影响更大,原因是____ 。
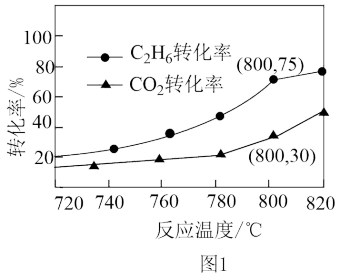
③0.1MPa时,向一恒容密闭容器中充入物质的量之比为2∶1的CO2(g)和C2H6(g),反应物转化率与反应温度的关系如图1所示。在800℃,C2H4(g)的选择性[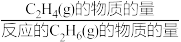 ×100%]为
×100%]为____ 。
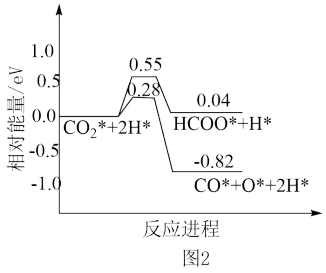
(2)CO2可制甲烷化,CO2可制甲烷化过程中,CO2活化的可能途径如图2所示。CO是CO2活化的优势中间体,可能的原因是___ 。
(3)CO2在熔融K2CO3中电解还原为正丙醇(CH3CH2CH2OH)的阴极反应式为____ 。
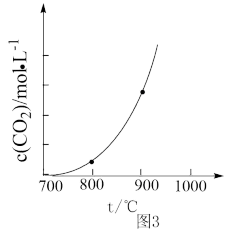
(4)CO2可用CaO吸收,发生反应:CaO(s)+CO2(g) CaCO3(s)。在不同温度下,达到平衡时体系中CO2物质的量浓度[c(CO2)]与温度的关系如图3所示。900℃下的c(CO2)远大于800℃下的c(CO2),其原因是
CaCO3(s)。在不同温度下,达到平衡时体系中CO2物质的量浓度[c(CO2)]与温度的关系如图3所示。900℃下的c(CO2)远大于800℃下的c(CO2),其原因是___ 。
(1)以CO2、C2H6为原料合成C2H4涉及的主要反应如下:
Ⅰ.CO2(g)+C2H6(g)=C2H4(g)+H2O(g)+CO(g) △H=+177kJ·mol-l(主反应)
Ⅱ.C2H6(g)=CH4(g)+H2(g)+C(s) △H=+9kJ·mol-l(副反应)
反应Ⅰ的反应历程可分为如下两步:
ⅰ.C2H6(g)=C2H4(g)+H2(g) △H1
ⅱ.H2(g)+CO2(g)=H2O(g)+CO(g) △H2=+41kJ·mol-l
①△H1=
②相比于提高c(C2H6),提高c(CO2)对反应Ⅰ速率影响更大,原因是
③0.1MPa时,向一恒容密闭容器中充入物质的量之比为2∶1的CO2(g)和C2H6(g),反应物转化率与反应温度的关系如图1所示。在800℃,C2H4(g)的选择性[
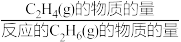 ×100%]为
×100%]为
(2)CO2可制甲烷化,CO2可制甲烷化过程中,CO2活化的可能途径如图2所示。CO是CO2活化的优势中间体,可能的原因是

(3)CO2在熔融K2CO3中电解还原为正丙醇(CH3CH2CH2OH)的阴极反应式为
(4)CO2可用CaO吸收,发生反应:CaO(s)+CO2(g)
 CaCO3(s)。在不同温度下,达到平衡时体系中CO2物质的量浓度[c(CO2)]与温度的关系如图3所示。900℃下的c(CO2)远大于800℃下的c(CO2),其原因是
CaCO3(s)。在不同温度下,达到平衡时体系中CO2物质的量浓度[c(CO2)]与温度的关系如图3所示。900℃下的c(CO2)远大于800℃下的c(CO2),其原因是
您最近一年使用:0次
【推荐2】铜、镍被广泛应用于石油化工、国防、冶金、电子等多个行业。从金川镍矿(铜镍硫化矿,主要含有NiS、CuS、Cu2S,还含有少量杂质SiO2、FeS、MgO等)中提取铜盐、镍盐的工艺流程如图所示。
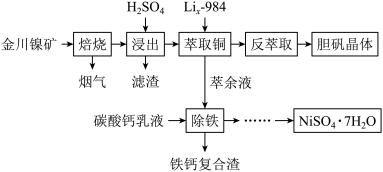
已知:表1金川镍矿全分析
表2 硫酸镍结晶水合物的形态与温度的关系:
(1)“焙烧”的作用为____ 。
(2)Lix-984(HR)萃取时的反应机理为:2HR+Cu2+ R2Cu+2H+ ∆H>0,铜离子在油水两相的分配比D=
R2Cu+2H+ ∆H>0,铜离子在油水两相的分配比D=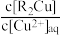 ,c[R2Cu]、c[Cu2+]aq分别表示微粒在平衡时油相、水相的浓度。已知初始时水相铜离子的浓度为0.032 mol/L,当络合萃取达到平衡时紫外分光光度计测得c[Cu2+]aq=25.6 mg/L,则D=
,c[R2Cu]、c[Cu2+]aq分别表示微粒在平衡时油相、水相的浓度。已知初始时水相铜离子的浓度为0.032 mol/L,当络合萃取达到平衡时紫外分光光度计测得c[Cu2+]aq=25.6 mg/L,则D=____ 。(假设油相与水相的体积相等,且忽略萃取过程中体积的变化);“反萃取”可选用的萃取试剂为____ 。
(3)计算Ni(OH)2的Ksp____ 。(已知:恰好沉淀完全时溶液中Ni2+浓度为1.0×10-5 mol/L)
(4)设计以除铁后的滤液制备纯净的NiSO4•7H2O的实验方案:向除铁后的滤液中____ ,洗涤,干燥得NiSO4•7H2O产品。(实验中须使用的试剂:2.0 mol/L硫酸、1.0 mol/LNa2CO3溶液,蒸馏水)
(5)NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiO(OH),该反应的离子方程式是____ 。

已知:表1金川镍矿全分析
| 沉淀物 | Fe(OH)3 | Mg(OH)2 | Ni(OH)2 |
| 开始沉淀时的pH | 2.7 | 9.4 | 7.2 |
| 沉淀完全时的pH | 3.7 | 12.4 | 8.7 |
| 温度 | 低于30.8℃ | 30.8℃~53.8℃ | 53.8℃~280℃ | 高于280℃ |
| 晶体形态 | NiSO4•7H2O | NiSO4•6H2O | 多种结晶水合物 | NiSO4 |
(2)Lix-984(HR)萃取时的反应机理为:2HR+Cu2+
 R2Cu+2H+ ∆H>0,铜离子在油水两相的分配比D=
R2Cu+2H+ ∆H>0,铜离子在油水两相的分配比D=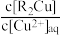 ,c[R2Cu]、c[Cu2+]aq分别表示微粒在平衡时油相、水相的浓度。已知初始时水相铜离子的浓度为0.032 mol/L,当络合萃取达到平衡时紫外分光光度计测得c[Cu2+]aq=25.6 mg/L,则D=
,c[R2Cu]、c[Cu2+]aq分别表示微粒在平衡时油相、水相的浓度。已知初始时水相铜离子的浓度为0.032 mol/L,当络合萃取达到平衡时紫外分光光度计测得c[Cu2+]aq=25.6 mg/L,则D=(3)计算Ni(OH)2的Ksp
(4)设计以除铁后的滤液制备纯净的NiSO4•7H2O的实验方案:向除铁后的滤液中
(5)NiSO4在强碱溶液中用NaClO氧化,可制得碱性镍镉电池电极材料NiO(OH),该反应的离子方程式是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】氮和碳的化合物在生产生活中应用广泛。
(1)①氯胺(NH2Cl)的电子式为_______________ 。
②NH2Cl与水反应生成强氧化性的物质,可作长效缓释消毒剂,该反应的化学方程式为__________________ 。
(2)用焦炭还原NO的反应为:2NO(g)+C(s) N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
①该反应为_______________ (填“放热”或“吸热”)反应。
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=___________ 。
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s) N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如下图所示:
N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如下图所示:

①A、B两点的浓度平衡常数关系:Kc(A)_____ Kc(B)(填“<”或“>”或“=”)。
②A、B、C三点中NO2的转化率最高的是__________ (填“A”或“B”或“C”)点。
③计算C点时该反应的压强平衡常数Kp(C)=________ (Kp是用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)最新研究发现,用隔膜电解法可以处理高浓度乙醛废水。原理:使用惰性电极电解,乙醛分别在阴、阳极转化为乙醇和乙酸,总反应为:2CH3CHO+H2O CH3CH2OH+CH3COOH。实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的 处理过程,其装置示意图如下图所示:
CH3CH2OH+CH3COOH。实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的 处理过程,其装置示意图如下图所示:
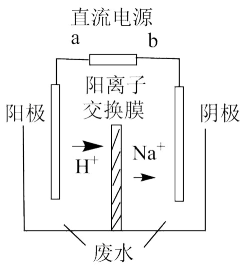
①试写出电解过程中,阴极的电极反应式:_________________________ 。
②在实际处理过程中,当电路中I=50A时,10min处理乙醛8.8g,则电流效率为__ (计算结果保留3位有效数字,每个电子的电量为1.6×10-19C,电流效率=实际反应所需电量/电路中通过电量×100%)。
(1)①氯胺(NH2Cl)的电子式为
②NH2Cl与水反应生成强氧化性的物质,可作长效缓释消毒剂,该反应的化学方程式为
(2)用焦炭还原NO的反应为:2NO(g)+C(s)
 N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g)+CO2(g),向容积均为1L的甲、乙、丙三个恒容恒温(反应温度分别为400℃、400℃、T℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:| t/min | 0 | 40 | 80 | 120 | 160 |
| n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
| n(NO)(乙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
| n(NO)(丙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
②乙容器在200min达到平衡状态,则0~200min内用NO的浓度变化表示的平均反应速率v(NO)=
(3)用焦炭还原NO2的反应为:2NO2(g)+2C(s)
 N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如下图所示:
N2(g)+2CO2(g),在恒温条件下,1mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如下图所示:
①A、B两点的浓度平衡常数关系:Kc(A)
②A、B、C三点中NO2的转化率最高的是
③计算C点时该反应的压强平衡常数Kp(C)=
(4)最新研究发现,用隔膜电解法可以处理高浓度乙醛废水。原理:使用惰性电极电解,乙醛分别在阴、阳极转化为乙醇和乙酸,总反应为:2CH3CHO+H2O
 CH3CH2OH+CH3COOH。实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的 处理过程,其装置示意图如下图所示:
CH3CH2OH+CH3COOH。实验室中,以一定浓度的乙醛-Na2SO4溶液为电解质溶液,模拟乙醛废水的 处理过程,其装置示意图如下图所示:
①试写出电解过程中,阴极的电极反应式:
②在实际处理过程中,当电路中I=50A时,10min处理乙醛8.8g,则电流效率为
您最近一年使用:0次



