与氨气相关的化学变化是氮循环和转化的重要一环,对生产、生活有重要的价值。
1.下图转化途径中属于“固氮”的是___________。
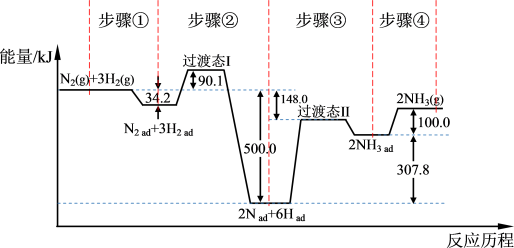
合成氨是目前转化空气中氮最有效的工业方法,其反应历程和能量变化的简图如下:(图中ad表示物质吸附在催化剂表面时的状态) 的
的
___________  ,对总反应速率影响较大的是步骤
,对总反应速率影响较大的是步骤___________ 。(填写编号)3.若改变某一条件,使合成氨的化学反应速率加快,下列解释正确的是___________。
4.氨是极具前景的氢能载体和性能卓越的“零碳”燃料,利用 的燃烧反应
的燃烧反应 能设计成燃料电池,其工作原理如图所示。电极
能设计成燃料电池,其工作原理如图所示。电极 为
为___________ (选填“正”或“负”)极;电极 的电极反应式为
的电极反应式为___________ ;当正负极共消耗3.136L(标准状况)气体时,通过负载的电子数为___________ 个。 等离子的废液,为了对废液进行处理,某同学采用硫化物沉淀法处理
等离子的废液,为了对废液进行处理,某同学采用硫化物沉淀法处理 。
。
已知:常温下
5.常温下,调节 溶液的
溶液的 ,比较溶液中含硫微粒浓度的大小
,比较溶液中含硫微粒浓度的大小___________ 。
6.常温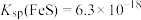 ,下列说法正确的是___________。
,下列说法正确的是___________。
1.下图转化途径中属于“固氮”的是___________。
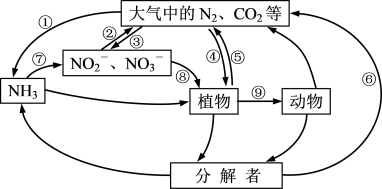
| A.④⑤⑥ | B.①③④ | C.①⑤⑦ | D.②⑧⑨ |
 的
的
 ,对总反应速率影响较大的是步骤
,对总反应速率影响较大的是步骤| A.升高温度,使单位体积内活化分子百分数增加 |
| B.增加反应物的浓度,使单位体积内活化分子百分数增加 |
| C.使用催化剂,能降低反应活化能,使单位体积内活化分子数增加 |
| D.增大压强,能降低反应的活化能,使单位体积内活化分子数增加 |
 的燃烧反应
的燃烧反应 能设计成燃料电池,其工作原理如图所示。电极
能设计成燃料电池,其工作原理如图所示。电极 为
为 的电极反应式为
的电极反应式为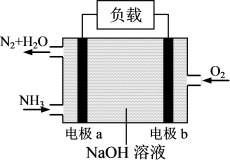
 等离子的废液,为了对废液进行处理,某同学采用硫化物沉淀法处理
等离子的废液,为了对废液进行处理,某同学采用硫化物沉淀法处理 。
。已知:常温下

5.常温下,调节
 溶液的
溶液的 ,比较溶液中含硫微粒浓度的大小
,比较溶液中含硫微粒浓度的大小6.常温
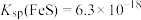 ,下列说法正确的是___________。
,下列说法正确的是___________。A.常温下, 的溶解度大于FeS 的溶解度大于FeS |
B.反应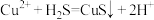 不能发生 不能发生 |
C.除去废液中的 ,可选用 ,可选用 作沉淀剂 作沉淀剂 |
D.常温下,向饱和 溶液中加入少量 溶液中加入少量 固体后, 固体后,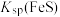 减小 减小 |
更新时间:2024-05-03 16:50:04
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】以煤为主要原料可以制备乙二醇,相关工艺流程如图:

①该反应能够自发进行,可以推出a_______ 0;(填“>”“<”或“=”)。
②在一定温度下,向体积为1L的恒容密闭容器中充入2mol 和3mol
和3mol ,反应前后压强之比为15∶7,则该温度下的化学平衡常数
,反应前后压强之比为15∶7,则该温度下的化学平衡常数
_______ 。
(2)方法2:在恒容密闭容器中投入草酸二甲酯和 发生如下反应:
发生如下反应:


为提高乙二醇的产量和速率,宜采用的措施是_______ (填字母)。
A.升高温度 B.增大压强 C.增大氢气浓度
(3)草酸二甲酯水解生成草酸:
①设计实验证明草酸为弱酸的方案及其现象均正确的有_______ 。
A.室温下,取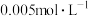 的
的 溶液,测其
溶液,测其
B.室温下,取 的
的 溶液,测其
溶液,测其
C.室温下,取 的
的 溶液稀释100倍后,测其
溶液稀释100倍后,测其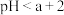
D.标准状况下,取 的
的 溶液100mL与足量锌粉反应,收集到
溶液100mL与足量锌粉反应,收集到 体积为224mL
体积为224mL
② 溶液显
溶液显_______ (填“酸性”、“中性”或“碱性”),溶液中各离子浓度从大到小的顺序为_______ 。
(4)乙二醇、空气在KOH溶液中构成燃料电池,加入乙二醇的电极为电源的_______ (填“正”或“负”)极,负极反应式为_______ 。
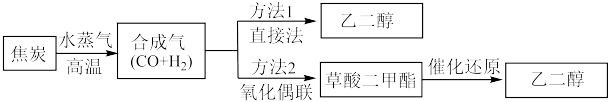


①该反应能够自发进行,可以推出a
②在一定温度下,向体积为1L的恒容密闭容器中充入2mol
 和3mol
和3mol ,反应前后压强之比为15∶7,则该温度下的化学平衡常数
,反应前后压强之比为15∶7,则该温度下的化学平衡常数
(2)方法2:在恒容密闭容器中投入草酸二甲酯和
 发生如下反应:
发生如下反应:

为提高乙二醇的产量和速率,宜采用的措施是
A.升高温度 B.增大压强 C.增大氢气浓度
(3)草酸二甲酯水解生成草酸:

①设计实验证明草酸为弱酸的方案及其现象均正确的有
A.室温下,取
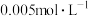 的
的 溶液,测其
溶液,测其
B.室温下,取
 的
的 溶液,测其
溶液,测其
C.室温下,取
 的
的 溶液稀释100倍后,测其
溶液稀释100倍后,测其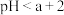
D.标准状况下,取
 的
的 溶液100mL与足量锌粉反应,收集到
溶液100mL与足量锌粉反应,收集到 体积为224mL
体积为224mL②
 溶液显
溶液显(4)乙二醇、空气在KOH溶液中构成燃料电池,加入乙二醇的电极为电源的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上生产硫酸时,将 氧化为
氧化为 是关键一步。
是关键一步。
(1)某温度下, 。开始时在10L的密闭容器中加入
。开始时在10L的密闭容器中加入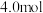
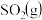 和
和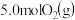 ,当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=
,当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=___________ 。
(2)一定条件下,向一带活塞的密闭容器中充入 和
和 ,发生下列反应:
,发生下列反应: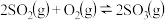 达到平衡后改变下述条件,
达到平衡后改变下述条件, 、
、 、
、 气体平衡浓度都比原来增大的是
气体平衡浓度都比原来增大的是 ___________ 。
A.保持温度和容器体积不变,充入2mol
B.保持温度和容器体积不变,充入2mol
C.保持温度和容器体积不变,充入
 和
和

D.保持温度和容器内压强不变,充入1mol
E.升高温度
F.移动活塞压缩气体
(3)某人设想以如图所示装置用电化学原理生产硫酸,写出通入 的电极的电极反应式:
的电极的电极反应式: ___________ 。
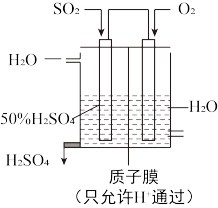
(4)在 的
的 溶液中,离子浓度由大到小的顺序是
溶液中,离子浓度由大到小的顺序是 ___________ 。
 氧化为
氧化为 是关键一步。
是关键一步。(1)某温度下,
 。开始时在10L的密闭容器中加入
。开始时在10L的密闭容器中加入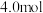
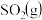 和
和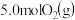 ,当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=
,当反应达到平衡时共放出热量196kJ,该温度下平衡常数K=(2)一定条件下,向一带活塞的密闭容器中充入
 和
和 ,发生下列反应:
,发生下列反应: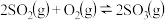 达到平衡后改变下述条件,
达到平衡后改变下述条件, 、
、 、
、 气体平衡浓度都比原来增大的是
气体平衡浓度都比原来增大的是 A.保持温度和容器体积不变,充入2mol

B.保持温度和容器体积不变,充入2mol

C.保持温度和容器体积不变,充入

 和
和

D.保持温度和容器内压强不变,充入1mol

E.升高温度
F.移动活塞压缩气体
(3)某人设想以如图所示装置用电化学原理生产硫酸,写出通入
 的电极的电极反应式:
的电极的电极反应式: 
(4)在
 的
的 溶液中,离子浓度由大到小的顺序是
溶液中,离子浓度由大到小的顺序是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】硫及其化合物在生产生活中应用广泛。回答下列问题:
(1)铁铵矾是一种化学物质,分子式是NH4Fe(SO4)2·12H2O,其溶于水后,溶液中的离子浓度大小关系为_____________________ 。
(2)已知某溶液中含有CO32-、SO42-等离子,取一定量的该溶液,向其中滴加BaCl2溶液,当CO32-开始沉淀时,溶液中 =
=_____ 。(已知Ksp(BaSO4)=1.0×10-10,Ksp(BaCO3)=2.5×10-9)
(3)已知:S2Cl2(l)+Cl2(g)=2SCl2(l) ΔH=-50.2 kJ·mol-1。断裂1mol Cl-Cl键、1mol S-S键分别需要吸收243kJ、268kJ的能量,则断裂1mol S-Cl键需要吸收的能量为_____________ kJ。
(4)某容积不变的密闭容器中发生如下反应:2SO2(g)+O2(g) 2SO3(g) △H=-197 kJ·mol-1。
2SO3(g) △H=-197 kJ·mol-1。
①下列能说明反应达到平衡状态的是________________
a.体系压强保持不变 b.混合气体的密度保持不变
c.SO3和O2的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol SO2
②向同温、同体积的两个密闭容器中分别充入气体:(甲)2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2 ;恒温、恒容下反应达平衡时,两个容器内的压强大小关系为____ (用p甲、p乙表示)。
(5)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可以制备H2SO4,其原理如下图所示(电极材料为石墨)。

阳极的电极反应式为___________________________________ 。
(1)铁铵矾是一种化学物质,分子式是NH4Fe(SO4)2·12H2O,其溶于水后,溶液中的离子浓度大小关系为
(2)已知某溶液中含有CO32-、SO42-等离子,取一定量的该溶液,向其中滴加BaCl2溶液,当CO32-开始沉淀时,溶液中
 =
=(3)已知:S2Cl2(l)+Cl2(g)=2SCl2(l) ΔH=-50.2 kJ·mol-1。断裂1mol Cl-Cl键、1mol S-S键分别需要吸收243kJ、268kJ的能量,则断裂1mol S-Cl键需要吸收的能量为
(4)某容积不变的密闭容器中发生如下反应:2SO2(g)+O2(g)
 2SO3(g) △H=-197 kJ·mol-1。
2SO3(g) △H=-197 kJ·mol-1。①下列能说明反应达到平衡状态的是
a.体系压强保持不变 b.混合气体的密度保持不变
c.SO3和O2的体积比保持不变 d.每消耗1 mol SO3的同时生成1 mol SO2
②向同温、同体积的两个密闭容器中分别充入气体:(甲)2 mol SO2和1 mol O2;(乙) 1 mol SO2和0.5 mol O2 ;恒温、恒容下反应达平衡时,两个容器内的压强大小关系为
(5)用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可以制备H2SO4,其原理如下图所示(电极材料为石墨)。

阳极的电极反应式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】硫酸锰在农业上是重要微量元素肥料,也是植物合成叶绿素的催化剂。一种以高硫锰矿(主要成分为含锰化合物及 )与氧化锰矿(主要成分为
)与氧化锰矿(主要成分为 等锰的氧化物)为原料制备硫酸锰的工艺流程如下:
等锰的氧化物)为原料制备硫酸锰的工艺流程如下:
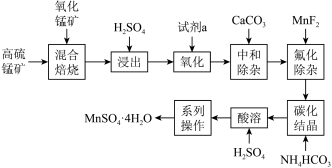
已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO。
②金属离子在水溶液中沉淀的 范围如下表所示(
范围如下表所示( );
);
③离子浓度 时,离子沉淀完全。
时,离子沉淀完全。
(1)“混合焙烧”时一般会将原料粉碎,这样做的主要目的是___________ 。
(2)“混合焙烧”后产生的 气体,不能通过___________溶液吸收。(单选)
气体,不能通过___________溶液吸收。(单选)
(3)若试剂a为 ,则氧化步骤发生反应的离子方程式为
,则氧化步骤发生反应的离子方程式为___________ ,若省略“氧化”步骤,造成的影响是___________ 。
(4)“中和除杂”时,应控制溶液的 范围是
范围是___________ 。
(5)“氟化除杂”后,溶液中 浓度为
浓度为 。则溶液中
。则溶液中 和
和 的比值为
的比值为___________ 。(已知: ;
;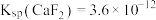 )
)
(6)“碳化结晶”时,加入碳酸氢铵,产生 沉淀。
沉淀。
①碳酸氢铵溶液的电荷守恒式为___________ 。
②“碳化结晶”时,发生反应的离子方程式为___________ 。
(7)“系列操作”为___________ ,___________ ,过滤,洗涤,干燥。
 )与氧化锰矿(主要成分为
)与氧化锰矿(主要成分为 等锰的氧化物)为原料制备硫酸锰的工艺流程如下:
等锰的氧化物)为原料制备硫酸锰的工艺流程如下:
已知:①“混合焙烧”后烧渣含MnSO4、Fe2O3及少量FeO、Al2O3、MgO。
②金属离子在水溶液中沉淀的
 范围如下表所示(
范围如下表所示( );
);| 物质 |  |  |  |  |
开始沉淀的 | 1.9 | 7.6 | 7.3 | 3.0 |
完全沉淀的 | 3.2 | 9.6 | 9.3 | 5.2 |
 时,离子沉淀完全。
时,离子沉淀完全。(1)“混合焙烧”时一般会将原料粉碎,这样做的主要目的是
(2)“混合焙烧”后产生的
 气体,不能通过___________溶液吸收。(单选)
气体,不能通过___________溶液吸收。(单选)A. | B.氨水 | C.酸性高锰酸钾 | D.稀硫酸 |
(3)若试剂a为
 ,则氧化步骤发生反应的离子方程式为
,则氧化步骤发生反应的离子方程式为(4)“中和除杂”时,应控制溶液的
 范围是
范围是(5)“氟化除杂”后,溶液中
 浓度为
浓度为 。则溶液中
。则溶液中 和
和 的比值为
的比值为 ;
;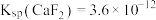 )
)(6)“碳化结晶”时,加入碳酸氢铵,产生
 沉淀。
沉淀。①碳酸氢铵溶液的电荷守恒式为
②“碳化结晶”时,发生反应的离子方程式为
(7)“系列操作”为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】锶(Sr)为第五周期ⅡA族元素,其化合物六水氯化锶(SrCl2·6H2O)是实验室重要的分析试剂,工业上常以天青石(主要成分为SrSO4)为原料制备,生产流程如下:
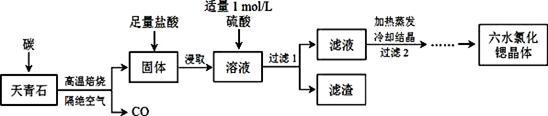
已知:① 经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质;
② SrSO4、BaSO4的溶度积常数分别为3.3×10-7、1.1×10-10;
③ SrCl2·6H2O的摩尔质量为:267 g/mol。
(1)天青石焙烧前先研磨粉碎,其目的是___________________ 。
(2)隔绝空气高温焙烧,若0.5 mol SrSO4中只有S被还原,转移了4 mol电子。写出该反应的化学方程式:_____________________________________________ 。
(3)为了得到较纯的六水氯化锶晶体,过滤2后还需进行的两步操作是_______________ 。
(4)加入硫酸的目的是______________________ 。为了提高原料的利用率,滤液中Sr2+的浓度应不高于_________ mol/L(注:此时滤液中Ba2+浓度为1×10-5mol/L)。
(5)产品纯度检测:称取1.000g产品溶解于适量水中,向其中加入含AgNO3 1.100×10-2mol的AgNO3溶液(溶液中除Cl―外,不含其它与Ag+反应的离子),待Cl―完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+ 以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是_________________________________________ 。
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为______ (保留4位有效数字)。

已知:① 经盐酸浸取后,溶液中除含有Sr2+和Cl-外,还含有少量Ba2+杂质;
② SrSO4、BaSO4的溶度积常数分别为3.3×10-7、1.1×10-10;
③ SrCl2·6H2O的摩尔质量为:267 g/mol。
(1)天青石焙烧前先研磨粉碎,其目的是
(2)隔绝空气高温焙烧,若0.5 mol SrSO4中只有S被还原,转移了4 mol电子。写出该反应的化学方程式:
(3)为了得到较纯的六水氯化锶晶体,过滤2后还需进行的两步操作是
(4)加入硫酸的目的是
(5)产品纯度检测:称取1.000g产品溶解于适量水中,向其中加入含AgNO3 1.100×10-2mol的AgNO3溶液(溶液中除Cl―外,不含其它与Ag+反应的离子),待Cl―完全沉淀后,用含Fe3+的溶液作指示剂,用0.2000 mol/L的NH4SCN标准溶液滴定剩余的AgNO3,使剩余的Ag+ 以AgSCN白色沉淀的形式析出。
①滴定反应达到终点的现象是
②若滴定过程用去上述浓度的NH4SCN溶液20.00 mL,则产品中SrCl2·6H2O的质量百分含量为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】金属钛(Ti)因其硬度大、熔点高、常温时耐酸碱腐蚀而被广泛用作高新科技材料,被誉为“未来金属”。以钛铁矿(主要成分钛酸亚铁)为主要原料冶炼金属钛同时获得副产品甲的工业生产流程如下。
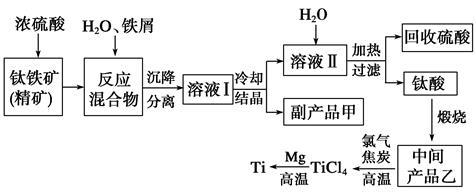
请回答下列问题。
(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为2R+C===2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为______ ;钛酸亚铁和浓H2SO4反应的产物之一是TiOSO4,反应中无气体生成,该反应的化学方程式为_________ 。
(2)上述生产流程中加入铁屑的目的是___________ 。此时溶液中含有Fe2+、TiO2+和少量Mg2+等阳离子。常温下,其对应氢氧化物的Ksp如下表所示。
①常温下,若所得溶液中Mg2+的物质的量浓度为0.001 8 mol/L,当溶液的pH等于________ 时,Mg(OH)2开始沉淀。
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方程式为____________ 。
(3)中间产品乙与焦炭、氯气在高温下发生反应制取TiCl4的方程式为_______ 。Mg还原TiCl4过程中必须在1070 K的温度下进行,你认为还应该控制的反应条件是_______ 。除去所得金属钛中少量的金属镁可用的试剂是______ 。
(4)在800~1 000 ℃时电解TiO2也可制得海绵钛,装置如下图所示。
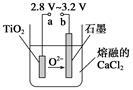
图中b是电源的________ 极,阴极的电极反应式为________ 。

请回答下列问题。
(1)钛酸亚铁(用R表示)与碳在高温下反应的化学方程式为2R+C===2Fe+2TiO2+CO2↑,钛酸亚铁的化学式为
(2)上述生产流程中加入铁屑的目的是
| 氢氧化物 | Fe(OH)2 | TiO(OH)2 | Mg(OH)2 |
| Ksp | 8.0×10-16 | 1.0×10-29 | 1.8×10-11 |
①常温下,若所得溶液中Mg2+的物质的量浓度为0.001 8 mol/L,当溶液的pH等于
②若将含有Fe2+、TiO2+和Mg2+的溶液加水稀释,立即析出大量白色沉淀,该反应的离子方程式为
(3)中间产品乙与焦炭、氯气在高温下发生反应制取TiCl4的方程式为
(4)在800~1 000 ℃时电解TiO2也可制得海绵钛,装置如下图所示。

图中b是电源的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】甲烷和甲醇(CH3OH)既是重要的化工原料,又是未来重要的能源物质。
(1)该反应为 ,反应过程中能量变化如图所示。则1molCO(g)和2molH2(g)的总能量
,反应过程中能量变化如图所示。则1molCO(g)和2molH2(g)的总能量___________ (填“>”、“<”或“=”)1molCH3OH(g)的能量。

(2)在容积为1L的恒容密闭容器中投入等物质的量的CO2(g)和H2(g),进行反应: 。CO2(g)、CH3OH(g)的物质的量随时间变化关系如图所示:
。CO2(g)、CH3OH(g)的物质的量随时间变化关系如图所示:

图中,表示正反应速率与逆反应速率相等的点是___________ (填“a”、“b”、“c”或“d”)。用同一物质表示反应速率时,a、c两点的正反应速率:υa___________ υc (填“>”、“<”或“=”,下同),该反应达到平衡时,CO2的转化率___________ 50%。
(3)将2.0molCH4(g)和3.0molH2O(g)通入容积为2L的恒容密闭容器中,恒温条件下发生反应: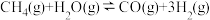 。测得在10min时反应达到平衡,此时CH4的物质的量为1.6mol,则0~10min内,用CO表示该反应的平均反应速率υ(CO)=
。测得在10min时反应达到平衡,此时CH4的物质的量为1.6mol,则0~10min内,用CO表示该反应的平均反应速率υ(CO)=___________ 。下列描述中能说明该反应已达平衡状态的是___________ (填标号)。
a. 断裂3mol H−H键时,生成2mol H−O键 b. 容器内混合气体的平均摩尔质量保持不变
c. 容器内混合气体的压强保持不变 d. 容器内CO与H2的体积之比保持不变
(4)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如图所示:

①外电路电子移动方向:___________ (填“a→b”或“b→a”)。
②a电极的电极方程式为___________ 。
③标准状况下消耗5.6LO2,外电路中通过导线的电子的数目为___________ 。
(1)该反应为
 ,反应过程中能量变化如图所示。则1molCO(g)和2molH2(g)的总能量
,反应过程中能量变化如图所示。则1molCO(g)和2molH2(g)的总能量
(2)在容积为1L的恒容密闭容器中投入等物质的量的CO2(g)和H2(g),进行反应:
 。CO2(g)、CH3OH(g)的物质的量随时间变化关系如图所示:
。CO2(g)、CH3OH(g)的物质的量随时间变化关系如图所示:
图中,表示正反应速率与逆反应速率相等的点是
(3)将2.0molCH4(g)和3.0molH2O(g)通入容积为2L的恒容密闭容器中,恒温条件下发生反应:
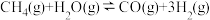 。测得在10min时反应达到平衡,此时CH4的物质的量为1.6mol,则0~10min内,用CO表示该反应的平均反应速率υ(CO)=
。测得在10min时反应达到平衡,此时CH4的物质的量为1.6mol,则0~10min内,用CO表示该反应的平均反应速率υ(CO)=a. 断裂3mol H−H键时,生成2mol H−O键 b. 容器内混合气体的平均摩尔质量保持不变
c. 容器内混合气体的压强保持不变 d. 容器内CO与H2的体积之比保持不变
(4)甲烷可直接应用于燃料电池,该电池采用KOH溶液为电解质,其工作原理如图所示:

①外电路电子移动方向:
②a电极的电极方程式为
③标准状况下消耗5.6LO2,外电路中通过导线的电子的数目为
您最近一年使用:0次
【推荐2】根据题意请回答有关氮的氧化物和氢化物的问题:
(1)随着人类社会的发展,氮氧化物的排放导致一系列问题。NO形成硝酸型酸雨的化学方程式为_______ 。一定条件下,用甲烷可以消除氮的氧化物(NOx)的污染。已知:①CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ΔH1=-574.1 kJ·mol-1,
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160.6 kJ·mol-1则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=___________ 。
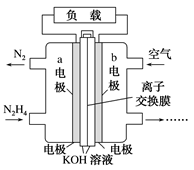
(2)肼(N2H4)可以用作燃料电池的原料。肼的电子式为_________ ,一种以液态肼为燃料的电池装置如图所示,该电池用空气中的氧气作为氧化剂,KOH溶液作为电解质溶液。b电极是_____ 极(填“正”或“负”),a电极的电极反应式:__________________ 。
(3)25 ℃时,Kb(NH3·H2O)=1.8×10-5 mol·L-1,向含a mol NH4NO3的溶液中滴加b L氨水呈中性,则所滴加氨水的浓度为___________ 。
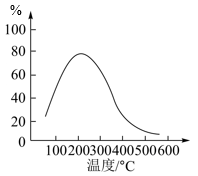
(4)在体积恒定的密闭容器中有可逆反应: 2NO(g)+O2(g) 2NO2(g) ΔH<0 ,NO和O2的起始浓度之比为2:1,反应经历相同时间,测得不同温度下NO转化为NO2的转化率如图,则150 ℃时,v(正)
2NO2(g) ΔH<0 ,NO和O2的起始浓度之比为2:1,反应经历相同时间,测得不同温度下NO转化为NO2的转化率如图,则150 ℃时,v(正)________ v(逆)(填“>”或“<”)。
(5)判断在恒温恒容条件下该反应已达到平衡状态的是_____
A 2v正(NO2)=v逆(O2) B 反应容器中压强不随时间变化而变化
C 混合气体颜色深浅保持不变 D 混合气体平均相对分子质量保持不变
(1)随着人类社会的发展,氮氧化物的排放导致一系列问题。NO形成硝酸型酸雨的化学方程式为
②CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ΔH2=-1160.6 kJ·mol-1则CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g) ΔH=
(2)肼(N2H4)可以用作燃料电池的原料。肼的电子式为

(3)25 ℃时,Kb(NH3·H2O)=1.8×10-5 mol·L-1,向含a mol NH4NO3的溶液中滴加b L氨水呈中性,则所滴加氨水的浓度为
(4)在体积恒定的密闭容器中有可逆反应: 2NO(g)+O2(g)
 2NO2(g) ΔH<0 ,NO和O2的起始浓度之比为2:1,反应经历相同时间,测得不同温度下NO转化为NO2的转化率如图,则150 ℃时,v(正)
2NO2(g) ΔH<0 ,NO和O2的起始浓度之比为2:1,反应经历相同时间,测得不同温度下NO转化为NO2的转化率如图,则150 ℃时,v(正)
(5)判断在恒温恒容条件下该反应已达到平衡状态的是
A 2v正(NO2)=v逆(O2) B 反应容器中压强不随时间变化而变化
C 混合气体颜色深浅保持不变 D 混合气体平均相对分子质量保持不变
您最近一年使用:0次
【推荐3】Ⅰ.如图所示,U形管内盛有100mL的溶液,按要求回答下列问题:

(1)打开K2 ,合并K1,若所盛溶液为CuSO4溶液: B极的电极反应式为______
(2)打开K1,合并K2,若所盛溶液为滴有酚酞的KCl溶液,则:总反应化学方程式是__________________ 。
(3)反应一段时间后打开K2,若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2mL,将溶液充分混合,常温下溶液的pH约为________ 。若要使电解质溶液恢复到原状态,需向U形管内加入或通入一定量的 __________ 。
Ⅱ.CO用途广泛,工业应用时离不开平衡思想的指导:在某一容积为5L的体积不变的密闭容器内,加入0.3 mol 的CO和0.3mol的H 2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H20(g) CO2(g)+H2(g) △H>0,反应中CO2的浓度随时间变化情况如下图:
CO2(g)+H2(g) △H>0,反应中CO2的浓度随时间变化情况如下图:

(1)根据图上数据,该温度(800℃)下的平衡常数K=____________________________ 。
(2)在体积不变的条件下,改变下列条件能使平衡常数K增大的有______________ (填字母)
(3)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3mol的水蒸气,重新达到平衡后,H2O的转化率______________ (填“升高”、“降低”、“不变”)。
(4)在催化剂和800℃的条件下,在某一时刻测得c(CO)=c(H2O)= 0.09mol·L-1;c(CO2)=c(H2)= 0.13 mol·L-1,则此时正、逆反应速率的大小:υ正_________ υ逆(填“>”、“<”或“=”)。

(1)打开K2 ,合并K1,若所盛溶液为CuSO4溶液: B极的电极反应式为
(2)打开K1,合并K2,若所盛溶液为滴有酚酞的KCl溶液,则:总反应化学方程式是
(3)反应一段时间后打开K2,若忽略溶液的体积变化和气体的溶解,B极产生气体的体积(标准状况)为11.2mL,将溶液充分混合,常温下溶液的pH约为
Ⅱ.CO用途广泛,工业应用时离不开平衡思想的指导:在某一容积为5L的体积不变的密闭容器内,加入0.3 mol 的CO和0.3mol的H 2O,在催化剂存在和800℃的条件下加热,发生如下反应:CO(g)+H20(g)
 CO2(g)+H2(g) △H>0,反应中CO2的浓度随时间变化情况如下图:
CO2(g)+H2(g) △H>0,反应中CO2的浓度随时间变化情况如下图:
(1)根据图上数据,该温度(800℃)下的平衡常数K=
(2)在体积不变的条件下,改变下列条件能使平衡常数K增大的有
A.升高温度 B.降低温度 C.增大压强 D.减小压强 E.加入催化剂 G.移出一氧化碳气体
(3)若保持温度和容器的体积不变,在(1)中上述平衡体系中,再充入0.3mol的水蒸气,重新达到平衡后,H2O的转化率
(4)在催化剂和800℃的条件下,在某一时刻测得c(CO)=c(H2O)= 0.09mol·L-1;c(CO2)=c(H2)= 0.13 mol·L-1,则此时正、逆反应速率的大小:υ正
您最近一年使用:0次



