工业上利用铁的氧化物在高温条件下循环裂解水制氢气的流程如下图所示。
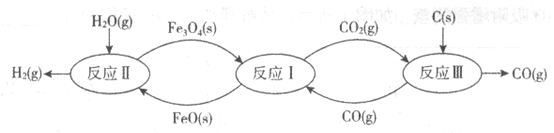
(1)反应I的化学方程式为:Fe3O4(s)+CO(g) 3FeO(s)+CO2(g),反应Ⅱ的化学方程式为
3FeO(s)+CO2(g),反应Ⅱ的化学方程式为_________ ,对比反应I、Ⅱ,铁的氧化物在循环裂解水制氢气过程中的作用是_________ 。用化学方程式表示反应I、Ⅱ、Ⅲ的总结果:_________ 。
(2)反应III为:CO2(g)+C(s) 2CO(g)
2CO(g)  H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有
H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有_________ (任写一条措施)。
(3)上述流程中铁的氧化物可用来制备含有Fe3+的刻蚀液,用刻蚀液刻蚀铜板时,可观察到溶液颜色逐渐变蓝,该反应的离子方程式为_________ 。刻蚀液使用一段时间后会失效,先加酸,再加入过氧化氢溶液,可实现刻蚀液中Fe3+的再生,该反应的离子方程式为_________ 。
(4)上述流程中碳的氧化物可用来制备碳酰肼[CO(NHNH2)2,其中碳元素为+4价]。加热条件下,碳酰肼能将锅炉内表面锈蚀后的氧化铁转化为结构紧密的四氧化三铁保护层,并生成氮气、水和二氧化碳。该反应的化学方程式为_________ 。

(1)反应I的化学方程式为:Fe3O4(s)+CO(g)
 3FeO(s)+CO2(g),反应Ⅱ的化学方程式为
3FeO(s)+CO2(g),反应Ⅱ的化学方程式为(2)反应III为:CO2(g)+C(s)
 2CO(g)
2CO(g)  H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有
H>0。为了提高达平衡后CO的产量,理论上可以采取的合理措施有(3)上述流程中铁的氧化物可用来制备含有Fe3+的刻蚀液,用刻蚀液刻蚀铜板时,可观察到溶液颜色逐渐变蓝,该反应的离子方程式为
(4)上述流程中碳的氧化物可用来制备碳酰肼[CO(NHNH2)2,其中碳元素为+4价]。加热条件下,碳酰肼能将锅炉内表面锈蚀后的氧化铁转化为结构紧密的四氧化三铁保护层,并生成氮气、水和二氧化碳。该反应的化学方程式为
更新时间:2018-11-13 16:44:25
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】高铁酸钾(K2FeO4)是一种高效多功能水处理剂。实验室模拟工业生产K2FeO4的流程如下:

(1) K2FeO4既能杀菌消毒,又能沉降水中悬浮物,其原因是:_________________________________________ 。
(2)无隔膜法电解饱和NaCl溶液制备NaClO总反应的离子方程式为:__________________ 。
(3)“氧化”时发生反应的化学方程式为:_________________________________________ 。Na2FeO4、FeCl3、NaClO氧化性由强到弱的顺序为_________________________________ 。
(4)“过滤”所得滤液中,除OH-外,一定存在的阴离子为_____________________ (填离子符号)。
(5) 试从沉淀溶解平衡的角度解释“转化”得以顺利实现的原因___________________________ 。

(1) K2FeO4既能杀菌消毒,又能沉降水中悬浮物,其原因是:
(2)无隔膜法电解饱和NaCl溶液制备NaClO总反应的离子方程式为:
(3)“氧化”时发生反应的化学方程式为:
(4)“过滤”所得滤液中,除OH-外,一定存在的阴离子为
(5) 试从沉淀溶解平衡的角度解释“转化”得以顺利实现的原因
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】配平下列方程式:
(1) ____P+____Br2+____H2O=____H3PO4+____HBr________
(2) ___KMnO4+___HCl(浓)=___KCl+___MnCl2+___Cl2↑+___H2O r________
(3)___FeSO4 + ___H2O + ___O2 = ___Fe2(SO4)3 + ___Fe(OH)3 r________
(1) ____P+____Br2+____H2O=____H3PO4+____HBr
(2) ___KMnO4+___HCl(浓)=___KCl+___MnCl2+___Cl2↑+___H2O r
(3)___FeSO4 + ___H2O + ___O2 = ___Fe2(SO4)3 + ___Fe(OH)3 r
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某一反应体系中有反应物和生成物共八种物质:KMnO4、SO2、CuS、H2SO4、CuSO4、K2SO4、MnSO4、H2O。反应中氧化过程如下:CuS→SO2。
(1)该反应中被还原的元素是_______ ,CuS发生氧化反应的实质是_______ 。
(2)若反应过程中转移了3mol电子,则参加反应的CuS的物质的量为_______ mol。
(3)写出并配平该反应的化学方程式_______ 。
(4)当KMnO4过量时,KMnO4会继续与SO2发生加下反应:2KMnO4+5SO2+2H2O→2H2SO4+K2SO4+2MnSO4。标出上述反应的电子转移数目和方向:_______ 该反应中氧化产物与还原产物的物质的量之比为_______ 。
(1)该反应中被还原的元素是
(2)若反应过程中转移了3mol电子,则参加反应的CuS的物质的量为
(3)写出并配平该反应的化学方程式
(4)当KMnO4过量时,KMnO4会继续与SO2发生加下反应:2KMnO4+5SO2+2H2O→2H2SO4+K2SO4+2MnSO4。标出上述反应的电子转移数目和方向:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】如图所示是铁及其化合物的“价类”二维图。

(1)X、Y分别代表___________ 、___________ ;Z在空气中转化为W的化学方程式为___________ 。
(2)某小组研究 性质,预测
性质,预测 能与
能与___________ 发生氧化还原反应(填序号)。
①NaOH溶液 ②氯水 ③稀盐酸 ④酸性 溶液 ⑤
溶液 ⑤ 溶液 ⑥碳酸钠
溶液 ⑥碳酸钠
(3)铁盐溶液可用于金属刻蚀。如用 溶液刻蚀铜制电路板,
溶液刻蚀铜制电路板, 被
被___________ (填“还原”或“氧化”)为 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、___________ ,然后取少许滤液于试管中进行实验。
(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用NaClO氧化 的方法制备
的方法制备 ,其原理为
,其原理为 ,用
,用单线桥法 表示该反应的电子转移方向和数目。____________ 。

(1)X、Y分别代表
(2)某小组研究
 性质,预测
性质,预测 能与
能与①NaOH溶液 ②氯水 ③稀盐酸 ④酸性
 溶液 ⑤
溶液 ⑤ 溶液 ⑥碳酸钠
溶液 ⑥碳酸钠(3)铁盐溶液可用于金属刻蚀。如用
 溶液刻蚀铜制电路板,
溶液刻蚀铜制电路板, 被
被 ,该反应的离子方程式为
,该反应的离子方程式为(4)为检验食品中的铁元素,可将菠菜剪碎、研磨、溶解、
(5)高铁酸钠是一种能杀菌、脱色、除臭的新型高效水处理剂。工业上可用NaClO氧化
 的方法制备
的方法制备 ,其原理为
,其原理为 ,用
,用
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。
(1)检验溶液中Fe3+存在的试剂是___ ,证明Fe3+存在的现象是___ 。
(2)写出FeCl3溶液与金属铜发生反应的离子方程式___ 。
(3)某工程师为了从使用过的腐蚀废液(主要含Fe3+、Fe2+、Cu2+、Cl-)中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:
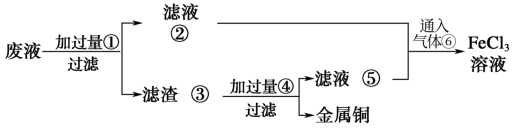
请写出上述实验中加入或生成的有关物质的化学式。
①___ ,④___ 。
(4))写出向②⑤的混合液中通入⑥的离子方程式:___ 。
(5)将铜片放入0.1mol/LFeCl3溶液中,反应一段时间后取出铜片,溶液中c(Fe3+):c(Fe2+)=2:3,则此时溶液中的Cu2+与Fe3+的物质的量之比为___ 。
(1)检验溶液中Fe3+存在的试剂是
(2)写出FeCl3溶液与金属铜发生反应的离子方程式
(3)某工程师为了从使用过的腐蚀废液(主要含Fe3+、Fe2+、Cu2+、Cl-)中回收铜,并重新获得纯净的FeCl3溶液,准备采用下列步骤:

请写出上述实验中加入或生成的有关物质的化学式。
①
(4))写出向②⑤的混合液中通入⑥的离子方程式:
(5)将铜片放入0.1mol/LFeCl3溶液中,反应一段时间后取出铜片,溶液中c(Fe3+):c(Fe2+)=2:3,则此时溶液中的Cu2+与Fe3+的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】在一定条件下,二氧化硫和氧气发生如下反应:2SO2(g)+O2(g) 2SO3(g) ∆H<0。
2SO3(g) ∆H<0。
(1)写出该反应的化学平衡常数表达式K=___________
(2)降低温度,该反应K值___________ ,二氧化硫转化率___________ ,化学反应速率___________ (以上均填增大、减小或不变)。
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态时间是___________ 。
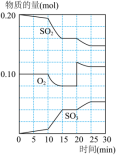
(4)据图判断,反应进行至20min时,曲线发生变化的原因是___________ (用文字表达)。
(5)若该反应的密闭容器为2L,则反应15min时,v(SO2)=___________ (取近似值)。
(6)为使该反应的反应速率增大,且平衡向正反应方向移动的是___________。
 2SO3(g) ∆H<0。
2SO3(g) ∆H<0。(1)写出该反应的化学平衡常数表达式K=
(2)降低温度,该反应K值
(3)600℃时,在一密闭容器中,将二氧化硫和氧气混合,反应过程中SO2、O2、SO3物质的量变化如图,反应处于平衡状态时间是

(4)据图判断,反应进行至20min时,曲线发生变化的原因是
(5)若该反应的密闭容器为2L,则反应15min时,v(SO2)=
(6)为使该反应的反应速率增大,且平衡向正反应方向移动的是___________。
| A.及时分离出SO3气体 | B.适当升高温度 |
| C.增大O2的浓度 | D.选择高效的催化剂 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2 (g)+3H2 (g) 2NH3(g)
2NH3(g)
(1)已知每破坏1mol有关化学键需要的能量如下表:
则反应物的总能量_________ (填“>”或 “<”)生成物的总能量
(2)在一定温度下、向2L密闭容器中加入2 molN2、6 mol H2,在适当的催化剂作用下,发生反应 N2 (g)+3H2 (g) 2NH3(g),10min后达到平衡,此时剩余4.5mol H2,请回答
2NH3(g),10min后达到平衡,此时剩余4.5mol H2,请回答
①下列叙述能说明此反应达到平衡状态的是________________________ 。
a.容器内总压强不变 b.v(H2)正=v(H2)逆
c.N2和H2的转化率相等 d.混合气体的密度保持不变
e.2 mol NH3生成的同时有3 mol H—H键断裂 f.NH3的浓度不再改变
②1)0--10 min内的平均反应速率v(H2) 是___________ mol/L•min;
2)平衡时,NH3的浓度是____________ mol/L;
3)平衡时,N2的转化率是____________ 。
 2NH3(g)
2NH3(g) (1)已知每破坏1mol有关化学键需要的能量如下表:
| H-H | N-H | N-N | N≡N |
| 435.9KJ | 390.8KJ | 192.8KJ | 945.8KJ |
则反应物的总能量
(2)在一定温度下、向2L密闭容器中加入2 molN2、6 mol H2,在适当的催化剂作用下,发生反应 N2 (g)+3H2 (g)
 2NH3(g),10min后达到平衡,此时剩余4.5mol H2,请回答
2NH3(g),10min后达到平衡,此时剩余4.5mol H2,请回答①下列叙述能说明此反应达到平衡状态的是
a.容器内总压强不变 b.v(H2)正=v(H2)逆
c.N2和H2的转化率相等 d.混合气体的密度保持不变
e.2 mol NH3生成的同时有3 mol H—H键断裂 f.NH3的浓度不再改变
②1)0--10 min内的平均反应速率v(H2) 是
2)平衡时,NH3的浓度是
3)平衡时,N2的转化率是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在200 ℃,将1 mol H2(g)和2 mol I2(g)充入到体积为V L的密闭容器中,发生反应:I2(g)+H2(g)  2HI(g) ΔH=-c kJ/mol
2HI(g) ΔH=-c kJ/mol
(1)反应刚开始时,由于c(H2)=______ mol/L,c(I2)=______ mol/L,而c(HI)=_____ ,所以化学反应速率 _______ 最大,而________ 最小(为零)。
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c(H2)_____ ,c(I2)_____ ,而c(HI)________ ,从而化学反应速率v(正)______ ,而v(逆)_____ 。(以上填“增大”“减小”或“不变”)
(3)当反应进行到v(正)与v(逆)_______ 时,此可逆反应就达到了平衡。若保持外界条件不变时,反应混合物的总物质的量为_______ mol。此时放出的热量Q_______ (填“>”“<”或“=”)c kJ。
 2HI(g) ΔH=-c kJ/mol
2HI(g) ΔH=-c kJ/mol(1)反应刚开始时,由于c(H2)=
(2)随着反应的进行,反应混合物中各组分浓度的变化趋势为c(H2)
(3)当反应进行到v(正)与v(逆)
您最近一年使用:0次



