t℃时,将3 mol A和2 mol B气体通入体积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g) 2C(g),2 min时反应达到平衡状态(温度不变),测得C的浓度为0.2 mol/L,请填写下列空白:
2C(g),2 min时反应达到平衡状态(温度不变),测得C的浓度为0.2 mol/L,请填写下列空白:
(1)该过程用A表示的反应速率为:v(A)=_______ ;该温度下该反应的化学平衡常数表达式为__________ 。
(2)比较达到平衡时,A、B两反应物的转化率:α(A)______ α(B)(填“>”、“=”或“<”)。
(3)判断反应达到平衡状态的依据是(填字母序号)__________ 。
a.生成C的速率与消耗B的速率相等 b.混合气体的密度不变
c.混合气体的相对平均分子质量不变 d.A的质量分数不再发生变化
(4)若升高温度,再次达平衡时,平衡常数数值变大,则该反应的 H
H_____ 0(填“>”、“=”或“<”)。
(5)若保持温度不变时,继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,则化学反应速率会__________ (填“加快”、“减慢”或“不变”),化学平衡将_________ (填“正反应方向移动”、“逆反应方向移动”或“不移动”)。
(6)在恒温恒容密闭容器中进行上述反应,起始投料时各物质的浓度如下表:
按投料I进行反应,测得达到化学平衡状态时A的转化率为40%,若按投料II进行反应,起始时反应进行的方向为________ (填“正向”、“逆向”或“不移动)。
 2C(g),2 min时反应达到平衡状态(温度不变),测得C的浓度为0.2 mol/L,请填写下列空白:
2C(g),2 min时反应达到平衡状态(温度不变),测得C的浓度为0.2 mol/L,请填写下列空白:(1)该过程用A表示的反应速率为:v(A)=
(2)比较达到平衡时,A、B两反应物的转化率:α(A)
(3)判断反应达到平衡状态的依据是(填字母序号)
a.生成C的速率与消耗B的速率相等 b.混合气体的密度不变
c.混合气体的相对平均分子质量不变 d.A的质量分数不再发生变化
(4)若升高温度,再次达平衡时,平衡常数数值变大,则该反应的
 H
H(5)若保持温度不变时,继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,则化学反应速率会
(6)在恒温恒容密闭容器中进行上述反应,起始投料时各物质的浓度如下表:
| A | B | C | |
| 投料I | 3.0 mol/L | 1.0 mol/L | 0 |
| 投料II | 2.0 mol/L | 1.0 mol/L | 2.0 mol/L |
更新时间:2018-12-06 11:09:31
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】宋应星《天工开物》载有一种矿石“银矿铅”,该矿石是与辉银矿(主要成分为 )共生的方铅矿(主要成分为
)共生的方铅矿(主要成分为 )。由于中国古代对银的需求量高,故对该矿大量开采以弥补银的短缺情况。古人在劳动过程中发现两种矿石常共生,故有“上有铅者,其下有银”(《管子·地数篇》)的说法。现利用该矿石制备铅蓄电池正极材料
)。由于中国古代对银的需求量高,故对该矿大量开采以弥补银的短缺情况。古人在劳动过程中发现两种矿石常共生,故有“上有铅者,其下有银”(《管子·地数篇》)的说法。现利用该矿石制备铅蓄电池正极材料 和超细银粉,工艺流程如下:
和超细银粉,工艺流程如下: 杂质;
杂质;
②“酸化”过程中 会与热的浓盐酸反应生成
会与热的浓盐酸反应生成 (微溶);在浓盐酸中有
(微溶);在浓盐酸中有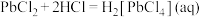 ,而
,而 与热的浓盐酸不反应,但可以与氰化物反应生成二氰合银离子;
与热的浓盐酸不反应,但可以与氰化物反应生成二氰合银离子; 和
和 可以类似的形成四氰合锌离子。
可以类似的形成四氰合锌离子。
③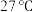 下,
下,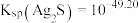 ,反应
,反应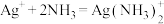 的平衡常数
的平衡常数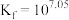 。
。
回答下列问题:
(1)浮选剂是头部为亲硫基、尾部为长烃链(憎水基)的分子,可吸引粉碎后的矿物中的含硫基团,从而完成对矿物中硫化物的富集。“浮选”步骤的目的是_______ 。
(2)“还原”步骤发生反应的离子方程式为_______ ,流程中可重复利用的物质是_______ (填化学式)。
(3)有同学认为在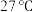 下“溶银”过程可以用浓氨水代替
下“溶银”过程可以用浓氨水代替 溶液,但经实验二者混合后无明显现象,请通过计算溶液中
溶液,但经实验二者混合后无明显现象,请通过计算溶液中 的浓度达到
的浓度达到 所需要的最小氨浓度解释其原因
所需要的最小氨浓度解释其原因_______ 。(计算结果保留指数形式,忽略 与
与 之间的转化)
之间的转化)
(4)“酸化”过程中生成的 会威胁人体健康。已知
会威胁人体健康。已知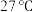 下某车间(空气体积为
下某车间(空气体积为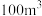 )
) 的挥发速率
的挥发速率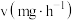 与时间
与时间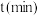 有
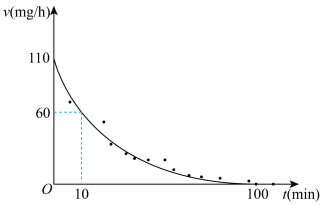
有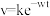 成立,式中k,w为常数。气相色谱仪测定车间
成立,式中k,w为常数。气相色谱仪测定车间 浓度结果拟合为如图所示的曲线,则
浓度结果拟合为如图所示的曲线,则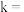
_______ , 的挥发半衰期(挥发
的挥发半衰期(挥发 的量首次达到挥发
的量首次达到挥发 总量的一半的时间)
总量的一半的时间)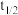
_______ (填“>”“<”“=”或“不确定”) ;
; 的最高容许浓度为
的最高容许浓度为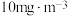 ,则该车间环境
,则该车间环境_______ (填“是”或“否”)符合国家标准。
 )共生的方铅矿(主要成分为
)共生的方铅矿(主要成分为 )。由于中国古代对银的需求量高,故对该矿大量开采以弥补银的短缺情况。古人在劳动过程中发现两种矿石常共生,故有“上有铅者,其下有银”(《管子·地数篇》)的说法。现利用该矿石制备铅蓄电池正极材料
)。由于中国古代对银的需求量高,故对该矿大量开采以弥补银的短缺情况。古人在劳动过程中发现两种矿石常共生,故有“上有铅者,其下有银”(《管子·地数篇》)的说法。现利用该矿石制备铅蓄电池正极材料 和超细银粉,工艺流程如下:
和超细银粉,工艺流程如下: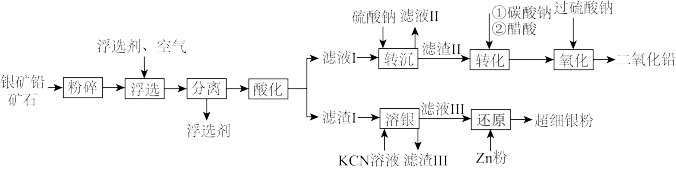
 杂质;
杂质;②“酸化”过程中
 会与热的浓盐酸反应生成
会与热的浓盐酸反应生成 (微溶);在浓盐酸中有
(微溶);在浓盐酸中有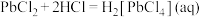 ,而
,而 与热的浓盐酸不反应,但可以与氰化物反应生成二氰合银离子;
与热的浓盐酸不反应,但可以与氰化物反应生成二氰合银离子; 和
和 可以类似的形成四氰合锌离子。
可以类似的形成四氰合锌离子。③
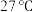 下,
下,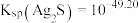 ,反应
,反应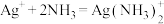 的平衡常数
的平衡常数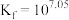 。
。回答下列问题:
(1)浮选剂是头部为亲硫基、尾部为长烃链(憎水基)的分子,可吸引粉碎后的矿物中的含硫基团,从而完成对矿物中硫化物的富集。“浮选”步骤的目的是
(2)“还原”步骤发生反应的离子方程式为
(3)有同学认为在
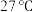 下“溶银”过程可以用浓氨水代替
下“溶银”过程可以用浓氨水代替 溶液,但经实验二者混合后无明显现象,请通过计算溶液中
溶液,但经实验二者混合后无明显现象,请通过计算溶液中 的浓度达到
的浓度达到 所需要的最小氨浓度解释其原因
所需要的最小氨浓度解释其原因 与
与 之间的转化)
之间的转化)(4)“酸化”过程中生成的
 会威胁人体健康。已知
会威胁人体健康。已知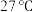 下某车间(空气体积为
下某车间(空气体积为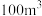 )
) 的挥发速率
的挥发速率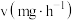 与时间
与时间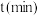 有
有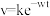 成立,式中k,w为常数。气相色谱仪测定车间
成立,式中k,w为常数。气相色谱仪测定车间 浓度结果拟合为如图所示的曲线,则
浓度结果拟合为如图所示的曲线,则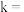
 的挥发半衰期(挥发
的挥发半衰期(挥发 的量首次达到挥发
的量首次达到挥发 总量的一半的时间)
总量的一半的时间)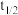
 ;
;
 的最高容许浓度为
的最高容许浓度为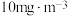 ,则该车间环境
,则该车间环境
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
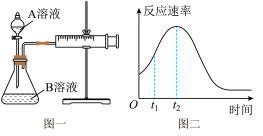
【推荐2】某实验小组用酸性KMnO4溶液和H2C2O4(草酸)反应研究影响反应速率的因素。他们通过测定单位时间内生成CO2的体积,探究某种影响化学反应速率的因素,设计方案如下(KMnO4溶液已酸化):
(1)酸性KMnO4溶液中所加的酸应是(填字母序号)______。
(2)写出酸性KMnO4溶液和H2C2O4反应离子方程式:______ 。
(3)该实验探究的是______ 对化学反应速率的影响。
(4)实验停止前,相同时间内针筒中所得CO2体积较大是______ (填实验序号)。
(5)若实验①在2min末注射器的活塞从最左端向右移动到了VmL的位置,则这段时间内的平均反应速率可表示为
______  。
。
(6)若实验②在tmin收集了2.24mLCO2(标准状况),则tmin末 的物质的量浓度为
的物质的量浓度为______  。
。
(7)该小组同学发现反应速率总是如图二,其中 时间内速率变快的主要原因可能是:①
时间内速率变快的主要原因可能是:①______ 。②______ 。
| 实验序号 | A溶液 | B溶液 |
| ① | 20mL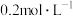 H2C2O4溶液 H2C2O4溶液 | 30mL KMnO4溶液 KMnO4溶液 |
| ② | 20mL H2C2O4溶液 H2C2O4溶液 | 30mL KMnO4溶液 KMnO4溶液 |
(1)酸性KMnO4溶液中所加的酸应是(填字母序号)______。
| A.硫酸 | B.盐酸 | C.硝酸 | D.以上三种酸都可 |
(2)写出酸性KMnO4溶液和H2C2O4反应离子方程式:
(3)该实验探究的是
(4)实验停止前,相同时间内针筒中所得CO2体积较大是
(5)若实验①在2min末注射器的活塞从最左端向右移动到了VmL的位置,则这段时间内的平均反应速率可表示为

 。
。(6)若实验②在tmin收集了2.24mLCO2(标准状况),则tmin末
 的物质的量浓度为
的物质的量浓度为 。
。(7)该小组同学发现反应速率总是如图二,其中
 时间内速率变快的主要原因可能是:①
时间内速率变快的主要原因可能是:①
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】根据要求,回答下列问题:
(1)为比较 、
、 对
对 分解的催化效果,某实验小组同学设计了如图所示的实验。通过观察
分解的催化效果,某实验小组同学设计了如图所示的实验。通过观察______ (填实验现象),即可得出 、
、 的催化效果的差异。有同学提出将
的催化效果的差异。有同学提出将 溶液改为
溶液改为 溶液更合理,其理由是
溶液更合理,其理由是______  和
和 (草酸)反应速率的影响,设计实验方案如下:
(草酸)反应速率的影响,设计实验方案如下:
上述反应的离子方程式为______ ,该实验是探究______ 对反应速率的影响。
(3)工业制硫酸的反应之一为 ,在2L恒温恒容密闭容器中投入2mol
,在2L恒温恒容密闭容器中投入2mol 和1mol
和1mol 在一定条件下充分反应,下图是
在一定条件下充分反应,下图是 和
和 随时间的变化曲线。
随时间的变化曲线。 的平均反应速率为
的平均反应速率为______ 。
(2)A点的
______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(1)为比较
 、
、 对
对 分解的催化效果,某实验小组同学设计了如图所示的实验。通过观察
分解的催化效果,某实验小组同学设计了如图所示的实验。通过观察 、
、 的催化效果的差异。有同学提出将
的催化效果的差异。有同学提出将 溶液改为
溶液改为 溶液更合理,其理由是
溶液更合理,其理由是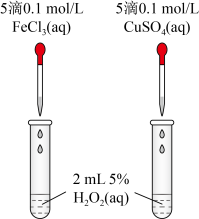
 和
和 (草酸)反应速率的影响,设计实验方案如下:
(草酸)反应速率的影响,设计实验方案如下:实验序号 | 草酸溶液 | 酸性高锰酸钾溶液 |
① |
|
|
② |
|
|
(3)工业制硫酸的反应之一为
 ,在2L恒温恒容密闭容器中投入2mol
,在2L恒温恒容密闭容器中投入2mol 和1mol
和1mol 在一定条件下充分反应,下图是
在一定条件下充分反应,下图是 和
和 随时间的变化曲线。
随时间的变化曲线。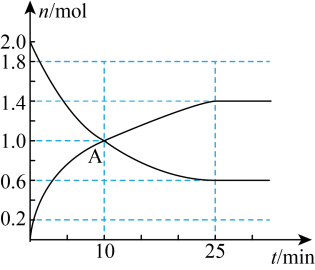
 的平均反应速率为
的平均反应速率为(2)A点的

 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
您最近一年使用:0次
【推荐1】CH4重整技术对温室气体的减排具有重要意义,不仅能缓解大气变暖,对日益枯竭的石油资源也有一定的补充作用。体系内发生了如下反应:
反应Ⅰ:CH4(g) + H2O(g) CO(g) + 3H2(g)
CO(g) + 3H2(g)  = a kJ·mol-1
= a kJ·mol-1
反应Ⅱ: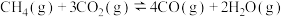
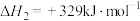
反应Ⅲ:_______。
(1)①断开(或形成) 化学键的能量变化数据如表中所示,则a=
化学键的能量变化数据如表中所示,则a=_______ 。
②反应Ⅲ是由反应Ⅱ中的生成物转化成H2和CO2,写出该反应的热化学方程式:_______ 。
(2)反应Ⅰ、反应Ⅱ、反应Ⅲ的平衡常数分别记作K1、K2、K3,,则K1=_______ (用含K2、K3,的表达式表达)
(3)T℃时,向2L恒容密闭容器中通入1mol CH4(g)和2mol H2O(g),仅发生反应Ⅰ,经过10min,反应达到平衡,此时c(CH4)=0.20 mol•L-1。
① 0~10min内,该反应的平均反应速率v(H2)=_______ 。
② 下列表述能说明该反应已达化学平衡状态的是_______ 。
A.混合气体的密度不变
B.混合气体的平均相对分子质量不变
C.反应速率v(CH4):v(H2)=1:3
D.断裂4mol C-H键的同时断裂3mol H-H键
(4)已知反应Ⅲ的正反应速率 v=k·c3(CO2) (k为正反应的速率常数),某温度时测得数据如表中所示。则此温度下表中b=_______ 。
反应Ⅰ:CH4(g) + H2O(g)
 CO(g) + 3H2(g)
CO(g) + 3H2(g)  = a kJ·mol-1
= a kJ·mol-1反应Ⅱ:
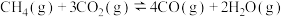
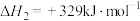
反应Ⅲ:_______。
(1)①断开(或形成)
 化学键的能量变化数据如表中所示,则a=
化学键的能量变化数据如表中所示,则a=| 化学键 | H-H | C-O | C=O | C≡O | C-H | O-H |
键能/ | 436 | 326 | 803 | 1072 | 414 | 465 |
(2)反应Ⅰ、反应Ⅱ、反应Ⅲ的平衡常数分别记作K1、K2、K3,,则K1=
(3)T℃时,向2L恒容密闭容器中通入1mol CH4(g)和2mol H2O(g),仅发生反应Ⅰ,经过10min,反应达到平衡,此时c(CH4)=0.20 mol•L-1。
① 0~10min内,该反应的平均反应速率v(H2)=
② 下列表述能说明该反应已达化学平衡状态的是
A.混合气体的密度不变
B.混合气体的平均相对分子质量不变
C.反应速率v(CH4):v(H2)=1:3
D.断裂4mol C-H键的同时断裂3mol H-H键
(4)已知反应Ⅲ的正反应速率 v=k·c3(CO2) (k为正反应的速率常数),某温度时测得数据如表中所示。则此温度下表中b=
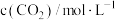 | 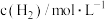 | 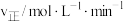 | |
| 1 | 0.01 | 0.01 |  |
| 2 | 0.02 | 0.01 | b |
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】在T℃条件下,向1L固定体积的密闭容器M中加入2 mol X和1 mol Y,发生如下反应: 2X(g) + Y(g)  a Z(g) + W(g) △H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则
a Z(g) + W(g) △H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则
(1)化学计量数a的值为____________________ ;此反应的逆反应△S__________ 0 (填﹤,﹥,﹦)。
(2)下列说法中能说明该反应达到了化学平衡状态的是___________________________ 。
A、容器内压强一定 B、v(X)正=2 v (Y)逆
C、容器内Z分子数一定 D、容器内气体的质量一定
E、容器内气体的密度一定 F:X、Y、Z、W的浓度之比为2∶1∶a∶1
(3)维持温度不变,若起始时向该容器中加入的物质的量如下列各项,则反应达到平衡后(稀有气体不参与反应),与之是等效平衡的是______________ 。
A.2 mol X、1mol Y、1mol Ar B.a mol Z、1mol W
C.1 molX、0.5mol Y、0.5a mol Z、0.5 mol W D.2 mol X、1mol Y、1mol Z
(4)维持温度不变,若起始时向容器中加入4mol X和6 mol Y,若达平衡时容器内的压强减小了15%,则反应中放出的热量为___________________ kJ。
(5)已知:该反应的平衡常数随温度的变化如下表:
试回答下列问题:
若在某温度下,2 mol X和1 mol Y在该容器中反应达平衡, X的平衡转化率为50%,则该温度为__________________ ℃。
 a Z(g) + W(g) △H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则
a Z(g) + W(g) △H = -Q kJ·mol-1 (Q>0)。当反应达到平衡后,反应放出的热量为Q1 kJ,物质X的转化率为α;若平衡后再升高温度,混合气体的平均相对分子质量减小,则(1)化学计量数a的值为
(2)下列说法中能说明该反应达到了化学平衡状态的是
A、容器内压强一定 B、v(X)正=2 v (Y)逆
C、容器内Z分子数一定 D、容器内气体的质量一定
E、容器内气体的密度一定 F:X、Y、Z、W的浓度之比为2∶1∶a∶1
(3)维持温度不变,若起始时向该容器中加入的物质的量如下列各项,则反应达到平衡后(稀有气体不参与反应),与之是等效平衡的是
A.2 mol X、1mol Y、1mol Ar B.a mol Z、1mol W
C.1 molX、0.5mol Y、0.5a mol Z、0.5 mol W D.2 mol X、1mol Y、1mol Z
(4)维持温度不变,若起始时向容器中加入4mol X和6 mol Y,若达平衡时容器内的压强减小了15%,则反应中放出的热量为
(5)已知:该反应的平衡常数随温度的变化如下表:
| 温度/℃ | 150 | 200 | 250 | 300 | 350 |
| 平衡常数K | 9.94 | 5.2 | 1 | 0.5 | 0.21 |
若在某温度下,2 mol X和1 mol Y在该容器中反应达平衡, X的平衡转化率为50%,则该温度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】在氮及其化合物的化工生产中,对有关反应的反应原理进行研究有着重要意义。
(1)一定温度下,将2mol 和6mol
和6mol 置于1L的恒容密闭容器中发生如下反应:
置于1L的恒容密闭容器中发生如下反应: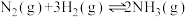
 ,测得不同温度、不同时间段内合成氨反应中
,测得不同温度、不同时间段内合成氨反应中 的转化率,数据如下:
的转化率,数据如下:
①上表中
_________  (填“>”或“<”或“=”),其中a、b、80%三者的大小关系是
(填“>”或“<”或“=”),其中a、b、80%三者的大小关系是_________ (用含“>”“<”“=”的关系式表示)。
②研究表明,合成氨的速率与相关物质的浓度关系为 ,k为速率常数。以下说法正确的是
,k为速率常数。以下说法正确的是_________ (填字母序号)。
A.升高温度,k值增大
B. ℃时若容器内混合气体平均相对分子质量保持不变,则反应达到平衡状态
℃时若容器内混合气体平均相对分子质量保持不变,则反应达到平衡状态
C.一定温度下将原容器中的 及时分离出来可使v减小
及时分离出来可使v减小
D.合成氨达到平衡后,增大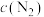 可使正反应速率在达到新平衡的过程中始终增大。
可使正反应速率在达到新平衡的过程中始终增大。
③已知某温度下该反应达平衡时各物质均为1mol,容器容积为1L,保持温度和压强不变,又充入3mol 后,平衡
后,平衡_________ (填“向左移动”“向右移动”或“不移动”)。
(2)在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应: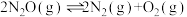 ,容器Ⅰ、Ⅱ、Ⅲ中
,容器Ⅰ、Ⅱ、Ⅲ中 的平衡转化率如图乙所示:
的平衡转化率如图乙所示:

①该反应的△H_________ 0(填“>”或“<”)。
②若容器Ⅰ的体积为2L,反应在370℃下进行,20s后达到平衡,则0~20s内容器Ⅰ中用 表示的反应速率为
表示的反应速率为_________ 。B点对应的平衡常数K=_________ (保留两位有效数字)
(1)一定温度下,将2mol
 和6mol
和6mol 置于1L的恒容密闭容器中发生如下反应:
置于1L的恒容密闭容器中发生如下反应: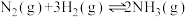
 ,测得不同温度、不同时间段内合成氨反应中
,测得不同温度、不同时间段内合成氨反应中 的转化率,数据如下:
的转化率,数据如下:| 1小时 | 2小时 | 3小时 | 4小时 | |
 | 30% | 50% | 80% | 80% |
 | 35% | 60% | a | b |

 (填“>”或“<”或“=”),其中a、b、80%三者的大小关系是
(填“>”或“<”或“=”),其中a、b、80%三者的大小关系是②研究表明,合成氨的速率与相关物质的浓度关系为
 ,k为速率常数。以下说法正确的是
,k为速率常数。以下说法正确的是A.升高温度,k值增大
B.
 ℃时若容器内混合气体平均相对分子质量保持不变,则反应达到平衡状态
℃时若容器内混合气体平均相对分子质量保持不变,则反应达到平衡状态C.一定温度下将原容器中的
 及时分离出来可使v减小
及时分离出来可使v减小D.合成氨达到平衡后,增大
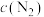 可使正反应速率在达到新平衡的过程中始终增大。
可使正反应速率在达到新平衡的过程中始终增大。③已知某温度下该反应达平衡时各物质均为1mol,容器容积为1L,保持温度和压强不变,又充入3mol
 后,平衡
后,平衡(2)在四个不同容积的恒容密闭容器中按图甲充入相应的气体,发生反应:
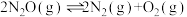 ,容器Ⅰ、Ⅱ、Ⅲ中
,容器Ⅰ、Ⅱ、Ⅲ中 的平衡转化率如图乙所示:
的平衡转化率如图乙所示:
①该反应的△H
②若容器Ⅰ的体积为2L,反应在370℃下进行,20s后达到平衡,则0~20s内容器Ⅰ中用
 表示的反应速率为
表示的反应速率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】可逆反应Fe(s)+CO2(g) FeO(s)+CO(g),已知 938K 时平衡常数 K=1.47,1173K 时平衡常数 K=2.15。
FeO(s)+CO(g),已知 938K 时平衡常数 K=1.47,1173K 时平衡常数 K=2.15。
(1)该反应的平衡常数表达式为___________ ,是_____________ (填“吸热”或“放热”)反应,理由是_________________________________________________ 。
(2)若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,能判断该反应达到平衡的依据是_______________________ 。
A. 容器内压强不变 B. c(CO)不变了 C. FeO 的质量不变 D. 混合气体的密度不变如果改变下列条件再达平衡后(选填“增大”“减小”或“不变”):
①再通入 CO2,CO2的转化率__________________ ;
②增大容器的体积,混合气体的平均相对分子质量_____________ 。
(3)该反应的逆速率随时间变化情况如图:

①从图中看到,反应在 t2时达平衡,在 t1时改变了某种条件,改变的条件可能是________________________ (请 写出两种)。
②如果在 t3时再增加 CO2的量,t4时反应又处于新平衡状态,请在图上画出 t3~t5时间的 v 逆变化曲线。___
 FeO(s)+CO(g),已知 938K 时平衡常数 K=1.47,1173K 时平衡常数 K=2.15。
FeO(s)+CO(g),已知 938K 时平衡常数 K=1.47,1173K 时平衡常数 K=2.15。(1)该反应的平衡常数表达式为
(2)若该反应在体积固定的密闭容器中进行,在一定条件下达到平衡状态,能判断该反应达到平衡的依据是
A. 容器内压强不变 B. c(CO)不变了 C. FeO 的质量不变 D. 混合气体的密度不变如果改变下列条件再达平衡后(选填“增大”“减小”或“不变”):
①再通入 CO2,CO2的转化率
②增大容器的体积,混合气体的平均相对分子质量
(3)该反应的逆速率随时间变化情况如图:

①从图中看到,反应在 t2时达平衡,在 t1时改变了某种条件,改变的条件可能是
②如果在 t3时再增加 CO2的量,t4时反应又处于新平衡状态,请在图上画出 t3~t5时间的 v 逆变化曲线。
您最近一年使用:0次
【推荐2】合成氨工业对国民经济和社会发展具有重要的意义,回答以下问题:
(1)如图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量的变化示意图,正反应的活化能为___________ kJ/mol。

(2)请写出N2和H2反应的热化学方程式:___________ 。
(3)合成氨反应的化学平衡常数表达式为
___________ 。
(4)根据温度对化学平衡的影响规律可知,对于该反应温度越高,其化学平衡常数的值___________ 。(填“越大”、“越小”或“不变”)
(5)某温度下,若把 与
与 置于体积为
置于体积为 的密闭容器内,反应达到平衡状态时,测得混合气体的压强变为开始时的
的密闭容器内,反应达到平衡状态时,测得混合气体的压强变为开始时的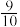 ,则平衡时氢气的转化率
,则平衡时氢气的转化率 =
=___________ (用百分数表示 。能说明该反应达到化学平衡状态的是
。能说明该反应达到化学平衡状态的是___________  填字母
填字母 。
。
a.容器内的密度保持不变 b.容器内压强保持不变
c.v正(N2)=2v逆(NH3) d.混合气体中c(NH3)不变
(6)对于合成氨反应而言,下列有关图象一定正确的是(选填序号)___________ 。
A. B.
B.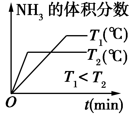 C.
C.
(7)用NH3催化还原NOx还可以消除氮氧化物的污染。已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)∆H=—a kJ/mol ①
N2(g)+O2(g)=2NO(g) ∆H=+b kJ/mol②
求:若1molNH3还原NO至N2,则该反应过程中的反应热∆H=___________ kJ/mol(用含a、b的式子表示)。
(1)如图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量的变化示意图,正反应的活化能为

(2)请写出N2和H2反应的热化学方程式:
(3)合成氨反应的化学平衡常数表达式为

(4)根据温度对化学平衡的影响规律可知,对于该反应温度越高,其化学平衡常数的值
(5)某温度下,若把
 与
与 置于体积为
置于体积为 的密闭容器内,反应达到平衡状态时,测得混合气体的压强变为开始时的
的密闭容器内,反应达到平衡状态时,测得混合气体的压强变为开始时的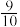 ,则平衡时氢气的转化率
,则平衡时氢气的转化率 =
= 。能说明该反应达到化学平衡状态的是
。能说明该反应达到化学平衡状态的是 填字母
填字母 。
。a.容器内的密度保持不变 b.容器内压强保持不变
c.v正(N2)=2v逆(NH3) d.混合气体中c(NH3)不变
(6)对于合成氨反应而言,下列有关图象一定正确的是(选填序号)
A.
 B.
B. C.
C.
(7)用NH3催化还原NOx还可以消除氮氧化物的污染。已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g)∆H=—a kJ/mol ①
N2(g)+O2(g)=2NO(g) ∆H=+b kJ/mol②
求:若1molNH3还原NO至N2,则该反应过程中的反应热∆H=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】“低碳经济”已成为全世界科学家研究的重要课题。为减小和消除CO2对环境的影响,一方面世界各国都在限制其排放量,另一方面科学家加强了对CO2创新利用的研究。
(1)已知:①CO(g)+H2O(g) H2(g)+CO2(g) ΔH=−41 kJ·mol−1
H2(g)+CO2(g) ΔH=−41 kJ·mol−1
②C(s)+2H2(g) CH4(g) ΔH=−73 kJ·mol−1
CH4(g) ΔH=−73 kJ·mol−1
③2CO(g) C(s)+CO2(g) ΔH=−171 kJ·mol−1
C(s)+CO2(g) ΔH=−171 kJ·mol−1
写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:__________________ 。
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,在容积为2 L的密闭容器中,充入1 mol CO2和3.25 mol H2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如图所示:

①反应的化学方程式为:___________________________ 。
②从反应开始到平衡,氢气的平均反应速率v(H2)=_____________ mol/(L∙min)。
(3)煤化工通常研究不同条件下CO转化率以解决实际问题。已知在催化剂存在条件下反应:CO(g)+H2O(g) H2(g)+CO2(g)中CO的平衡转化率随
H2(g)+CO2(g)中CO的平衡转化率随 及温度变化关系如图所示:[p(H2O)、p(CO)表示H2O、CO的平衡分压,分压=总压×物质的量分数]:
及温度变化关系如图所示:[p(H2O)、p(CO)表示H2O、CO的平衡分压,分压=总压×物质的量分数]:
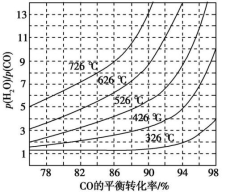
上述反应的逆反应方向是_____________ 反应(填“吸热”或“放热”);
②对于气相反应,用某组分(B)的平衡分压(pB)代替平衡浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=______________ ,提高 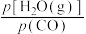 ,则Kp
,则Kp_____________ (填“变大”、“变小”或“不变”)。使用铁镁催化剂的实际工业流程中,一般采用400 ℃左右、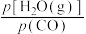 =3~5,采用此条件的原因可能是
=3~5,采用此条件的原因可能是___________ 。
(1)已知:①CO(g)+H2O(g)
 H2(g)+CO2(g) ΔH=−41 kJ·mol−1
H2(g)+CO2(g) ΔH=−41 kJ·mol−1②C(s)+2H2(g)
 CH4(g) ΔH=−73 kJ·mol−1
CH4(g) ΔH=−73 kJ·mol−1③2CO(g)
 C(s)+CO2(g) ΔH=−171 kJ·mol−1
C(s)+CO2(g) ΔH=−171 kJ·mol−1写出CO2与H2反应生成CH4和H2O(g)的热化学方程式:
(2)目前工业上有一种方法是用CO2来生产燃料甲醇。为探究该反应原理,在容积为2 L的密闭容器中,充入1 mol CO2和3.25 mol H2在一定条件下发生反应,测得CO2、CH3OH(g)和H2O(g)的物质的量(n)随时间的变化如图所示:

①反应的化学方程式为:
②从反应开始到平衡,氢气的平均反应速率v(H2)=
(3)煤化工通常研究不同条件下CO转化率以解决实际问题。已知在催化剂存在条件下反应:CO(g)+H2O(g)
 H2(g)+CO2(g)中CO的平衡转化率随
H2(g)+CO2(g)中CO的平衡转化率随 及温度变化关系如图所示:[p(H2O)、p(CO)表示H2O、CO的平衡分压,分压=总压×物质的量分数]:
及温度变化关系如图所示:[p(H2O)、p(CO)表示H2O、CO的平衡分压,分压=总压×物质的量分数]:
上述反应的逆反应方向是
②对于气相反应,用某组分(B)的平衡分压(pB)代替平衡浓度(cB)也可以表示平衡常数(记作Kp),则该反应的Kp=
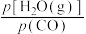 ,则Kp
,则Kp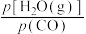 =3~5,采用此条件的原因可能是
=3~5,采用此条件的原因可能是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】“VHRO”系统(V、H、R、O分别表示相应反应容器中所发生反应的催化剂)是一种净化柴油机尾气中NOx的系统,工作示意图及对应反应热化学方程式如下

(1)反应⑤:4NH3(g)+4NO(g)+O2(g) 4N2(g)+6H2O(g)的ΔH=
4N2(g)+6H2O(g)的ΔH=____ kJ·mol—1。
(2)设计反应④目的是_____________________________________ 。
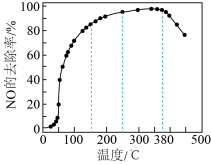
(3)富氧条件下,控制 比例一定时,将氨气和NO通入装有催化剂的反应容器中发生反应⑤,下图表示在相同反应时间时,测得NO的去除率随温度变化的曲线。请分析温度高于380℃时,NO的去除率迅速下降的可能原因是
比例一定时,将氨气和NO通入装有催化剂的反应容器中发生反应⑤,下图表示在相同反应时间时,测得NO的去除率随温度变化的曲线。请分析温度高于380℃时,NO的去除率迅速下降的可能原因是_______________ (一种即可)。
(4)反应①分两步进行,反应历程如图所示。则第一步反应的化学方程式为____ ;总反应速率由第________ 步(填“一”或“二”)反应决定。

(5)在10L恒容密闭容器中进行反应:2NO(g)+O2(g) 2NO2(g)
2NO2(g)  N2O4(g),其中NO2二聚为N2O4的反应可以迅速达到平衡。T℃时,在容器中充入3.2 molNO和2molO2,达到平衡后,NO2的体积分数为
N2O4(g),其中NO2二聚为N2O4的反应可以迅速达到平衡。T℃时,在容器中充入3.2 molNO和2molO2,达到平衡后,NO2的体积分数为 ,其中NO2的物质的量为N2O4的4倍。试求O2平衡转化率α(O2)=
,其中NO2的物质的量为N2O4的4倍。试求O2平衡转化率α(O2)=___ %,该温度下反应①的平衡常数K=_________ 。

(1)反应⑤:4NH3(g)+4NO(g)+O2(g)
 4N2(g)+6H2O(g)的ΔH=
4N2(g)+6H2O(g)的ΔH=(2)设计反应④目的是
(3)富氧条件下,控制
 比例一定时,将氨气和NO通入装有催化剂的反应容器中发生反应⑤,下图表示在相同反应时间时,测得NO的去除率随温度变化的曲线。请分析温度高于380℃时,NO的去除率迅速下降的可能原因是
比例一定时,将氨气和NO通入装有催化剂的反应容器中发生反应⑤,下图表示在相同反应时间时,测得NO的去除率随温度变化的曲线。请分析温度高于380℃时,NO的去除率迅速下降的可能原因是
(4)反应①分两步进行,反应历程如图所示。则第一步反应的化学方程式为

(5)在10L恒容密闭容器中进行反应:2NO(g)+O2(g)
 2NO2(g)
2NO2(g)  N2O4(g),其中NO2二聚为N2O4的反应可以迅速达到平衡。T℃时,在容器中充入3.2 molNO和2molO2,达到平衡后,NO2的体积分数为
N2O4(g),其中NO2二聚为N2O4的反应可以迅速达到平衡。T℃时,在容器中充入3.2 molNO和2molO2,达到平衡后,NO2的体积分数为 ,其中NO2的物质的量为N2O4的4倍。试求O2平衡转化率α(O2)=
,其中NO2的物质的量为N2O4的4倍。试求O2平衡转化率α(O2)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】氨在能源、化肥生产等领域有着非常重要的用途。
(1)在一定条件下, 和
和 反应生成0.2mol
反应生成0.2mol ,放出9.24kJ的热量,写出该可逆反应的热化学方程式:
,放出9.24kJ的热量,写出该可逆反应的热化学方程式:___________ 。在下图中画出合成氨反应过程中焓(H)的变化示意图___________ 。

(2)将 和
和 通入体积为2L的恒温恒容密闭容器中5min后达到化学平衡,测得
通入体积为2L的恒温恒容密闭容器中5min后达到化学平衡,测得 的浓度为0.2mol/L,这段时间内用
的浓度为0.2mol/L,这段时间内用 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为___________ mol/(L•min)。
(3)理论上,为了提高 的平衡转化率,可以采取的措施是
的平衡转化率,可以采取的措施是___________ (写出一条即可)。
(4)下图是某压强下 和
和 按物质的量之比1∶3投料进行反应,反应混合物中
按物质的量之比1∶3投料进行反应,反应混合物中 的物质的量分数随温度的变化曲线。Ⅰ是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是
的物质的量分数随温度的变化曲线。Ⅰ是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是___________ 。
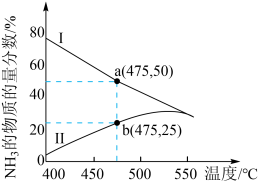
A.图中a点,容器内
B.图中b点,
C.400~530℃,Ⅱ中 的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
(5)在固定体积的密闭容器中,进行反应:
 其平衡常数K与温度T的关系如下表:
其平衡常数K与温度T的关系如下表:
①
___________  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
②一定温度下,在1L密闭容器中充入1mol 和3mol
和3mol 并发生反应,10min达到平衡时,气体的总物质的量变为原来的
并发生反应,10min达到平衡时,气体的总物质的量变为原来的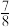 ,则
,则 的转化率
的转化率
___________ 。
(1)在一定条件下,
 和
和 反应生成0.2mol
反应生成0.2mol ,放出9.24kJ的热量,写出该可逆反应的热化学方程式:
,放出9.24kJ的热量,写出该可逆反应的热化学方程式:
(2)将
 和
和 通入体积为2L的恒温恒容密闭容器中5min后达到化学平衡,测得
通入体积为2L的恒温恒容密闭容器中5min后达到化学平衡,测得 的浓度为0.2mol/L,这段时间内用
的浓度为0.2mol/L,这段时间内用 的浓度变化表示的反应速率为
的浓度变化表示的反应速率为(3)理论上,为了提高
 的平衡转化率,可以采取的措施是
的平衡转化率,可以采取的措施是(4)下图是某压强下
 和
和 按物质的量之比1∶3投料进行反应,反应混合物中
按物质的量之比1∶3投料进行反应,反应混合物中 的物质的量分数随温度的变化曲线。Ⅰ是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是
的物质的量分数随温度的变化曲线。Ⅰ是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是
A.图中a点,容器内

B.图中b点,

C.400~530℃,Ⅱ中
 的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大(5)在固定体积的密闭容器中,进行反应:

 其平衡常数K与温度T的关系如下表:
其平衡常数K与温度T的关系如下表:| T/K | 298 | 398 | 498 |
| 平衡常数K | 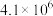 |  |  |

 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。②一定温度下,在1L密闭容器中充入1mol
 和3mol
和3mol 并发生反应,10min达到平衡时,气体的总物质的量变为原来的
并发生反应,10min达到平衡时,气体的总物质的量变为原来的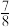 ,则
,则 的转化率
的转化率
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】二氧化碳催化加氢制甲醇,有利于减少温室气体二氧化碳。回答下列问题:
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g) CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:
CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:
①CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ•mol-1
②CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ•mol-1
总反应的ΔH=___________ kJ•mol-1;若反应①为慢反应,下列示意图中能体现上述反应能量变化的是 ___________ (填标号)。
A.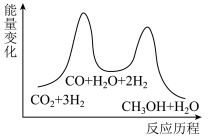 B.
B. 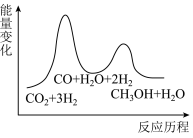
C.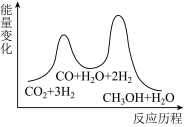 D.
D. 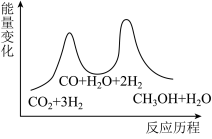
(2)合成总反应在起始物 3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下,x(CH3OH)与压强的关系(x(CH3OH)~p)和在p=5×105Pa下,x(CH3OH)与温度的关系(x(CH3OH)~t)分别如图所示,请回答下列问题:
3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下,x(CH3OH)与压强的关系(x(CH3OH)~p)和在p=5×105Pa下,x(CH3OH)与温度的关系(x(CH3OH)~t)分别如图所示,请回答下列问题:
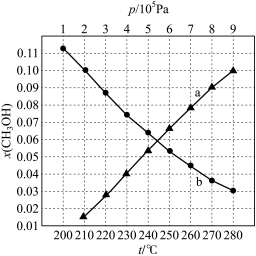
①图中对应等压过程的曲线是___________ ,判断的理由是 ___________ 。
②当x(CH3OH)=0.10时,CO2的平衡转化率α=___________ (保留两位有效数字),反应条件可能为 ___________ 。
(1)二氧化碳加氢制甲醇的总反应可表示为:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:
CH3OH(g)+H2O(g),该反应一般认为通过如下步骤来实现:①CO2(g)+H2(g)=CO(g)+H2O(g) ΔH1=+41kJ•mol-1
②CO(g)+2H2(g)=CH3OH(g) ΔH2=-90kJ•mol-1
总反应的ΔH=
A.
 B.
B. 
C.
 D.
D. 
(2)合成总反应在起始物
 3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下,x(CH3OH)与压强的关系(x(CH3OH)~p)和在p=5×105Pa下,x(CH3OH)与温度的关系(x(CH3OH)~t)分别如图所示,请回答下列问题:
3时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为x(CH3OH),在t=250℃下,x(CH3OH)与压强的关系(x(CH3OH)~p)和在p=5×105Pa下,x(CH3OH)与温度的关系(x(CH3OH)~t)分别如图所示,请回答下列问题:
①图中对应等压过程的曲线是
②当x(CH3OH)=0.10时,CO2的平衡转化率α=
您最近一年使用:0次

 、30mL
、30mL 、20mL
、20mL

