设 NA 为阿伏伽德罗常数的值。下列说法正确的是
| A.密闭容器中,2 mol SO2 和足量 O2 充分反应,产物的分子数为 2 NA |
| B.含 NA 个 CO32-的 Na2CO3 溶液中,Na+数目为 2 NA |
| C.11.2 L 甲烷和乙烯的混合物中含氢原子数目为 2 NA |
| D.4.0 g CO2 气体中含电子数目为 2 NA |
更新时间:2018-12-20 22:23:04
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】设 为阿伏伽德罗常数的值。下列说法不正确的是
为阿伏伽德罗常数的值。下列说法不正确的是
 为阿伏伽德罗常数的值。下列说法不正确的是
为阿伏伽德罗常数的值。下列说法不正确的是A. 乙烯和丙烯的混合气体中含有原子的数目为 乙烯和丙烯的混合气体中含有原子的数目为 |
B.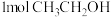 分子中含有的共价键数目为 分子中含有的共价键数目为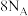 |
C.标准状况下, 二氯甲烷所含分子数为 二氯甲烷所含分子数为 |
D.由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极生成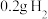 ,则电路通过电子 ,则电路通过电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】实验室中利用硫化亚铁和硫化锌混合物进行如图实验(忽略 在水中的溶解)。下列说法错误的是。
在水中的溶解)。下列说法错误的是。

 在水中的溶解)。下列说法错误的是。
在水中的溶解)。下列说法错误的是。
| A.“4.5g固体”一定是铁锌混合物 | B.“溶液2”中的溶质只有 |
| C.混合物中硫元素的质量分数约为38% | D.反应②能生成标准状况下 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】设 为阿伏加德罗常数的值,下列有关说法不正确的是
为阿伏加德罗常数的值,下列有关说法不正确的是
 为阿伏加德罗常数的值,下列有关说法不正确的是
为阿伏加德罗常数的值,下列有关说法不正确的是A.常温常压下,18g水含有的电子数为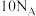 |
B.在1mol/L的NaCl溶液中, 的数目为 的数目为 |
C.16g氧气和臭氧的混合气体中含有 个氧原子 个氧原子 |
D.足量的Fe与1mol氯气充分反应,则转移电子数为 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】NA是阿伏伽德罗常数的值,下列说法正确的是
| A.16.25 g FeCl3 水解形成的 Fe(OH)3 胶体粒子数为 0.1 NA |
| B.一定条件下,6.4g 铜与过量的硫反应,转移电子数为 0.2NA |
| C.常温常压下,22.4LSO2 中含有的分子数小于 NA |
| D.6.4gCaC2 中所含的共价键数为 0.2NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】设 为阿伏加德罗常数值,下列有关叙述正确的是
为阿伏加德罗常数值,下列有关叙述正确的是
 为阿伏加德罗常数值,下列有关叙述正确的是
为阿伏加德罗常数值,下列有关叙述正确的是A.14g乙烯和丙烯混合气体中的氢原子数为2 |
B.1molCH4 与4molCl2反应生成的CCl4分子数为 |
C.1mol CnH2n+2分子结构式中 键数为(3n+2) 键数为(3n+2)  |
D.标准状况下,2.24L苯含有的C-H共价键数为0.6 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设NA表示阿伏加德罗常数的值。下列叙述正确的是
| A.标准状况下,22.4L氯乙烷所含分子数为NA |
| B.25℃时,pH=14的NaOH溶液中阴、阳离子总数为2NA |
C. 和 和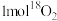 充分反应,产物中含 充分反应,产物中含 原子数为2NA 原子数为2NA |
D.78g苯和立方烷(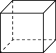 )的混合物中,C-H键数目为6NA )的混合物中,C-H键数目为6NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】设NA为阿伏加德罗常数的值,下列说法正确的是
| A.标准状况下,将22.4 L Cl2溶于水配成500 mL新制氯水,氯水中含氯微粒总数为2NA |
| B.0.1 mol FeCl3与水充分反应形成Fe(OH)3胶体粒子数为0.1NA |
C.标准状况下,1个氧气分子体积为 |
| D.标准状况下,22.4 LCO和CO2混合气体中分子数为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温下,下列说法正确的是
| A.将pH=2的盐酸和pH=4的硫酸等体积混合,所得溶液pH=3 |
| B.HF比HCN易电离,则NaF溶液的pH比同浓度NaCN溶液的pH大 |
| C.将10 mL pH=3的HA溶液稀释到100 mL,若溶液的pH<4,则HA为弱酸 |
D.向0.1 mol/L氨水中加入少量硫酸铵固体,溶液中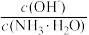 增大 增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】借助pH传感器测得0.1mol•L-1NaHCO3溶液在先升温、后降温过程中pH变化如图所示。下列分析不合理的是
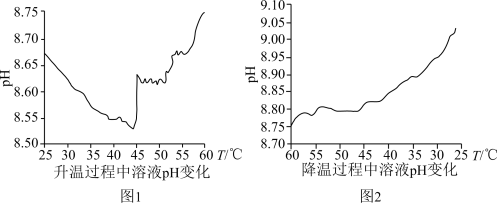

A.图甲中25℃时,溶液中存在关系:c(Na+)=c(HCO )+c(H2CO3)+c(CO )+c(H2CO3)+c(CO ) ) |
B.图甲中25~45℃过程,溶液pH逐渐减小,说明HCO 的电离平衡对pH影响较大 的电离平衡对pH影响较大 |
| C.图甲中45~60℃过程,溶液pH逐渐增大,可能是NaHCO3分解生成Na2CO3导致的结果 |
D.图乙中降温过程,溶液pH逐渐增大,可能是HCO 或CO 或CO 水解平衡正移所致 水解平衡正移所致 |
您最近一年使用:0次

 为阿伏加德罗常数的值,下列叙述错误的是
为阿伏加德罗常数的值,下列叙述错误的是
 溶液中滴加
溶液中滴加 溶液至中性,所得溶液中
溶液至中性,所得溶液中 的数目小于0.1
的数目小于0.1 的分子数为0.1
的分子数为0.1 中的分子数目小于
中的分子数目小于
 晶体所含离子总数为2
晶体所含离子总数为2 可以大量存在的体系:
可以大量存在的体系: 、
、 、
、
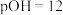 的溶液
的溶液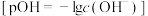 :
: 、
、
 、
、
 、
、 、
、


