CO2的转化一直是全球研究的热点,其中将CO2和H2合成甲醇及二甲醚具备相对成熟的技术。工业生产中,有以下相关反应(热效应都是在25 ℃,1.01105Pa下测定):
①CO2(g) + 3H2(g) ⇌CH3OH(l) + H2O(l) ΔH =-49.01 kJ·mol-1
②2CH3OH(l)⇌CH3OCH3(g) + H2O(l) ΔH =-24.52 kJ·mol-1
③CO(g) + H2O(l)⇌CO2(g) + H2(g) ΔH = -41.17 kJ·mol-1
(1)工业上用CO2和H2合成二甲醚的热化学方程式为_______ 。
(2)反应①的平衡常数表达式K=_______ 。
(3)在一常温恒容的密闭容器中,放入一定量的甲醇发生如②式化学反应并建立平衡,以下说法正确并可以作为该反应达到平衡状态的判断依据的是_______ (填字母)。
A.容器内气体相对分子质量保持不变 B. 容器内气体压强不变
C.相同时间内消耗甲醇的量是消耗二甲醚的两倍 D.甲醇和二甲醚物质的量相等
(4)在三个体积相同的密闭容器中加入相同物质的量的CO和H2O,在不同温度下发生反应③,经过相同时间后测得容器中的CO物质的量与温度的关系如图:
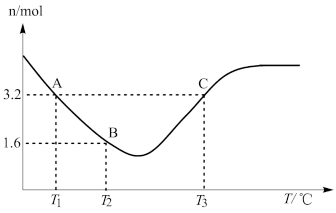
I.A、C两点的速率大小v(A)_______ (填“大于”“小于”“等于”或“无 法判断”)v(C)。
II.请解释曲线中CO的物质的量先减小后增大的原因_______ 。
①CO2(g) + 3H2(g) ⇌CH3OH(l) + H2O(l) ΔH =-49.01 kJ·mol-1
②2CH3OH(l)⇌CH3OCH3(g) + H2O(l) ΔH =-24.52 kJ·mol-1
③CO(g) + H2O(l)⇌CO2(g) + H2(g) ΔH = -41.17 kJ·mol-1
(1)工业上用CO2和H2合成二甲醚的热化学方程式为
(2)反应①的平衡常数表达式K=
(3)在一常温恒容的密闭容器中,放入一定量的甲醇发生如②式化学反应并建立平衡,以下说法正确并可以作为该反应达到平衡状态的判断依据的是
A.容器内气体相对分子质量保持不变 B. 容器内气体压强不变
C.相同时间内消耗甲醇的量是消耗二甲醚的两倍 D.甲醇和二甲醚物质的量相等
(4)在三个体积相同的密闭容器中加入相同物质的量的CO和H2O,在不同温度下发生反应③,经过相同时间后测得容器中的CO物质的量与温度的关系如图:

I.A、C两点的速率大小v(A)
II.请解释曲线中CO的物质的量先减小后增大的原因
更新时间:2018-12-29 11:47:50
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】工业上利用反应:
 可减少
可减少 的排放。
的排放。
(1)已知:

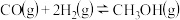
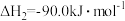

___________
(2)工业上为提高 产率,理论上应采用的条件是___________(填字母)。
产率,理论上应采用的条件是___________(填字母)。
(3)能判断工业上合成甲醇反应达到化学平衡状态的依据是___________(填字母)。
(4)在容积为1L的恒温密闭容器中充入
 和
和
 ,一定条件下发生反应,测得
,一定条件下发生反应,测得 和
和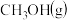 的浓度随时间变化如图所示:
的浓度随时间变化如图所示:

①0~3min
___________ (保留两位小数)
② 的平衡转化率是
的平衡转化率是___________ %
③平衡常数
___________ (保留两位小数)
(5)催化剂和反应条件与反应物转化率和产物的选择性有高度相关。控制相同投料比和相同反应时间,四组实验数据如下:
(注:甲醇选择性是指转化的 中生成甲醇的百分含量),根据上表所给数据,用
中生成甲醇的百分含量),根据上表所给数据,用 生产甲醇的最优选项为
生产甲醇的最优选项为___________ (填字母)。

 可减少
可减少 的排放。
的排放。(1)已知:


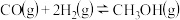
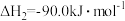

(2)工业上为提高
 产率,理论上应采用的条件是___________(填字母)。
产率,理论上应采用的条件是___________(填字母)。| A.高温高压 | B.低温低压 | C.高温低压 | D.低温高压 |
| A.容器内压强不变 | B.混合气体中 不变 不变 |
C. | D. |

 和
和
 ,一定条件下发生反应,测得
,一定条件下发生反应,测得 和
和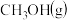 的浓度随时间变化如图所示:
的浓度随时间变化如图所示:
①0~3min

②
 的平衡转化率是
的平衡转化率是③平衡常数

(5)催化剂和反应条件与反应物转化率和产物的选择性有高度相关。控制相同投料比和相同反应时间,四组实验数据如下:
| 实验编号 | 温度(K) | 催化剂 |  转化率(%) 转化率(%) | 甲醇选择性(%) |
| A | 543 |  / / 纳米棒 纳米棒 | 12.3 | 42.3 |
| B | 543 |  / / 纳米片 纳米片 | 11.9 | 72.7 |
| C | 553 |  / / 纳米棒 纳米棒 | 15.3 | 39.1 |
| D | 553 |  / / 纳米片 纳米片 | 12.0 | 70.6 |
 中生成甲醇的百分含量),根据上表所给数据,用
中生成甲醇的百分含量),根据上表所给数据,用 生产甲醇的最优选项为
生产甲醇的最优选项为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】雾霾严重影响人们的生活,汽车尾气的排放是造成雾霾天气的重要原因之一。已知汽车尾气排放时容易发生以下反应:
①N2(g)+O2(g) 2NO(g) △H1= a kJ·mol-1
2NO(g) △H1= a kJ·mol-1
②CO(g)+1/2 O2(g) CO2(g) △H2= b kJ·mol-1
CO2(g) △H2= b kJ·mol-1
③2CO(g)+2NO(g) N2(g)+2CO2(g) △H3
N2(g)+2CO2(g) △H3
请回答下列问题:
(1)△H3=_________ kJ·mol-1(用含a、b的代数式表示)。
(2)对于有气体参与的反应,则反应①的平衡常数表达式K=___________ 。
(3)能说明反应③已达平衡状态的标志是________ (填字母)。
A.单位时间内生成1mol CO2的同时消耗了lmol CO
B.在恒温恒容的容器中,混合气体的密度保持不变
C.在绝热恒容的容器中,反应的平衡常数不再变化
D.在恒温恒压的容器中,NO的体积分数保持不变
(4)在一定温度下,向体积为VL的恒容密闭容器中充入一定量的NO和CO,发生反应③。在t1时刻达到平衡,此时n(CO)=xmol,n(NO)=2xmol,n(N2)=ymol,则NO的平衡转化率为____________ (用含x、y的代数式表示);t2时刻再向容器中充入ymolCO2,则此时v(正)_________ (填“>”、“<”或“=”)v(逆)。
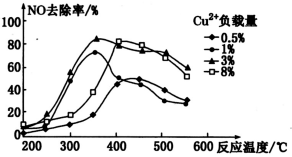
(5)烟气中也含有氮氧化物,C2H4可用于烟气脱硝。为研究温度、催化剂中Cu2+负载量对NO去除率的影响,控制其它条件一定,实验结果如右图所示。为达到最高的NO去除率,应选择的反应温度约为______ ,Cu2+负载量为_________ 。
①N2(g)+O2(g)
 2NO(g) △H1= a kJ·mol-1
2NO(g) △H1= a kJ·mol-1②CO(g)+1/2 O2(g)
 CO2(g) △H2= b kJ·mol-1
CO2(g) △H2= b kJ·mol-1③2CO(g)+2NO(g)
 N2(g)+2CO2(g) △H3
N2(g)+2CO2(g) △H3请回答下列问题:
(1)△H3=
(2)对于有气体参与的反应,则反应①的平衡常数表达式K=
(3)能说明反应③已达平衡状态的标志是
A.单位时间内生成1mol CO2的同时消耗了lmol CO
B.在恒温恒容的容器中,混合气体的密度保持不变
C.在绝热恒容的容器中,反应的平衡常数不再变化
D.在恒温恒压的容器中,NO的体积分数保持不变
(4)在一定温度下,向体积为VL的恒容密闭容器中充入一定量的NO和CO,发生反应③。在t1时刻达到平衡,此时n(CO)=xmol,n(NO)=2xmol,n(N2)=ymol,则NO的平衡转化率为
(5)烟气中也含有氮氧化物,C2H4可用于烟气脱硝。为研究温度、催化剂中Cu2+负载量对NO去除率的影响,控制其它条件一定,实验结果如右图所示。为达到最高的NO去除率,应选择的反应温度约为

您最近一年使用:0次
【推荐3】二氧化碳、甲烷等是主要的温室气体。研发二氧化碳和甲烷的利用技术对治理生态环境具有重要意义。
(1)已知: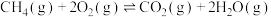
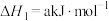




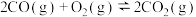
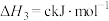

则催重整反应 的
的
___________ ,平衡常数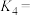
___________ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
(2)催化重整反应 中,测得
中,测得 的平衡转化率与温度及压强的关系如下图所示:
的平衡转化率与温度及压强的关系如下图所示:
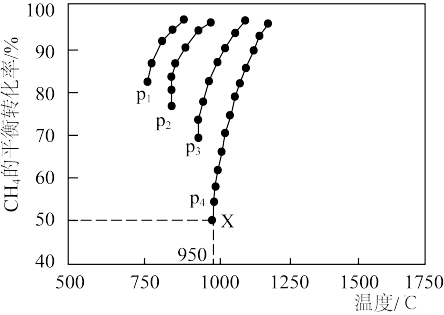
在压强为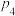 、投料比
、投料比 、950℃的条件下,X点平衡常数
、950℃的条件下,X点平衡常数
___________ 。
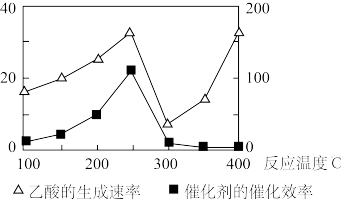
(3)以二氧化钛表面覆盖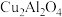 为催化剂,还可以将
为催化剂,还可以将 和
和 直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率却在降低的原因是
直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率却在降低的原因是___________ 。
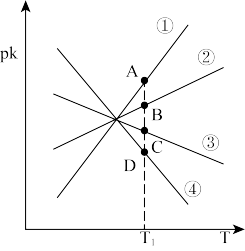
(4)反应
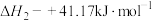 的正、逆反应速率可分别表示为
的正、逆反应速率可分别表示为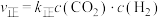 、
、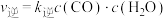 ,则如图所示的四条斜线中,能表示
,则如图所示的四条斜线中,能表示 随T变化关系的是
随T变化关系的是___________ (填序号)。
(5)一种以甲醇为原料,利用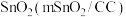 和CuO纳米片(CuONS/CF)作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。
和CuO纳米片(CuONS/CF)作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。
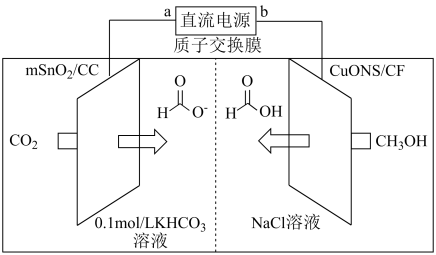
①电解过程中阳极电极反应式为___________ 。
②当有4mol 通过质子交换膜时,装置中生成
通过质子交换膜时,装置中生成 和HC0OH共计
和HC0OH共计___________ mol。
(1)已知:
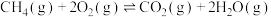
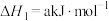




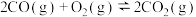
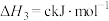

则催重整反应
 的
的
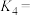
 、
、 、
、 的代数式表示)。
的代数式表示)。(2)催化重整反应
 中,测得
中,测得 的平衡转化率与温度及压强的关系如下图所示:
的平衡转化率与温度及压强的关系如下图所示:
在压强为
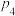 、投料比
、投料比 、950℃的条件下,X点平衡常数
、950℃的条件下,X点平衡常数
(3)以二氧化钛表面覆盖
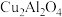 为催化剂,还可以将
为催化剂,还可以将 和
和 直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率却在降低的原因是
直接转化成乙酸。在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,温度升高而乙酸的生成速率却在降低的原因是
(4)反应

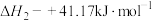 的正、逆反应速率可分别表示为
的正、逆反应速率可分别表示为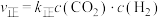 、
、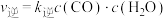 ,则如图所示的四条斜线中,能表示
,则如图所示的四条斜线中,能表示 随T变化关系的是
随T变化关系的是
(5)一种以甲醇为原料,利用
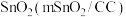 和CuO纳米片(CuONS/CF)作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。
和CuO纳米片(CuONS/CF)作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示。
①电解过程中阳极电极反应式为
②当有4mol
 通过质子交换膜时,装置中生成
通过质子交换膜时,装置中生成 和HC0OH共计
和HC0OH共计
您最近一年使用:0次
【推荐1】目前“低碳经济”正成为科学家研究的主要课题。请回答下列问题:
利用I2O5消除CO污染的反应为5CO(g)+I2O5(s) 5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4molCO,测得CO2的体积分数随时间t变化曲线如下图。请回答:
5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4molCO,测得CO2的体积分数随时间t变化曲线如下图。请回答:
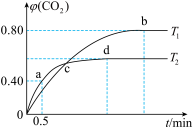
(1)以CnH2nOn、O2为原料,H2SO4溶液为电解质设计成燃料电池,则负极的电极反应式为______________________ 。
(2)T2时,0~0.5min内的反应速率v(CO)=________________ 。
(3)T1时化学平衡常数K=________ 。
(4)下列说法不正确的是________ (填标号)。
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的压强相等
C.d点时,增大体系压强,CO的转化率不变
D.b点和d点时化学平衡常数的大小关系:Kb<Kd
利用I2O5消除CO污染的反应为5CO(g)+I2O5(s)
 5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4molCO,测得CO2的体积分数随时间t变化曲线如下图。请回答:
5CO2(g)+I2(s),不同温度下,向装有足量I2O5固体的2L恒容密闭容器中通入4molCO,测得CO2的体积分数随时间t变化曲线如下图。请回答:
(1)以CnH2nOn、O2为原料,H2SO4溶液为电解质设计成燃料电池,则负极的电极反应式为
(2)T2时,0~0.5min内的反应速率v(CO)=
(3)T1时化学平衡常数K=
(4)下列说法不正确的是
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的压强相等
C.d点时,增大体系压强,CO的转化率不变
D.b点和d点时化学平衡常数的大小关系:Kb<Kd
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】实验室制取SO2的反应原理为:Na2SO3+H2SO4(浓) Na2SO4+SO2↑+H2O。请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:
Na2SO4+SO2↑+H2O。请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:

(1)装置的连接顺序(按气体左右的方向)是____ →_____ →_____ →_____ →_______ →_____ →_____ →_____ (填各接口的编号)。
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是__________________________________________________ 。
(3)Ⅳ处观察到的现象是___________________________________________ 。
(4)若II中反应在适当的反应状况下,反应达最大限度以后,下列说法正确的是__________ 。
A.SO2浓度必定等于O2浓度的两倍
B.SO2、O2、SO3的分子数之比是2∶1∶2
C.SO2与O2不再化合生成SO3
D.反应混合物各成分的百分组成不再变化
(5)在Ⅰ处用大火加热烧瓶时,SO2的转化率会_______ (填“增大”“不变”或“减小”)。
(6)用nmol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得III处增重mg,则本实验中SO2的转化率为______________________ 。(用n、m表示)
 Na2SO4+SO2↑+H2O。请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:
Na2SO4+SO2↑+H2O。请用下列装置设计一个实验,以测定SO2转化为SO3的转化率:
(1)装置的连接顺序(按气体左右的方向)是
(2)从乙处均匀通入O2,为使SO2有较高的转化率,实验时Ⅰ处滴入浓硫酸与Ⅱ处加热催化剂的先后顺序是
(3)Ⅳ处观察到的现象是
(4)若II中反应在适当的反应状况下,反应达最大限度以后,下列说法正确的是
A.SO2浓度必定等于O2浓度的两倍
B.SO2、O2、SO3的分子数之比是2∶1∶2
C.SO2与O2不再化合生成SO3
D.反应混合物各成分的百分组成不再变化
(5)在Ⅰ处用大火加热烧瓶时,SO2的转化率会
(6)用nmol Na2SO3粉末与足量浓硫酸进行此实验,当反应结束时,继续通入O2一段时间后,称得III处增重mg,则本实验中SO2的转化率为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】氨气可作为脱硝剂。回答下列问题:
(1)在恒温恒容密闭容器中充入一定量的NO和 ,在一定条件下发生反应
,在一定条件下发生反应
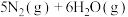 。
。
①能说明该反应已达到平衡状态标志的是___________ (填标号)。
a.反应速率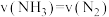
b.容器内压强不再随时间而发生变化
c.容器内 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化
d.容器内
②某次实验中测得容器内NO及 的物质的量随时间的变化如图所示,图中b点对应的反应速率关系是
的物质的量随时间的变化如图所示,图中b点对应的反应速率关系是
___________  (填“
(填“ ” “
” “ ”或“
”或“ ”)。
”)。
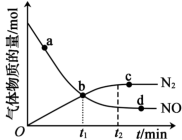
(2)一定温度下,在2L恒容密闭容器内发生反应 ,
,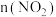 随时间的变化如下表:
随时间的变化如下表:
①0~2s内,该反应的平均速率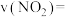
___________ 。
②根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是___________ 。
③该温度下,反应 的平衡常数
的平衡常数
___________  。
。
(3)对于反应 ,用平衡时各组分压强关系表达的平衡常数
,用平衡时各组分压强关系表达的平衡常数 。在一定条件下
。在一定条件下 与
与 的消耗速率与自身压强间存在关系:
的消耗速率与自身压强间存在关系: ,
,
 。其中
。其中 、
、 是与反应及温度有关的常数。相应的消耗速率跟压强的关系如图所示:
是与反应及温度有关的常数。相应的消耗速率跟压强的关系如图所示:

一定温度下, 、
、 与平衡常数
与平衡常数 的关系是
的关系是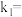
___________ 。在图标出的点中,指出能表示反应达到平衡状态的点并说明理由:___________ 。
(1)在恒温恒容密闭容器中充入一定量的NO和
 ,在一定条件下发生反应
,在一定条件下发生反应
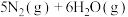 。
。①能说明该反应已达到平衡状态标志的是
a.反应速率
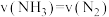
b.容器内压强不再随时间而发生变化
c.容器内
 的物质的量分数不再随时间而发生变化
的物质的量分数不再随时间而发生变化d.容器内

②某次实验中测得容器内NO及
 的物质的量随时间的变化如图所示,图中b点对应的反应速率关系是
的物质的量随时间的变化如图所示,图中b点对应的反应速率关系是
 (填“
(填“ ” “
” “ ”或“
”或“ ”)。
”)。
(2)一定温度下,在2L恒容密闭容器内发生反应
 ,
,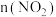 随时间的变化如下表:
随时间的变化如下表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
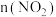 /mol /mol | 0.040 | 0.020 | 0.010 | 0.005 | 0.005 | 0.005 |
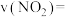
②根据上表可以看出,随着反应进行,反应速率逐渐减小,其原因是
③该温度下,反应
 的平衡常数
的平衡常数
 。
。(3)对于反应
 ,用平衡时各组分压强关系表达的平衡常数
,用平衡时各组分压强关系表达的平衡常数 。在一定条件下
。在一定条件下 与
与 的消耗速率与自身压强间存在关系:
的消耗速率与自身压强间存在关系: ,
,
 。其中
。其中 、
、 是与反应及温度有关的常数。相应的消耗速率跟压强的关系如图所示:
是与反应及温度有关的常数。相应的消耗速率跟压强的关系如图所示:
一定温度下,
 、
、 与平衡常数
与平衡常数 的关系是
的关系是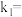
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】一定条件下CO和H2能够合成再生能源甲醇,发生的反应为:CO(g)+2H2(g)⇌CH3OH(g)△H
(1)已知:
上述反应的△H=______ kJ·mol-1
(2)一定条件下,将n(CO):n(H2)=1:1的混合气体充入绝热恒容密闭容器中,下列事实可以说明上述反应已达到平衡的是________ (填字母)
A.容器内气体密度保持不变 B.CO的体积分数保持不变
C.CO的消耗速率等于CH3OH的消耗速率 D.反应的平衡常数保持不变
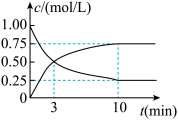
(3)为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1 mol CO和2.5molH2,一定温度下发生反应CO(g)+2H2(g)⇌CH3OH(g),测得CO和CH3OH(g)的浓度时间变化如下图所示。则从反应开始到平衡CH3OH的平均反应速率v(CH3OH)=________ ,H2的转化率α(H2)=________ 。
(4)下图为绿色电源“甲醇燃料电池”的工作原理示意图,Pt(a)电极的反应式为________ ,若该燃料电池工作时电路中通过6mol电子,则消耗的O2有____ mol,工作一段时间后,电解质溶液的pH将____ (填“增大”、“减小”或“不变”)。
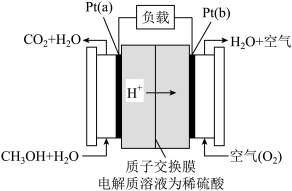
(1)已知:
| 化学键 | H-H | C-O | C≡O | H-O | C-H |
| 键能/kJ·mol-1 | 436 | 326 | 1072 | 464 | 414 |
上述反应的△H=
(2)一定条件下,将n(CO):n(H2)=1:1的混合气体充入绝热恒容密闭容器中,下列事实可以说明上述反应已达到平衡的是
A.容器内气体密度保持不变 B.CO的体积分数保持不变
C.CO的消耗速率等于CH3OH的消耗速率 D.反应的平衡常数保持不变
(3)为探究反应原理,现进行如下实验,在体积为1L的密闭容器中,充入1 mol CO和2.5molH2,一定温度下发生反应CO(g)+2H2(g)⇌CH3OH(g),测得CO和CH3OH(g)的浓度时间变化如下图所示。则从反应开始到平衡CH3OH的平均反应速率v(CH3OH)=

(4)下图为绿色电源“甲醇燃料电池”的工作原理示意图,Pt(a)电极的反应式为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】化学反应速率、限度及能量变化与生活、生产密切相关。
(1)由 和
和 转化为
转化为 的催化反应历程示意图如图。该历程中,①→②的过程中,
的催化反应历程示意图如图。该历程中,①→②的过程中,___________ (填“吸收”或“放出”)能量,涉及___________ (填标号,下同)键的形成,甲烷→①的过程中涉及___________ 键的断裂。

a. b.C—H c.C—C d.O—H e.C—O
b.C—H c.C—C d.O—H e.C—O
(2)在容积为2L的恒容密闭容器中充入2mol 和4mol
和4mol ,在一定温度下发生反应:
,在一定温度下发生反应: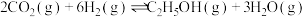 ,10min反应达到平衡时,测得
,10min反应达到平衡时,测得 。
。
①0~10min内,
___________  ,
, 的体积分数为
的体积分数为___________ 。
②上述反应达到平衡时,混合气体的平均摩尔质量为___________  。
。
③能说明该反应已达到平衡状态的是___________ (填标号)。
a. b.容器内压强保持不变
b.容器内压强保持不变
c.每断裂1molH—H,形成1molO—H d.容器内混合气体的密度保持不变
(3) 、
、 和熔融
和熔融 可制作燃料电池(反应原理为
可制作燃料电池(反应原理为 ),其工作原理如图所示。该电池在放电过程中生成氧化物Y,Y可循环使用,则石墨Ⅱ电极为
),其工作原理如图所示。该电池在放电过程中生成氧化物Y,Y可循环使用,则石墨Ⅱ电极为___________ (填“正极”或“负极”),负极的电极反应式为___________ 。

(1)由
 和
和 转化为
转化为 的催化反应历程示意图如图。该历程中,①→②的过程中,
的催化反应历程示意图如图。该历程中,①→②的过程中,
a.
 b.C—H c.C—C d.O—H e.C—O
b.C—H c.C—C d.O—H e.C—O(2)在容积为2L的恒容密闭容器中充入2mol
 和4mol
和4mol ,在一定温度下发生反应:
,在一定温度下发生反应: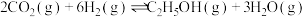 ,10min反应达到平衡时,测得
,10min反应达到平衡时,测得 。
。①0~10min内,

 ,
, 的体积分数为
的体积分数为②上述反应达到平衡时,混合气体的平均摩尔质量为
 。
。③能说明该反应已达到平衡状态的是
a.
 b.容器内压强保持不变
b.容器内压强保持不变c.每断裂1molH—H,形成1molO—H d.容器内混合气体的密度保持不变
(3)
 、
、 和熔融
和熔融 可制作燃料电池(反应原理为
可制作燃料电池(反应原理为 ),其工作原理如图所示。该电池在放电过程中生成氧化物Y,Y可循环使用,则石墨Ⅱ电极为
),其工作原理如图所示。该电池在放电过程中生成氧化物Y,Y可循环使用,则石墨Ⅱ电极为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】对温室气体二氧化碳的处理是化学工作者实现“碳中和”的重点研究课题。一种新的循环利用方案是利用 和
和 制取重要的化工原料甲醇。
制取重要的化工原料甲醇。
(1)已知:



则反应 的
的
___________  。该反应可以在进行
。该反应可以在进行___________ (填序号)。
A.低温自发 B.高温自发 C.高、低温均能自发 D.高、低温均不自发
(2)在恒容密闭容器中,发生反应 ,下列叙述中正确的是___________。
,下列叙述中正确的是___________。
(3)利用 和
和 合成甲醇,在催化剂
合成甲醇,在催化剂 作用下可发生如下两个平行反应。
作用下可发生如下两个平行反应。
主反应 :
:
副反应 :
: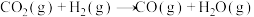
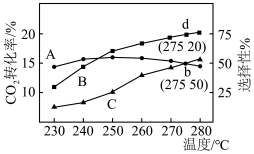
温度对 转化率及产物甲醇和
转化率及产物甲醇和 选择性的影响如图所示。产物的选择性(如甲醇的选择性
选择性的影响如图所示。产物的选择性(如甲醇的选择性 )。
)。___________ (填A、B、C)是表示 的选择性随温度的变化。
的选择性随温度的变化。
②A曲线温度达到250℃后随温度增大而降低的原因是___________ 。
③下列措施有利于提高 转化为
转化为 的平衡转化率的有
的平衡转化率的有___________ 。
A.增大体系压强
B.提高 和
和 的投料比
的投料比
C.体积和投料比不变,提高反应物浓度
D.选择合适的催化剂
④若按投料比1:3投入 和
和 ,在一定条件下进行上述主反应
,在一定条件下进行上述主反应 和副反应
和副反应 。图中d为曲线B上的一点,坐标为
。图中d为曲线B上的一点,坐标为 ,曲线A、C相交于b点
,曲线A、C相交于b点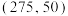 ,在275℃时测得达平衡时,压强为
,在275℃时测得达平衡时,压强为 ,则此时主反应的
,则此时主反应的
___________ (列出计算式,用含 的式子表示)。
的式子表示)。
 和
和 制取重要的化工原料甲醇。
制取重要的化工原料甲醇。(1)已知:




则反应
 的
的
 。该反应可以在进行
。该反应可以在进行A.低温自发 B.高温自发 C.高、低温均能自发 D.高、低温均不自发
(2)在恒容密闭容器中,发生反应
 ,下列叙述中正确的是___________。
,下列叙述中正确的是___________。A.及时分离出 ,可以加快化学反应速率 ,可以加快化学反应速率 |
| B.恒容时,充入He增大压强,化学反应速率不变 |
| C.容器内压强不再变化,说明该反应已达到最大的限度 |
D.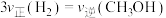 ,说明该反应已达到平衡状态 ,说明该反应已达到平衡状态 |
(3)利用
 和
和 合成甲醇,在催化剂
合成甲醇,在催化剂 作用下可发生如下两个平行反应。
作用下可发生如下两个平行反应。主反应
 :
:
副反应
 :
: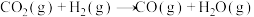
温度对
 转化率及产物甲醇和
转化率及产物甲醇和 选择性的影响如图所示。产物的选择性(如甲醇的选择性
选择性的影响如图所示。产物的选择性(如甲醇的选择性 )。
)。
 的选择性随温度的变化。
的选择性随温度的变化。②A曲线温度达到250℃后随温度增大而降低的原因是
③下列措施有利于提高
 转化为
转化为 的平衡转化率的有
的平衡转化率的有A.增大体系压强
B.提高
 和
和 的投料比
的投料比C.体积和投料比不变,提高反应物浓度
D.选择合适的催化剂
④若按投料比1:3投入
 和
和 ,在一定条件下进行上述主反应
,在一定条件下进行上述主反应 和副反应
和副反应 。图中d为曲线B上的一点,坐标为
。图中d为曲线B上的一点,坐标为 ,曲线A、C相交于b点
,曲线A、C相交于b点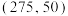 ,在275℃时测得达平衡时,压强为
,在275℃时测得达平衡时,压强为 ,则此时主反应的
,则此时主反应的
 的式子表示)。
的式子表示)。
您最近一年使用:0次
【推荐1】超音速飞机在平流层飞行时,尾气中的NO会破坏臭氧层。科学家正在研究利用催化技术将尾气中的NO和CO转变成CO2和N2,化学方程式如下:2NO+2CO  2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
请回答下列问题(均不考虑温度变化对催化剂催化效率的影响):
(1)在上述条件下反应能够自发进行,则反应的△H______ 0(填写“>”、“<”、“=”。
(2)前2s内的平均反应速率v(N2)=_____________ 。
(3)在该温度下,反应的平衡常数K=______________ 。
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是_____ 。
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
①请在上表格中填入剩余的实验条件数据________________ 。
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号________________ 。

 2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:
2CO2+N2,为了测定在某种催化剂作用下的反应速率,在某温度下用气体传感器测得不同时间的NO和CO浓度如表:| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| c(NO)/mol/L | 1.00×10-3 | 4.50×10-4 | 2.50×10-4 | 1.50×10-4 | 1.00×10-4 | 1.00×10-4 |
| c(CO)/mol/L | 3.60×10-3 | 3.05×10-3 | 2.85×10-3 | 2.75×10-3 | 2.70×10-3 | 2.70×10-3 |
(1)在上述条件下反应能够自发进行,则反应的△H
(2)前2s内的平均反应速率v(N2)=
(3)在该温度下,反应的平衡常数K=
(4)假设在密闭容器中发生上述反应,达到平衡时下列措施能提高NO转化率的是
A.选用更有效的催化剂 B.升高反应体系的温度
C.降低反应体系的温度 D.缩小容器的体积
(5)研究表明:在使用等质量催化剂时,增大催化剂比表面积可提高化学反应速率。为了分别验证温度、催化剂比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面实验设计表中。
| 实验编号 | T/℃ | NO初始浓度mol/L | CO初始浓度mol/L | 催化剂的比表面积m2/g |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ | 124 | |||
| Ⅲ | 350 | 124 |
②请在给出的坐标图中,画出上表中的三个实验条件下混合气体中NO浓度随时间变化的趋势曲线图,并标明各条曲线的实验编号

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】无水硫酸铜在强热下会发生分解反应:CuSO4 CuO + SO3↑,2SO3
CuO + SO3↑,2SO3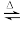 2SO2↑+ O2↑。用下图所示装置(夹持仪器已略去),根据D管在反应前后的质量差计算出分解了的无水硫酸铜的质量。
2SO2↑+ O2↑。用下图所示装置(夹持仪器已略去),根据D管在反应前后的质量差计算出分解了的无水硫酸铜的质量。
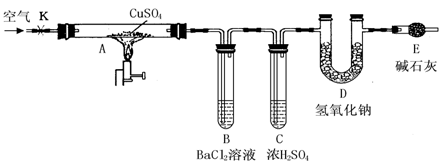
实验步骤:
①称量反应前D管的质量。
②连接好装置,关闭K,加热硬质玻璃管A一段时间后,停止加热。
③待硬质玻璃管A冷却后,打开K,通入一段时间的已除去二氧化碳等酸性气体的空气。
④再称量D管,得其反应前后的质量差为m。
回答下列问题:
(1)反应2SO3(g)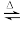 2SO2(g) + O2(g)的平衡常数表达式为K=
2SO2(g) + O2(g)的平衡常数表达式为K=__________ 。
(2)B管中除温度明显升高外,还可看到的现象是________ ,而温度明显升高的主要原因是________ ;B管中发生反应的有关离子方程式是_________ 。
(3)仪器E的作用是______ 。
(4)按上述方法实验,假设B、C、D对气体的吸收均完全,并忽略空气中CO2的影响,能否根据m计算出分解了的无水CuSO4的质量?(任选其一回答)
①如果能,则分解的无水CuSO4的质量为__________ (用m表示)。
②如果不能,则原因是___________ 。为了能测得分解了的无水硫酸铜的质量,你的简单实验方案是___________ 。
 CuO + SO3↑,2SO3
CuO + SO3↑,2SO3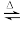 2SO2↑+ O2↑。用下图所示装置(夹持仪器已略去),根据D管在反应前后的质量差计算出分解了的无水硫酸铜的质量。
2SO2↑+ O2↑。用下图所示装置(夹持仪器已略去),根据D管在反应前后的质量差计算出分解了的无水硫酸铜的质量。
实验步骤:
①称量反应前D管的质量。
②连接好装置,关闭K,加热硬质玻璃管A一段时间后,停止加热。
③待硬质玻璃管A冷却后,打开K,通入一段时间的已除去二氧化碳等酸性气体的空气。
④再称量D管,得其反应前后的质量差为m。
回答下列问题:
(1)反应2SO3(g)
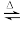 2SO2(g) + O2(g)的平衡常数表达式为K=
2SO2(g) + O2(g)的平衡常数表达式为K=(2)B管中除温度明显升高外,还可看到的现象是
(3)仪器E的作用是
(4)按上述方法实验,假设B、C、D对气体的吸收均完全,并忽略空气中CO2的影响,能否根据m计算出分解了的无水CuSO4的质量?(任选其一回答)
①如果能,则分解的无水CuSO4的质量为
②如果不能,则原因是
您最近一年使用:0次
【推荐3】据统计,约有90%以上的工业过程中需要使用催化剂,因此,对催化剂的研究已成为重要课题。
I.结合实验与计算机模拟结果,研究了N2与H2在固体催化剂表面合成NH3的反应历程。图示为反应历程中的势能面图(部分数据省略),其中吸附在催化剂表面的物种用*标注。

(1) 氨气的脱附是___________ (填“吸热”或“放热”)过程,合成氨的热化学方程式为___________ 。
(2) 当使用铁催化剂时,合成氨的速率方程式为w = k1•p(N2) -k2
-k2 ,其中w为反应的瞬时总速率,等于正反应速率和逆反应速率之差,k1、k2是正、逆反应速率常数,则合成氨反应N2+3H2
,其中w为反应的瞬时总速率,等于正反应速率和逆反应速率之差,k1、k2是正、逆反应速率常数,则合成氨反应N2+3H2 2NH3的平衡常数Kp=
2NH3的平衡常数Kp=___________ (用k1、k2表示)。
(3) 在使用同一催化剂时,将2.0molN2和6.0molH2 通入体积为1L的密闭容器中,分别在T1和T2温度下进行反应。曲线A表示T2时n(H2)的变化,曲线B表示T1时n(NH3)的变化,T2时反应到a点恰好达到平衡。
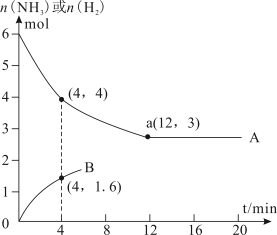
①T2温度下反应进行到某时刻,测得容器内气体的压强为起始时的80%,则此时v(正)___________ v(逆)(填“>”、“<”或“=”)。
②能否由图中数据得出温度T1>T2,试说明理由___________ 。
Ⅱ.用催化剂Fe3(CO)12/ZSM-5催化CO2加氢合成乙烯的过程中,还会生成CH4、C3H6、C4H8等副产物,若在催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性(选择性指的是转化的CO2中生成C2H4的百分比)。在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表:
(4) 欲提高单位时间内乙烯的产量,在Fe3(CO)12/ZSM-5中添加___________ 助剂效果最好;加入助剂能提高单位时间内乙烯产量的根本原因是___________ 。
I.结合实验与计算机模拟结果,研究了N2与H2在固体催化剂表面合成NH3的反应历程。图示为反应历程中的势能面图(部分数据省略),其中吸附在催化剂表面的物种用*标注。

(1) 氨气的脱附是
(2) 当使用铁催化剂时,合成氨的速率方程式为w = k1•p(N2)
 -k2
-k2 ,其中w为反应的瞬时总速率,等于正反应速率和逆反应速率之差,k1、k2是正、逆反应速率常数,则合成氨反应N2+3H2
,其中w为反应的瞬时总速率,等于正反应速率和逆反应速率之差,k1、k2是正、逆反应速率常数,则合成氨反应N2+3H2 2NH3的平衡常数Kp=
2NH3的平衡常数Kp=(3) 在使用同一催化剂时,将2.0molN2和6.0molH2 通入体积为1L的密闭容器中,分别在T1和T2温度下进行反应。曲线A表示T2时n(H2)的变化,曲线B表示T1时n(NH3)的变化,T2时反应到a点恰好达到平衡。

①T2温度下反应进行到某时刻,测得容器内气体的压强为起始时的80%,则此时v(正)
②能否由图中数据得出温度T1>T2,试说明理由
Ⅱ.用催化剂Fe3(CO)12/ZSM-5催化CO2加氢合成乙烯的过程中,还会生成CH4、C3H6、C4H8等副产物,若在催化剂中添加Na、K、Cu助剂后(助剂也起催化作用)可改变反应的选择性(选择性指的是转化的CO2中生成C2H4的百分比)。在其他条件相同时,添加不同助剂,经过相同时间后测得CO2转化率和各产物的物质的量分数如下表:
| 助剂 | CO2转化率(%) | 各产物在所有产物中的占比(%) | ||
| C2H4 | C3H6 | 其他 | ||
| Na | 42.5 | 35.9 | 39.6 | 24.5 |
| K | 27.2 | 75.6 | 22.8 | 1.6 |
| Cu | 9.8 | 80.7 | 12.5 | 6.8 |
您最近一年使用:0次



