三种常见元素结构信息如下表,试根据信息回答有关问题:
(1)写出B原子的基态电子排布式__ ;
(2)用氢键表示式写出A的氢化物溶液中存在的氢键__ (任写一种);A的氢化物分子结合一个H+形成阳离子后,其键角__ (填写“变大”、“变小”、“不变”);
(3)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为__ ,简要描述该配合物中化学键的成键情况__ ;
(4)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“○”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.
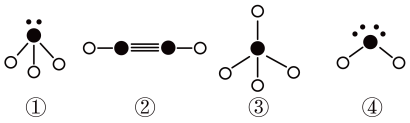
在以上分子中,中心原子采用sp3杂化形成化学键是__ (填写序号);在②的分子中有__ 个σ键和__ 个π键。
| 元素 | A | B | C |
| 结构信息 | 基态原子核外有两个电子层,最外层有3个未成对电子 | 基态原子的M层有1对成对的p电子 | 基态原子核外电子排布为[Ar]3d104sx,有+1、+2两种常见化合价 |
(2)用氢键表示式写出A的氢化物溶液中存在的氢键
(3)往C元素的硫酸盐溶液中逐滴加入过量A元素的氢化物水溶液,可生成的配合物的化学式为
(4)下列分子结构图中的“●”表示上述相关元素的原子中除去最外层电子的剩余部分,“○”表示氢原子,小黑点“•”表示没有形成共价键的最外层电子,短线表示共价键.

在以上分子中,中心原子采用sp3杂化形成化学键是
更新时间:2019-01-24 20:25:34
|
相似题推荐
【推荐1】硅是无机非金属材料的主角,硅材料在生活中占有重要地位,硅的氧化物和硅酸盐约占地壳质量的90%以上。请回答下列问题:
(1)基态硅原子核外电子云有___________ 种不同的伸展方向,有___________ 种形状的电子云,核外存在___________ 对自旋相反的电子。
(2)硅原子2p能级的三个轨道之间具有不同的___________。
(3)某元素位于第四周期第Ⅷ族,其基态原子的未成对电子数与基态硅原子的未成对电子数相同,则其基态原子的价层电子排布式为___________ 。
(4)由硅原子核形成的三种微粒,电子排布式分别为:①[Ne]3s23p2、②[Ne)3s23p1、③[Ne]3s13p14s1,有关这些微粒的叙述,正确的是___________。
(5)Si(NH2)4分子的空间结构(以Si为中心)名称为___________ ,分子中氮原子的杂化轨道类型是___________ ,Si(NH2)4受热分解生成Si3N4和NH3,其受热不稳定的原因是___________ 。
(6)晶体硅的结构跟金刚石相似,图1中原子坐标参数A为(0,0,0),B为( ,0,
,0, ),C(
),C( ,
, ,0),在立方晶胞中,与晶胞体对角线垂直的面,在晶体学中称为(1,1,1)晶面,如图2所示。
,0),在立方晶胞中,与晶胞体对角线垂直的面,在晶体学中称为(1,1,1)晶面,如图2所示。

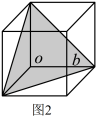
l mol晶体硅中所含有硅硅单键的数目是___________ ,图 1中原子坐标参数D为___________ ,图2立方晶胞中可以称为(1,1,1) 晶面的面共有___________ 个。
(1)基态硅原子核外电子云有
(2)硅原子2p能级的三个轨道之间具有不同的___________。
| A.能量 | B.形状 | C.空间伸展方向 | D.可容纳电子数 |
(3)某元素位于第四周期第Ⅷ族,其基态原子的未成对电子数与基态硅原子的未成对电子数相同,则其基态原子的价层电子排布式为
(4)由硅原子核形成的三种微粒,电子排布式分别为:①[Ne]3s23p2、②[Ne)3s23p1、③[Ne]3s13p14s1,有关这些微粒的叙述,正确的是___________。
| A.微粒半径:③>①>② | B.电子排布属于基态原子(或离子)的是:①② |
| C.电离一个电子所需最低能量:①>②>③ | D.得电子能力:①>② |
(5)Si(NH2)4分子的空间结构(以Si为中心)名称为
(6)晶体硅的结构跟金刚石相似,图1中原子坐标参数A为(0,0,0),B为(
 ,0,
,0, ),C(
),C( ,
, ,0),在立方晶胞中,与晶胞体对角线垂直的面,在晶体学中称为(1,1,1)晶面,如图2所示。
,0),在立方晶胞中,与晶胞体对角线垂直的面,在晶体学中称为(1,1,1)晶面,如图2所示。

l mol晶体硅中所含有硅硅单键的数目是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
【推荐2】2021年2月10日,我国自主研发的“天问一号”成功被火星捕获,开始绕火星飞行。“天问一号”的制作材料中包含了 、
、 、C、
、C、 、P等多种元素。回答下列问题:
、P等多种元素。回答下列问题:
(1)碳元素有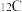 、
、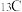 、
、 等核素,基态
等核素,基态 原子核外有
原子核外有___________ 种空间运动状态的电子,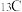 原子价电子轨道表达式为
原子价电子轨道表达式为___________ 。
(2)铁与氨气在高温时可发生置换反应,产物之一的晶胞结构如图所示,则该反应的化学方程式为:___________ ,反应中所涉及元素基态原子的第一电离能由大到小的顺序是___________ ; 具有较强的还原性,原因是
具有较强的还原性,原因是___________ 。

(3)与 同周期的所有元素的基态原子中,未成对电子数与
同周期的所有元素的基态原子中,未成对电子数与 相同的元素有
相同的元素有___________ (填元素符号)。
(4)碳元素的单质有多种形式,其中石墨的结构如下图,则石墨晶体中含有的六边形个数与 键数目之比为
键数目之比为___________ 。建立如下图的原子坐标系,原子A的分数坐标为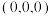 ,C的分数坐标为
,C的分数坐标为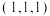 ,则B的分数坐标为
,则B的分数坐标为___________ 。

 、
、 、C、
、C、 、P等多种元素。回答下列问题:
、P等多种元素。回答下列问题:(1)碳元素有
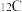 、
、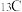 、
、 等核素,基态
等核素,基态 原子核外有
原子核外有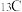 原子价电子轨道表达式为
原子价电子轨道表达式为(2)铁与氨气在高温时可发生置换反应,产物之一的晶胞结构如图所示,则该反应的化学方程式为:
 具有较强的还原性,原因是
具有较强的还原性,原因是
(3)与
 同周期的所有元素的基态原子中,未成对电子数与
同周期的所有元素的基态原子中,未成对电子数与 相同的元素有
相同的元素有(4)碳元素的单质有多种形式,其中石墨的结构如下图,则石墨晶体中含有的六边形个数与
 键数目之比为
键数目之比为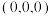 ,C的分数坐标为
,C的分数坐标为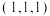 ,则B的分数坐标为
,则B的分数坐标为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】自然界中许多元素存在“共生”现象,如铜与锌、磷与砷等。回答下列问题:
(1)基态锌原子核外能量不同的电子有_______ 种;锌的第二电离能I2(Zn)小于铜的第二电离能I2(Cu),其原因是_______ 。
(2)已知次磷酸H3PO2为一元弱酸,其酸根的VSEPR构型为_______ 。
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+ 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数,对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,对于基态的磷原子,其价电子自旋磁量子数的代数和为_______ 。
(4)砷化镉的晶胞结构如图,As为面心立方最密堆积,Cd占据As围成的_______ 空隙,空隙占有率75%,故Cd为“具有两个真空的立方晶格”,如图①和②位是“真空”。建立如图的原子坐标系,①号位的坐标为( ,
, ,
, ),则③号位原子坐标参数为
),则③号位原子坐标参数为_______ 。设晶胞边长为apm,阿伏加德罗常数的值为NA,砷化镉的摩尔质量为Mg·mol-1,则该晶胞的密度为_______ g·cm-3(列出计算式即可)

(1)基态锌原子核外能量不同的电子有
(2)已知次磷酸H3PO2为一元弱酸,其酸根的VSEPR构型为
(3)原子中运动的电子有两种相反的自旋状态,若一种自旋状态用+
 表示,与之相反的用-
表示,与之相反的用- 表示,称为电子的自旋磁量子数,对于基态的磷原子,其价电子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,对于基态的磷原子,其价电子自旋磁量子数的代数和为(4)砷化镉的晶胞结构如图,As为面心立方最密堆积,Cd占据As围成的
 ,
, ,
, ),则③号位原子坐标参数为
),则③号位原子坐标参数为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】氮化铬常用于薄膜涂层,是一种良好的耐磨材料,同时在超级电容器领域有良好的应用前景。工业上以铬铁矿( )为原料,经过一系列反应,制备氮化铬和铬单质的工艺流程如图:
)为原料,经过一系列反应,制备氮化铬和铬单质的工艺流程如图:

(1)基态铬原子的价层电子轨道表示式为_______ 。
(2)制备 时,发生的主要反应为
时,发生的主要反应为
 。
。
①光气( )分子中碳原子的杂化方式为
)分子中碳原子的杂化方式为_______ ,光气分子的空间结构是_______ 。
② 的熔点(83℃)比
的熔点(83℃)比 的熔点(1100℃)低得多,这是由于
的熔点(1100℃)低得多,这是由于_______ 。
(3)氨解 制备氮化铬:先将
制备氮化铬:先将 装入石英舟,再将石英舟放入反应炉中,通入氨气,在高温下保温5小时,即得到结晶性能良好的纯立方相
装入石英舟,再将石英舟放入反应炉中,通入氨气,在高温下保温5小时,即得到结晶性能良好的纯立方相 粉末。氮化铬的熔点为1770℃,它的一种晶体的立方晶胞结构如图所示,则该晶胞中含有
粉末。氮化铬的熔点为1770℃,它的一种晶体的立方晶胞结构如图所示,则该晶胞中含有 的数目为
的数目为_______ ,若其密度为 ,设NA为阿伏加德罗常数的值,则
,设NA为阿伏加德罗常数的值,则 的晶胞边长a=
的晶胞边长a=_______ (列出计算式)nm。

 )为原料,经过一系列反应,制备氮化铬和铬单质的工艺流程如图:
)为原料,经过一系列反应,制备氮化铬和铬单质的工艺流程如图:
(1)基态铬原子的价层电子轨道表示式为
(2)制备
 时,发生的主要反应为
时,发生的主要反应为
 。
。①光气(
 )分子中碳原子的杂化方式为
)分子中碳原子的杂化方式为②
 的熔点(83℃)比
的熔点(83℃)比 的熔点(1100℃)低得多,这是由于
的熔点(1100℃)低得多,这是由于(3)氨解
 制备氮化铬:先将
制备氮化铬:先将 装入石英舟,再将石英舟放入反应炉中,通入氨气,在高温下保温5小时,即得到结晶性能良好的纯立方相
装入石英舟,再将石英舟放入反应炉中,通入氨气,在高温下保温5小时,即得到结晶性能良好的纯立方相 粉末。氮化铬的熔点为1770℃,它的一种晶体的立方晶胞结构如图所示,则该晶胞中含有
粉末。氮化铬的熔点为1770℃,它的一种晶体的立方晶胞结构如图所示,则该晶胞中含有 的数目为
的数目为 ,设NA为阿伏加德罗常数的值,则
,设NA为阿伏加德罗常数的值,则 的晶胞边长a=
的晶胞边长a=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】铁触媒是重要的催化剂,CO易与铁触媒作用导致其失去催化活性:Fe+5CO=Fe(CO)5;除去CO的化学反应方程式为[Cu(NH3)2]OOCCH3+CO+NH3=[Cu(NH3)3(CO)]OOCCH3。请回答下列问题:
(1)C、N、O的第一电离能由大到小的顺序为_______ ,基态铁原子的价电子排布式为_______ 。
(2)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是_______ ,Fe(CO)5在空气中燃烧后剩余固体呈红棕色,其化学方程式为_______ 。
(3)配合物[Cu(NH3)2]OOCCH3中碳原子的杂化类型有_______ 。
(4)单质铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为_______ ,面心立方堆积(铁原子在面对角线方向相切)与体心立方堆积(铁原子在体对角线方向相切)的两种铁晶体的密度之比为_______ (写出已化简的比例式即可)。
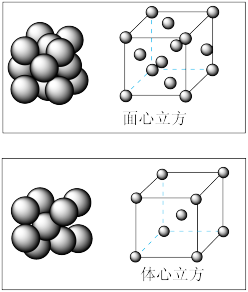
(1)C、N、O的第一电离能由大到小的顺序为
(2)Fe(CO)5又名羰基铁,常温下为黄色油状液体,则Fe(CO)5的晶体类型是
(3)配合物[Cu(NH3)2]OOCCH3中碳原子的杂化类型有
(4)单质铁的晶体在不同温度下有两种堆积方式,晶胞分别如图所示,面心立方晶胞和体心立方晶胞中实际含有的铁原子个数之比为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】2019年诺贝尔化学奖由来自美、英、日的三人分获,以表彰他们在锂离子电池研究方面做出的贡献,他们最早发明用LiCoO2作离子电池的正极,用聚乙炔作负极。回答下列问题:
(1)基态Co原子价电子排布图为____ 。第四电离能Ⅰ4(Co)比Ⅰ4(Fe)小,是因为____ 。
(2)LiCl的熔点(605℃)比LiF的熔点(848℃)低,其原因是___ 。
(3)乙炔(C2H2)分子中σ键与π键的数目之比为____ 。
(4)锂离子电池的导电盐有LiBF4等,碳酸亚乙酯( )是一种锂离子电池电解液的添加剂。
)是一种锂离子电池电解液的添加剂。
①LiBF4中阴离子的空间构型是___ 。
②碳酸亚乙酯分子中碳原子的杂化方式有___ 。
(5)Li2S是目前正在开发的锂离子电池的新型固体电解质,其晶胞结构如图所示,已知晶胞参数acm。

①S2-的配位数为____ 。
②设NA为阿伏加德罗常数的值,Li2S的晶胞密度为___ g·cm-3(列出计算式)。
(1)基态Co原子价电子排布图为
(2)LiCl的熔点(605℃)比LiF的熔点(848℃)低,其原因是
(3)乙炔(C2H2)分子中σ键与π键的数目之比为
(4)锂离子电池的导电盐有LiBF4等,碳酸亚乙酯(
 )是一种锂离子电池电解液的添加剂。
)是一种锂离子电池电解液的添加剂。①LiBF4中阴离子的空间构型是
②碳酸亚乙酯分子中碳原子的杂化方式有
(5)Li2S是目前正在开发的锂离子电池的新型固体电解质,其晶胞结构如图所示,已知晶胞参数acm。

①S2-的配位数为
②设NA为阿伏加德罗常数的值,Li2S的晶胞密度为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐1】早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成,回答下列问题:
(1)①铜元素位于周期表中_______ 区。Cu2+离子的价层轨道表示式为_______ 。
②锰、铁、钴三种元素的逐级电离能如下表:
铁元素的第三电离能明显低于锰元素和钴元素,其原因是_______ 。
③实验室可用赤血盐K3[Fe(CN)6]检验Fe2+离子,在赤血盐中铁元素的化合价为_______ ,中心离子的配位数为_______ 。
(2)利用反应:X+C2H2+NH3→Cu2C2+NH4Cl(未配平)可检验乙炔。
①化合物X晶胞结构如图,据此可知X的化学式为_______ 。

②乙炔分子中σ键与π键数目之比为_______ ,碳原子的杂化方式为_______ ;NH 空间构型为
空间构型为_______ (用文字描述)。
(3)①下列三种化合物a.AlCl3 b.NaCl c.Al2O3沸点由高到低依次是_______ (填编号),其原因是_______ 。
②Al单质中原子采取面心立方最密堆积,其晶胞边长为0.405nm,列式表示Al单质的密度_______ g/cm3(不必计算出结果)。
(1)①铜元素位于周期表中
②锰、铁、钴三种元素的逐级电离能如下表:
电离能/KJ/mol | I1 | I2 | I 3 | I4 |
Mn | 717.3 | 1509.0 | 3248 | 4940 |
Fe | 762.5 | 1561.9 | 2957 | 5290 |
Co | 760.4 | 1648 | 3232 | 4950 |
铁元素的第三电离能明显低于锰元素和钴元素,其原因是
③实验室可用赤血盐K3[Fe(CN)6]检验Fe2+离子,在赤血盐中铁元素的化合价为
(2)利用反应:X+C2H2+NH3→Cu2C2+NH4Cl(未配平)可检验乙炔。
①化合物X晶胞结构如图,据此可知X的化学式为

②乙炔分子中σ键与π键数目之比为
 空间构型为
空间构型为(3)①下列三种化合物a.AlCl3 b.NaCl c.Al2O3沸点由高到低依次是
②Al单质中原子采取面心立方最密堆积,其晶胞边长为0.405nm,列式表示Al单质的密度
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】金属镍及其化合物在合金材料以及催化剂等方面应用广泛。回答下列问题:
(1)基态Ni原子的核外电子排布式为____________________ ,有__________ 个未成对电子。
(2)已知镍与铜的第二电离能分别为INi=1753 kJ·mol-1,ICu=1958 kJ·mol-1,ICu>INi的原因是______________________________________________________________________ 。
(3)Ni2+常与丁二酮肟(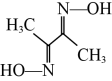 )形成图A所示的配合物,图B是硫代氧的结果:
)形成图A所示的配合物,图B是硫代氧的结果:
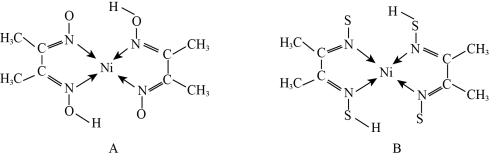
①熔点大小:A_________ (填“>”或“<”)B,其原因是____________________________ 。
②Ni2+与丁二酮肟之间形成的化学键称为__________ 。
③A中碳原子的杂化轨道类型是__________ 。
(4)硝酸镍[Ni(NO3)2]常用于有机化学合成中,阴离子的空间构型为__________ 。
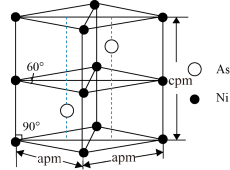
(5)某砷镍合金的晶胞结构如图所示。阿伏加 德罗常数的值为NA,该晶体的密度ρ=_________ g·cm-3(列出计算式即可)。
(1)基态Ni原子的核外电子排布式为
(2)已知镍与铜的第二电离能分别为INi=1753 kJ·mol-1,ICu=1958 kJ·mol-1,ICu>INi的原因是
(3)Ni2+常与丁二酮肟(
 )形成图A所示的配合物,图B是硫代氧的结果:
)形成图A所示的配合物,图B是硫代氧的结果:
①熔点大小:A
②Ni2+与丁二酮肟之间形成的化学键称为
③A中碳原子的杂化轨道类型是
(4)硝酸镍[Ni(NO3)2]常用于有机化学合成中,阴离子的空间构型为
(5)某砷镍合金的晶胞结构如图所示。阿伏加 德罗常数的值为NA,该晶体的密度ρ=

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】前四周期元素X、Y、Z、M、E的原子序数依次增大,其中元素X的基态原子有3个不同的能级,且3个能级中的电子数均相等。元素Y的核外p电子总数比s电子总数少1。元素Z的核外s电子总数与p电子总数相等,且与Y元素在同一周期。元素M的主族序数与周期数的差为4。元素E位于周期表的第10列。
(1)元素X、Y、Z的第一电离能由小到大的顺序为_____________ (用元素符号表示)。
(2)常温下,配合物Fe(XZ)5为黄色液体,易溶于非极性溶剂,熔点为215K,沸点为376K。据此推断Fe(XZ)5 晶体属于_____________ 晶体。配合物Fe(XZ)5的中心原子的基态核外电子排布式为_____________ 。
(3)XZM2分子中所有原子最外电子层均形成8电子稳定结构,XZM2分子中σ键和π键的个数比为_____________ ,中心原子的杂化方式为_____________ 。

(4)E和La的合金是目前使用广泛的储氢材料,在我国已实现了产业化。该合金的晶胞结构如图所示,则该晶体的化学式为_____________ (用元素符号表示)。
(1)元素X、Y、Z的第一电离能由小到大的顺序为
(2)常温下,配合物Fe(XZ)5为黄色液体,易溶于非极性溶剂,熔点为215K,沸点为376K。据此推断Fe(XZ)5 晶体属于
(3)XZM2分子中所有原子最外电子层均形成8电子稳定结构,XZM2分子中σ键和π键的个数比为

(4)E和La的合金是目前使用广泛的储氢材料,在我国已实现了产业化。该合金的晶胞结构如图所示,则该晶体的化学式为
您最近一年使用:0次
【推荐1】氢能被视为21世纪最具发展潜力的清洁能源。
(1)水是制取H2的常见原料,下列有关水的说法正确的是______ .
a.水分子是一种极性分子,水分子空间结构呈直线型
b.1个H2O分子中有2个由s轨道与sp3杂化轨道形成的σ键
c.水分子间通过H﹣O键形成冰晶体
d.冰晶胞中水分子的空间排列方式与干冰晶胞类似
(2)氢气的安全贮存和运输是氢能应用的关键。
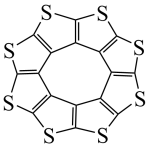
①最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(如图1所示),每个平面上下两侧最多可存10个H2分子.分子中C原子的杂化轨道类型为______ ,C16S8中σ键与π键之比为______ ,C16S8与H2微粒间的作用力是______ 。
②氨硼烷化合物(NH3BH3)是最近密切关注的一种新型化学氢化物储氢材料.请画出含有配位键(用“→”表示)的氨硼烷的结构式_____ ;与氨硼烷互为等电子体的有机小分子是___ (写结构简式)。
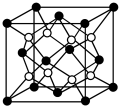
③某种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中.若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(晶胞结构如图)的结构相似,该晶体储氢后Cu:Au:H为______ 。
④MgH2是金属氢化物储氢材料,其晶胞如图所示,已知该晶体的密度ag·cm-3,则晶胞的体积为______________ cm3(用含a、NA的代数式表示,NA表示阿伏加 德罗常数)。

(1)水是制取H2的常见原料,下列有关水的说法正确的是
a.水分子是一种极性分子,水分子空间结构呈直线型
b.1个H2O分子中有2个由s轨道与sp3杂化轨道形成的σ键
c.水分子间通过H﹣O键形成冰晶体
d.冰晶胞中水分子的空间排列方式与干冰晶胞类似
(2)氢气的安全贮存和运输是氢能应用的关键。
①最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(如图1所示),每个平面上下两侧最多可存10个H2分子.分子中C原子的杂化轨道类型为

②氨硼烷化合物(NH3BH3)是最近密切关注的一种新型化学氢化物储氢材料.请画出含有配位键(用“→”表示)的氨硼烷的结构式
③某种具有储氢功能的铜合金晶体具有立方最密堆积的结构,晶胞中Cu原子处于面心,Au原子处于顶点位置,氢原子可进入到由Cu原子与Au原子构成的四面体空隙中.若将Cu原子与Au原子等同看待,该晶体储氢后的晶胞结构与CaF2(晶胞结构如图)的结构相似,该晶体储氢后Cu:Au:H为

④MgH2是金属氢化物储氢材料,其晶胞如图所示,已知该晶体的密度ag·cm-3,则晶胞的体积为

您最近一年使用:0次
【推荐2】已知A、B、D、E、G、X、Y、Z八种元素的原子序数依次增大。其中,A原子核外电子只有1种运动状态;基态B、E原子的2p轨道均含2个未成对电子;G是周期表中电负性最大的元素;Y和G同主族,X和Y同周期,且X离子是同周期元素简单离子中半径最小的;Z是八种元素中唯一的第四周期元素位于ds区,且基态原子核外只有1个未成对电子其余均为成对电子。推断出元素符号及相应化学式,并回答下列问题:
(1)基态Z原子的简化核外电子排布式:_______ ,基态E原子价层电子轨道表达式:_______ ,基态X原子的核外电子排布共有_______ 个能级。
(2)键能:G-G_______ Y-Y(填“>或<”,后同);B和D的第三电离能:B_______ D。
(3)A2E分子的VSEPR理想模型为_______ ;已知DA3溶于A2E溶液呈碱性,试在方框内画出DA3与A2E的分子间形成的氢键_______ 。

(4)B2A2分子中σ键和π键的比例_______ ;B2A2、E2在NaOH溶液中可构建燃料电池,试写出该燃料电池负极的电极反应式:_______ 。
(1)基态Z原子的简化核外电子排布式:
(2)键能:G-G
(3)A2E分子的VSEPR理想模型为

(4)B2A2分子中σ键和π键的比例
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐3】元素和物质的性质与其结构有着密切的联系。
(1)铁的一种配合物为[FeM2Cl2]ClO4,其中配体M的结构如图1所示。该配合物中心原子的化合价为_______ ,配体M与中心原子形成配位键的原子是_______ 。

(2)Li2O是离子晶体,其晶格能可通过如图2的BornHaber循环计算得到。

可知,Li原子的第一电离能为_______ kJ·mol-1,Li2O晶格能为_______ kJ·mol-1。
(3)铝镁合金是优质储钠材料,原子位于面心和顶点,其晶胞如图3所示,则1个铝原子周围距离最近且相等的镁原子的数目为_______ 个。

(4)在硼酸盐中,阴离子有链状、环状等多种结构形式。如图4是一种链状结构的多硼酸根,则多硼酸根离子符号为_______ 。

(5)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危害人们健康。苏丹红常见有Ⅰ、Ⅱ、Ⅲ、Ⅳ4种类型,苏丹红Ⅰ的分子结构如图5所示。苏丹红Ⅰ在水中的溶解度很小,微溶于乙醇,有人把羟基取代在对位形成如图5所示的结构。

则修饰后的分子在水中的溶解度会_______ (填“增大”或“减小”),原因是_______ 。
(6)已知Zn2+、Au+均能与CN-形成配离子,Zn2+与CN-形成的配离子为正四面体形,Au+与CN-形成的配离子为直线形,工业上常用Au+和CN-形成的配离子与Zn单质反应来提取Au单质,写出该反应的离子方程式:_______ 。
(1)铁的一种配合物为[FeM2Cl2]ClO4,其中配体M的结构如图1所示。该配合物中心原子的化合价为

(2)Li2O是离子晶体,其晶格能可通过如图2的BornHaber循环计算得到。

可知,Li原子的第一电离能为
(3)铝镁合金是优质储钠材料,原子位于面心和顶点,其晶胞如图3所示,则1个铝原子周围距离最近且相等的镁原子的数目为

(4)在硼酸盐中,阴离子有链状、环状等多种结构形式。如图4是一种链状结构的多硼酸根,则多硼酸根离子符号为

(5)苏丹红颜色鲜艳、价格低廉,常被一些企业非法作为食品和化妆品等的染色剂,严重危害人们健康。苏丹红常见有Ⅰ、Ⅱ、Ⅲ、Ⅳ4种类型,苏丹红Ⅰ的分子结构如图5所示。苏丹红Ⅰ在水中的溶解度很小,微溶于乙醇,有人把羟基取代在对位形成如图5所示的结构。

则修饰后的分子在水中的溶解度会
(6)已知Zn2+、Au+均能与CN-形成配离子,Zn2+与CN-形成的配离子为正四面体形,Au+与CN-形成的配离子为直线形,工业上常用Au+和CN-形成的配离子与Zn单质反应来提取Au单质,写出该反应的离子方程式:
您最近一年使用:0次



