锂离子电池应用十分广泛,从废旧钻酸锂(LiCoO2)锂离子电池中回收铝、铁、钴、锂等元素成了重要的研究课题。现欲利用图19所示的工艺流程回收废旧电池中的某些金属资源(部分条件未给出)。回答下列问题:

已知:①滤液1中阳离子有H+、Co2+、Fe2+、Al3+、Li+等;
②两种物质不同温度下的溶解度如下表所示:
(1)钴酸锂( LiCoO2)钴元素的化合价为___________ 。
(2)浸泡时加入Na2SO3的主要目的是______________________ ;可用盐酸代替H2SO4和Na2SO3的混合液,但缺点是______________________ 。
(3)滤液1中加入NaClO3的主要目的是______________________ (用离子方程式表示)。
(4)为了使Fe3+、Al3+沉淀完全(通常认为金属离子浓度小于或等于10-5mo·L-1时已沉淀完全)加入氨水调节pH的最小值是___________ 。【已知:Ksp[Fe(OH)3]=1.0×10-39,Ksp[Al(OH)3]=2.7×10-34,1g3=0.52】
(5)滤液3中加入饱和Na2CO3溶液,过滤后,需要用“热水洗涤”的原因是___________ 。
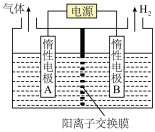
(6)利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,利用如图所示的装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液为___________ (填化学式)溶液;阳极电极反应式为______________________ ;电解过程中Li+向___________ (填“A”或“B”)电极迁移。

已知:①滤液1中阳离子有H+、Co2+、Fe2+、Al3+、Li+等;
②两种物质不同温度下的溶解度如下表所示:
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
(2)浸泡时加入Na2SO3的主要目的是
(3)滤液1中加入NaClO3的主要目的是
(4)为了使Fe3+、Al3+沉淀完全(通常认为金属离子浓度小于或等于10-5mo·L-1时已沉淀完全)加入氨水调节pH的最小值是
(5)滤液3中加入饱和Na2CO3溶液,过滤后,需要用“热水洗涤”的原因是
(6)利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,利用如图所示的装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液为

更新时间:2019-03-01 09:41:58
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】近年来,人们发现 不仅在颜料、防腐工业等方面具有广泛的用途,而且
不仅在颜料、防腐工业等方面具有广泛的用途,而且 的大单晶体是一种很重要的电光调制晶体,也是有机合成中性能优良的催化剂。研究发现一种利用低品位铜矿(含
的大单晶体是一种很重要的电光调制晶体,也是有机合成中性能优良的催化剂。研究发现一种利用低品位铜矿(含 、
、 和
和 等)为原料制取
等)为原料制取 的工艺流程如下:
的工艺流程如下:
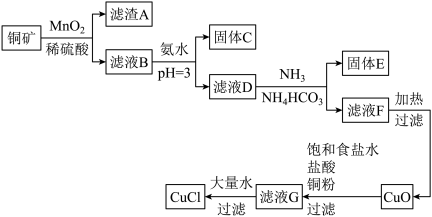
已知:i.水溶液中不存在碳酸铜,碳酸铜遇水立即水解为碱式碳酸铜和氢氧化铜。
ii.室温时, 的溶度积常数
的溶度积常数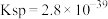 。
。
(1)铜矿中未被 氧化的物质有
氧化的物质有___________ 。
(2)滤液D中铁离子的浓度约为___________ 。
(3)向滤液D中先通氨气的目的是___________。
(4)固体E主要是 ,生成
,生成 的离子方程式是
的离子方程式是___________ 。
(5)滤液F加热生成 、
、 和
和 ,反应的化学方程式是
,反应的化学方程式是___________ 。
(6)若要制取99.5g ,理论上至少需要质量分数为25%的
,理论上至少需要质量分数为25%的 的铜矿粉的质量为
的铜矿粉的质量为___________ g。
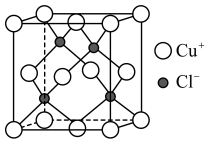
(7)查阅资料: 立方晶胞结构如下图所示,其晶胞参数为apm,
立方晶胞结构如下图所示,其晶胞参数为apm, 以配位键与
以配位键与 相结合,其中
相结合,其中 的配位数为
的配位数为___________ , 晶体密度为
晶体密度为___________  。
。
 不仅在颜料、防腐工业等方面具有广泛的用途,而且
不仅在颜料、防腐工业等方面具有广泛的用途,而且 的大单晶体是一种很重要的电光调制晶体,也是有机合成中性能优良的催化剂。研究发现一种利用低品位铜矿(含
的大单晶体是一种很重要的电光调制晶体,也是有机合成中性能优良的催化剂。研究发现一种利用低品位铜矿(含 、
、 和
和 等)为原料制取
等)为原料制取 的工艺流程如下:
的工艺流程如下:
已知:i.水溶液中不存在碳酸铜,碳酸铜遇水立即水解为碱式碳酸铜和氢氧化铜。
ii.室温时,
 的溶度积常数
的溶度积常数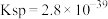 。
。(1)铜矿中未被
 氧化的物质有
氧化的物质有(2)滤液D中铁离子的浓度约为
(3)向滤液D中先通氨气的目的是___________。
A.中和溶液中的 | B.调节溶液 值,生成 值,生成 沉淀 沉淀 |
C.有利于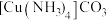 的生成 的生成 | D.增加 的溶解度 的溶解度 |
(4)固体E主要是
 ,生成
,生成 的离子方程式是
的离子方程式是(5)滤液F加热生成
 、
、 和
和 ,反应的化学方程式是
,反应的化学方程式是(6)若要制取99.5g
 ,理论上至少需要质量分数为25%的
,理论上至少需要质量分数为25%的 的铜矿粉的质量为
的铜矿粉的质量为(7)查阅资料:
 立方晶胞结构如下图所示,其晶胞参数为apm,
立方晶胞结构如下图所示,其晶胞参数为apm, 以配位键与
以配位键与 相结合,其中
相结合,其中 的配位数为
的配位数为 晶体密度为
晶体密度为 。
。
您最近一年使用:0次
【推荐2】一种以铬铁矿【主要含有Fe(CrO2)2,同时含有Al2O3、SiO2】为主要原料制备K2Cr2O7的工艺流程如图所示:

(1)基态铬原子的单电子数为________ ,铬铁矿中元素第一电离能Al________ Si(填“大于”、“小于”或“等于”)。
(2)焙烧时Fe(CrO2)2转化为Na2CrO4,同时杂质A12O3、SiO2转化为可溶性钠盐,焙烧时Fe(CrO2)2发生反应的的化学方程式为________ 。
(3)滤渣a中除A1(OH)3外还有________ 。(填化学式)
(4)已知,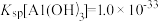 ,酸化时发生
,酸化时发生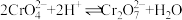 ,
,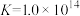 ,测得滤液2中pH=5,含铬微粒只有
,测得滤液2中pH=5,含铬微粒只有 和
和 ,其中c(
,其中c( )=1.0mol/L,则滤液2中c(Al3+)=
)=1.0mol/L,则滤液2中c(Al3+)=________ mol/L, 的转化率为
的转化率为_______ 。(结果保留3位有效数字)
(5)已知相同温度下Na2Cr2O7的溶解度显著高于K2Cr2O7,可利用两者溶解度的不同实现转化,操作X的具体过程为:加热浓缩、_______ 、冷却结晶、过滤、洗涤干燥,得到较纯净的K2Cr2O7晶体。
(6)将15kg铬铁矿按上述流程制得K2Cr2O7产品,假设各步损失铬元素总计9.0%,干燥称量得14kg该产品,滴定分析产品中K2Cr2O7的纯度为99.2%,则铬铁矿中铬元素的质量分数为_______ 。

(1)基态铬原子的单电子数为
(2)焙烧时Fe(CrO2)2转化为Na2CrO4,同时杂质A12O3、SiO2转化为可溶性钠盐,焙烧时Fe(CrO2)2发生反应的的化学方程式为
(3)滤渣a中除A1(OH)3外还有
(4)已知,
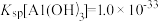 ,酸化时发生
,酸化时发生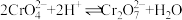 ,
,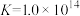 ,测得滤液2中pH=5,含铬微粒只有
,测得滤液2中pH=5,含铬微粒只有 和
和 ,其中c(
,其中c( )=1.0mol/L,则滤液2中c(Al3+)=
)=1.0mol/L,则滤液2中c(Al3+)= 的转化率为
的转化率为(5)已知相同温度下Na2Cr2O7的溶解度显著高于K2Cr2O7,可利用两者溶解度的不同实现转化,操作X的具体过程为:加热浓缩、
(6)将15kg铬铁矿按上述流程制得K2Cr2O7产品,假设各步损失铬元素总计9.0%,干燥称量得14kg该产品,滴定分析产品中K2Cr2O7的纯度为99.2%,则铬铁矿中铬元素的质量分数为
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐3】硫酸锰是一种重要的化工中间体。一种以高硫锰矿(主要成分为含锰化合物及)与氧化锰矿(主要成分为等锰的氧化物)为原料制备硫酸锰的工艺流程如下:

已知:①“混合焙烧”后烧渣含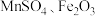 及少量
及少量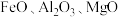 。
。
②金属离子在水溶液中沉淀的 范围如下表所示(
范围如下表所示( ):
):
③离子浓度 时,离子沉淀完全。
时,离子沉淀完全。
(1)“混合焙烧”的主要目的是_______ 。
(2)若试剂a为 ,则氧化步骤发生反应的离子方程式为
,则氧化步骤发生反应的离子方程式为_______ ,若省略“氧化”步骤,造成的影响是_______ 。
(3)“中和除杂”时,应控制溶液的 范围是
范围是_______ 。
(4)“氟化除杂”后,溶液中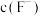 浓度为
浓度为 。则溶液中
。则溶液中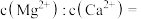
_______ [已知: ;
;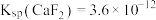 ]。
]。
(5)“碳化结晶”时发生反应的离子方程式为_______ 。

已知:①“混合焙烧”后烧渣含
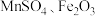 及少量
及少量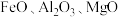 。
。②金属离子在水溶液中沉淀的
 范围如下表所示(
范围如下表所示( ):
):| 物质 |  |  |  |  |
开始沉淀的 | 1.9 | 7.6 | 7.3 | 3.0 |
完全沉淀的 | 3.2 | 9.6 | 9.3 | 5.2 |
③离子浓度
 时,离子沉淀完全。
时,离子沉淀完全。(1)“混合焙烧”的主要目的是
(2)若试剂a为
 ,则氧化步骤发生反应的离子方程式为
,则氧化步骤发生反应的离子方程式为(3)“中和除杂”时,应控制溶液的
 范围是
范围是(4)“氟化除杂”后,溶液中
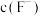 浓度为
浓度为 。则溶液中
。则溶液中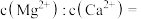
 ;
;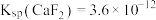 ]。
]。(5)“碳化结晶”时发生反应的离子方程式为
您最近一年使用:0次
【推荐1】甲醇是一种重要的化工原料,在生产生活中应用广泛,可用多种原料合成,回答下列问题:
(1)已知甲烷、甲醇、氢气的标准燃烧热分别为-890.3 、-726.5
、-726.5 、-285.8
、-285.8 ,则反应
,则反应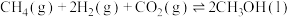 的△H=
的△H=_______  。
。
(2) 在NiO支撑的
在NiO支撑的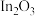 (110)D催化剂表面合成甲醇的反应历程如图,TS表示过渡态。
(110)D催化剂表面合成甲醇的反应历程如图,TS表示过渡态。

①基态Ni原子中占据最高能层的电子所在轨道的电子云轮廓图为_______ 形。
②该过程中决速步骤的活化能为_______ eV。
(3)一定条件下,CO与 经催化也可以合成甲醇,反应原理为
经催化也可以合成甲醇,反应原理为 。
。
①该反应分为两步,通过对反应历程进行研究发现催化剂表面出现HCHO,其物质的量先增大后减小,请推测出现该现象的原因:_______ 。
②T℃下,向一体积为2L的恒温恒容密闭容器中充入1mol CO、3mol 发生该反应,达到平衡时,CO与
发生该反应,达到平衡时,CO与 的物质的量之比为2:3,气体总压为1.4MPa,则
的物质的量之比为2:3,气体总压为1.4MPa,则 的平衡转化率为
的平衡转化率为_______ ,该反应的压强平衡常数 为
为_______  (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。
(4)以酸性甲醇燃料电池作为外接电源电解As制备 的装置如图所示,酸性甲醇燃料电池的负极应连接
的装置如图所示,酸性甲醇燃料电池的负极应连接_______ (填“X”或“Y”)极,写出X电极生成 的电极反应式:
的电极反应式:_______ 。

(1)已知甲烷、甲醇、氢气的标准燃烧热分别为-890.3
 、-726.5
、-726.5 、-285.8
、-285.8 ,则反应
,则反应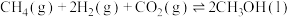 的△H=
的△H= 。
。(2)
 在NiO支撑的
在NiO支撑的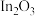 (110)D催化剂表面合成甲醇的反应历程如图,TS表示过渡态。
(110)D催化剂表面合成甲醇的反应历程如图,TS表示过渡态。
①基态Ni原子中占据最高能层的电子所在轨道的电子云轮廓图为
②该过程中决速步骤的活化能为
(3)一定条件下,CO与
 经催化也可以合成甲醇,反应原理为
经催化也可以合成甲醇,反应原理为 。
。①该反应分为两步,通过对反应历程进行研究发现催化剂表面出现HCHO,其物质的量先增大后减小,请推测出现该现象的原因:
②T℃下,向一体积为2L的恒温恒容密闭容器中充入1mol CO、3mol
 发生该反应,达到平衡时,CO与
发生该反应,达到平衡时,CO与 的物质的量之比为2:3,气体总压为1.4MPa,则
的物质的量之比为2:3,气体总压为1.4MPa,则 的平衡转化率为
的平衡转化率为 为
为 (以分压表示,分压=总压×物质的量分数)。
(以分压表示,分压=总压×物质的量分数)。(4)以酸性甲醇燃料电池作为外接电源电解As制备
 的装置如图所示,酸性甲醇燃料电池的负极应连接
的装置如图所示,酸性甲醇燃料电池的负极应连接 的电极反应式:
的电极反应式:
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
解题方法
【推荐2】乙烯是重要的有机合成原料。由乙烷制备乙烯主要涉及如下反应。
反应i(主反应):2C2H6(g)+O2(g) 2C2H4(g)+2H2O(g) △H1=-230kJ•mol-1
2C2H4(g)+2H2O(g) △H1=-230kJ•mol-1
反应ii(副反应):2C2H6(g)+5O2(g) 4CO(g)+6H2O(g) △H2=-2456kJ•mol-1
4CO(g)+6H2O(g) △H2=-2456kJ•mol-1
回答下列问题:
(1)反应C2H4(g)+2O2(g) 2CO(g)+2H2O(g)的△H3=
2CO(g)+2H2O(g)的△H3=______ 。
(2)利用电解池原理,在活性固体氧化物(可产生活性O2-)电解槽中电解乙烷可以制取乙烯,写出生成乙烯的电极反应式:______ 。活性Fe2O3是常用的一种固体氧化物,检验活性Fe2O3中的铁元素可以选用的试剂为______ (填字母)。
A.稀硫酸 B.KMnO4溶液 C.KSCN溶液 D.氯水
(3)一定条件下,向密闭容器中充入物质的量之比为2∶1的C2H6和O2发生反应i和ii。恒压条件下(总压强为pkPa)反应达到平衡时,C2H6的转化率为20%,CO的选择性为40%[CO的选择性= ×100%],则平衡时O2的转化率为
×100%],则平衡时O2的转化率为______ ,反应i的平衡常数Kp=______ (Kp为用分压表示的平衡常数,分压=总压×物质的量分数,列出计算式即可)。
反应i(主反应):2C2H6(g)+O2(g)
 2C2H4(g)+2H2O(g) △H1=-230kJ•mol-1
2C2H4(g)+2H2O(g) △H1=-230kJ•mol-1反应ii(副反应):2C2H6(g)+5O2(g)
 4CO(g)+6H2O(g) △H2=-2456kJ•mol-1
4CO(g)+6H2O(g) △H2=-2456kJ•mol-1回答下列问题:
(1)反应C2H4(g)+2O2(g)
 2CO(g)+2H2O(g)的△H3=
2CO(g)+2H2O(g)的△H3=(2)利用电解池原理,在活性固体氧化物(可产生活性O2-)电解槽中电解乙烷可以制取乙烯,写出生成乙烯的电极反应式:
A.稀硫酸 B.KMnO4溶液 C.KSCN溶液 D.氯水
(3)一定条件下,向密闭容器中充入物质的量之比为2∶1的C2H6和O2发生反应i和ii。恒压条件下(总压强为pkPa)反应达到平衡时,C2H6的转化率为20%,CO的选择性为40%[CO的选择性=
 ×100%],则平衡时O2的转化率为
×100%],则平衡时O2的转化率为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
【推荐3】一种混合动力车,可以分别用电动机、内燃机或者二者结合推动车轮。汽车上坡或加速时,电动机提供推动力,降低汽油的消耗;在刹车和下坡时内燃机提供推动力,使电动机处于充电状态。目前内燃机以汽油为燃料,电动机一般使用镍氢电池(KOH作电解液)。
试分析回答下列问题:
(1)已知汽车在刹车和下坡时,镍氢电池两电极反应分别为:
甲电极:M+H2O+e-→MH+OH(M为储氢合金,MH为吸附了氢原子的储氢合金)
乙电极:Ni(OH)2+OH--e—→NiOOH+H2O
则在这一过程中甲、乙两电极的名称分别是:甲:______ ;乙:_____ 。
(2)当汽车上坡或加速时,镍氢电池两电极反应分别为:
甲电极:_______ ;乙电极:_______ ;
电极周围溶液的pH变化是(选填“增大”或“不变”或“减小",下同)甲_____ ;乙___________ 。
(3)内燃机工作时因为部分汽油不完全燃烧会产生污染大气的CO,已知在常温常压下:
C8H18(1)+ O2(g)=8CO2(g)+9 H2O(g);△H=-5121.9kJ/mol
O2(g)=8CO2(g)+9 H2O(g);△H=-5121.9kJ/mol
2CO(g)+O2(g)=2CO2(g);△H=-566.0kJ/mol
H2 O(g)=H2O(1);△H=-44.0kJ/mol
写出汽油不完全燃烧生成一氧化碳和液态水的热化学方程式:________ 。
(4)为降低汽车尾气中的一氧化碳的浓度,可采取在汽车的排气管上增加一个补燃器,通过下列反应来实现转化:2 CO(g)+O2(g) 2CO2(g)
2CO2(g)
已知在温度为T的条件下,当补燃器中化学反应速率 (正)=v(逆)时,各物质浓度存在下列恒定关系:
(正)=v(逆)时,各物质浓度存在下列恒定关系:
在温度为T的条件下,若某汽车排入补燃器的CO、CO2的浓度分别为1.0×10-5mol·L-1和1.01×10-4mol·L-1,要在该温度下使最终尾气中CO的浓度降为1.0×10-6mol·L-1,则补燃器中应不断补充O2,并使O2浓度保持在_____ mol·L-1。
试分析回答下列问题:
(1)已知汽车在刹车和下坡时,镍氢电池两电极反应分别为:
甲电极:M+H2O+e-→MH+OH(M为储氢合金,MH为吸附了氢原子的储氢合金)
乙电极:Ni(OH)2+OH--e—→NiOOH+H2O
则在这一过程中甲、乙两电极的名称分别是:甲:
(2)当汽车上坡或加速时,镍氢电池两电极反应分别为:
甲电极:
电极周围溶液的pH变化是(选填“增大”或“不变”或“减小",下同)甲
(3)内燃机工作时因为部分汽油不完全燃烧会产生污染大气的CO,已知在常温常压下:
C8H18(1)+
 O2(g)=8CO2(g)+9 H2O(g);△H=-5121.9kJ/mol
O2(g)=8CO2(g)+9 H2O(g);△H=-5121.9kJ/mol2CO(g)+O2(g)=2CO2(g);△H=-566.0kJ/mol
H2 O(g)=H2O(1);△H=-44.0kJ/mol
写出汽油不完全燃烧生成一氧化碳和液态水的热化学方程式:
(4)为降低汽车尾气中的一氧化碳的浓度,可采取在汽车的排气管上增加一个补燃器,通过下列反应来实现转化:2 CO(g)+O2(g)
 2CO2(g)
2CO2(g)已知在温度为T的条件下,当补燃器中化学反应速率
 (正)=v(逆)时,各物质浓度存在下列恒定关系:
(正)=v(逆)时,各物质浓度存在下列恒定关系:
在温度为T的条件下,若某汽车排入补燃器的CO、CO2的浓度分别为1.0×10-5mol·L-1和1.01×10-4mol·L-1,要在该温度下使最终尾气中CO的浓度降为1.0×10-6mol·L-1,则补燃器中应不断补充O2,并使O2浓度保持在
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】硫酸亚铁铵 是一种重要的化学试剂,某兴趣小组在课本合成方案的基础上进行了改进,流程如下:
是一种重要的化学试剂,某兴趣小组在课本合成方案的基础上进行了改进,流程如下:
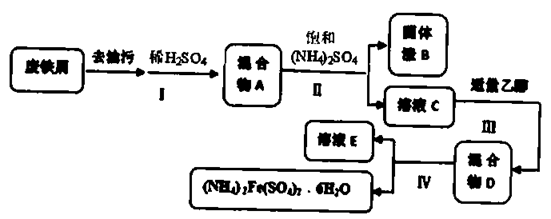
(1)下列说法正确的是_________ 。
A.废铁屑需用 溶液除去表面的油污,通常采用抽滤除去碱液
溶液除去表面的油污,通常采用抽滤除去碱液
B.实验中使用的蒸馏水均需煮沸除氧
C.在加入硫酸铵前,应该把硫酸亚铁溶液的pH值控制在强酸性范围内
D.鉴定所得晶体中含有 ,可以取少量样品于试管中,加水溶解,加入NaOH溶液,露置于空气中,观察现象
,可以取少量样品于试管中,加水溶解,加入NaOH溶液,露置于空气中,观察现象

(2)废铁屑含有碳、硫、硅等杂质,为较快地制得较纯净的 ,该兴趣小组设计图甲装置来制备产品,并选用了以下试剂中的一部分来完成实验。
,该兴趣小组设计图甲装置来制备产品,并选用了以下试剂中的一部分来完成实验。
a. 溶液 b.碳粉 c.
溶液 b.碳粉 c. 溶液 e.
溶液 e. 溶液 f.乙醇
溶液 f.乙醇
①在去油污后的废铁屑中加入一种物质,该物质可以为_________ 。
②在洗气瓶中装入一种物质,该物质可以为_________ 。
(3)步骤Ⅲ的具体操作:迅速取滤液置于容器中,沿器壁缓慢加入适量乙醇,使之覆盖在液面上,随着乙醇在溶液中不断扩散,硫酸亚铁铵逐渐结晶析出。该方法的优点是(写出至少两点)_________ 。
(4)制得 后,需要对晶体进行干燥,课本用干净的滤纸吸干,该兴趣小组同学经过讨论,决定用减压干燥,装置如图乙所示。将产品放入干燥器后、用水泵抽至盖子推不动即可。干燥结束后,启盖前,必须
后,需要对晶体进行干燥,课本用干净的滤纸吸干,该兴趣小组同学经过讨论,决定用减压干燥,装置如图乙所示。将产品放入干燥器后、用水泵抽至盖子推不动即可。干燥结束后,启盖前,必须__________________ ,然后启盖。
(5)产品中铁含量的测定可以采用酸性高锰酸钾滴定的方法。高锰酸钾标准溶液可用性质稳定,摩尔质量较大的基准物质草酸钠进行标定,反应原理为:
 。
。
实验步骤如下:
步骤一:先粗配浓度约为 的高锰酸钾溶液250mL;
的高锰酸钾溶液250mL;
步骤二:称取草酸钠固体m g放入锥形瓶中,加入适量水溶解并加硫酸酸化,加热到 ,立即用
,立即用 滴定,从而标定
滴定,从而标定 浓度为
浓度为 ;
;
步骤三:称取样品2.031g,放入锥形瓶并用适量水溶解;
步骤四:用标准 溶液滴定步骤三所配样品溶液,达到终点时消耗标准液45.00mL.
溶液滴定步骤三所配样品溶液,达到终点时消耗标准液45.00mL.
①步骤一中至少需要用到的玻璃仪器有烧杯、___________ 、___________ 。
②步骤二中需要对m的值进行预估,你的预估依据是____________ 。
a.所加硫酸的体积和浓度 b.反应的定量关系
c.滴定管的最大容量 d.用于溶解草酸钠的水的体积
③实验过程中需要进行多次滴定,在滴定步骤前要进行一系列操作,请选择合适的编号,按正确的顺序排列____________ 。
a.向酸式滴定管中间装入操作液至“0”刻度以上;
b.用蒸馏水洗涤滴定管;
c.将滴定管内装满水,直立于滴定管夹上约2min;
d.用操作溶液润洗滴定管;
e.将活塞旋转 后,再次观察;
后,再次观察;
f.将滴定管直立于滴定管夹上,静置Ⅰ分钟左右,读数;
g.右手拿住滴定管使其倾斜 ,左手迅速打开活塞。
,左手迅速打开活塞。
 是一种重要的化学试剂,某兴趣小组在课本合成方案的基础上进行了改进,流程如下:
是一种重要的化学试剂,某兴趣小组在课本合成方案的基础上进行了改进,流程如下:
(1)下列说法正确的是
A.废铁屑需用
 溶液除去表面的油污,通常采用抽滤除去碱液
溶液除去表面的油污,通常采用抽滤除去碱液B.实验中使用的蒸馏水均需煮沸除氧
C.在加入硫酸铵前,应该把硫酸亚铁溶液的pH值控制在强酸性范围内
D.鉴定所得晶体中含有
 ,可以取少量样品于试管中,加水溶解,加入NaOH溶液,露置于空气中,观察现象
,可以取少量样品于试管中,加水溶解,加入NaOH溶液,露置于空气中,观察现象
(2)废铁屑含有碳、硫、硅等杂质,为较快地制得较纯净的
 ,该兴趣小组设计图甲装置来制备产品,并选用了以下试剂中的一部分来完成实验。
,该兴趣小组设计图甲装置来制备产品,并选用了以下试剂中的一部分来完成实验。a.
 溶液 b.碳粉 c.
溶液 b.碳粉 c. 溶液 e.
溶液 e. 溶液 f.乙醇
溶液 f.乙醇①在去油污后的废铁屑中加入一种物质,该物质可以为
②在洗气瓶中装入一种物质,该物质可以为
(3)步骤Ⅲ的具体操作:迅速取滤液置于容器中,沿器壁缓慢加入适量乙醇,使之覆盖在液面上,随着乙醇在溶液中不断扩散,硫酸亚铁铵逐渐结晶析出。该方法的优点是(写出至少两点)
(4)制得
 后,需要对晶体进行干燥,课本用干净的滤纸吸干,该兴趣小组同学经过讨论,决定用减压干燥,装置如图乙所示。将产品放入干燥器后、用水泵抽至盖子推不动即可。干燥结束后,启盖前,必须
后,需要对晶体进行干燥,课本用干净的滤纸吸干,该兴趣小组同学经过讨论,决定用减压干燥,装置如图乙所示。将产品放入干燥器后、用水泵抽至盖子推不动即可。干燥结束后,启盖前,必须(5)产品中铁含量的测定可以采用酸性高锰酸钾滴定的方法。高锰酸钾标准溶液可用性质稳定,摩尔质量较大的基准物质草酸钠进行标定,反应原理为:
 。
。实验步骤如下:
步骤一:先粗配浓度约为
 的高锰酸钾溶液250mL;
的高锰酸钾溶液250mL;步骤二:称取草酸钠固体m g放入锥形瓶中,加入适量水溶解并加硫酸酸化,加热到
 ,立即用
,立即用 滴定,从而标定
滴定,从而标定 浓度为
浓度为 ;
;步骤三:称取样品2.031g,放入锥形瓶并用适量水溶解;
步骤四:用标准
 溶液滴定步骤三所配样品溶液,达到终点时消耗标准液45.00mL.
溶液滴定步骤三所配样品溶液,达到终点时消耗标准液45.00mL.①步骤一中至少需要用到的玻璃仪器有烧杯、
②步骤二中需要对m的值进行预估,你的预估依据是
a.所加硫酸的体积和浓度 b.反应的定量关系
c.滴定管的最大容量 d.用于溶解草酸钠的水的体积
③实验过程中需要进行多次滴定,在滴定步骤前要进行一系列操作,请选择合适的编号,按正确的顺序排列
a.向酸式滴定管中间装入操作液至“0”刻度以上;
b.用蒸馏水洗涤滴定管;
c.将滴定管内装满水,直立于滴定管夹上约2min;
d.用操作溶液润洗滴定管;
e.将活塞旋转
 后,再次观察;
后,再次观察;f.将滴定管直立于滴定管夹上,静置Ⅰ分钟左右,读数;
g.右手拿住滴定管使其倾斜
 ,左手迅速打开活塞。
,左手迅速打开活塞。
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐2】以软锰矿(主要成分为MnO2,还含有少量的Fe2O3、FeO、Al2O3和SiO2)为原料制备马日夫盐[Mn(H2PO4)2·2H2O(磷酸二氢锰)]的主要工艺流程如图:
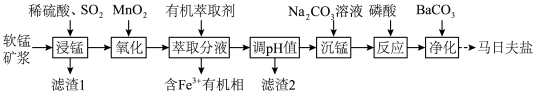
(1)用MnO2“氧化”时发生反应的离子方程式为__________________________________ 。
(2)如何检验“沉锰”已完成_____________________________________________________ 。
(3)铁离子的萃取率与接触时间和溶液的pH之间的关系如图1、2所示,则应选择的接触时间为_______ ;pH>1.7,铁离子的萃取率急剧下降的原因可能为____________________ 。
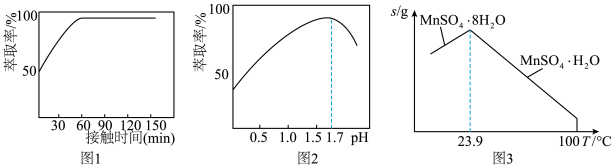
(4)结合图3的溶解度曲线,请补充完整由浸锰得到的溶液制备MnSO4·H2O的实验方案:边搅拌边向溶液中滴加适量的双氧水,再向滤液中加入MnCO3粉末调节溶液的pH范围为_________ ,过滤洗涤,将滤液与洗涤液合并,控制温度在80℃~90℃之间蒸发浓缩、______________ ,(填操作名称)得到MnSO4·H2O,用80℃~90℃的蒸馏水洗涤2~3次,放在真空干燥箱中低温干燥。[已知该溶液中pH=7.8时Mn(OH)2开始沉淀:pH=5.0时Fe(OH)3、Al(OH)3沉淀完全,pH=8.8时Fe(OH)2沉淀完全]。

(1)用MnO2“氧化”时发生反应的离子方程式为
(2)如何检验“沉锰”已完成
(3)铁离子的萃取率与接触时间和溶液的pH之间的关系如图1、2所示,则应选择的接触时间为

(4)结合图3的溶解度曲线,请补充完整由浸锰得到的溶液制备MnSO4·H2O的实验方案:边搅拌边向溶液中滴加适量的双氧水,再向滤液中加入MnCO3粉末调节溶液的pH范围为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
解题方法
【推荐3】氢化铝锂( )以其优良的还原性广泛应用于医药、农药、香料、染料等行业,实验室按如图流程、装置开展制备实验(夹持、尾气处理装置已省略)。
)以其优良的还原性广泛应用于医药、农药、香料、染料等行业,实验室按如图流程、装置开展制备实验(夹持、尾气处理装置已省略)。
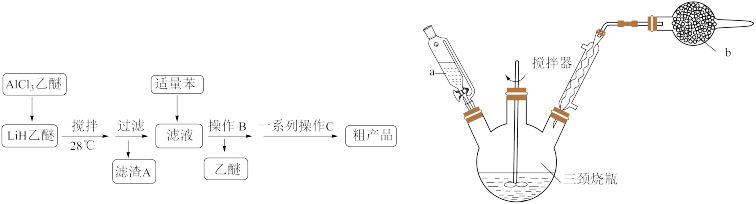
已知:① 难溶于烃,可溶于乙醚、四氢呋喃;
难溶于烃,可溶于乙醚、四氢呋喃;
②LiH、 在潮湿的空气中均会发生剧烈水解;
在潮湿的空气中均会发生剧烈水解;
③乙醚,沸点34.5℃,易燃,一般不与金属单质反应。请回答下列问题:
(1)仪器a的名称是___________ ;装置b的作用是___________ 。
(2)乙醚中的少量水分也会对 的制备产生严重的影响,以下试剂或操作可有效降低市售乙醚(含水体积分数为0.2%)含水量的是
的制备产生严重的影响,以下试剂或操作可有效降低市售乙醚(含水体积分数为0.2%)含水量的是___________ 。
a.钠 b.分液 c.五氧化二磷 d.通入乙烯
(3)下列说法正确的是___________
a. 能溶于乙醚,可能与
能溶于乙醚,可能与 可以形成二聚体有关
可以形成二聚体有关
b.滤渣A的主要成分是LiCl
c.为提高过滤出滤渣A的速度,可先加水让滤纸紧贴漏斗内壁
d.为提高合成 的速率,可将反应温度提高到50℃
的速率,可将反应温度提高到50℃
e.操作B可以在分液漏斗中进行
(4)该制备原理的不足之处是___________ 。
(5) (不含LiH)纯度可采用如下方法测定(装置如图所示):25℃,常压下,准确称取产品
(不含LiH)纯度可采用如下方法测定(装置如图所示):25℃,常压下,准确称取产品 ,记录量气管B起始体积读数
,记录量气管B起始体积读数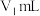 ,在分液漏斗中准确加入过量的四氢呋喃、水混合液15.0mL,打开旋塞至滴加完所有液体,立即关闭旋塞,调整量气管B,读数
,在分液漏斗中准确加入过量的四氢呋喃、水混合液15.0mL,打开旋塞至滴加完所有液体,立即关闭旋塞,调整量气管B,读数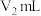 ,过量四氢呋喃的作用
,过量四氢呋喃的作用___________ ; 的质量分数为
的质量分数为___________ (已知25℃时,气体摩尔体积为 ,列出计算式即可)。
,列出计算式即可)。
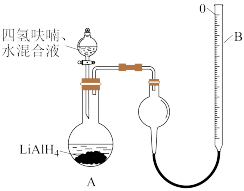
 )以其优良的还原性广泛应用于医药、农药、香料、染料等行业,实验室按如图流程、装置开展制备实验(夹持、尾气处理装置已省略)。
)以其优良的还原性广泛应用于医药、农药、香料、染料等行业,实验室按如图流程、装置开展制备实验(夹持、尾气处理装置已省略)。
已知:①
 难溶于烃,可溶于乙醚、四氢呋喃;
难溶于烃,可溶于乙醚、四氢呋喃;②LiH、
 在潮湿的空气中均会发生剧烈水解;
在潮湿的空气中均会发生剧烈水解;③乙醚,沸点34.5℃,易燃,一般不与金属单质反应。请回答下列问题:
(1)仪器a的名称是
(2)乙醚中的少量水分也会对
 的制备产生严重的影响,以下试剂或操作可有效降低市售乙醚(含水体积分数为0.2%)含水量的是
的制备产生严重的影响,以下试剂或操作可有效降低市售乙醚(含水体积分数为0.2%)含水量的是a.钠 b.分液 c.五氧化二磷 d.通入乙烯
(3)下列说法正确的是
a.
 能溶于乙醚,可能与
能溶于乙醚,可能与 可以形成二聚体有关
可以形成二聚体有关b.滤渣A的主要成分是LiCl
c.为提高过滤出滤渣A的速度,可先加水让滤纸紧贴漏斗内壁
d.为提高合成
 的速率,可将反应温度提高到50℃
的速率,可将反应温度提高到50℃e.操作B可以在分液漏斗中进行
(4)该制备原理的不足之处是
(5)
 (不含LiH)纯度可采用如下方法测定(装置如图所示):25℃,常压下,准确称取产品
(不含LiH)纯度可采用如下方法测定(装置如图所示):25℃,常压下,准确称取产品 ,记录量气管B起始体积读数
,记录量气管B起始体积读数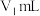 ,在分液漏斗中准确加入过量的四氢呋喃、水混合液15.0mL,打开旋塞至滴加完所有液体,立即关闭旋塞,调整量气管B,读数
,在分液漏斗中准确加入过量的四氢呋喃、水混合液15.0mL,打开旋塞至滴加完所有液体,立即关闭旋塞,调整量气管B,读数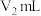 ,过量四氢呋喃的作用
,过量四氢呋喃的作用 的质量分数为
的质量分数为 ,列出计算式即可)。
,列出计算式即可)。
您最近一年使用:0次



