钛由于其稳定的化学性质,良好的耐高温、耐低温、抗强酸、抗强碱以及高强度、低密度,被美誉为“未来钢铁”、“战略金属”。
(1)基态钛原子核外共有_______ 种运动状态不相同的电子,价电子排布式_______ ;与钛同周期的元素中,基态原子的未成对电子数与钛相同的有________ 种。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是_________ 。
(3)TiCl4是氧化法制取钛的中间产物。TiCl4分子结构与CCl4相同,在常温下都是液体。TiCl4分子的空间构型是_______ ;TiCl4稳定性比CCl4差,试从结构分析其原因:_______ 。
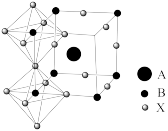
(4)钙钛矿材料是一类有着与钛酸钙相同晶体结构的材料,这种奇特的晶体结构让它具备了很多独特的理化性质,比如吸光性、电催化性等。钛酸钙晶体结构如图所示。其中,A代表Ca2+,Ti原子位于由O原子构成的正八面体的中心,则钛酸钙的化学式为______ ,Ca2+的配位数是________ 。
(1)基态钛原子核外共有
(2)钛比钢轻、比铝硬,是一种新兴的结构材料。钛硬度比铝大的原因是
(3)TiCl4是氧化法制取钛的中间产物。TiCl4分子结构与CCl4相同,在常温下都是液体。TiCl4分子的空间构型是
(4)钙钛矿材料是一类有着与钛酸钙相同晶体结构的材料,这种奇特的晶体结构让它具备了很多独特的理化性质,比如吸光性、电催化性等。钛酸钙晶体结构如图所示。其中,A代表Ca2+,Ti原子位于由O原子构成的正八面体的中心,则钛酸钙的化学式为

更新时间:2019-05-28 19:45:23
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】氮、磷、砷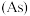 、锑
、锑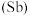 、铋
、铋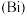 、镆
、镆 为元素周期表中原子序数依次增大的同族元素。回答下列问题:
为元素周期表中原子序数依次增大的同族元素。回答下列问题:
(1)砷在元素周期表中的位置_______ ;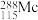 的中子数为
的中子数为_______ 。
(2)已知:
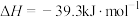

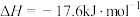
由此推知,其中最稳定的磷单质是_______ 。
(3)氮、磷、砷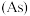 、锑
、锑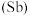 、铋
、铋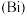 、镆
、镆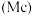 电负性依次
电负性依次_______ (增大或减小)。
(4) 和
和 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对 与
与 反应产物的推断正确的是
反应产物的推断正确的是_______ (填序号)。
a.不能与 反应 b.含离子键、共价键 c.能与水反应
反应 b.含离子键、共价键 c.能与水反应
(5) 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应的键角如图所示。
的空间结构和相应的键角如图所示。
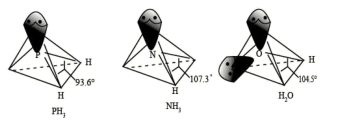
 中P的杂化类型是
中P的杂化类型是_______ ; 的键角小于
的键角小于 的,分析原因
的,分析原因_______ 。
(6)在1L真空密闭容器中加入amol 固体,t℃时发生如下反应:
固体,t℃时发生如下反应:
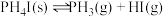 ①
①
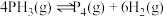 ②
②
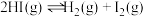 ③
③
达平衡时,体系中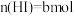 ,
, ,
,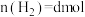 ,则t℃时反应①的平衡常数K值为
,则t℃时反应①的平衡常数K值为_______ (用字母表示)。
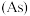 、锑
、锑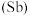 、铋
、铋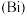 、镆
、镆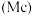 为元素周期表中原子序数依次增大的同族元素。回答下列问题:
为元素周期表中原子序数依次增大的同族元素。回答下列问题:(1)砷在元素周期表中的位置
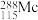 的中子数为
的中子数为(2)已知:

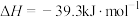

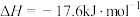
由此推知,其中最稳定的磷单质是
(3)氮、磷、砷
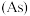 、锑
、锑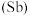 、铋
、铋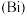 、镆
、镆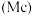 电负性依次
电负性依次(4)
 和
和 与卤化氢的反应相似,产物的结构和性质也相似。下列对
与卤化氢的反应相似,产物的结构和性质也相似。下列对 与
与 反应产物的推断正确的是
反应产物的推断正确的是a.不能与
 反应 b.含离子键、共价键 c.能与水反应
反应 b.含离子键、共价键 c.能与水反应(5)
 中配体分子
中配体分子 、
、 以及分子
以及分子 的空间结构和相应的键角如图所示。
的空间结构和相应的键角如图所示。
 中P的杂化类型是
中P的杂化类型是 的键角小于
的键角小于 的,分析原因
的,分析原因(6)在1L真空密闭容器中加入amol
 固体,t℃时发生如下反应:
固体,t℃时发生如下反应: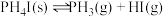 ①
①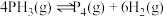 ②
②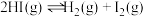 ③
③达平衡时,体系中
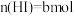 ,
, ,
,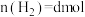 ,则t℃时反应①的平衡常数K值为
,则t℃时反应①的平衡常数K值为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】硅材料和铝材料在生产生活中应用广泛。回答下列问题:
(1)一种磷酸硅铝分子筛常用于催化甲醇制烯烃的反应。由硅原子核形成的三种微粒:a.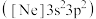 、b.
、b.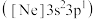 、c.
、c.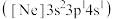 ,半径由大到小的顺序为
,半径由大到小的顺序为___________ (填标号);第三周期元素中,第一电离能介于A1和P之间的元素有___________ 种。
(2) 是一种高介电常数材料。已知:
是一种高介电常数材料。已知: 中
中 键角120°,
键角120°, 中
中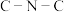 键角111°。共价键的极性Si—N
键角111°。共价键的极性Si—N___________ C—N(填“>”、“=”或“<”)。下列划线原子与 中N原子杂化类型相同的是
中N原子杂化类型相同的是___________ (填标号)。
A.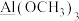 B.NH3BH3 C. N(CH3)3 D.NH4NO3
B.NH3BH3 C. N(CH3)3 D.NH4NO3
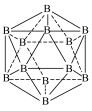
(3)铝硼中间合金在铝生产中应用广泛。金属铝熔点为660.3℃,晶体硼熔点为2300℃,晶体硼熔点高于铝的原因是___________ 。晶体硼的结构单元是正二十面体,每个单元中有12个硼原子,结构如图。若其中有两个原子为 ,其余为
,其余为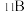 ,则该结构单元有
,则该结构单元有___________ 种。
(4)已知合金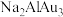 的立方晶胞结构如图1,Na原子以金刚石方式堆积,八面体空隙和半数的四面体空隙中填入
的立方晶胞结构如图1,Na原子以金刚石方式堆积,八面体空隙和半数的四面体空隙中填入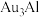 四面体;图2为沿x轴投影晶胞中所有Na原子的分布图。
四面体;图2为沿x轴投影晶胞中所有Na原子的分布图。
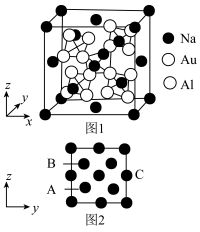
每个Na周围距离其最近的Na有___________ 个;以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如A点的分数坐标为 ,则B点的分数坐标为
,则B点的分数坐标为___________ ;设 为阿佛加德罗常数的值,
为阿佛加德罗常数的值,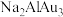 的摩尔质量为Mg·mol
的摩尔质量为Mg·mol ,晶体的密度为ρg⋅cm
,晶体的密度为ρg⋅cm ,则A、C两原子间的距离为
,则A、C两原子间的距离为___________ pm(列出计算表达式)。
(1)一种磷酸硅铝分子筛常用于催化甲醇制烯烃的反应。由硅原子核形成的三种微粒:a.
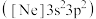 、b.
、b.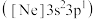 、c.
、c.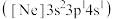 ,半径由大到小的顺序为
,半径由大到小的顺序为(2)
 是一种高介电常数材料。已知:
是一种高介电常数材料。已知: 中
中 键角120°,
键角120°, 中
中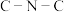 键角111°。共价键的极性Si—N
键角111°。共价键的极性Si—N 中N原子杂化类型相同的是
中N原子杂化类型相同的是A.
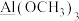 B.NH3BH3 C. N(CH3)3 D.NH4NO3
B.NH3BH3 C. N(CH3)3 D.NH4NO3(3)铝硼中间合金在铝生产中应用广泛。金属铝熔点为660.3℃,晶体硼熔点为2300℃,晶体硼熔点高于铝的原因是
 ,其余为
,其余为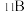 ,则该结构单元有
,则该结构单元有
(4)已知合金
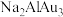 的立方晶胞结构如图1,Na原子以金刚石方式堆积,八面体空隙和半数的四面体空隙中填入
的立方晶胞结构如图1,Na原子以金刚石方式堆积,八面体空隙和半数的四面体空隙中填入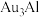 四面体;图2为沿x轴投影晶胞中所有Na原子的分布图。
四面体;图2为沿x轴投影晶胞中所有Na原子的分布图。
每个Na周围距离其最近的Na有
 ,则B点的分数坐标为
,则B点的分数坐标为 为阿佛加德罗常数的值,
为阿佛加德罗常数的值,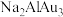 的摩尔质量为Mg·mol
的摩尔质量为Mg·mol ,晶体的密度为ρg⋅cm
,晶体的密度为ρg⋅cm ,则A、C两原子间的距离为
,则A、C两原子间的距离为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】日常生活中常用A的单质通入自来水中杀菌消毒,B的单质或合金做电线的导体部分。A的负一价离子的最外层电子数和次外层电子数相同。B为第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。
(1)A单质通入水中发生反应的离子方程式:___________ ;写出起到杀菌作用的产物的电子式:___________ 。
(2)B元素在周期表中的位置是___________ ;B金属晶体的空间堆积方式为___________ ;B原子的配位数为___________ 。
(3)A与B形成的一种化合物的立方晶胞如图所示:
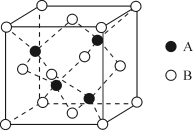
①该化合物的化学式为___________ 。
②该晶胞棱长为0.542 nm,则晶体的密度为___________  (写出计算式即可,不计算结果)。
(写出计算式即可,不计算结果)。
③该化合物难溶于水易溶于氨水,是因为 可与氨形成易溶于水的配位化合物,若配位数是4,则络离子的化学式为
可与氨形成易溶于水的配位化合物,若配位数是4,则络离子的化学式为___________ 。
该络离子在空气中易被氧化而导致溶液呈现___________ 色。
(4)如图A、B形成离子晶体的晶格能为___________ kJ/mol。
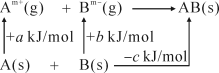
(1)A单质通入水中发生反应的离子方程式:
(2)B元素在周期表中的位置是
(3)A与B形成的一种化合物的立方晶胞如图所示:

①该化合物的化学式为
②该晶胞棱长为0.542 nm,则晶体的密度为
 (写出计算式即可,不计算结果)。
(写出计算式即可,不计算结果)。③该化合物难溶于水易溶于氨水,是因为
 可与氨形成易溶于水的配位化合物,若配位数是4,则络离子的化学式为
可与氨形成易溶于水的配位化合物,若配位数是4,则络离子的化学式为该络离子在空气中易被氧化而导致溶液呈现
(4)如图A、B形成离子晶体的晶格能为
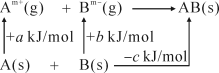
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】铜的相关化合物在化工、材料等领域有着广泛的应用。回答下列问题:
(1)基态Cu原子中,核外电子占据的最高能层的符号是___________ ,占据该能层电子的电子云轮廓图形状为__________ ;Cu2+价层电子的轨道表达式(电子排布图)为___________ 。
(2)Cu2O熔点(1235℃)比Cu2S熔点(113℃)高,它们均属于___________ 晶体,前者熔点较高的原因是_________________________________ 。
(3)Cu可与N、S,O等元素形成化合物,N、S、O三种元素的第一电离能由大到小的顺序为______________ ;在Cu的催化作用下,乙醇可被氧化为乙醛,乙醛分子中碳原子的杂化方式是________________ 。
(4)1mo[Cu(NH3)4]SO4中含有σ键的数目为___________ (用NA表示阿伏伽德罗常数)。
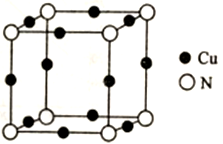
(5)Cu与N所形成的某种晶体的立方晶胞如图所示,其晶胞参数为amm。该晶体的化学式为___________ ,晶体的密度为___________ g·cm-3(列出计算式即可,用NA表示阿伏伽德罗常数)。
(1)基态Cu原子中,核外电子占据的最高能层的符号是
(2)Cu2O熔点(1235℃)比Cu2S熔点(113℃)高,它们均属于
(3)Cu可与N、S,O等元素形成化合物,N、S、O三种元素的第一电离能由大到小的顺序为
(4)1mo[Cu(NH3)4]SO4中含有σ键的数目为
(5)Cu与N所形成的某种晶体的立方晶胞如图所示,其晶胞参数为amm。该晶体的化学式为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】钢化玻璃因其优良的性能广泛应用于日常生活,但由于制作玻璃时里面含有极少量硫化镍,使得钢化玻璃在极限条件下的使用受到限制。
(1)基态硫原子价层电子的轨道表达式(电子排布图)为________ ;Ni(CO)4空间构型与甲烷相同,中心原子的杂化轨道类型为________
(2)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱____ >______
(3)H2S的键角_______ (填“大于”“小于”“等于”)H2O的键角,请从电负性的角度说明理由_____
(4)Cu3N的晶胞结构如图,N3-的配位数为______ ,Cu+半径为apm,N3-半径为bpm,阴阳离子看成刚性小球,并彼此相切,则Cu3N的密度为_____ g·cm-3。(阿伏加德罗常数用NA表示,列出表达式即可)

(1)基态硫原子价层电子的轨道表达式(电子排布图)为
(2)与硫同族的硒元素有两种常见的二元含氧酸,请比较它们酸性强弱
(3)H2S的键角
(4)Cu3N的晶胞结构如图,N3-的配位数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
【推荐3】元素周期表中前四周期的元素A、B、C、D、E,原子序数依次增大。对于它们的基态原子而言,A的核外电子总数与其电子层数相同;B的价电子层中有3个未成对电子;C的最外层电子数为其内层电子数的3倍;D与C同主族;E的最外层只有1个电子,但次外层有18个电子。回答下列问题。
(1)B、C、D中第一电离能最大的是__________ (填元素符号)。
(2)A和其他元素形成的二元共价化合物中,分子呈三角锥形结构的化合物,其中心原子的杂化方式为__________ ;既含有极性共价键又含有非极性共价键的化合物是__________ 、__________ 。(填化学式,写两种)。
(3)这些元素形成的含氧酸中,酸根离子呈三角锥形结构的是__________ (填化学式)。
(4)这五种元素形成的一种1∶1型离子化合物中,阴离子呈四面体形结构,阳离子如图所示,呈狭长的八面体形结构。该化合物中阴离子为__________ (填化学式),该化合物加热时首先失去的组分是__________ (填化学式)。

(5) 极易溶于水的原因与氢键有关,
极易溶于水的原因与氢键有关, 的一水合物的合理结构式为
的一水合物的合理结构式为__________ 。
(1)B、C、D中第一电离能最大的是
(2)A和其他元素形成的二元共价化合物中,分子呈三角锥形结构的化合物,其中心原子的杂化方式为
(3)这些元素形成的含氧酸中,酸根离子呈三角锥形结构的是
(4)这五种元素形成的一种1∶1型离子化合物中,阴离子呈四面体形结构,阳离子如图所示,呈狭长的八面体形结构。该化合物中阴离子为

(5)
 极易溶于水的原因与氢键有关,
极易溶于水的原因与氢键有关, 的一水合物的合理结构式为
的一水合物的合理结构式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】 (五氧化二钒)常作为化学工业中的催化剂,广泛用于冶金化工等行业,工业上以石煤(含有
(五氧化二钒)常作为化学工业中的催化剂,广泛用于冶金化工等行业,工业上以石煤(含有 等)来制备
等)来制备 的一种工艺流程如下:
的一种工艺流程如下:
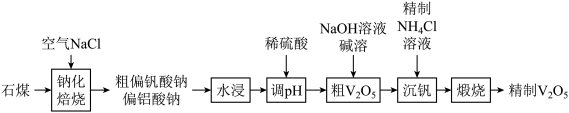
已知:① (偏钒酸铵)是白色粉末,微溶于冷水,可溶于热水。
(偏钒酸铵)是白色粉末,微溶于冷水,可溶于热水。
②
 沉淀生成和溶解的
沉淀生成和溶解的 如表所示:
如表所示:
回答下列问题:
(1)V在元素周期表中的位置:___________ 。
(2)“钠化焙烧”过程中 转化为可溶性
转化为可溶性 ,同时有黄绿色气体生成,其化学方程式为
,同时有黄绿色气体生成,其化学方程式为___________ 。
(3)粗 中含有
中含有 ,可通过
,可通过 溶液碱溶除去,需调节
溶液碱溶除去,需调节 的范围为
的范围为___________ 。
(4)已知:室温下,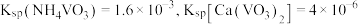 ,向偏钒酸铵的悬浊液中加入
,向偏钒酸铵的悬浊液中加入 ,当溶液中
,当溶液中 时,溶液中的
时,溶液中的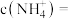
___________ 。
(5)产品纯度测定:将 产品溶于足量稀硫酸配成
产品溶于足量稀硫酸配成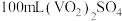 溶液。取
溶液。取 该溶液于锥形瓶中,用
该溶液于锥形瓶中,用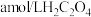 标准液进行满定,经过三次滴定,达到滴定终点时平均消耗标准液的体积为
标准液进行满定,经过三次滴定,达到滴定终点时平均消耗标准液的体积为 。已知:
。已知: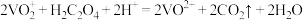 ,则该产品中
,则该产品中 的质量分数是
的质量分数是___________ %。
(6)钒的一种配合物的结构简式为 ,该配合物分子中含有的化学键类型有___________(填字母)。
,该配合物分子中含有的化学键类型有___________(填字母)。
 (五氧化二钒)常作为化学工业中的催化剂,广泛用于冶金化工等行业,工业上以石煤(含有
(五氧化二钒)常作为化学工业中的催化剂,广泛用于冶金化工等行业,工业上以石煤(含有 等)来制备
等)来制备 的一种工艺流程如下:
的一种工艺流程如下:
已知:①
 (偏钒酸铵)是白色粉末,微溶于冷水,可溶于热水。
(偏钒酸铵)是白色粉末,微溶于冷水,可溶于热水。②

 沉淀生成和溶解的
沉淀生成和溶解的 如表所示:
如表所示:溶液 | ||||
| 物质 | 开始沉淀 | 完全沉淀 | 沉淀开始溶解 | 沉淀完全溶解 |
 | 2.2 | 5.1 | 7.1 | 8.1 |
 | 3.3 | 4.7 | 8.7 | 12.8 |
(1)V在元素周期表中的位置:
(2)“钠化焙烧”过程中
 转化为可溶性
转化为可溶性 ,同时有黄绿色气体生成,其化学方程式为
,同时有黄绿色气体生成,其化学方程式为(3)粗
 中含有
中含有 ,可通过
,可通过 溶液碱溶除去,需调节
溶液碱溶除去,需调节 的范围为
的范围为(4)已知:室温下,
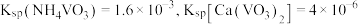 ,向偏钒酸铵的悬浊液中加入
,向偏钒酸铵的悬浊液中加入 ,当溶液中
,当溶液中 时,溶液中的
时,溶液中的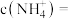
(5)产品纯度测定:将
 产品溶于足量稀硫酸配成
产品溶于足量稀硫酸配成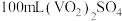 溶液。取
溶液。取 该溶液于锥形瓶中,用
该溶液于锥形瓶中,用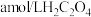 标准液进行满定,经过三次滴定,达到滴定终点时平均消耗标准液的体积为
标准液进行满定,经过三次滴定,达到滴定终点时平均消耗标准液的体积为 。已知:
。已知: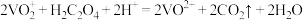 ,则该产品中
,则该产品中 的质量分数是
的质量分数是(6)钒的一种配合物的结构简式为
 ,该配合物分子中含有的化学键类型有___________(填字母)。
,该配合物分子中含有的化学键类型有___________(填字母)。| A.离子键 | B.极性键 | C.非极性键 | D.配位键 |
您最近一年使用:0次
【推荐2】氮元素可以形成多种化合物。回答以下问题:
(1)氮原子的最外层的轨道表示式是_______ ; 氮元素有多种化合价,列举一例含2种氮元素化合价的化合物_______ (化学式)。
(2)肼(N2H4)分 子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。NH3分子的空间构型是_______ ;与N2H4分子具有相同电子数的分子有多种,其中具有可燃性的物质是_____ (写化学式)。
(3)肼可用作火箭燃料,燃烧时发生的反应是:N2O4(1)+ 2N2H4(1)→3N2(g)+4H2O(g) +1038.7 kJ,若该反应中有4 mol N-H键断裂,则生成的气体有_____ mol,其中转移电子数目为________ 。
(4)肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在_____ (填标号)
a.离子键 b.共价键 c.金属键 d.范德华力
(1)氮原子的最外层的轨道表示式是
(2)肼(N2H4)分 子可视为NH3分子中的一个氢原子被-NH2(氨基)取代形成的另一种氮的氢化物。NH3分子的空间构型是
(3)肼可用作火箭燃料,燃烧时发生的反应是:N2O4(1)+ 2N2H4(1)→3N2(g)+4H2O(g) +1038.7 kJ,若该反应中有4 mol N-H键断裂,则生成的气体有
(4)肼能与硫酸反应生成N2H6SO4。N2H6SO4晶体类型与硫酸铵相同,则N2H6SO4的晶体内不存在
a.离子键 b.共价键 c.金属键 d.范德华力
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】现有A、B、C、D四种短周期元素,它们的相关结构和性质信息如下表所示,请结合相关信息,完成相关的问题:
(1)表中所述A的单质晶体中微粒间的相互作用有_______ 、_______ 。
(2)B元素的氧化物所对应的晶体属于__________ 晶体(填“分子”、“原子”、“离子”、“金属”),工业上制备B元素单质的化学方程式:________ 。
(3)C元素的气态氢化物的分子为__________ (填“极性”或“非极性”)分子,其溶于水后溶液呈碱性的原因____ (用方程式表示),C元素原子核外最外层电子的轨道表示式为_______ 。
(4)与D同主族的短周期元素,其单质及其化合物与D的单质及其化合物均具有的性质为______ (填序号)。
A 常温下单质跟水剧烈反应并放出氧气 B 气态氢化物具有很强的热稳定性
C 气态氢化物极易溶于水并呈强酸性 D 在HXO中X的化合价均为+1价
| 元素 | 相关结构和性质 |
| A | 其单质的一种晶体虽不是金属晶体,但是电的良导体,且难熔、质软并有润滑性,可用作原子核反应堆的慢化剂、火箭发动机喷管和电极材料等。 |
| B | 其单质既能与强酸溶液反应,又能与强碱溶液反应,其简单离子在第三周期单核离子中半径最小。 |
| C | 是蛋白质的组成元素之一,原子核外有3种不同能量的电子,且未成对电子数最多。 |
| D | 原子核外最外层电子排布式为nsnnp2n+1 |
(2)B元素的氧化物所对应的晶体属于
(3)C元素的气态氢化物的分子为
(4)与D同主族的短周期元素,其单质及其化合物与D的单质及其化合物均具有的性质为
A 常温下单质跟水剧烈反应并放出氧气 B 气态氢化物具有很强的热稳定性
C 气态氢化物极易溶于水并呈强酸性 D 在HXO中X的化合价均为+1价
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】卤素可形成许多结构和性质特殊的化合物。回答下列问题:
(1)-40 ℃时,F2与冰反应生成HOF和HF.常温常压下,HOF为无色气体,固态HOF的晶体类型为___________ ,HOF水解反应的产物为___________ (填化学式)。
(2)ClO2中心原子为Cl,Cl2O中心原子为O,二者均为V形结构,但ClO2中存在大π键_______________________________ ;O—Cl—O键角___________ Cl—O—Cl键角(填“>”“<”或“=”)。比较ClO2与Cl2O中Cl—O键的键长并说明原因___________ 。
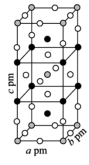
(3)一定条件下,CuCl2、K和F2反应生成KCl和化合物X。已知X属于四方晶系,晶胞结构如图所示(晶胞参数a=b≠c,α=β=γ=90°),其中Cu化合价为+2.上述反应的化学方程式为___________ 。 若阿伏加德罗常数的值为NA,化合物X的密度ρ=___________ g·cm-3(用含NA的代数式表示)。
(1)-40 ℃时,F2与冰反应生成HOF和HF.常温常压下,HOF为无色气体,固态HOF的晶体类型为
(2)ClO2中心原子为Cl,Cl2O中心原子为O,二者均为V形结构,但ClO2中存在大π键
(3)一定条件下,CuCl2、K和F2反应生成KCl和化合物X。已知X属于四方晶系,晶胞结构如图所示(晶胞参数a=b≠c,α=β=γ=90°),其中Cu化合价为+2.上述反应的化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
解题方法
【推荐2】硼族元素在科学研究领域有重要应用,回答下列问题:
(1)Ga是硼族元素,写出其M能层的电子排布式_______ 。
(2)B是硼族元素中唯一的非金属性元素。
①Li、Be、C、Al中第一电离能比B大的是_______
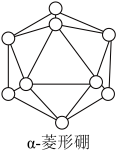
②α-菱形硼晶体结构单元是如图所示的正二十面体,该结构单元由_______ 个硼原子构成。
(3)Al单质的熔点为660℃,Ga单质的熔点为30℃,Al比Ga熔点高的原因是_______
(4)Al存在 、
、 、[AlF6]3-等多种配离子。
、[AlF6]3-等多种配离子。
① 的立体构型为
的立体构型为_______ , ,结构如图所示:
,结构如图所示: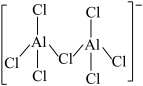 其中Cl杂化方式为
其中Cl杂化方式为_______ 。
②存在 、[AlF6]3-,能形成[AlF6]3-的原因是
、[AlF6]3-,能形成[AlF6]3-的原因是_______ 。
(5)氮化镓为六方晶胞,结构如图所示。
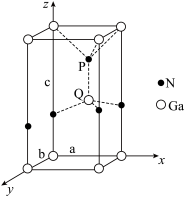
①画出晶胞中Q原子沿z轴在xy平面上的投影_______ 。
②该晶体密度为ρg·m-3,晶胞参数a-=b≠c(单位:nm),a、b夹角为120°,阿伏伽德罗常数的值为NA,则晶胞参数c=_______ nm(用含a、b、ρ、NA的代数式表示)。
(1)Ga是硼族元素,写出其M能层的电子排布式
(2)B是硼族元素中唯一的非金属性元素。
①Li、Be、C、Al中第一电离能比B大的是
②α-菱形硼晶体结构单元是如图所示的正二十面体,该结构单元由

(3)Al单质的熔点为660℃,Ga单质的熔点为30℃,Al比Ga熔点高的原因是
(4)Al存在
 、
、 、[AlF6]3-等多种配离子。
、[AlF6]3-等多种配离子。①
 的立体构型为
的立体构型为 ,结构如图所示:
,结构如图所示: 其中Cl杂化方式为
其中Cl杂化方式为②存在
 、[AlF6]3-,能形成[AlF6]3-的原因是
、[AlF6]3-,能形成[AlF6]3-的原因是(5)氮化镓为六方晶胞,结构如图所示。

①画出晶胞中Q原子沿z轴在xy平面上的投影
②该晶体密度为ρg·m-3,晶胞参数a-=b≠c(单位:nm),a、b夹角为120°,阿伏伽德罗常数的值为NA,则晶胞参数c=
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐3】磷及其化合物在工业生产中起着重要的作用。
(1)基态磷原子价电子的轨道表示式是_______ 。
(2)磷元素有白磷、黑磷等常见的单质。
①白磷(P4)是分子晶体,易溶于CS2,难溶于水,可能原因是_______ 。
②黑磷晶体是一种比石墨烯更优秀的新型材料,其晶体是与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是_______ (填字母序号)
b.分子中磷原子杂化方式为sp2杂化
c.是混合型晶体
(3)Fe3+与水会形成黄色的配离子[Fe(OH)]2+,为避免颜色干扰,常在Fe3+溶液中加入H3PO4形成无色的[Fe(PO4)2]3-。由此推测与Fe3+形成的配离子更稳定的配体是_______ ,其空间构型是_______ 。
(4)第IIIA族磷化物均为共价化合物,被广泛用于高温技术、新型电子产品等领域。
①实验测定磷化铝和磷化铟的熔点分别为2000、1070℃,从结构角度说明其熔点差异的原因_____ 。
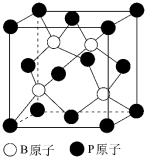
②磷化硼是一种半导体材料,晶胞结构如下图所示。已知晶胞边长apm,阿伏加德罗常数为NA,磷化硼晶体的密度是_______ g/cm3.(1pm=10-10cm)
(1)基态磷原子价电子的轨道表示式是
(2)磷元素有白磷、黑磷等常见的单质。
①白磷(P4)是分子晶体,易溶于CS2,难溶于水,可能原因是
②黑磷晶体是一种比石墨烯更优秀的新型材料,其晶体是与石墨类似的层状结构,如图所示。下列有关黑磷晶体的说法正确的是

b.分子中磷原子杂化方式为sp2杂化
c.是混合型晶体
(3)Fe3+与水会形成黄色的配离子[Fe(OH)]2+,为避免颜色干扰,常在Fe3+溶液中加入H3PO4形成无色的[Fe(PO4)2]3-。由此推测与Fe3+形成的配离子更稳定的配体是
(4)第IIIA族磷化物均为共价化合物,被广泛用于高温技术、新型电子产品等领域。
①实验测定磷化铝和磷化铟的熔点分别为2000、1070℃,从结构角度说明其熔点差异的原因
②磷化硼是一种半导体材料,晶胞结构如下图所示。已知晶胞边长apm,阿伏加德罗常数为NA,磷化硼晶体的密度是
您最近一年使用:0次



