在一定体积的密闭容器中进行如下化学反应:CO2(g)+H2(g)  CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=________ 。
(2)该反应为________ (填“吸热”或“放热”)反应,理由是__________ 。
(3)能判断该反应达到化学平衡状态的依据是________ 。
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为______ ℃。
(5)在800 ℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2 mol·L-1,c(H2)为1.5 mol·L-1,c(CO)为1 mol·L-1,c(H2O)为3 mol·L-1,则下一时刻,反应向_____ (填“正向”或“逆向”)进行。
 CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:
CO(g)+H2O(g),其化学平衡常数(K)和温度(t)的关系如下表所示:| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=
(2)该反应为
(3)能判断该反应达到化学平衡状态的依据是
A.容器中压强不变 B.混合气体中c(CO)不变
C.v正(H2)=v逆(H2O) D.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
(5)在800 ℃时,发生上述反应,某一时刻测得容器内各物质的浓度分别为c(CO2)为2 mol·L-1,c(H2)为1.5 mol·L-1,c(CO)为1 mol·L-1,c(H2O)为3 mol·L-1,则下一时刻,反应向
更新时间:2019-05-27 10:59:08
|
相似题推荐
【推荐1】二甲醚(CH3OCH3)是一种清洁能源由合成气(CO,H2)制备二甲醚的反应原理如下:
反应Ⅰ:CO(g) +2H2(g)⇌CH3OH(g)△H1
反应Ⅱ:2CH3OH(g)⇌CH3OCH3(g) +H2O(g)△H2
回答下列问题:
(1)上述反应符合“原子经济”原则的是____ (填“反应Ⅰ”或“反应Ⅱ”)。下图中使曲线a对应反应按曲线b进行的措施是____ ,该反应自发进行的条件为____ (填“低温”或“高温")。
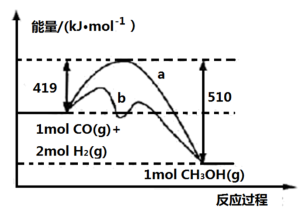
(2)已知△H2=-20.0kJ ·mol-1;H2O(l)=H2O (g)△H= +44.0 kJ·mol-1,则由合成气(CO、H2)制备1 mol CH3OCH3(g),且生成H2O (l)的热化学方程式为____ ;
(3)模拟该制备原理,起始时在某容器中充入2 mol CO和4 mol H2合成CH3OCH3(g),平衡时混合物中氢气的体积分数与温度、压强的关系如下图所示。
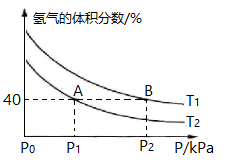
①下列有关说法能够证明恒温恒压时,反应2CO(g) +4H2(g)⇌CH3OCH3(g)+H2O (g)一定达到平衡状态的是 (填序号)___ 。
a.CO和H2的转化率相等
b.反应体系中混合气体密度保持不变
c. c(H2):c( CH3OCH3)的值保持不变
d.反应体系压强保持不变
②上图中T1____ (填“>”、“ <””或“=”,下同)T2;在A、B两点条件下,该反应从开始到平衡时生成二甲醚的平均速率:v (A)_____ v(B)。
③A点对应的CH3OCH3(g)的体积分数为_______ ,B点对应的Kp=_______ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
反应Ⅰ:CO(g) +2H2(g)⇌CH3OH(g)△H1
反应Ⅱ:2CH3OH(g)⇌CH3OCH3(g) +H2O(g)△H2
回答下列问题:
(1)上述反应符合“原子经济”原则的是

(2)已知△H2=-20.0kJ ·mol-1;H2O(l)=H2O (g)△H= +44.0 kJ·mol-1,则由合成气(CO、H2)制备1 mol CH3OCH3(g),且生成H2O (l)的热化学方程式为
(3)模拟该制备原理,起始时在某容器中充入2 mol CO和4 mol H2合成CH3OCH3(g),平衡时混合物中氢气的体积分数与温度、压强的关系如下图所示。

①下列有关说法能够证明恒温恒压时,反应2CO(g) +4H2(g)⇌CH3OCH3(g)+H2O (g)一定达到平衡状态的是 (填序号)
a.CO和H2的转化率相等
b.反应体系中混合气体密度保持不变
c. c(H2):c( CH3OCH3)的值保持不变
d.反应体系压强保持不变
②上图中T1
③A点对应的CH3OCH3(g)的体积分数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】某学习小组在实验室用 和
和 模拟工业合成氨。某温度下,在容积恒定为2.0L的密闭容器中充入
模拟工业合成氨。某温度下,在容积恒定为2.0L的密闭容器中充入 和
和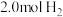 ,一段时间后反应达到平衡状态。
,一段时间后反应达到平衡状态。
(1)已知在该条件下, 与
与 反应生成
反应生成 ,每转移
,每转移 电子放出
电子放出 的热量,则该反应的热化学方程式为
的热量,则该反应的热化学方程式为_______ 。
(2)一定条件下,能说明该反应达到平衡状态的是_______(填标号)。
(3)反应过程中的实验数据如下表所示:
①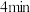 内用
内用 表示的平均反应速率为
表示的平均反应速率为_______ 。
②平衡时 的物质的量浓度为
的物质的量浓度为_______ 。
 和
和 模拟工业合成氨。某温度下,在容积恒定为2.0L的密闭容器中充入
模拟工业合成氨。某温度下,在容积恒定为2.0L的密闭容器中充入 和
和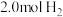 ,一段时间后反应达到平衡状态。
,一段时间后反应达到平衡状态。(1)已知在该条件下,
 与
与 反应生成
反应生成 ,每转移
,每转移 电子放出
电子放出 的热量,则该反应的热化学方程式为
的热量,则该反应的热化学方程式为(2)一定条件下,能说明该反应达到平衡状态的是_______(填标号)。
A. 的物质的量不再改变 的物质的量不再改变 | B.反应停止进行 |
C. 、 、 和 和 的反应速率之比为1∶3∶2 的反应速率之比为1∶3∶2 | D.混合气体总压强不再改变 |
 | 0 | 1 | 2 | 4 | 6 |
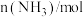 | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
 内用
内用 表示的平均反应速率为
表示的平均反应速率为②平衡时
 的物质的量浓度为
的物质的量浓度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】当今世界多国相继规划了碳达峰、碳中和的时间节点,因此研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。
(1)CH4-CO2催化重整不仅对温室气体的减排有重要意义,还可以得到合成气(CO和H2)。已知:
①CH4(g)+H2O(g)=CO(g)+3H2(g) ∆H1=+206.2 kJ∙mol-1
②CH4(g)+2H2O(g)=CO2(g)+4H2(g) ∆H2=+165.0 kJ∙mol-1
写出该催化重整反应的热化学方程式:_______ 。
(2)在恒容密闭容器中通入等物质的量的CO2和H2并发生反应CO2(g)+4H2(g)=CH4(g)+2H2O(g),300℃下,CO2物质的量浓度c(CO2)随时间t变化的曲线如图所示:
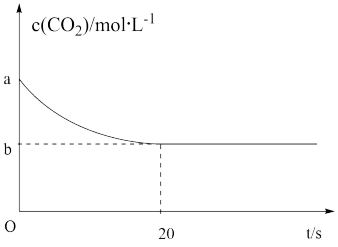
此条件下反应前20s的平均反应速率v(H2)=_______ (用含a、b的代数式表示)。当混合气体的某项物理量保持不变时,可认为反应达到了平衡状态,该物理量可能是_______ (填序号)。
a.压强 b.密度 c.平均摩尔质量 d.颜色
(3)已知:NH3∙H2O的Kb=1.7×10-5,H2CO3的Ka1=4.3×10-7,Ka2=5.6×10-11。工业生产尾气中的CO2捕获技术之一是氨水溶液吸收技术,工艺流程是将烟气冷却至20℃后用氨水吸收过量的CO2。吸收反应的化学方程式为_______ ,所得溶液显_______ (填”酸性"”碱性"或”中性",不考虑二氧化碳的溶解)。
(1)CH4-CO2催化重整不仅对温室气体的减排有重要意义,还可以得到合成气(CO和H2)。已知:
①CH4(g)+H2O(g)=CO(g)+3H2(g) ∆H1=+206.2 kJ∙mol-1
②CH4(g)+2H2O(g)=CO2(g)+4H2(g) ∆H2=+165.0 kJ∙mol-1
写出该催化重整反应的热化学方程式:
(2)在恒容密闭容器中通入等物质的量的CO2和H2并发生反应CO2(g)+4H2(g)=CH4(g)+2H2O(g),300℃下,CO2物质的量浓度c(CO2)随时间t变化的曲线如图所示:

此条件下反应前20s的平均反应速率v(H2)=
a.压强 b.密度 c.平均摩尔质量 d.颜色
(3)已知:NH3∙H2O的Kb=1.7×10-5,H2CO3的Ka1=4.3×10-7,Ka2=5.6×10-11。工业生产尾气中的CO2捕获技术之一是氨水溶液吸收技术,工艺流程是将烟气冷却至20℃后用氨水吸收过量的CO2。吸收反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】CO和H2可作为能源和化工原料,应用十分广泛。
(1)已知:C(s)+O2(g)===CO2(g)ΔH1=-393.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g)ΔH2=-483.6 kJ·mol-1
C(s)+H2O(g)===CO(g)+H2(g)ΔH3=131.3 kJ·mol-1
则反应CO(g)+H2(g)+O2(g)===H2O(g)+CO2(g)的ΔH=________ kJ·mol-1。标准状况下的煤气(CO、H2)44.8 L与氧气反应生成CO2和H2O,反应过程中转移________ mol电子。
(2)密闭容器中充有10 mol CO与20 mol H2,在催化剂作用下反应生成甲醇:
CO(g)+2H2(g) CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如图所示。
CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如图所示。
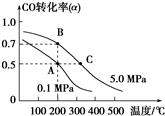
①若A、B两点表示在某时刻达到的平衡状态,此时在B点时容器的体积为6 L,则该温度下的平衡常数K=________ ;此时在A点时容器的体积VA_______ 6 L(填“大于”“小于”或“等于”)。该反应为________ (填“放热反应”或“吸热反应”)。
②若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA________ tC(填“大于”“小于”或“等于”)。
(1)已知:C(s)+O2(g)===CO2(g)ΔH1=-393.5 kJ·mol-1
2H2(g)+O2(g)===2H2O(g)ΔH2=-483.6 kJ·mol-1
C(s)+H2O(g)===CO(g)+H2(g)ΔH3=131.3 kJ·mol-1
则反应CO(g)+H2(g)+O2(g)===H2O(g)+CO2(g)的ΔH=
(2)密闭容器中充有10 mol CO与20 mol H2,在催化剂作用下反应生成甲醇:
CO(g)+2H2(g)
 CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如图所示。
CH3OH(g);CO的平衡转化率(α)与温度、压强的关系如图所示。
①若A、B两点表示在某时刻达到的平衡状态,此时在B点时容器的体积为6 L,则该温度下的平衡常数K=
②若A、C两点都表示达到的平衡状态,则自反应开始到达平衡状态所需的时间tA
您最近一年使用:0次
【推荐2】研究NO2、SO2 、CO等大气污染气体的处理具有重要意义。
(1)NO2可用水吸收,相应的化学反应方程式为_____________ 。利用反应6NO2+ 8NH3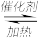 7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是________ L。
(2)已知:2SO2(g)+O2(g) 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-1
2NO(g)+O2(g) 2NO2(g) ΔH=-113.0 kJ·mol
2NO2(g) ΔH=-113.0 kJ·mol
则反应NO2(g)+SO2(g) SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=_____________ kJ·mol-1。一定条件下,将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是________ 。
a 体系压强保持不变 b 混合气体颜色保持不变
c SO3和NO的体积比保持不变 d 每消耗1 mol SO3的同时生成1 molNO2
该温度下,此反应的平衡常数表达式K=__________ 。
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g) CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH______ 0(填“>”或“ <”)。
(1)NO2可用水吸收,相应的化学反应方程式为
 7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是
7N2+12 H2O也可处理NO2。当转移1.2mol电子时,消耗的NO2在标准状况下是(2)已知:2SO2(g)+O2(g)
 2SO3(g) ΔH=-196.6 kJ·mol-1
2SO3(g) ΔH=-196.6 kJ·mol-12NO(g)+O2(g)
 2NO2(g) ΔH=-113.0 kJ·mol
2NO2(g) ΔH=-113.0 kJ·mol则反应NO2(g)+SO2(g)
 SO3(g)+NO(g)的ΔH=
SO3(g)+NO(g)的ΔH=a 体系压强保持不变 b 混合气体颜色保持不变
c SO3和NO的体积比保持不变 d 每消耗1 mol SO3的同时生成1 molNO2
该温度下,此反应的平衡常数表达式K=
(3)CO可用于合成甲醇,反应方程式为CO(g)+2H2(g)
 CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH
CH3OH(g)。CO在不同温度下的平衡转化率与压强的关系如图所示。该反应ΔH
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】二甲醚可用作溶剂冷冻剂喷雾剂等,科学家提出利用CO2和H2合成二甲醚,反应原理为2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) ∆H。
CH3OCH3(g)+3H2O(g) ∆H。
(1)已知①H2O(g)+CO(g) CO2(g)+H2(g) ∆H=+42 kJ·mol-1;
CO2(g)+H2(g) ∆H=+42 kJ·mol-1;
②CH3OCH3(g)+H2O(g) 2CH3OH(g) ∆H1=+24.52 kJ·mol-1;
2CH3OH(g) ∆H1=+24.52 kJ·mol-1;
③CH3OH(g) CO(g)+2H2(g) ∆H2=+90.73 kJ·mol-1。
CO(g)+2H2(g) ∆H2=+90.73 kJ·mol-1。
则∆H=_______ kJ·mol-1。
(2)对于恒温恒容条件下进行的反应①,下列说法能说明反应已达平衡的是_______ 。
A.混合气体密度不发生改变 B.混合气体的平均相对分子质量不再发生改变
C.v(CO)正=v(H2)逆 D.n(CO)与n(H2)的比值不变
(3)一定温度下,在一个2 L的密闭容器中充入2 mol CO2和6 mol H2发生上述反应,经过5 min反应达到平衡,此时容器中压强与起始压强之比为3:4,则用CH3OCH3表示的平均反应速率为_______ ,H2的转化率为_______ ;此时,若向体系中再加入2 mol CO2和1.5 mol H2O(g),平衡_______ 移动(填“正向”“逆向”或“不”)。
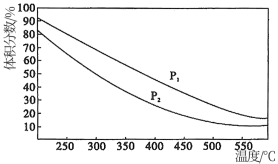
(4)一定温度下,密闭容器中进行的反应③,测得平衡时混合物中某物质的体积分数在不同压强下随温度的变化如图所示,则纵坐标表示的物质是_______ ,压强P1_______ P2(填“>”或“<”)。
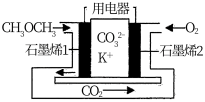
(5)科学家利用石墨烯设计的二甲醚熔融燃料电池工作原理如图所示,工作时,通入氧气的电极为_______ (填负或正)极,负极的电极反应式为_______ 。
 CH3OCH3(g)+3H2O(g) ∆H。
CH3OCH3(g)+3H2O(g) ∆H。(1)已知①H2O(g)+CO(g)
 CO2(g)+H2(g) ∆H=+42 kJ·mol-1;
CO2(g)+H2(g) ∆H=+42 kJ·mol-1;②CH3OCH3(g)+H2O(g)
 2CH3OH(g) ∆H1=+24.52 kJ·mol-1;
2CH3OH(g) ∆H1=+24.52 kJ·mol-1;③CH3OH(g)
 CO(g)+2H2(g) ∆H2=+90.73 kJ·mol-1。
CO(g)+2H2(g) ∆H2=+90.73 kJ·mol-1。则∆H=
(2)对于恒温恒容条件下进行的反应①,下列说法能说明反应已达平衡的是
A.混合气体密度不发生改变 B.混合气体的平均相对分子质量不再发生改变
C.v(CO)正=v(H2)逆 D.n(CO)与n(H2)的比值不变
(3)一定温度下,在一个2 L的密闭容器中充入2 mol CO2和6 mol H2发生上述反应,经过5 min反应达到平衡,此时容器中压强与起始压强之比为3:4,则用CH3OCH3表示的平均反应速率为
(4)一定温度下,密闭容器中进行的反应③,测得平衡时混合物中某物质的体积分数在不同压强下随温度的变化如图所示,则纵坐标表示的物质是

(5)科学家利用石墨烯设计的二甲醚熔融燃料电池工作原理如图所示,工作时,通入氧气的电极为

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】页岩气是从页岩层中开采的一种非常重要的天然气资源,页岩气的主要成分是甲烷,是公认的洁净能源。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和 ),
), 与
与 通入聚焦太阳能反应器,发生反应
通入聚焦太阳能反应器,发生反应
 。已知:
。已知:
①

②

③

则
___________ (用含 、
、 、
、 的代数式表示)
的代数式表示)
(2)用合成气生成甲醇的反应为
 ,在10L恒容密闭容器中按物质的量之比1:2充入CO和
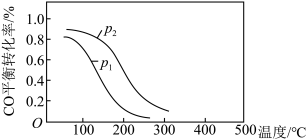
,在10L恒容密闭容器中按物质的量之比1:2充入CO和 ,测得CO的平衡转化率与温度和压强的关系如图所示:
,测得CO的平衡转化率与温度和压强的关系如图所示:
200℃时 随时间的变化如表所示:
随时间的变化如表所示:
①该反应的平衡常数表达式为
___________ ;
___________ (填“>”“<”或“=”)0。
②写出一条可同时提高反应速率和CO转化率的措施:___________ 。
③下列说法正确的是___________ (填字母)。
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强: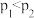
④0~1min内用 表示的反应速率
表示的反应速率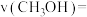
___________  。
。
⑤向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、4 mol 、2 mol
、2 mol  ,保持温度不变,则化学平衡
,保持温度不变,则化学平衡___________ (填“正向”“逆向”或“不”)移动。
(1)页岩气不仅能用作燃料,还可用于生产合成气(CO和
 ),
), 与
与 通入聚焦太阳能反应器,发生反应
通入聚焦太阳能反应器,发生反应
 。已知:
。已知:①


②


③
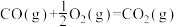

则

 、
、 、
、 的代数式表示)
的代数式表示)(2)用合成气生成甲醇的反应为

 ,在10L恒容密闭容器中按物质的量之比1:2充入CO和
,在10L恒容密闭容器中按物质的量之比1:2充入CO和 ,测得CO的平衡转化率与温度和压强的关系如图所示:
,测得CO的平衡转化率与温度和压强的关系如图所示:
200℃时
 随时间的变化如表所示:
随时间的变化如表所示:| t/min | 0 | 1 | 3 | 5 |
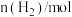 | 8.0 | 5.4 | 4.0 | 4.0 |


②写出一条可同时提高反应速率和CO转化率的措施:
③下列说法正确的是
a.温度越高,该反应的平衡常数越大
b.达平衡后再充入稀有气体,CO的转化率提高
c.容器内气体压强不再变化时,反应达到最大限度
d.图中压强:
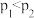
④0~1min内用
 表示的反应速率
表示的反应速率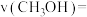
 。
。⑤向上述200℃达到平衡的恒容密闭容器中再加入2 mol CO、4 mol
 、2 mol
、2 mol  ,保持温度不变,则化学平衡
,保持温度不变,则化学平衡
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】碘及其化合物在人类活动中占有重要地位。回答下列问题:
(1)“大象牙膏”实验中,将 、
、 和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:
和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:
第一步:
 慢反应
慢反应
第二步:
 快反应
快反应
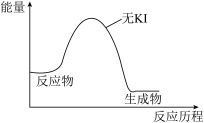
①该反应的催化剂为_______ ,总反应方程式为_______ ;
②在下图中画出有 参与的两步反应的能量历程图。
参与的两步反应的能量历程图。_______
(2)已知:25℃下,
(i)
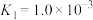
(ii)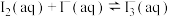

(iii)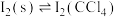
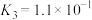
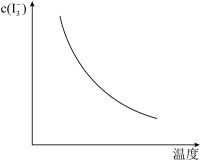
其中,反应ⅱ的平衡时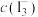 随温度的变化如图:
随温度的变化如图:
烧杯甲:将mg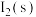 加入20mL水中(含
加入20mL水中(含 沉淀);
沉淀);
烧杯乙:将mg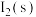 加入20mL
加入20mL 溶液(含
溶液(含 沉淀)。
沉淀)。
①甲中存在平衡i,乙中存在平衡i和ii,不考虑碘与水的反应以及其它反应,下列说法正确的是_______ 。
A.烧杯乙中剩余的 沉淀质量比甲的
沉淀质量比甲的 沉淀质量小
沉淀质量小
B.室温下,甲中加少量水,溶液中 浓度一定减小
浓度一定减小
C.乙中通入少量 ,
, 浓度降低
浓度降低
D.升高温度,反应ⅱ的平衡常数大于640
②为了探究乙中溶液含碘微粒的存在形式,进行实验:恒温25℃向10mL一定浓度的 溶液中加入10mL
溶液中加入10mL
 溶液(混合后的体积变化可忽略),反应结束后硝元素的微粒主要存在平衡ⅱ,相关微粒浓度如下:
溶液(混合后的体积变化可忽略),反应结束后硝元素的微粒主要存在平衡ⅱ,相关微粒浓度如下:
其中
_______ (用含c的代数式表示),若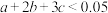 ,说明平衡体系中
,说明平衡体系中_______ (“含”或“不含”) 沉淀。
沉淀。
③计算25℃下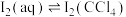 的平衡常数K=
的平衡常数K=_______ 。
(1)“大象牙膏”实验中,将
 、
、 和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:
和洗洁精混合后,短时间内产生大量的泡沫。其反应过程分为两步:第一步:

 慢反应
慢反应第二步:

 快反应
快反应①该反应的催化剂为
②在下图中画出有
 参与的两步反应的能量历程图。
参与的两步反应的能量历程图。
(2)已知:25℃下,
(i)

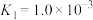
(ii)
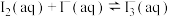

(iii)
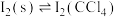
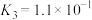
其中,反应ⅱ的平衡时
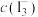 随温度的变化如图:
随温度的变化如图:
烧杯甲:将mg
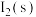 加入20mL水中(含
加入20mL水中(含 沉淀);
沉淀);烧杯乙:将mg
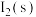 加入20mL
加入20mL 溶液(含
溶液(含 沉淀)。
沉淀)。①甲中存在平衡i,乙中存在平衡i和ii,不考虑碘与水的反应以及其它反应,下列说法正确的是
A.烧杯乙中剩余的
 沉淀质量比甲的
沉淀质量比甲的 沉淀质量小
沉淀质量小B.室温下,甲中加少量水,溶液中
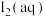 浓度一定减小
浓度一定减小C.乙中通入少量
 ,
, 浓度降低
浓度降低D.升高温度,反应ⅱ的平衡常数大于640
②为了探究乙中溶液含碘微粒的存在形式,进行实验:恒温25℃向10mL一定浓度的
 溶液中加入10mL
溶液中加入10mL
 溶液(混合后的体积变化可忽略),反应结束后硝元素的微粒主要存在平衡ⅱ,相关微粒浓度如下:
溶液(混合后的体积变化可忽略),反应结束后硝元素的微粒主要存在平衡ⅱ,相关微粒浓度如下:| 微粒 |  | 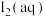 |  |
浓度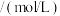 | a | b | c |

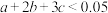 ,说明平衡体系中
,说明平衡体系中 沉淀。
沉淀。③计算25℃下
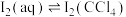 的平衡常数K=
的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】在恒压、将一定量的NO和O2混合,一定的条件下,反应相同时间,测得不同温度下NO转化为NO2的转化率如图所示。回答下列问题:
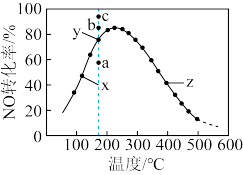
(1)由图可知,反应2NO(g)+O2(g) 2NO2(g)的ΔH
2NO2(g)的ΔH___ 0(填>,<,=)。
(2)图中___ 点(填x,y,z)在该温度下达到了平衡状态。
(3)图中y点所示条件下,增加O2的浓度___ 提高NO转化率(填能或不能)。
(4)380℃下,c起始(O2)=c起始(NO)=5.0×10-4mol·L-1,NO平衡转化率为50%,则平衡常数K___ 2000(填>,<,=)。
(5)图中x点,其v正___ v逆的(填>,<,=)。
(6)y点所对应的温度下,NO的平衡转化率对应的点是___ (填a,b,c)。

(1)由图可知,反应2NO(g)+O2(g)
 2NO2(g)的ΔH
2NO2(g)的ΔH(2)图中
(3)图中y点所示条件下,增加O2的浓度
(4)380℃下,c起始(O2)=c起始(NO)=5.0×10-4mol·L-1,NO平衡转化率为50%,则平衡常数K
(5)图中x点,其v正
(6)y点所对应的温度下,NO的平衡转化率对应的点是
您最近一年使用:0次



