某温度下,向10 mL 0.1 mol·L-lNaCl溶液和10 mL 0.1 mol·L-lK2CrO4溶液中分别滴加0.1 mol·L-lAgNO3溶液。滴加过程中pM[-lgc(Cl-)或-lgc(CrO42-)]与所加AgNO3溶液体积之间的关系如下图所示。已知Ag2CrO4为红棕色沉淀。下列说法错误的是


| A.该温度下,Ksp(Ag2CrO4)=4×10-12 |
| B.al、b、c三点所示溶液中c(Ag+):al>b>c |
| C.若将上述NaCl溶液浓度改为0.2mol·L-1,则a1点会平移至a2点 |
| D.用AgNO3标准溶液滴定NaCl溶液时,可用K2CrO4溶液作指示剂 |
2019·山东济南·一模 查看更多[8]
更新时间:2019-05-28 14:17:52
|
相似题推荐
【推荐1】 时,用
时,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为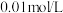 的
的 溶液,所得的沉淀溶解平衡图象分别是下图中的N和M。下列叙述
溶液,所得的沉淀溶解平衡图象分别是下图中的N和M。下列叙述不正确 的是

 时,用
时,用 溶液分别滴定浓度均为
溶液分别滴定浓度均为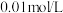 的
的 溶液,所得的沉淀溶解平衡图象分别是下图中的N和M。下列叙述
溶液,所得的沉淀溶解平衡图象分别是下图中的N和M。下列叙述
A.a点对 或 或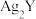 都是过饱和溶液 都是过饱和溶液 |
B.向b点的溶液中加入少量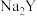 固体,b点可变到c点 固体,b点可变到c点 |
C. 时, 时,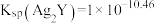 |
D.向 的混合液中滴入 的混合液中滴入 溶液时, 溶液时, 先沉淀 先沉淀 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列说法正确的是
| A.自然界地表层原生铜的硫化物经一系列转化变成CuSO4溶液,向地下层渗透,遇到难溶的ZnS或PbS,慢慢转变为铜蓝(CuS),整个过程只涉及复分解反应 |
B.用饱和Na2CO3溶液处理锅炉水垢中的CaSO4的离子方程式:Ca2++CO =CaCO3↓ =CaCO3↓ |
| C.向AgCl悬浊液中加入NaI溶液时出现黄色沉淀,说明Ksp(AgCl)<Ksp(AgI) |
D.25℃时,在含有大量PbI2的饱和溶液中存在着平衡PbI2(s) Pb2+(aq)+2I-(aq),加入KI固体,溶液中Pb2+浓度减小 Pb2+(aq)+2I-(aq),加入KI固体,溶液中Pb2+浓度减小 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】Fe2+、Fe3+、Zn2+较完全地形成氢氧化物沉淀的pH分别为6.7、3.7、4.6。某硫酸锌酸性溶液中含有少量Fe2+、Fe3+杂质离子,为除去这些离子制得纯净的ZnSO4,应加入的试剂是
| A.NaOH溶液 | B.氨水 |
| C.KMnO4、ZnCO3 | D.H2O2、ZnO |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
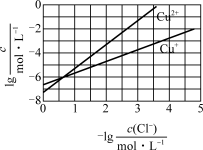
【推荐2】一定温度时,Cu2+、Mn2+、Fe2+、Zn2+等四种金属离子(M2+)形成硫化物沉淀所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)的关系如图所示。下列有关判断不正确的是


| A.该温度下,Ksp(MnS)大于1.0×10-35 |
| B.向含Mn2+、Zn2+的稀溶液中滴加Na2S溶液,Mn2+最有可能先沉淀 |
| C.向c(Fe2+)=0.1mol·L-1的溶液中加入CuS粉末,有FeS沉淀析出 |
| D.该温度下,溶解度:CuS>MnS>FeS>ZnS |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】根据下列实验操作和现象所得到的结论不正确的是
| 选项 | 实验操作和现象 | 结论 |
| A | 向浓度均为0.1mol/L的MgCl2、CuC12混合溶液中逐滴加入氨水,先出现蓝色沉淀 | Ksp[Mg(OH)2]>Ksp[Cu(OH)2] |
| B | 向溶有SO2的BaCl2溶液中通入气体X,出现白色沉淀 | X不一定具有氧化性 |
| C | 某溶液中加入盐酸酸化的氯化钡溶液,有白色沉淀生成 | 不能说明该溶液中一定含有SO42- |
| D | 加热盛有(NH4)2CO3固体的试管,并在试管口放置湿润的红色石蕊试纸,试纸变蓝 | (NH4)2CO3显碱性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】已知:①Ksp[Al(OH)3]=1.3×10-33,Ksp[Cr(OH)3]>Ksp[Al(OH)3];
②Cr(OH)3和Al(OH)3类似,是两性氢氧化物;
③离子浓度为10-5mol/L时可认为沉淀完全。
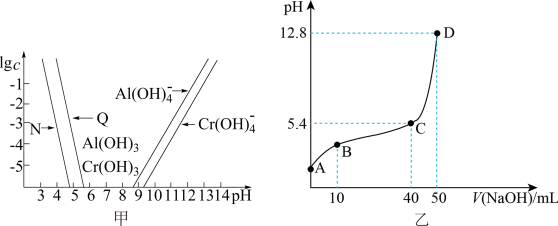
图甲为Cr和Al两种元素在水溶液中的存在形式与pH的关系,纵轴lgc表示lgc(M3+)或 。图乙为常温下,向含有物质的量浓度均为cmol/L的盐酸和CrCl3溶液中滴加浓度为cmol/L的NaOH溶液时pH与NaOH溶液体积的关系图。
。图乙为常温下,向含有物质的量浓度均为cmol/L的盐酸和CrCl3溶液中滴加浓度为cmol/L的NaOH溶液时pH与NaOH溶液体积的关系图。
下列说法正确的是
②Cr(OH)3和Al(OH)3类似,是两性氢氧化物;
③离子浓度为10-5mol/L时可认为沉淀完全。
图甲为Cr和Al两种元素在水溶液中的存在形式与pH的关系,纵轴lgc表示lgc(M3+)或
 。图乙为常温下,向含有物质的量浓度均为cmol/L的盐酸和CrCl3溶液中滴加浓度为cmol/L的NaOH溶液时pH与NaOH溶液体积的关系图。
。图乙为常温下,向含有物质的量浓度均为cmol/L的盐酸和CrCl3溶液中滴加浓度为cmol/L的NaOH溶液时pH与NaOH溶液体积的关系图。
下列说法正确的是
| A.图甲中Q代表Al3+ |
| B.图乙中,pH=5时,c(Cr3+)=1.0×10-3.8mol/L |
| C.图乙中,A到D过程中,溶液中水的电离程度先减小后增大 |
| D.根据图甲所示,若溶液中Al3+和Cr3+的起始浓度均为0.1mol/L,通过调节pH能实现两种元素的分离 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】用0.1000mol/LNa2SO4标准溶液滴定20.00mLBaCl2溶液,测得溶液电导率σ及-lgc(Ba2+)随滴入Na2SO4标准溶液的体积V(Na2SO4)的变化关系如图所示。下列说法不正确的是
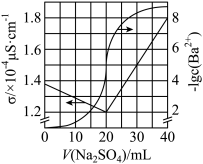

| A.BaCl2溶液的浓度为0.1000mol/L |
| B.Ksp(BaSO4)=10-10 |
| C.等浓度的Na+比Ba2+导电能力差 |
| D.若实验所用BaCl2溶液是用粗产品配制得来,则0.5000g粗产品中BaCl2•2H2O的质量分数为97.6% |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】以磷石膏(主要成分 ,杂质
,杂质 、
、 等)和氨水为原料可实现
等)和氨水为原料可实现 矿物封存同时制备轻质
矿物封存同时制备轻质 ,转化部分流程如图。
,转化部分流程如图。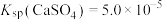 ,
,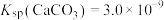 ,
,
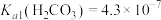 ,
,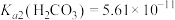 。
。
下列说法正确的是
 ,杂质
,杂质 、
、 等)和氨水为原料可实现
等)和氨水为原料可实现 矿物封存同时制备轻质
矿物封存同时制备轻质 ,转化部分流程如图。
,转化部分流程如图。
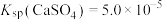 ,
,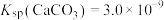 ,
,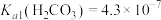 ,
,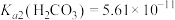 。
。下列说法正确的是
A.氨水中存在: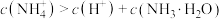 |
B.“转化”步骤,通入 后清液中始终存在 后清液中始终存在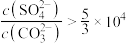 |
C.“转化”步骤,若通入 至溶液 至溶液 为6.5,此时溶液中 为6.5,此时溶液中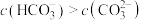 |
D.“滤液”中存在: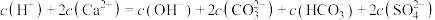 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】草酸亚铁(FeC2O4)是生产磷酸铁锂电池的原料,实验室可通过如图反应制取:
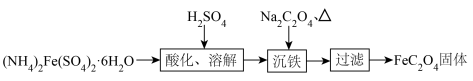
已知室温时:Ka1(H2C2O4)=5.6×10−2、Ka2(H2C2O4)=1.5×10−4、Ksp(FeC2O4)=2.1×10−7。
下列说法正确的是

已知室温时:Ka1(H2C2O4)=5.6×10−2、Ka2(H2C2O4)=1.5×10−4、Ksp(FeC2O4)=2.1×10−7。
下列说法正确的是
A.酸化、溶解后的溶液中存在:2c(Fe2+)+c(H+)<c(NH )+c(OH-) )+c(OH-) |
B.室温下,0.10 mol∙L−1NaHC2O4溶液中存在:c(C2O )<c(H2C2O4) )<c(H2C2O4) |
C.向稀硫酸酸化的KMnO4溶液中滴加Na2C2O4溶液至溶液褪色,反应的离子方程式为:5C2O +2MnO +2MnO +8H2O=10CO2↑+2Mn2++16OH- +8H2O=10CO2↑+2Mn2++16OH- |
| D.室温时反应Fe2++H2C2O4=FeC2O4+2H+的平衡常数K=40 |
您最近一年使用:0次


 为原料生产
为原料生产 ,对其工艺条件进行研究。现有含
,对其工艺条件进行研究。现有含 、
、 溶液,含
溶液,含 溶液。在一定pH范围内,四种溶液中
溶液。在一定pH范围内,四种溶液中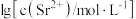 随pH的变化关系如图所示。下列说法错误的是
随pH的变化关系如图所示。下列说法错误的是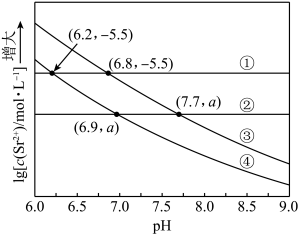
 的平衡常数
的平衡常数

 和
和 初始浓度均为
初始浓度均为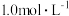 的混合溶液,
的混合溶液,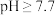 时才发生沉淀转化
时才发生沉淀转化

