某地菱锰矿的主要成分为MnCO3,还含有少量的FeCO3、CaCO3、Al2O3等杂质。工业上以菱锰矿为原料制备高纯度碳酸锰的流程如图所示:

已知:MnCO3+2NH4Cl=MnCl2+CO2↑+2NH3↑+H2O.
相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
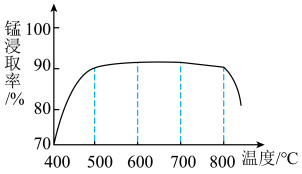
(1)焙烧时温度对锰浸取率的影响如图。焙烧时适宜的温度为___________ 左右;800℃以上锰的浸取率偏低,可能的原因是___________ 。
(2)净化包含三步:①加入少量MnO2,添加少量MnO2的作用是____________ 。发生反应的离子方程式为___________ 。
②加氨水调pH,溶液的pH范围应调节为___________ ~8.1之间。生成的沉淀主要是___________ 。
③加入MnF2,沉淀除去Ca2+,若溶液酸度过高,Ca2+沉淀不完全,原因是___________ 。
(3)碳化结晶中生成MnCO3的离子方程式为____________ 。

已知:MnCO3+2NH4Cl=MnCl2+CO2↑+2NH3↑+H2O.
相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 |

(2)净化包含三步:①加入少量MnO2,添加少量MnO2的作用是
②加氨水调pH,溶液的pH范围应调节为
③加入MnF2,沉淀除去Ca2+,若溶液酸度过高,Ca2+沉淀不完全,原因是
(3)碳化结晶中生成MnCO3的离子方程式为
更新时间:2019-07-12 20:18:22
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
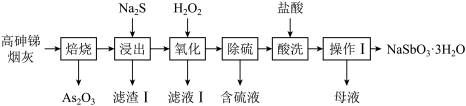
【推荐1】焦锑酸钠(NaSbO3·3H2O)可用于搪瓷的乳白剂及铁皮、钢板的抗酸漆。一种利用高砷锑烟灰(主要成分为Sb2O3、As2O3,还含Ag、Cu、Fe的氧化物)生产焦锑酸钠的工艺流程如下:
已知:i.Sb2O3、As2O3部分性质如下表:
ii.Ag、Cu、Fe的氧化物不溶于Na2S溶液
iii.Na2SbO4不溶于水;NaSbO3﹒3H2O既不溶于水,也不溶于酸。
请回答下列问题:
(1)“焙烧”的最低温度为_________ (填标号)
a.655℃ b.400℃ c.275℃ d.193℃
(2)“浸出”时,往往采取比常温稍高的浸液温度,且选用较高浓度的Na2S溶液,采取这些措施的目的是_________________________________________ 。“浸出”时,Sb2O3转化为Na3SbS3的化学方程式为__________________________________________ ,滤渣Ⅰ是____________ 。
(3)“氧化”时所用H2O2的电子式为___________ ,氧化产物为Na3SbO4和____________ .
(4)“酸洗”的作用是______________________ 。(用化学方程式表示)
(5)As2O3对应的酸为H3AsO3,测得某工业酸性废液中含H3AsO3和Fe2+,其浓度如表:
已知:iV.Ksp(FeAsO3)>Ksp(FeAsO4)=5.70×10-21。
V.H3AsO3的还原性比Fe2+强。
根据题目信息,则可采用______________ 方法除去该废水中的砷,除去砷后的废液中c(AsO43-)=__________________ (不考虑反应过程中溶液体积的微小变化)

已知:i.Sb2O3、As2O3部分性质如下表:
熔点/℃ | 沸点/℃ | 升华/℃ | |
Sb2O3 | 655 | 1550 | 400 |
As2O3 | 275 | 457 | 193 |
ii.Ag、Cu、Fe的氧化物不溶于Na2S溶液
iii.Na2SbO4不溶于水;NaSbO3﹒3H2O既不溶于水,也不溶于酸。
请回答下列问题:
(1)“焙烧”的最低温度为
a.655℃ b.400℃ c.275℃ d.193℃
(2)“浸出”时,往往采取比常温稍高的浸液温度,且选用较高浓度的Na2S溶液,采取这些措施的目的是
(3)“氧化”时所用H2O2的电子式为
(4)“酸洗”的作用是
(5)As2O3对应的酸为H3AsO3,测得某工业酸性废液中含H3AsO3和Fe2+,其浓度如表:
物质 | H3AsO3 | Fe2+ |
浓度/g·L-1 | 0.378 | 0.840 |
已知:iV.Ksp(FeAsO3)>Ksp(FeAsO4)=5.70×10-21。
V.H3AsO3的还原性比Fe2+强。
根据题目信息,则可采用
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
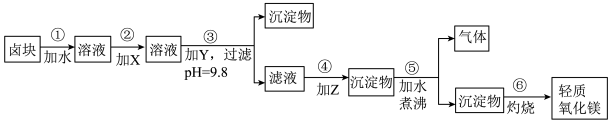
【推荐2】卤块的主要成分是MgCl2,此外还含Fe3+、Fe2+和Mn2+等离子。若以它为原料按下图所示工艺流程进行生产,可制得轻质氧化镁。
若要求产品尽量不含杂质,而且生产成本较低,请根据表1和表2提供的资料,填写空白:
表1 生成氢氧化物沉淀的pH
﹡Fe2+氢氧化物呈絮状,不易从溶液中除去,所以,常将它氧化为Fe3+,生成Fe(OH)3沉淀除去
表2 原料价格表
(1)在步骤②中加入的试剂X,最佳的选择是____________ ,其作用是_________________ ;
(2)在步骤③中加入的试剂应是_______________________ ;之所以要控制pH=9.8,其目的是___________________________________________________________ 。
(3)在步骤④中加入的试剂Z应是________________ ;
(4)在步骤⑤中发生反应的化学方程式是_____________________________________________ 。

若要求产品尽量不含杂质,而且生产成本较低,请根据表1和表2提供的资料,填写空白:
表1 生成氢氧化物沉淀的pH
| 物质 | 开始沉淀 | 沉淀完全 |
| Fe(OH)3 | 2.7 | 3.7 |
| Fe(OH)2 | 7.6 | 9.6﹡ |
| Mn(OH)2 | 8.3 | 9.8 |
| Mg(OH)2 | 9.6 | 11.1 |
表2 原料价格表
| 物质 | 价格/(元·吨-1) |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
(2)在步骤③中加入的试剂应是
(3)在步骤④中加入的试剂Z应是
(4)在步骤⑤中发生反应的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】碳酸亚铁( )是生产补血剂的重要原料,制取
)是生产补血剂的重要原料,制取 过程中涉及以下实验。
过程中涉及以下实验。
实验一:为探究某固体化合物X(仅含有三种元素)的组成和性质,设计并完成如下实验

已知:气体甲、气体乙均为短周期元素的单质。
请回答:
(1)化合物X含有的元素为___________ (写元素符号),化合物A的化学式为___________ 。写出A溶于足量稀硝酸的化学反应方程式为___________ 。
实验二:如图装置利用实验一所得溶液B制取 (白色固体,难溶于水):
(白色固体,难溶于水):

装置丙中,先将导管移出液面通入一段时间气体,再向 溶液(
溶液( )通入一段时间
)通入一段时间 至其pH为7,滴加一定量B溶液产生白色沉淀和无色气体,过滤、洗涤、干燥,得到
至其pH为7,滴加一定量B溶液产生白色沉淀和无色气体,过滤、洗涤、干燥,得到 固体。请回答:
固体。请回答:
(2)丙装置的反应仪器名称是___________ 。试剂a是___________ 。
(3)向 溶液通入
溶液通入 的目的是
的目的是___________ 。
(4)常温下,向 溶液(
溶液( )通入一段时间
)通入一段时间 至
至 时溶液中
时溶液中
___________ (已知 的
的 ,
, )。
)。
(5)丙装置中制取 的离子方程式为
的离子方程式为___________ 。
(6)检验溶液B中的金属阳离子可选用下列哪些试剂___________。
(7)100mL0.8mol/LB溶液完全反应,最终得到8.2克 固体,则产率为
固体,则产率为___________ (结果保留2位小数)。
 )是生产补血剂的重要原料,制取
)是生产补血剂的重要原料,制取 过程中涉及以下实验。
过程中涉及以下实验。实验一:为探究某固体化合物X(仅含有三种元素)的组成和性质,设计并完成如下实验

已知:气体甲、气体乙均为短周期元素的单质。
请回答:
(1)化合物X含有的元素为
实验二:如图装置利用实验一所得溶液B制取
 (白色固体,难溶于水):
(白色固体,难溶于水):
装置丙中,先将导管移出液面通入一段时间气体,再向
 溶液(
溶液( )通入一段时间
)通入一段时间 至其pH为7,滴加一定量B溶液产生白色沉淀和无色气体,过滤、洗涤、干燥,得到
至其pH为7,滴加一定量B溶液产生白色沉淀和无色气体,过滤、洗涤、干燥,得到 固体。请回答:
固体。请回答:(2)丙装置的反应仪器名称是
(3)向
 溶液通入
溶液通入 的目的是
的目的是(4)常温下,向
 溶液(
溶液( )通入一段时间
)通入一段时间 至
至 时溶液中
时溶液中
 的
的 ,
, )。
)。(5)丙装置中制取
 的离子方程式为
的离子方程式为(6)检验溶液B中的金属阳离子可选用下列哪些试剂___________。
| A.酸性高锰酸钾溶液 | B.NaOH |
C.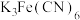 | D.KSCN |
 固体,则产率为
固体,则产率为
您最近一年使用:0次
解答题-原理综合题
|
较难
(0.4)
名校
解题方法
【推荐1】锌冶炼过程中产生的锌渣主要成分为铁酸锌(ZnFe2O4)和二氧化硅,以及少量的铜、铁、锌的氧化物和硫化物。利用酸溶的方法可溶出金属离子,使锌渣得到充分利用。
(1)铁酸锌酸溶。铁酸锌难溶于水,其晶胞由A、B结构按照1∶1交替累积而成,如图所示。将铁酸锌粉末投入到1L1mol·L-1H2SO4中,保温80℃,匀速搅拌。浸出液中Fe3+和Zn2+的浓度随时间的变化如表所示。
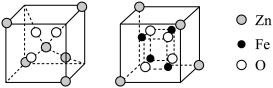
①B结构的化学式为___ 。
②铁酸锌和硫酸反应的离子方程式为___ 。
③酸溶时,溶出效率较高的金属离子是___ 。
(2)锌渣酸溶。将锌渣分别在SO2—1mol·L-1H2SO4、1mol·L-1H2SO4以及SO2—H2O三种体系中实验,均保持80℃,匀速搅拌,所得结果如图所示。已知:25℃时,Ksp(FeS)=6.3×10-17;Ksp(ZnS)=2.9×10-25;Ksp(CuS)=6.3×10-36;Ksp(Cu2S)=2.5×10-48;FeS和ZnS可溶于稀硫酸,CuS和Cu2S不溶于稀硫酸。
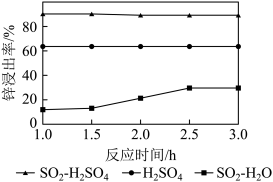
①在SO2—H2SO4体系中,Zn2+浸出率较高的原因是___ 。
②在SO2—H2SO4体系中,溶渣中Cu2S的质量增加,原因是___ 。
(1)铁酸锌酸溶。铁酸锌难溶于水,其晶胞由A、B结构按照1∶1交替累积而成,如图所示。将铁酸锌粉末投入到1L1mol·L-1H2SO4中,保温80℃,匀速搅拌。浸出液中Fe3+和Zn2+的浓度随时间的变化如表所示。

| 时间/h | 0.5 | 1.0 | 1.5 | 2.0 | 2.5 |
| c(Zn2+)/mol•L-1 | 0.10 | 0.11 | 0.15 | 0.21 | 0.21 |
| c(Fe3+)/mol•L-1 | 0.12 | 0.13 | 0.16 | 0.21 | 0.30 |
②铁酸锌和硫酸反应的离子方程式为
③酸溶时,溶出效率较高的金属离子是
(2)锌渣酸溶。将锌渣分别在SO2—1mol·L-1H2SO4、1mol·L-1H2SO4以及SO2—H2O三种体系中实验,均保持80℃,匀速搅拌,所得结果如图所示。已知:25℃时,Ksp(FeS)=6.3×10-17;Ksp(ZnS)=2.9×10-25;Ksp(CuS)=6.3×10-36;Ksp(Cu2S)=2.5×10-48;FeS和ZnS可溶于稀硫酸,CuS和Cu2S不溶于稀硫酸。

①在SO2—H2SO4体系中,Zn2+浸出率较高的原因是
②在SO2—H2SO4体系中,溶渣中Cu2S的质量增加,原因是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】硫酸锰(MnSO4·H2O)是一种粉色晶体,易溶于水,不溶于乙醇,是重要的微量元素肥料之一、工业上由天然二氧化锰粉与硫化锰矿(还含Fe、Al、Mg、Si等元素的氧化物)制备硫酸锰的工艺如下图所示。回答下列问题:
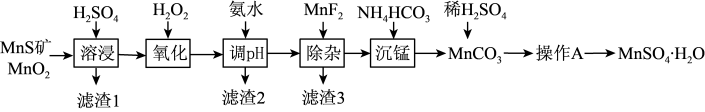
相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
(1)“滤渣1”中含有S和_______ ;“溶浸”时两种含锰化合物与H2SO4反应的化学方程式_______ 。
(2)加入H2O2的主要目的是_______ 。
(3)利用氨水调节溶液的pH范围在_______ 之间,“滤渣2”的成分为_______ 。
(4)“除杂”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是_______ 。
(5)“沉锰”反应的离子方程式_______ 。
(6)由图象可知,从“操作A”所得溶液中得到MnSO4·H2O晶体需进行的操作是_______ 、洗涤、干燥。若称取一定质量的MnSO4·H2O用标准BaCl2溶液滴定(操作过程产生的误差很小可忽略),计算所得样品质量分数大于100%,分析可能的原因是_______ 。


相关金属离子[c0(Mn+)=0.1mol·L-1]形成氢氧化物沉淀的pH范围如下:
| 金属离子 | Mn2+ | Fe2+ | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀的pH | 8.1 | 6.3 | 1.5 | 3.4 | 8.9 |
| 沉淀完全的pH | 10.1 | 8.3 | 2.8 | 4.7 | 10.9 |
(2)加入H2O2的主要目的是
(3)利用氨水调节溶液的pH范围在
(4)“除杂”的目的是生成MgF2沉淀除去Mg2+。若溶液酸度过高,Mg2+沉淀不完全,原因是
(5)“沉锰”反应的离子方程式
(6)由图象可知,从“操作A”所得溶液中得到MnSO4·H2O晶体需进行的操作是

您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】门捷列夫最早预言了具有半导体特性类硅元素锗(32Ge),工业上用精硫锗矿(主要成分为 )制取高纯度锗,其工艺流程如图所示:
)制取高纯度锗,其工艺流程如图所示:
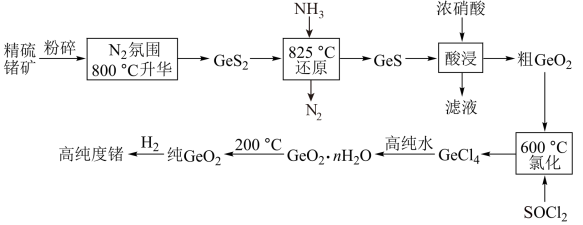
已知:①硅和锗是同主族相邻元素,结构和性质类似;
② 在
在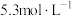 的盐酸中溶解度最小。
的盐酸中溶解度最小。
(1)基态锗原子的价层电子排布式为___________ ,晶体锗的晶体类型是___________ 。
(2)① ,使精硫锗矿在
,使精硫锗矿在 氛围中升华的原因是
氛围中升华的原因是___________ 。
②还原时发生反应:___________ ___________
___________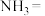 ___________
___________ ___________
___________ ___________
___________ 。配平上述反应的化学方程式,标出电子转移的方向和数目
。配平上述反应的化学方程式,标出电子转移的方向和数目______________ 。
③比较键角:
___________  (选填编号)。其原因是
(选填编号)。其原因是___________ 。
A.> B.< C.=
(3)酸浸时温度不能过高的原因是___________ 。氯化除生成 外,反应还生成一种V形分子,相应的化学方程式为
外,反应还生成一种V形分子,相应的化学方程式为___________ 。 水解得到
水解得到 ,该步骤高纯水不能过量,原因是
,该步骤高纯水不能过量,原因是___________ 。
(4) 与碱反应可生成锗酸盐,其中
与碱反应可生成锗酸盐,其中 是一种难溶电解质,一定温度下,
是一种难溶电解质,一定温度下, 在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(选填编号)。
在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(选填编号)。
 )制取高纯度锗,其工艺流程如图所示:
)制取高纯度锗,其工艺流程如图所示:
已知:①硅和锗是同主族相邻元素,结构和性质类似;
②
 在
在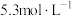 的盐酸中溶解度最小。
的盐酸中溶解度最小。(1)基态锗原子的价层电子排布式为
(2)①
 ,使精硫锗矿在
,使精硫锗矿在 氛围中升华的原因是
氛围中升华的原因是②还原时发生反应:___________
 ___________
___________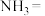 ___________
___________ ___________
___________ ___________
___________ 。配平上述反应的化学方程式,标出电子转移的方向和数目
。配平上述反应的化学方程式,标出电子转移的方向和数目③比较键角:

 (选填编号)。其原因是
(选填编号)。其原因是A.> B.< C.=
(3)酸浸时温度不能过高的原因是
 外,反应还生成一种V形分子,相应的化学方程式为
外,反应还生成一种V形分子,相应的化学方程式为 水解得到
水解得到 ,该步骤高纯水不能过量,原因是
,该步骤高纯水不能过量,原因是(4)
 与碱反应可生成锗酸盐,其中
与碱反应可生成锗酸盐,其中 是一种难溶电解质,一定温度下,
是一种难溶电解质,一定温度下, 在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(选填编号)。
在水中的沉淀溶解平衡曲线如图所示,下列说法正确的是___________(选填编号)。
A.n点与p点对应的 相等 相等 |
B.q点无 沉淀生成 沉淀生成 |
| C.通过蒸发可以使溶液由q点变到p点 |
D.加入 可以使溶液由n点变到m点 可以使溶液由n点变到m点 |
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
【推荐1】某工厂的工业废水中含有大量的 FeSO4、较多的 Cu2+和少量的 Na+。为了减少污染并变废为宝,工厂计划从该废水中回收硫酸亚铁和金属铜。请根据流程图完成回收硫酸亚铁和铜的简单实验方案,回答下列问题:(流程图中无需填写)

(1)试剂①为____ ,操作⑥名称为_______ 和洗涤,其中洗涤的操作方法是_______________ 。为检验沉淀是否洗涤干净,可向最后一次洗涤液中加入试剂:__________ 。
(2)试剂⑤的化学式为_____ ,所发生的化学方程式为___________________________ 。
(3)对④和⑧的混合溶液,不选用蒸发结晶(余热蒸干)获得FeSO4·7H2O,原因是_____ 、________ 。(说出两点原因)

(1)试剂①为
(2)试剂⑤的化学式为
(3)对④和⑧的混合溶液,不选用蒸发结晶(余热蒸干)获得FeSO4·7H2O,原因是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
【推荐2】银铜合金广泛用于航空工业。从切割废料中回收银并制备铜化工产品的工艺如下:
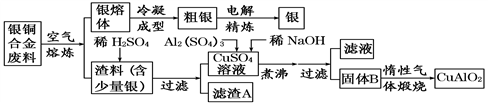
[注:Al(OH)3和Cu(OH)2 开始分解的温度分别为450℃和80℃]
(1)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学反应方程式为_________________ 。
(2)固体混合物B的组成为__________ 、__________ 。
(3)完成煅烧过程中一个反应的化学方程式:__________________________________ ↑。
(4)若银铜合金中铜的质量分数为64.0%,理论上5.0kg废料中的铜可完全转化为CuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液________ L。
(5)CuSO4溶液也可用于制备胆矾,其基本操作是___________ 、__________ 、过滤、洗涤和干燥。

[注:Al(OH)3和Cu(OH)2 开始分解的温度分别为450℃和80℃]
(1)滤渣A与稀HNO3反应,产生的气体在空气中迅速变为红棕色,该气体变色的化学反应方程式为
(2)固体混合物B的组成为
(3)完成煅烧过程中一个反应的化学方程式:
(4)若银铜合金中铜的质量分数为64.0%,理论上5.0kg废料中的铜可完全转化为CuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液
(5)CuSO4溶液也可用于制备胆矾,其基本操作是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
名校
解题方法
【推荐3】铊(Tl)在工业中的用途非常广泛,其中铊锡合金可作超导材料;铊镉合金是原子能工业中的重要材料。铊主要从铅精矿焙烧产生的富铊灰(主要成分PbO、ZnO、Fe2O3、FeO、Tl2O等)中提炼,具体工艺流程如图。

已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂CH3CONR2的二乙苯溶液,萃取过程的反应原理为H++CH3CONR2+TlCl
 [CH3CONR2H]TlCl4。
[CH3CONR2H]TlCl4。
回答下列问题:
(1)“浸取”过程中生成可溶性的TlCl ,该反应的离子方程式为
,该反应的离子方程式为___ 。
(2)残渣的主要成分为____ (填化学式);在实验室中,“萃取”和“反萃取”过程均必须使用的玻璃仪器的名称为___ 。
(3)“反萃取”过程中发生反应的化学方程式为___ 。
(4)“还原、氧化、沉淀”过程中TlCl 发生反应的离子方程式为
发生反应的离子方程式为___ 。
(5)流程中得到的“TlCl”需要用盐酸洗涤,用平衡原理解释与蒸馏水相比,盐酸洗涤的优点为___ 。
(6)电解Tl2SO4制备金属Tl的装置如图所示。阳极的电极反应式为___ ;当转移2mole-时,左侧电极室中溶液的质量减少___ g。


已知:萃取剂选用对铊有很高选择性的酰胺类萃取剂CH3CONR2的二乙苯溶液,萃取过程的反应原理为H++CH3CONR2+TlCl

 [CH3CONR2H]TlCl4。
[CH3CONR2H]TlCl4。回答下列问题:
(1)“浸取”过程中生成可溶性的TlCl
 ,该反应的离子方程式为
,该反应的离子方程式为(2)残渣的主要成分为
(3)“反萃取”过程中发生反应的化学方程式为
(4)“还原、氧化、沉淀”过程中TlCl
 发生反应的离子方程式为
发生反应的离子方程式为(5)流程中得到的“TlCl”需要用盐酸洗涤,用平衡原理解释与蒸馏水相比,盐酸洗涤的优点为
(6)电解Tl2SO4制备金属Tl的装置如图所示。阳极的电极反应式为

您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐1】实验室采用MgCl2、AlCl3混合溶液与过量氨水反应制备MgAl2O4,主要流程如下:

(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应容器中加入________ (填“A”、或“B”),再滴加另一反应物。
(2)实验室利用氯化铵和熟石灰反应制取氨气,写出反应的化学方程式________________________ 。
(3)判断流程中沉淀是否洗净所用的试剂是______________ ;高温焙烧时,用于盛放固体的仪器名称是__________________ 。
(4)无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。
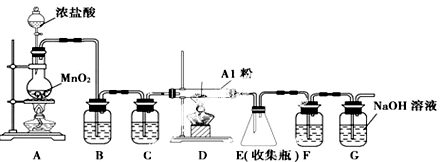
①写出装置A 中发生反应的离子方程式________________________ 。
②装置B中盛放饱和NaCl溶液,该装置的主要作用是__________ ;F中试剂的作用是__________ ;
用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为__________ 。
③实验步骤:如图连接装置后,先__________ (填实验操作),再装药品,然后点燃______ (填“ A” 或“C” )处酒精灯,当________ (填实验现象)时,再点燃另一处酒精灯。
④写出装置G 中发生反应的离子方程式________________________ 。

(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应容器中加入
(2)实验室利用氯化铵和熟石灰反应制取氨气,写出反应的化学方程式
(3)判断流程中沉淀是否洗净所用的试剂是
(4)无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。

①写出装置A 中发生反应的离子方程式
②装置B中盛放饱和NaCl溶液,该装置的主要作用是
用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为
③实验步骤:如图连接装置后,先
④写出装置G 中发生反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
名校
【推荐2】保险粉Na2S2O4大量用于印染业,并用来漂白纸张、纸浆和陶土等。某化学兴趣小组同学用甲酸法制取保险粉的装置如图所示(加持装置略去)。
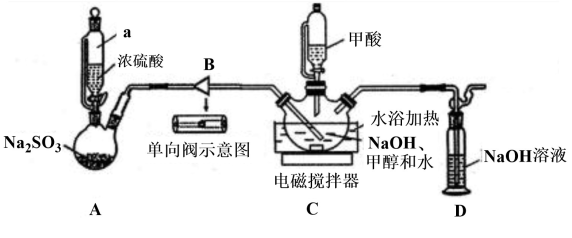
已知:保险粉易溶于水,不溶于甲醇,具有强还原性,在空气中易被氧化:2Na2S2O4+O2+2H2O=NaHSO3或Na2S2O4 +O2+H2O =NaHSO3+NaHSO4。实验时先把甲酸(HCOOH)与溶于甲醇和水混合溶剂的NaOH混合,再通入SO2气体。回答下列问题:
(1)仪器a的名称是______ ;装置B的作用是______ 。
(2)装置C中甲醇不参加反应,甲醇的作用是______ ;生成Na2S2O4的离子方程式为______ 。
(3)下列有关该实验的说法正确的是______ (填序号)。
A.可用硝酸和BaCl2溶液检验制得的Na2S2O4中是否混有NaHSO4
B.实验中甲酸和NaOH最合适的物质的量之比为1:1
C.用N2排尽装置内的空气,有利于提高 的Na2S2O4纯度
D.得到Na2S2O4固体后可用甲醇洗涤
(4)测定产品中Na2S2O4质量分数,其实验步骤如下,准确称取0.5000g产品放入锥形瓶中,加入适量水使其溶解。然后加入足量甲醛,充分反应,再滴加几滴指示剂,用0.2000mol·L-1的标准I2溶液滴定,至终点时,消耗25.00mL标准I2溶液。实验过程中涉及的反应:Na2S2O4+2HCHO+H2O =NaHSO3·HCHO+NaHSO2·HCHO;NaHSO2·HCHO+2I2+2H2O= NaHSO4+HCHO+4HI。该实验加入指示剂是______ ,产品Na2S2O4 (M=174g·mol-1)的质量分数为 ______ % (保留一位小数)。
(5)探究Na2S2O4的性质。隔绝空气加热Na2S2O4固体完全分解是到固体产物Na2SO3,Na2S2O3和SO2,但该兴趣小组没有做到完全隔绝空气,得到的固体产物中还含有Na2SO4。请设计实验证明该分解产物中含有Na2SO4。实验方案是______ 。(可选试剂:稀盐酸、稀硫酸、稀硝酸、BaCl2溶液、KMnO4溶液)

已知:保险粉易溶于水,不溶于甲醇,具有强还原性,在空气中易被氧化:2Na2S2O4+O2+2H2O=NaHSO3或Na2S2O4 +O2+H2O =NaHSO3+NaHSO4。实验时先把甲酸(HCOOH)与溶于甲醇和水混合溶剂的NaOH混合,再通入SO2气体。回答下列问题:
(1)仪器a的名称是
(2)装置C中甲醇不参加反应,甲醇的作用是
(3)下列有关该实验的说法正确的是
A.可用硝酸和BaCl2溶液检验制得的Na2S2O4中是否混有NaHSO4
B.实验中甲酸和NaOH最合适的物质的量之比为1:1
C.用N2排尽装置内的空气,有利于提高 的Na2S2O4纯度
D.得到Na2S2O4固体后可用甲醇洗涤
(4)测定产品中Na2S2O4质量分数,其实验步骤如下,准确称取0.5000g产品放入锥形瓶中,加入适量水使其溶解。然后加入足量甲醛,充分反应,再滴加几滴指示剂,用0.2000mol·L-1的标准I2溶液滴定,至终点时,消耗25.00mL标准I2溶液。实验过程中涉及的反应:Na2S2O4+2HCHO+H2O =NaHSO3·HCHO+NaHSO2·HCHO;NaHSO2·HCHO+2I2+2H2O= NaHSO4+HCHO+4HI。该实验加入指示剂是
(5)探究Na2S2O4的性质。隔绝空气加热Na2S2O4固体完全分解是到固体产物Na2SO3,Na2S2O3和SO2,但该兴趣小组没有做到完全隔绝空气,得到的固体产物中还含有Na2SO4。请设计实验证明该分解产物中含有Na2SO4。实验方案是
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】四氯化锡常温下是无色液体,在空气中极易水解,熔点-36℃,沸点114℃,金属锡的熔点为231℃。分液漏斗中放浓盐酸,仪器a中放MnO2,二者用于制氯气,用熔融的金属锡跟干燥的氯气直接作用制取无水四氯化锡(此反应过程放出大量的热)。请回答下列各问题。

(1)仪器a、b的名称分别是______ 、________ ,仪器b的作用是__________________ 。
(2)图中装置F与装置G之间连接干燥管的目的是______________________________ 。
(3)装置D中Sn发生反应的化学方程式为___________ ;装 置 G 的作用是____________ 。
(4)装置B中的试剂是______________________ ;装置C的作用是_________________ 。
(5)实验过程中。当观察到________ 时,即可熄灭装置D处的酒精灯。
(6)已知四氯化锡遇水强烈水解,产物之一是固态二氧化锡,请写出四氯化锡水解的化学方程式______________________________________ 。

(1)仪器a、b的名称分别是
(2)图中装置F与装置G之间连接干燥管的目的是
(3)装置D中Sn发生反应的化学方程式为
(4)装置B中的试剂是
(5)实验过程中。当观察到
(6)已知四氯化锡遇水强烈水解,产物之一是固态二氧化锡,请写出四氯化锡水解的化学方程式
您最近一年使用:0次



