335℃时,在恒容密闭反应器中1.00mol 催化脱氢的反应过程如下:
催化脱氢的反应过程如下:
反应1:
反应2:
测得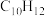 和
和 的产率
的产率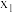 和
和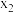 (以物质的量分数计)随时间的变化关系及反应过程中能量的变化如图所示。下列说法错误的是( )
(以物质的量分数计)随时间的变化关系及反应过程中能量的变化如图所示。下列说法错误的是( ) 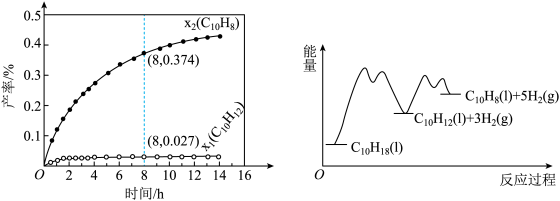
 催化脱氢的反应过程如下:
催化脱氢的反应过程如下:反应1:

反应2:

测得
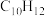 和
和 的产率
的产率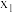 和
和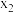 (以物质的量分数计)随时间的变化关系及反应过程中能量的变化如图所示。下列说法错误的是( )
(以物质的量分数计)随时间的变化关系及反应过程中能量的变化如图所示。下列说法错误的是( ) 
| A.使用催化剂能改变反应历程 |
B.更换催化剂后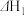 、 、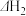 也会随之改变 也会随之改变 |
| C.8h时,反应1、2都未处于平衡状态 |
D.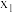 显著低于 显著低于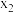 ,是由于反应2的活化能比反应1的小,反应1生成的 ,是由于反应2的活化能比反应1的小,反应1生成的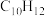 很快转变成 很快转变成 |
更新时间:2019-09-27 21:54:52
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】不能用勒夏特列原理解释的是
| A.热的纯碱溶液去污能力强 | B.新制的氯水在光照条件下颜色变浅 |
C.在钢铁船体上装一块 板防止腐蚀 板防止腐蚀 | D.打开冰镇啤酒,把啤酒倒入玻璃杯中看到大量泡沫 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】丁烯是一种重要的化工原料,可由丁烷催化脱氢制备。
已知:①C4H10(g)+ O2(g)=C4H8(g)+H2O(g)△H=-119kJ·mol-1
O2(g)=C4H8(g)+H2O(g)△H=-119kJ·mol-1
②H2(g)+ O2(g)=H2O(g)△H2=-242kJ·mol-1
O2(g)=H2O(g)△H2=-242kJ·mol-1
丁烷(C4H10)脱氢制丁烯(C4H8)的热化学方程式为C4H10(g) C4H8(g)+H2(g)△H3。
C4H8(g)+H2(g)△H3。
下列叙述正确的是
已知:①C4H10(g)+
 O2(g)=C4H8(g)+H2O(g)△H=-119kJ·mol-1
O2(g)=C4H8(g)+H2O(g)△H=-119kJ·mol-1②H2(g)+
 O2(g)=H2O(g)△H2=-242kJ·mol-1
O2(g)=H2O(g)△H2=-242kJ·mol-1丁烷(C4H10)脱氢制丁烯(C4H8)的热化学方程式为C4H10(g)
 C4H8(g)+H2(g)△H3。
C4H8(g)+H2(g)△H3。下列叙述正确的是
| A.△H3=-123kJ·mol-1 |
| B.其他条件不变时,反应平衡后升高温度,能提高该反应中丁烯产率 |
| C.恒温恒容条件下,反应平衡后再充入C4H10(g),混合气体中丁烯的百分含量增大 |
| D.其他条件不变时,反应平衡后增大压强,能提高该反应中丁烯产率 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐1】某温度下在2L密闭容器中加入一定量A,发生以下化学反应:2A(g) B(g)+C(g) ΔH =-48.25kJ/mol。反应过程中B、A的浓度比与时间t有右图所示关系,若测得第15min时c(B)=1.6mol/L,下列结论正确的是
B(g)+C(g) ΔH =-48.25kJ/mol。反应过程中B、A的浓度比与时间t有右图所示关系,若测得第15min时c(B)=1.6mol/L,下列结论正确的是

 B(g)+C(g) ΔH =-48.25kJ/mol。反应过程中B、A的浓度比与时间t有右图所示关系,若测得第15min时c(B)=1.6mol/L,下列结论正确的是
B(g)+C(g) ΔH =-48.25kJ/mol。反应过程中B、A的浓度比与时间t有右图所示关系,若测得第15min时c(B)=1.6mol/L,下列结论正确的是
| A.反应达平衡时,A的转化率为80% |
| B.A的初始物质的量为4mol |
| C.反应到达平衡时,放出的热量是193kJ |
| D.15min时,v正= v逆=0 |
您最近一年使用:0次
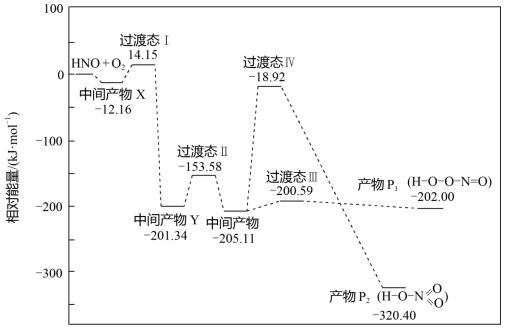
【推荐2】活泼自由基与氧气的反应一直是关注的热点。HNO自由基与 反应过程的能量变化如图所示。下列说法正确的是
反应过程的能量变化如图所示。下列说法正确的是
 反应过程的能量变化如图所示。下列说法正确的是
反应过程的能量变化如图所示。下列说法正确的是
| A.该反应为吸热反应 |
B.产物的稳定性: |
| C.升高温度,反应物活化分子百分数增大 |
D.相同条件下,由中间产物Z转化为产物的速率: |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】在2 L恒容密闭容器中充入2molH2、1 mol CO,在一定条件下发生如下反应:2H2(g)+CO(g) CH3OH(g) ∆H=-90.1kJ∙mol-1;CO的平衡转化率与温度、压强之间的关系如图所示。下列推断正确的是( )
CH3OH(g) ∆H=-90.1kJ∙mol-1;CO的平衡转化率与温度、压强之间的关系如图所示。下列推断正确的是( )

 CH3OH(g) ∆H=-90.1kJ∙mol-1;CO的平衡转化率与温度、压强之间的关系如图所示。下列推断正确的是( )
CH3OH(g) ∆H=-90.1kJ∙mol-1;CO的平衡转化率与温度、压强之间的关系如图所示。下列推断正确的是( )
| A.工业上,利用上述反应合成甲醇,温度越高越好 |
| B.图象中X代表温度,P(M2)>P(M1) |
| C.图象中P点代表的平衡常数K为4 |
| D.温度和容积不变,再充入2molH2、1 mol CO,达到平衡时CO转化率减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】符合如图的反应是( )


A.X(g)+3Y(g) 2Z(g) ΔH>0 2Z(g) ΔH>0 |
B.X(g)+3Y(g) 2Z(g) ΔH<0 2Z(g) ΔH<0 |
C.X(g)+2Y(g) 3Z(g) ΔH<0 3Z(g) ΔH<0 |
D.X(g)+2Y(g) 3Z(g) ΔH>0 3Z(g) ΔH>0 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐2】1,3-丁二烯和Br2以物质的量之比为1:1发生加成反应分两步:第一步Br+进攻1,3-丁二烯生成中间体C(溴正离子);第二步Br-进攻中间体C完成1,2-加成或1,4-加成。反应过程中的能量变化如下图所示,下列说法正确的是


| A.其它条件相同时,生成产物B的速率快于产物A的速率 |
| B.升高温度,1,3-丁二烯的平衡转化率增大 |
| C.该加成反应的反应热为Eb-Ea |
| D.该反应的速率主要取决于第一步反应的快慢 |
您最近一年使用:0次

 O2+[O]
O2+[O]


