醋酸溶液中存在电离平衡 CH3COOH CH3COO- + H+,下列叙述不正确的是
CH3COO- + H+,下列叙述不正确的是
 CH3COO- + H+,下列叙述不正确的是
CH3COO- + H+,下列叙述不正确的是| A.升高温度,平衡正向移动,醋酸的电离常数Ka增大 |
| B.CH3COOH溶液加少量的CH3COONa固体,平衡逆向移动 |
| C.室温下,欲使0.1 mol/L醋酸溶液的电离度α增大,可加入少量冰醋酸 |
| D.0.10 mol/L的CH3COOH 溶液加水稀释,溶液中c(CH3COOH)/c(CH3COO-)减小 |
更新时间:2019-12-07 13:02:33
|
相似题推荐
单选题
|
较易
(0.85)
解题方法
【推荐1】室温下,对于0.10mol·L-1的氨水,下列判断正确的是( )
| A.与AlCl3溶液反应的离子方程式为Al3++3OH-=Al(OH)3↓ |
| B.与等体积0.10mol·L-1HNO3溶液恰好完全中和 |
C.加水稀释后,溶液c(NH )·c(OH-)变大 )·c(OH-)变大 |
D.溶液中存在电离平衡:NH3·H2O=NH +OH- +OH- |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】常温下,下列说法错误的是
| A.物质的量浓度相同的NaHS溶液和Na2S溶液,前者的c(H2S)大 |
| B.CH3COONa溶液,随温度升高,溶液中c(OH-)增大,c(H+)可能减小 |
| C.向pH=11的氨水中滴加NaOH溶液,可能会促进NH3·H2O电离 |
| D.pH=7的CH3COONH4溶液和pH=7的NaCl溶液,两溶液中水的电离程度相等 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】已知:H2SO3;Ka1=1.3×10−2 Ka2=6.3×10−8
H2CO3:Ka1=4.2×10−7 Ka2=5.6×10−11
工业上以SO2和纯碱为原料制备无水NaHSO3的主要流程如图,下列说法错误的是

H2CO3:Ka1=4.2×10−7 Ka2=5.6×10−11
工业上以SO2和纯碱为原料制备无水NaHSO3的主要流程如图,下列说法错误的是

| A.吸收过程中有气体生成 |
| B.结晶后母液中含有两种溶质 |
| C.在热空气流中进行“气流干燥”,但温度不宜过高 |
| D.中和后溶液中含Na2SO3和NaHCO3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】常温下,在20.0mL0.10mol•L-1氨水中滴入0.10mol•L-1的盐酸,溶液的pH与所加盐酸的体积关系如图。已知0.10mol•L-1氨水的电离度为1.32%,下列叙述错误的是


| A.该滴定过程应该选择甲基橙作为指示剂 | B.M点对应的盐酸体积小于20.0mL |
| C.M点处的溶液中c(H+)=c(OH-) | D.N点处的溶液中pH>12 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列关于 NaOH 溶液和氨水的说法正确的是
| A.相同浓度两溶液中的 c(OH-) 相等 |
| B.pH=13 的两溶液稀释 100 倍,pH 都为 11 |
| C.100 mL 0.1 mol/L 的两溶液能中和等物质的量的盐酸 |
| D.两溶液中分别加入少量对应的 NaOH 固体,c(OH-) 均明显减小 |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】用蒸馏水逐渐稀释 的醋酸,若维持温度不变,则在稀释过程中逐渐增大的是
的醋酸,若维持温度不变,则在稀释过程中逐渐增大的是
 的醋酸,若维持温度不变,则在稀释过程中逐渐增大的是
的醋酸,若维持温度不变,则在稀释过程中逐渐增大的是A.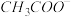 的物质的量浓度 的物质的量浓度 | B.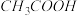 的物质的量浓度 的物质的量浓度 |
| C.H+的物质的量浓度 | D.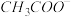 和H+的物质的量 和H+的物质的量 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】室温下,关于1.0mL0.1mol/L氨水。下列判断正确的是
| A.溶液的pH等于13 |
| B.加入少量NH4Cl固体,c (OH-)不变 |
C.c(OH-)=c ( )+c(H+) )+c(H+) |
| D.与1.0mL0.1mol/L盐酸混合后,溶液呈中性 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】在醋酸的电离平衡CH3COOH CH3COO-+H+中,要使电离平衡右移且c(H+)增大,应采取的措施是
CH3COO-+H+中,要使电离平衡右移且c(H+)增大,应采取的措施是
 CH3COO-+H+中,要使电离平衡右移且c(H+)增大,应采取的措施是
CH3COO-+H+中,要使电离平衡右移且c(H+)增大,应采取的措施是| A.加入NaOH(s) |
| B.通入HCl气体 |
| C.加蒸馏水 |
| D.升高温度 |
您最近一年使用:0次

 NH
NH
 的氨水,下列叙述正确的是
的氨水,下列叙述正确的是 的
的 溶液,混合液显中性
溶液,混合液显中性 不变
不变

